酸碱反应
一个方便的经验法则对酸碱反应
最后更新:2022年12月29日|
可逆与不可逆酸碱反应
上次我们了解了pK一个以及它如何是我们最接近的通用测量各种不同的酸和碱的优势。
我上一篇文章中也提到过如何用pK吗一个表(关键教训:较强的酸加给弱酸性和弱碱性强基地)。
我们可以使用pKa估计酸碱反应的平衡常数。
的一个方便的经验法则是,如果酸碱反应酸和共轭酸由超过10 pK吗一个单位,反应本质上是不可逆转的。
表的内容
- 一个不可逆转的酸碱反应:强酸(HCl) +强碱(氢氧化钠)提供水
- 一个容易可逆的酸碱反应:甲醇(pKa 15.2)与水(pKa 14)
- 在什么情况下,酸碱反应成为不可逆转的实用目的?
- 应用范围:克莱森缩合,酯的酸性比CH3哦,大约10 pK一个单位
- 笔记
1。一个不可逆转的酸碱反应:强酸(HCl) +强碱(氢氧化钠)提供水
在一个极端真的,我们有一摩尔的强酸,假设盐酸援助(HCl), pK一个8。为了它,我们添加(慢慢地)解决方案的水含有氢氧化钠(摩尔之一共轭碱的水,pK一个14)。
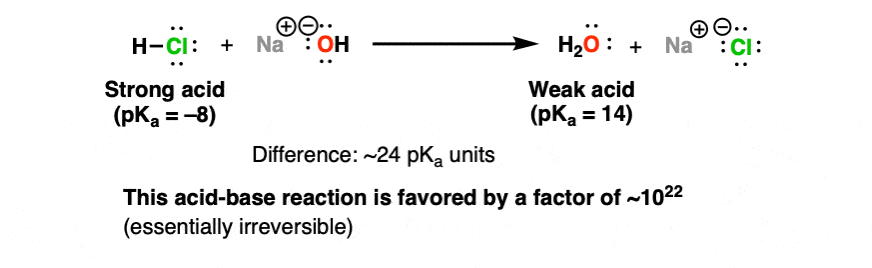
盐酸和氢氧化钠反应给水和氯化钠。怎么这个反应是有利的?我们可以做一个粗略的估计。的pK一个HCl是8。氢氧化钠是一共轭碱H2O (pK一个14)。
这是一个区别约22 pK一个单位,因为每个pK一个单位代表一个数量级,这个反应是有利的平衡常数约10至22的力量。
对于所有意图和目的,反应平衡常数这个巨大不可逆转的。
也就是说,盐酸和氢氧化钠反应时完全消耗,只给H2O和氯化钠。
2。一个容易可逆的酸碱反应:甲醇(pKa 15.2)与水(pKa 14)
什么另一个极端:甲醇的反应(pK一个与氢氧化钠(15.2)共轭碱的水,pK一个14)?
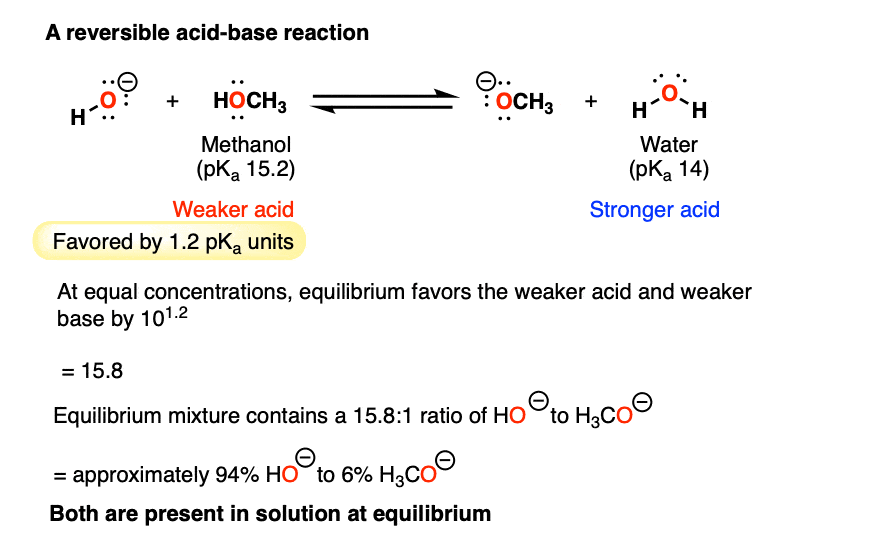
双方的酸碱反应强烈支持。这里我们在pK处理一个非常小的差别一个——只有1.2 pK一个单位。
这里的平衡常数只会10到1.2 - > 15.8的力量给较弱的酸(CH3OH)和较弱的基础(-)。
在平衡时我们会有一个混合的HO(-) 94%(较弱的基础)和6%的H3有限公司(-)更强的基础。
换句话说,两个物种出现在解决方案。
3所示。在什么情况下,酸碱反应成为不可逆转的实用目的?
所以我们能延伸多远?在这两个极端之间,在什么情况下,反应变得不可逆转的实际用途呢?
没有硬性规定。但为了实用的目的,一个好的经验法则是大约10 pK一个单位。
也就是说,如果在pK的区别一个酸和碱之间的(实际上,的共轭酸的基础)是大约10 pK一个单位或更少,它是有用的考虑他们的酸碱反应处于平衡状态。
想一想这意味着什么——比100亿年的一个分子可以使反应的差异!
一个在100亿年可能听起来不算很多。但是当你考虑到摩尔包含10的23个分子,和他们每个人碰撞每秒数百万次,几率并不像看上去的那么糟。
f你唯一的机会买一架私人飞机落在你赢得一个强力球彩票——但你可以填写每秒数十万条目,每一秒,你会的G5经销商在下周二。
这里有一个例子Org 2中你会看到。克莱森缩合开始的去质子化酯(pK一个~ 24)的醇盐离子(共轭碱一个酒精,pK一个~ 15)。(见文章:在克莱森缩合)
冷宫的大约10的9次方,因为我们要从一个较弱的基础(醇盐(deprotonated)一个更强大的基地酯,又酯烯醇化物)。
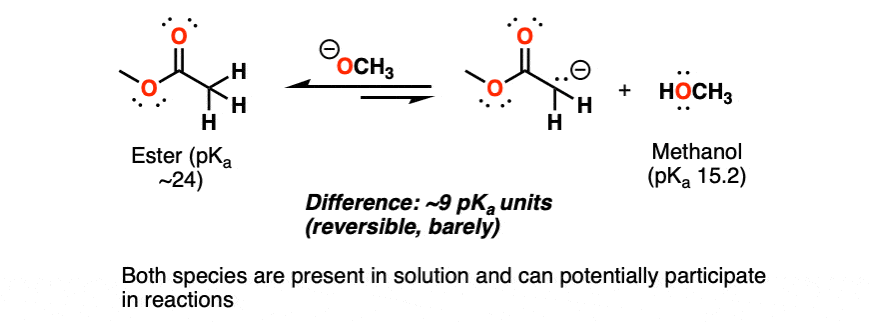
即使只有少量deprotonated酯在平衡时,这个可以足够的得到的反应!你可以相信我的话——这个经验法则适用,离开这里。
或者如果你想要通过这一概念的实际应用,我将结束。
4所示。应用范围:克莱森缩合,酯的酸性比CH3哦,大约10 pK一个单位
这个概念的一个应用程序可以找到的克莱森缩合酯类。克莱森缩合涉及deprotonated之外酯(一个“烯醇化物”)到另一个相当于酯通过添加-消去反应(见文章:在克莱森缩合)
第一步是去质子化的酯由一个醇盐离子(在本例中CH3O(-)如上所述。这烯醇化物可以攻击相当于第二个酯,然后消除了一个等价的醇盐离子。
这个反应可能也是可逆的。然而,新产品——“beta-keto的质子酯”——多酸性比开始酯,它(pK之间的酸碱反应一个12)和醇盐(pK一个15)相当有利。
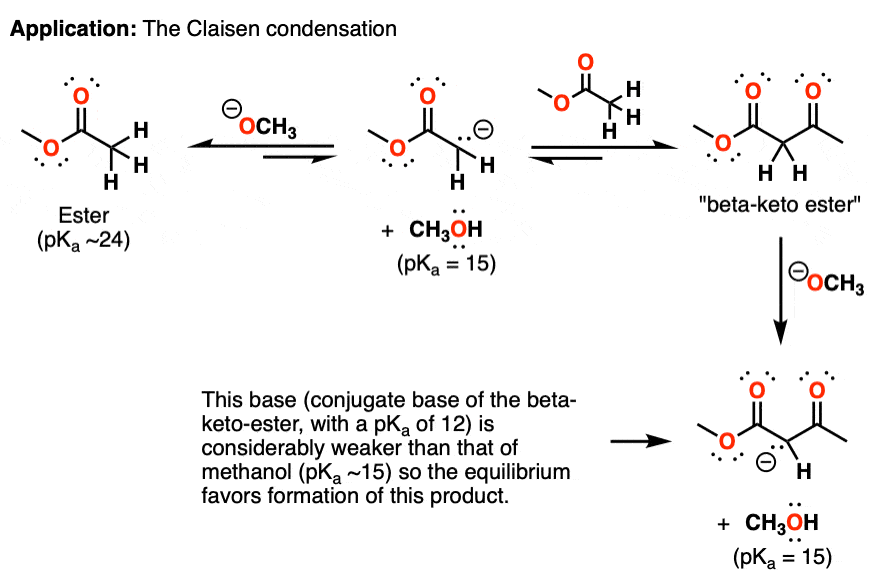
平衡最终倾向于最终产品,因为共轭碱的beta-keto酯(pK一个12)是大大低于甲醇(pK一个~ 15)。
换句话说,即使第一步是非常不好的,这是弥补的事实有一个很好的“驱动力”的后续反应。
在第二点说,水是弱酸性和CH3O——是较弱的反应我认为这是不正确的,因为它可以观察到水的pka(14)小于pka甲醇(15.2)所以,酸水是绝对强于甲醇。因为这个我不能够正确理解什么是第二点你能解释。
这是固定的。谢谢你带我的注意!
在水和甲醇反应,甲醇(pka - 15.2)不是一个弱酸性比水(pka-14) ?不平衡有利于甲醇? ?
这是一个错误。固定的。谢谢!
这些帖子都是有用的,谢谢你。在图形显示克莱森缩合反应,不是最终产品CH3OH,而不是CH3O ?别的,H上哪去了?也许我错过了一些. .
谢谢
纠正这个错误。谢谢你让我知道!
-哦和甲醇的反应将有利于左边不亦然。甲醇是一种弱酸性比水,因此MeO——是一个更强的基础。平衡将有利于甲醇和不水。
修正这个错误。谢谢你!
BJ
我通常发现没有任何问题,在这个网站上的帖子(它的美丽了有机化学物质)。
但是我认为我找到一些违规行为的信息。
我认为这可能是一个策略,让我们真正认真思考数字和辨别自己是否提供的信息是正确的。
不规则的这篇文章让我烦恼,是可逆氢氧化反应和甲醇之间创建h2o和methyloxide离子。
如果我们使用的pka值14 15.2对水和甲醇的反应应该继续从右到左,从弱酸性较强的酸。
因此,15.8:1的比例,如果这是正确的比例,应该methyloxide氢氧化,而不是它已经这样写。
同时,注意:感兴趣
我的有机化学教科书说水的酸度系数是15.7;这篇文章说14。另一个不规则。
很自然地,我谷歌了一下,共识似乎是15.7是错误的,和14是正确的。
所以,我的课本是不可靠的。太棒了。
我固定的错误对酸碱反应的好感度。谢谢。
做更多的研究之后,我认为我更好地理解你的文章,但我仍然有问题。请纠正我什么我写下面是不正确的。
1)所有的反应都是可逆的,这意味着所有的反应都有一个平衡(技术甚至我们说的反应是不可逆的,去完成是可逆的,但我们只把他们当作一种方式(单箭头)因为Ka太大。)
2)。此外,正向和反向反应永远不要停止发生但在某种程度上已不再是一个可观测的反应物和生成物的浓度的变化。当这发生了我们说的反应已达到一种平衡的状态。
3)。起始物料是转化为产品的程度是由热力学(能量)的变化。它有利于一个系统从高能低能量。因此,能量较低的一边是喜欢在平衡。
4)。我们使用Keq描述反应达到平衡,所以
Keq酸(Ka) =(产品)/(反应物)
如果Keq > 1[产品]>[反应物]。因此,因为这是它意味着产品大力支持(这意味着它们能量较低,因此更稳定)。因此,平衡会有一个更大的箭头指向右边小箭头指向左边的反应。
如果Keq < 1[产品]<(反应物)。在这种情况下,因为有更多的反应物这表明他们大力支持,因此更稳定。因此,平衡将有利于反应物在产品。这leads to a bigger arrow pointing towards the reactant and a smaller pointing towards the products.
如果Keq = 1[产品]=(反应物)。也比其他更青睐,所以箭头是平等的长度和指向相反的方向。
现在你的文章信息。
1)。第一部分——我假设当你用你的经验法则暗示任何差异的pKa的酸和共轭酸大于10 pKa单位是一个不可逆反应?我看到您用于实践问题的方法得到10 ^ 22。但是你不能用10 ^ deltapKa(即10 ^ pKa (conjacid) pKa(酸)。)
2)。我继续第二部分-1.2 pKa区别在使用你的方法。所以,到底发生了什么事?pKa的差异被认为是一个绝对的价值?也,你让那些其他数值在本部分15.8比1的比率等吗?
3)。第三部分,根据你的方便的规则,我们可以假定每一个酸/碱rxn大约有10或更少的pKa区别酸和连词酸将永远被视为或视为一个可逆反应?
最后,在第三部分,我得到9 pka差异与最终的反应。为什么我得到一个负值,当我计算出不同但你得到正数?最后,你说的反应是“冷宫约10的9次方,因为我们从一个较弱的基础(醇盐)更强的基础”。这是否意味着反应不好如果我们看看它前进的方向?
我在这一节的分析可能是错的,所以如果我错了,请纠正我。
1)高度的酸/碱反应会有不同的pKa大于10。所以,如果你看到一个不同的pKa酸和共轭酸之间超过你知道反应是非常有利的,要去完成。
2)。任何酸/碱反应与酸和共轭酸的pKa区别大约10或更少的反应被认为处于平衡状态。因为平衡双方的反应是反应的发生,即使反应不是很有利。诀窍就是找出哪一方的平衡比另一个更有利的。
我意识到我可能是错的,请纠正我与任何你认为合适的其他分析使用。
当你说,“不同的酸和碱之间的pKa(实际上,基地的共轭酸),“这是不是意味着我们要比较酸的pKa的左边和右边的共轭酸吗?
这是第一篇文章的酸/碱信息我发现是令人困惑的。我猜我盲/无知,但我似乎无法获得所有的基本要点这里正在说什么。第一部分讨论不可逆反应。我可以看到有一个10 ^ 22 pKa的之间的大小差异。(In the Acid/Base questions you use a technique of Keq=Ka(reactant)/Ka(product)=10^-pKa/10^-pKa. Where does this idea come from and can you use it with any acid/ base problem?)
的大大小10 ^ 22暗示反应是非常有利的,它必须去完成吗?
第二部分我完全迷路了。为什么这是一个可逆反应?为什么它甚至继续当我们从弱酸性/基础较强的酸/强基地吗?我想反应只有收益当你有更强的酸弱/强基础较弱的酸/碱吗?还是这个想法只与有利的反应是如何呢?我们怎么知道平衡存在吗?(I assume its based on the handy rule of thumb below?)And why is weaker acid/ base favored at equilibrium?
注:您所使用的技术上的酸/碱问题似乎没有工作,我越来越10 ^ -1.2的负数。
你说,“如果pKa的差异之间的酸和碱(实际上,基地的共轭酸)是大约10 pKa单位或更少,它是有用的考虑他们的酸碱反应处于平衡状态。“所以,我认为任何大于10 pKa的差异将是一个不可逆的反应,对吗?这也意味着,任何酸/连词酸不同,不到10 pka总是继续处于平衡状态?
任何帮助将不胜感激。短简洁底线版本的这个页面也会帮助。
甲醇比水更强的酸吗?
在许多书pKa的水被列为15.7。然而似乎有一些错误在这个数字是如何到达的。我有纠正这篇文章的早期版本中,有价值,取而代之的是一个14的价值,所以,甲醇并不比水更酸。
我不明白你的意思。在之前的帖子你说,如果你做一个酸碱反应和产品碱/酸比反应物反应不会发生。甲醇的酸度系数15.2,水14,所以比甲醇水(产品)是更强的酸。因此甲醇(产品)比哦,强大的基础。为什么比反应发生的?
固定的。谢谢你!
如果一个酸和碱的物种pka区别是明显大于10。我知道的反应将是不可逆转的,但实际吗?(说例如,Na + Cl -和CH4)
通常不适合pKa差异> 10。
绝对不是实际生理盐水和甲烷。我们说的55个数量级,至少。如果你等待宇宙从一开始直到今天,你可能会看到没有看到它发生。
氢氧化钠不是H2O的共轭碱。氢氧化钠不是布仑斯惕物种。
HO - H2O的共轭碱。
在实践中我们标签氢氧化钠强碱。事实上它是一种强电解质和含有强碱HO -。严格,HO -不是一个强碱,在弱和强基地之间的边界。
氢氧化钠不是H2O的共轭碱。氢氧化钠不是布仑斯惕物种。
HO - H2O的共轭碱。
在实践中我们标签氢氧化钠强碱。事实上它是一种强电解质和含有强碱HO -。严格,HO -不是一个强碱,在弱和强基地之间的边界。
我们继续沿着pKa表,然后。终端炔烃吗?弱酸。乙炔化物离子是强大的基地。仲胺?布仑斯惕基础薄弱。其共轭基地是强大的基础。烷烃极其弱酸,烷基离子非常弱的基地。我不能看到的共轭碱弱酸弱碱”成立。
我有一些困惑关于pKa的甲醇和甲醇水…我预计比氢氧离子离子更不稳定。
但是一些谷歌搜索建议pKa值不是常数在溶剂…
在水、甲醇比水的酸性弱但在DMSO,反之亦然!
绝对让人困惑。
亲爱的詹姆斯,谢谢发帖,但我还有些混乱。如果强酸和强碱弱酸和弱碱反应得到,你怎么知道哪个方向平衡谎言吗?
在你的第一个例子,盐酸(强酸)形成水(弱酸性)。我不能简单地说你有水(强基地)和盐酸(较弱的基础)。这将意味着盐酸形成被看好。很明显,这是不正确的,所以我做错了吗?有任何使用pKa或pKb的一般规则,帮助预测呢?感谢任何见解。
嗨,所不同的是,在相反的方向上,“酸”的身份“基地”,“共轭酸”和“共轭碱”开关。
酸:债券的物种H断裂
基础:债券H形式的物种
共轭酸:成为基础一旦增加了债券的H
的共轭碱:变得酸一旦失去了H的债券
如果你要画水之间的反应和生理盐水给盐酸和氢氧化钠:
酸:水
基地:Cl -
共轭酸:盐酸
共轭碱:氢氧化钠
共轭酸(盐酸、pKa 8)显然比酸(水、pKa 15)。因此这个反应将不会继续。
很容易做出判断与pka的电话因为这些测量是现成的。通常我们不处理pKb的。
谢谢你的回应。如果我理解正确的话,HCl的pKa较低所以它强酸意义Cl -必须是一个软弱的共轭碱。水具有较高的pKa所以它弱酸意义哦,必须是一个强壮的共轭碱。在你的例子中,强酸和强碱都在反应物的方程而弱酸和弱碱在产品方面。平衡和热力学反应说谎言弱侧?
你给我困惑hydroxide-methanol反应。由于甲醇是一种弱酸性水,不应该比氢氧化甲氧基是一个强大的基础吗?我似乎记得,醇盐比氢氧化物强壮基地从有机化学课。如果你能请解释这一点,那就太好了。
谢谢,
约旦
别介意,我误读了pka,抱歉的混乱。
谢谢你的这篇文章很有用的。
然而我发现缺少的一件事是发生什么,例如,如果你做了一个2:1(不等于)甲氧基/甲醇水溶液吗?比你会得到什么呢?
谢谢你!
我不认为你会是一个集中的解决方案。如果你物质的量浓度的计算,形成的“解决方案”说,从1 L甲醇(791克,或24摩尔)你必须添加你需要添加48摩尔NaOMe(2.6公斤)。我不认为这是可以做到的。
这回答了你的问题吗?