消除反应
消除反应的热量
最后更新:2022年12月2日|
消除反应的热量
- 消除反应往往与替代竞争反应
- 一般来说,增加热倾向于增加的比例消除产品相对于替换产品
- 原因是消除导致大量物种的解决方案,从而增加熵,(ΔS)和增加温度使
-TΔS项方程,吉布斯自由能增大。
表的内容
- 在其他条件保持不变的情况下,消除反应是受欢迎的置换反应越来越火
- 加热导致逐渐增加的淘汰和替换
- 消除反应导致的物种数量增加解决方案;置换反应不
- 越来越多的物种在解决方案意味着更大的熵,这意味着-TΔS术语在吉布斯方程中增加价值随着温度(T)的增加
- 笔记
- (高级)引用和进一步阅读
1。在其他条件保持不变的情况下,消除反应是受欢迎的置换反应越来越火
我们看到一些回传消除反应往往与替代竞争反应。
我们如何知道当一个反应途径将是优先于另一个?我们会看到,会有几个组件完全回答这个问题,但是今天我们要讨论一个简单的经验法则。
假设你有这样的反应。可以替换或消除产品形成的。[我保持基地和衬底的身份模糊的。
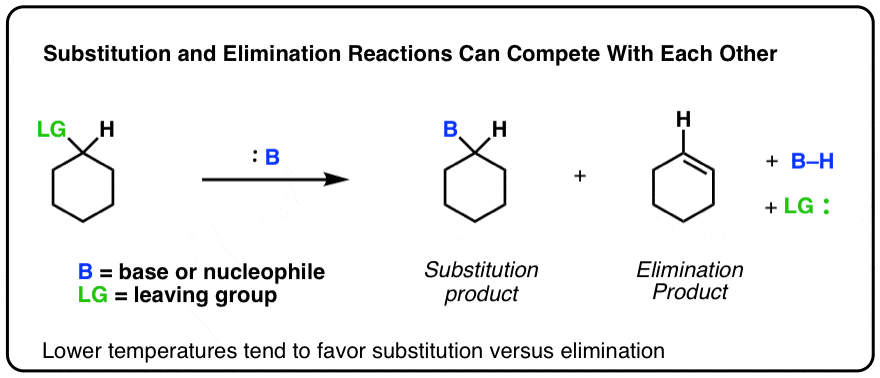
随着温度增加,相对数量的消除产品将增加相对于替代产品。你可以想象它看起来像这样。
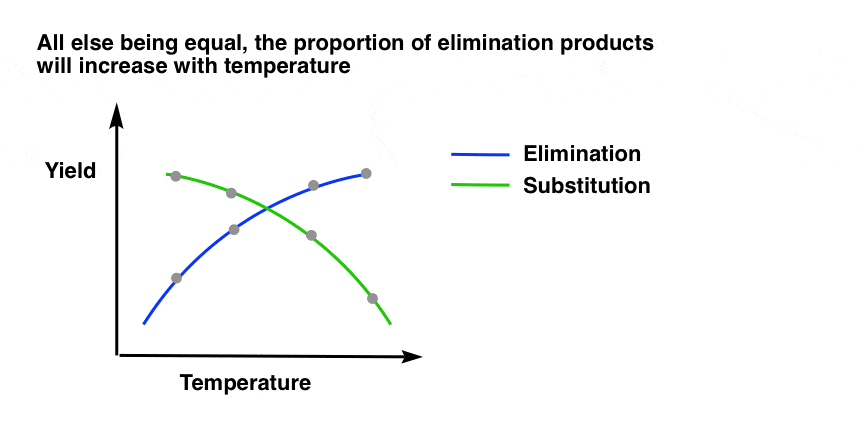
2。加热导致逐渐增加的淘汰和替换
再次注意到有机化学是如何工作的。好像不是加热是一个开/关开关,导致消除置换反应从100%到100%。相反,温度上升导致循序渐进的消除产品相对于增加替换。这是因为温度逐渐消除导致增加的速率常数与替换的速率常数。
这里发生了什么?
这里有一件事我们可以满怀信心地说:低温,取代反应的活化能低于消除反应。记住,活化能越低,反应速率越高。这可能有助于解释我们的产品分布:当我们增加温度,提供更多的能量,所以原料可以提升活化障碍提供了消除反应。这符合观察到的东西。
然而,有一个更根本的原因为什么我们可能会看到更多的消除产品随着热量的增加,这与一些属性我们知道热力学速率常数(活化能)温度的依赖。
3所示。消除反应导致的物种数量增加解决方案;置换反应不
让我们再看一遍(通用)的反应:
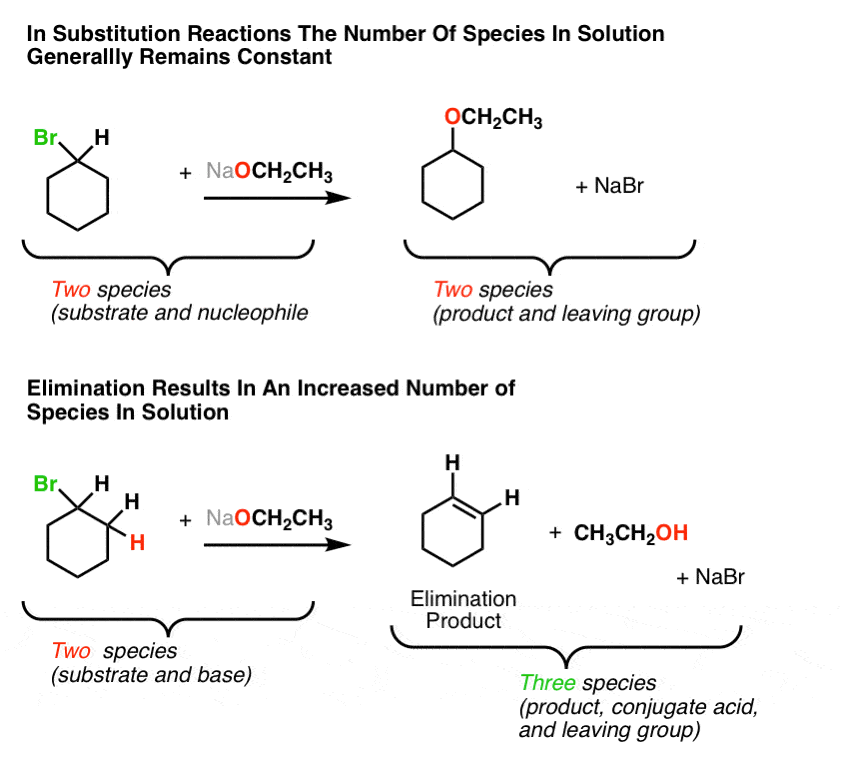
我们注意到什么?注意,取代反应我们从开始的2种材料2种产品。但在消除反应,我们要从2种起始物料中3种产品。增加!
4所示。越来越多的物种在解决方案意味着更大的熵,这意味着-TΔS术语在吉布斯方程中增加价值随着温度(T)的增加
因为我们这里在溶液中诞生一个新物种,这将导致一个熵的增加。如果你认为那样的普通化学,吉布斯方程告诉我们这种关系:
ΔG =ΔH - TΔS
记住-ΔG越多,越有利的反应。随着温度的增加,TΔS项开始变得越来越大;这将使ΔG越来越消极。在某种程度上,随着温度的增加,消除ΔG将成为替代消极比δG。换句话说,更有利。

不过有一件事要谨慎!当我们讨论ΔG,我们真的应该谈论的ΔG过渡态,而不是最终产品。(为什么不呢?因为稳定的产品不相关的反应速率(如果是的话,我们的身体就会燃烧,有限公司2和H2很久以前啊!)。我们给一个特殊的名称过渡态的热力学条件——我们给他们一点double-dagger。这样的:ΔG‡。这种“吉布斯能量激活”如何定义一个反应的活化能。
通过分析这一项,所以你可以看到活化能随温度改变!
在低温下,吉布斯能量激活的替换(ΔG‡)较低的能量比消除(负面)。但在高温下吉布斯能量激活(ΔG‡)为消除开始较低的在能源比置换反应,因此我们得到消除产品的数量的增加。
ΔG‡=ΔH‡-TΔS‡
再一次,底线是,在其他条件保持不变的情况下,热量会倾向于消除反应。
笔记
(高级)引用和进一步阅读
- 消除反应的机制。第七部分。溶剂的影响率和product-proportions uni -和bi-molecular替换和消除反应的卤代烃和锍盐hydroxylic溶剂
k·a·库珀·m·l·达·e·d·休斯,c·k·英格尔德b和l . j . MacNulty伍尔夫
j .化学。Soc。1948年,2043 - 2049
DOI:10.1039 / JR9480002043 - 消除反应的机制。八世。温度影响利率和product-proportions uni -和bi-molecular替换和消除反应的烷基卤化物和hydroxylic锍盐溶剂
k·a·库珀·e·d·休斯,c·k·英格尔德,b . j . MacNulty
j .化学。Soc。1948年,2049 - 2054
DOI:10.1039 / JR9480002049
这是论文的关键。英格尔德表示:“[. .]对于任何给定的同时有两个分子的过程,消除了在每个调查的情况下,一个阿伦尼乌斯的能量激活位于陪同替换高于1 - 2千卡/ g.-mol。消除因此一直较大的温度系数,所以温度的上升增加了烯烃组成的比例。” - 消除反应的机制。烯烃的x动力学部分消除异丙基,sec.-butyl, 2-n-amyl, 3-n-amyl陈词滥调在酸性和碱性酒精媒体
m·l·达·e·d·休斯和c·k·英格尔德
j .化学。Soc。1948年,2058 - 2065
DOI:10.1039 / JR9480002058
好的例子热的影响消除。表我在本文中显示的2 -溴丁烷溶剂分解1 M NaOEt在乙醇为82%的收益率烯烃25°C,但类似溶剂分解烯烃的80°C提供了91.4%的收益率。
晶莹剔透的解释谢谢先生
你好,我不理解单位“千卡/ g-mol”中提到的第二个研究论文,你能解释吗?
感谢你的这些文章,他们如此有用,清晰,和容易理解,我研究了我的期中考试! !
太棒了,谢谢你让我知道塞布丽娜!
举个例子你能2-bromo-3-ethylpentane和治疗用氢氧化钠(在说-78摄氏度)获得多数2-ol产品而不是ene ?
我认为你会发现反应非常慢,温度。如果局限于氢氧化钠作为亲核试剂,一种更好的方式来试图让替换将尝试使用相转移催化(18-crown-6)与氢氧化钠在极性非质子溶剂温度有点低。
我得到了部分消除更由熵的由于产品种类数量的增加,但是如果你说我们应该只考虑过渡态的ΔG不都只有一个“过渡物种”?为什么这个熵推理应用于过渡态?
*两个意义两种反应
* *我想问的是如果我们应该只考虑过渡态的活化能(而不是产品),为什么本文主要涵盖了ΔG的产品吗?
会有权宣称,这同样适用于过渡态?(消除反应的过渡态比竞争SN反应还包括更多的物种)
嗯,我confued。也许是因为文本关注DeltaG反应时,它实际上是关于DeltaG‡吗?我可以看到,有一些基本的差异,就像这一事实而三角洲~ 0 substituation和三角洲> 0消除,三角洲‡* - *的反应。这意味着DeltaG‡会*更多posive * temperatre时,这将减缓两种反应。但这并不是我们所看到的实验。我们怎么能理解呢?
同样,如果我们想要解释观察到的热量赞成取消,我想我们必须证明增量‡少* - *消除比替换。我们可以确信是这样,只是通过比较和两个反应的δ指出更积极消除?我不是entierly信服。也许你可以帮助我吗?
你好!谢谢你发布这样一个伟大的解释性的文章。然而,我有一个调查关于一个语句。你说温度的增加降低了活化能。我认为温度实际上并不降低活化能,而是增加了碰撞频率和能源因素的阿仑尼乌斯方程,在这一过程中,增加了速度。我想唯一实际上降低了活化能是催化剂。
优秀的点。你是正确的,我将解决这个问题。
这个错误被修正了吗?
之前我删除一个图。