二烯烃和MO理论
添加更多的1、2和1、4二烯烃
最后更新:2023年2月14日|
两个二烯反应:二烯烃自由基增加哈佛商业评论,Br2对二烯烃
在前文中我们覆盖1、2和1、4增加双烯,特别添加强酸(如盐酸或哈佛商业评论)二烯烃。
你可能会理所当然地问,“是吗?”。还有其他的例子反应给“1、2”与“1、4”产品?
是的,谢谢你的邀请。今天我们将通过两个:二烯烃自由基增加哈佛商业评论,Br的加法2二烯烃。
哦,我们还将通过三个1,2 -和1、4 -产品实践问题。
表的内容
- 回顾:“1、2”和“4”二烯烃,和“运动控制”和“热力学控制”
- 自由基的哈佛商业评论二烯烃也受动力学和热力学控制bdapp平台
- 在激进的哈佛商业评论丁二烯、1,2 -产品动力产品和1、4 -产品是热力学
- 添加溴2(和其他卤素)二烯烃
- 1、2 - 1、4 -产品除了Br2对丁二烯
- 温度的作用在决定产品的比例1,2 - 1,4 - Br2对丁二烯
- 不同的合理化的原因1、2 -产品是动能:离子配对
- 思考“动力”和“热力学”控制——三个实践问题
- 问题# 1。环戊二烯
- 问题# 2(2,5二甲基hexa-2-4-diene)
- 问题# 3:1号环己二烯
- 结论
- 笔记
- (高级)引用和进一步阅读
1。回顾:“1、2”和“4”二烯烃,和“运动控制”和“热力学控制”
事件回放:在组织1中我们了解到,盐酸和哈佛商业评论正常,孤立烯烃(如1-butene)只给一个产品——Markvonikoff产品(“加法”)和H亲核试剂(例如Br -)在相邻的碳原子,和Br增加了最取代碳。
然而,添加的酸二烯结果在一个共轭碳正离子上,可以进行攻击的亲核试剂在两个可能的位置,从而可能导致两个不同的产品。
两个不同的产品是“加法”产品,在H和Br在相邻的碳原子,和“1,4-addition”产品,碳轴承H和Br相距一个双键。
温度在决定产品销售中发挥着关键作用。在较低的温度下,反应是不可逆的,所得的产品最低过渡态(即形成的产品最快!)是青睐。我们合理化这说,袭击发生在碳最能稳定正电荷(我。e“共振”与最稳定的碳正离子)。在更高的温度,反应变得可逆,最多的青睐产品将取代双键(不像扎伊采夫规则)我们叫这两种情况分别动力学和热力学控制控制。
我们完成了测试,我复制在这里。
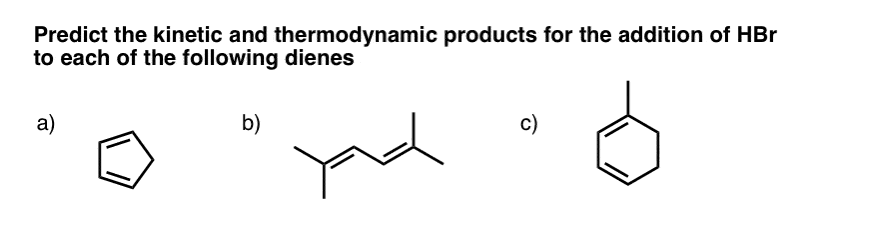
我们将深入研究对这些问题的回答在底部。
但首先,出于完整性的考虑,让我们两个其他二烯烃的反应会导致1、2 - 1、4 -添加产品。
- 哈佛商业评论与二烯烃自由基条件
- 添加溴2(和其他dihalogens如Cl2和我2二烯烃。
很可能你可能永远不会看到这些二烯烃的反应在你的课程。所以你可以认为这是一个额外的话题。
2。自由基的哈佛商业评论二烯烃也受动力学和热力学控制bdapp平台
你可能记得,除了哈佛商业评论二烯烃自由基的条件下比普通遵循不同的反应途径的哈佛商业评论。具体来说,在自由基引发剂的存在加热哈佛商业评论(di过氧化叔丁基、过氧化苯甲酰等,AIBN,或只是“过氧化物”)导致溴激进Br•的形成,这增加了烯烃以这种方式支持最稳定的激进的中间。(看到帖子:自由基加成]
在实践中,这将导致“anti-Markovnikov“除了一个烯烃,Br•增加了至少取代碳双键,和最激进的最终取代碳(因此最稳定)。
当Br•补充道二烯,我们获得共轭自由基上。这种激进的将有两个重要的共振形式,两种产品可能形式,取决于激进的抽象一个氢从H-Br c - 2或c - 4。
下面,我们这样子的Br•丁二烯。(为简便起见,我们跳过写出机制和激进的起始步骤,但它的覆盖帖子上面引用的如果你需要复习)。
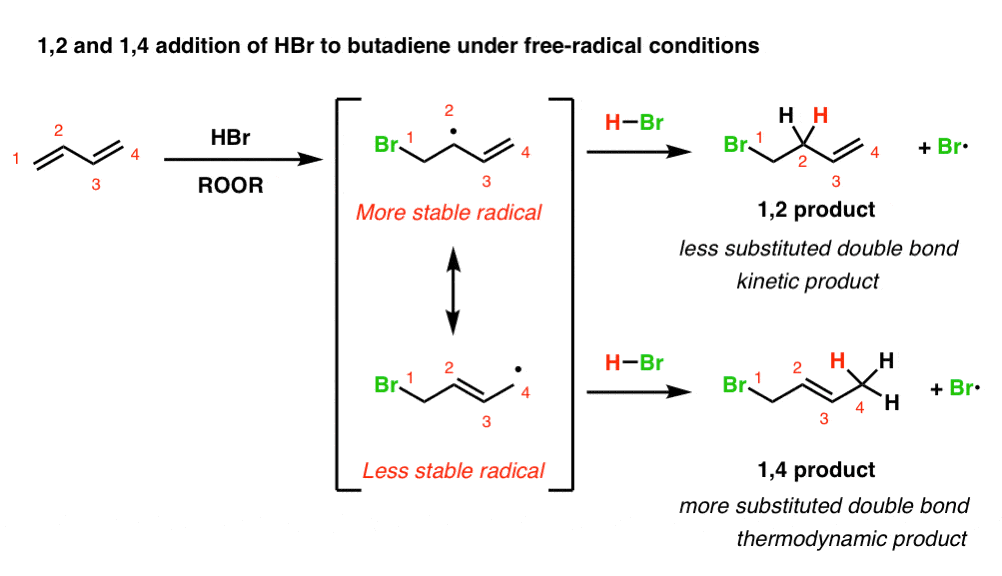
(义务提醒:共振形成不平衡。他们只是做出不同贡献共振杂化)
3所示。在激进的哈佛商业评论丁二烯、1,2 -产品动力产品和1、4 -产品是热力学
注意颈- 1攻击的Br•丁二烯导致一对共振形式就像哈佛商业评论的共振形成我们看到的除了非激进的条件下。像碳正离子,稳定自由基增加附加碳原子数量的增加。
我们应该期望,共振形式(仲碳,激进的c - 2)的主导因素共振混合,和底部共振形式(激进的主要碳,c - 4)是次要因素共振杂化。
[为什么Br•颈- 1攻击(或c - 4,因为丁二烯是对称的)?因为这将产生一个(稳定)烯丙基的自由基。攻击在c - 2或颈不给共轭自由基,因此上不支持)
自1,2 -产品通过一个较长的(即更稳定)形成过渡态,我们可能期望它永远是主要产品。事实上,在较低的温度下,反应是不可逆转的,是这种情况。
然而,您可能还记得扎伊采夫规则的热力学稳定性烯烃增加的碳氢键烯烃是碳碳键的交换。因此,1、4产品(di-substituted烯烃)热力学稳定大于1,2-product (mono-substituted烯烃)。
在更高的温度,反应可逆,我们会因此预计1,产品占据主导地位。
这将出现建立一个这样的情况添加哈佛商业评论二烯烃在非激进的条件下,我们有一个动力(1、2)产品和热力学(1、4)产品,可以控制产品销售和热量。然而在实践中,很难看到“纯”激进之外没有碳正离子的干扰途径,特别是在更高的温度。
4所示。添加溴2(和其他卤素)二烯烃
另一个家庭的亲电试剂,可以执行1、4二烯烃dihalogens如Cl2、溴2,我2。
你可能记得从Org 1dihalogens添加到烯烃生成1,2二卤化物(也称为“本地的”二卤化物)并通过起诉,这个反应所得三人环中间(如“bromonium离子”)。这三人环中间通常是相当稳定的,就是明证,除了一般的立体化学反。(自由碳正离子在场时,我们会得到混合物syn和反,因为碳正离子是平的和可以接受的亲核试剂从两个方向)。
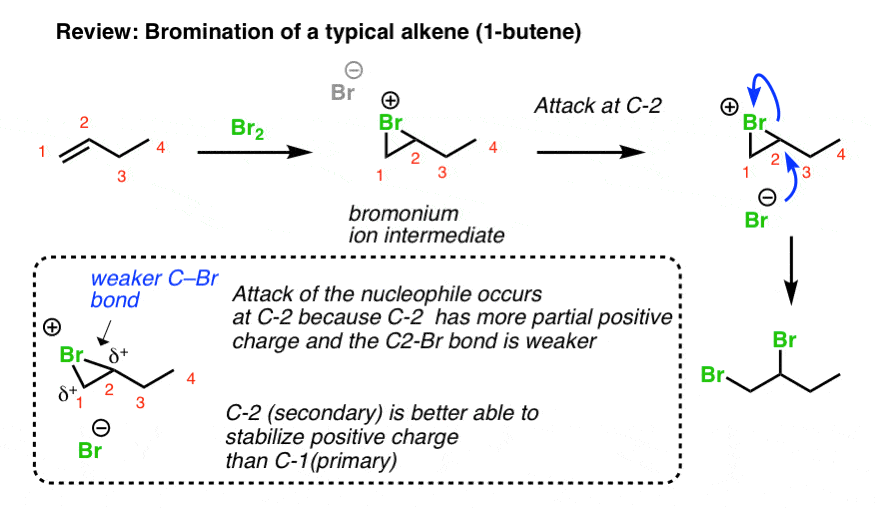
你可以把这个过程的第二步(Br)的攻击是一个混合的年代N1和年代N2反应。的年代N1反应,攻击是青睐的碳最能稳定正电荷(一般来说,最取代碳正离子)。的年代N2反应(与SN1),攻击发生反转的配置。
5。1、2 - 1、4 -产品除了Br2对丁二烯
当一个dihalogen Br等2添加到二烯丁二烯等bromonium离子中间会形成的双键。攻击的亲核试剂可以发生在两个不同位置。攻击c - 2提供了1,2-product。攻击在c - 4提供了产品。
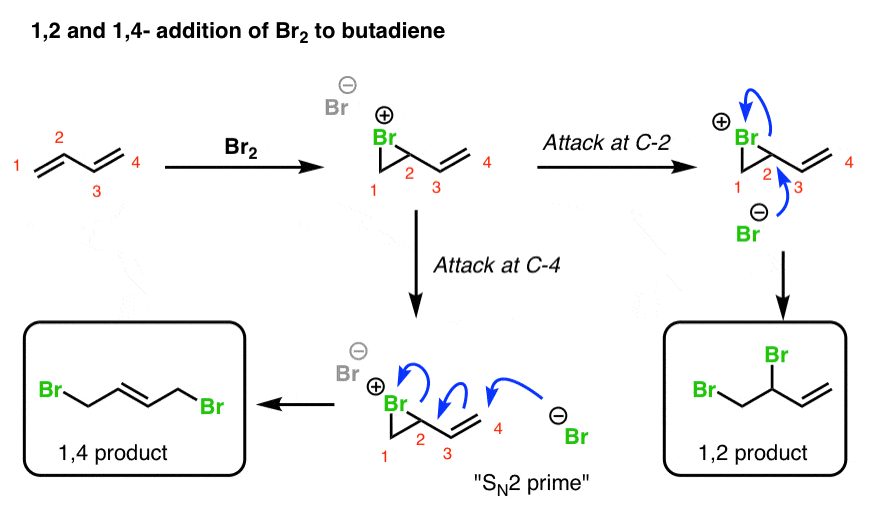
等等!你可能会问。这是如何工作的呢?c - 4甚至没有离去基团! !
真的!然而,在是一个好的离去基团在c - 2 (Br),和有一个颈- c - 4之间的π键。所以你可以想象以下一系列事件发生:
- Br c - 4(-)攻击,形成C-Br,
- …导致破损颈- 3之间的π键和c - 4,形成一个新的c - 2之间的π键和c - 3,
- …这取代离去基团在c - 2
换句话说,它可能是有用的,中间双键亲核试剂“推”Br离去基团在c - 2。
这个过程是让人联想到的年代N2反应,除了一个双键之间的干预亲核试剂和离去基团。因此这种类型的反应通常被称为一个年代N2′反应(“SN2'”)。它不会出现那么多的介绍有机化学课程,但当它出现…它往往是考试!
那么青睐的是哪个产品呢?
6。温度的作用在决定产品的比例1,2 - 1,4 - Br2对丁二烯
让我们看看当温度变化的结果。
- 在低温下,丁二烯的加法是占主导地位的(比例在-15°C)。
- 在更高的温度,1,4 -产品主要(挺60°C)。
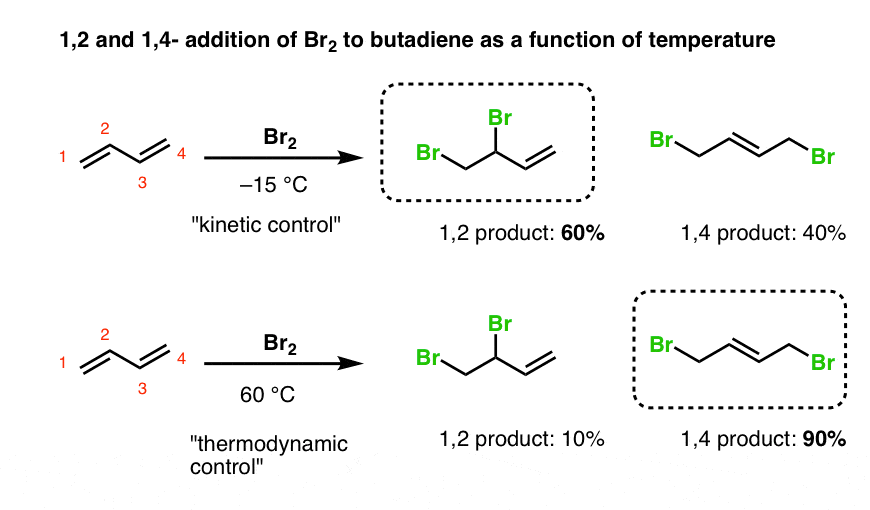
丁二烯,我们又有一个情况“加法”产品是“动力产品”,“1 4产品”是热力学的产品(即有一个更稳定的双键)。
似乎可以理解,产品是热力学的产品,因为它最代替双键。
但似乎有点奇怪,1,2-product动能。毕竟,我们不处理自由碳正离子。
这两个想法。首先,它可以帮助把bromonium离子是在平衡自由碳正离子。碳最能稳定这个正电荷是c - 2,因为它是次要的和共轭系统。
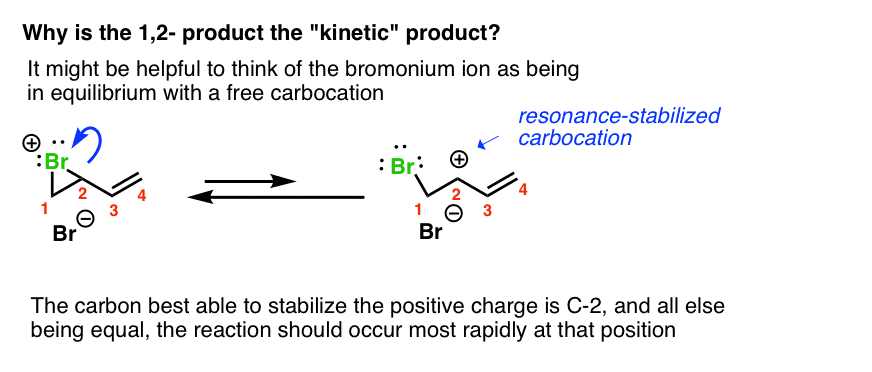
如果你这样看,这导致的路径”1,攻击产生的加法碳最能稳定正电荷”,就像我们见过的。
7所示。不同的合理化的原因1、2 -产品是动能:离子配对
还有一个方式来看待它。“动力产品”也可能是由于这一事实Br(-)形成一个相对紧张离子对与bromonium离子。这里的想法是,在低温下Br(-)紧密bromonium离子通过静电吸引,从而将攻击最接近亲电试剂(c - 2)。
所以这是对吧?1、加法发生得更快,因为碳是最能稳定正电荷,还是快因为离子配对?
在这个例子中,“最稳定的碳正离子”和“紧离子对“合理化发生给你相同的结果。不幸的是,这些合理化可以给不同的结果与一些更复杂的双烯,合理化使用和教科书的冲突。
这给我们带来了我们的实践问题。
8。思考“动力”和“热力学”控制——三个实践问题
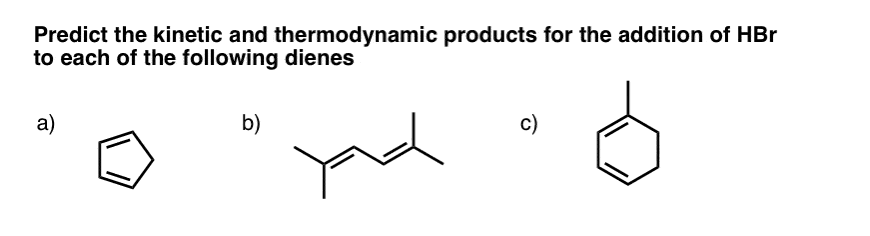
在这篇文章中,在之前,我们已经看到,有两个因素要考虑当评估产品是否“动能”或“热力学”。
- 相对稳定的碳正离子中间体共振形式
- 相对稳定的双键在最后的产品
就是这样。面临的挑战是
- 画中间共轭碳正离子(s)上,
- 画的产品将从攻击的结果亲核试剂在这些共振形式。
让我们通过这三个例子。
9。问题# 1。环戊二烯
第一个例子(环戊二烯)是一个技巧问题,尽管是一个相当简单的。为什么?
看看发生了什么当我们颈- 1使质子化。我们得到两个相同的共振形式。这意味着无论Br(-)攻击,它会导致同样的产品。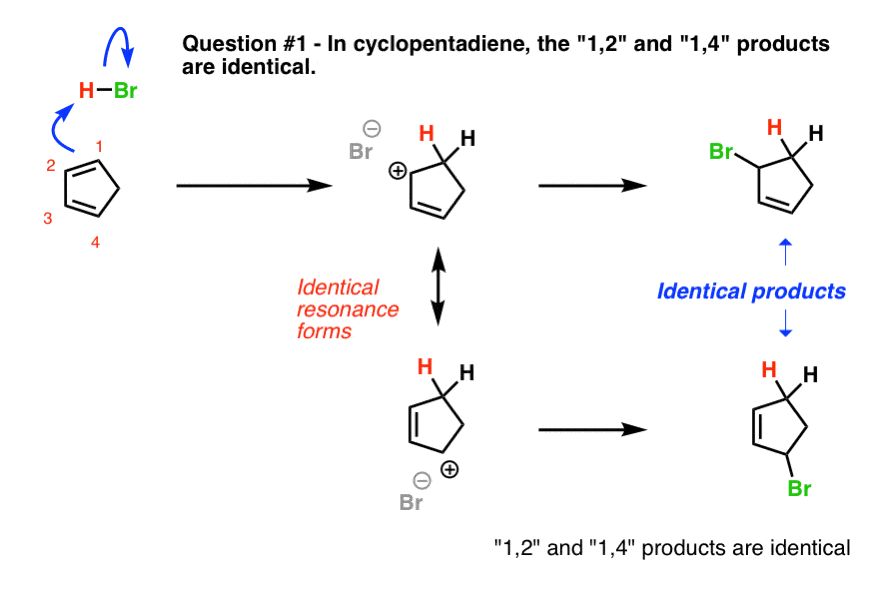
换句话说,1,2 - 1,4 -产品是完全一样的!(注1]
10。例2(2,5二甲基hexa-2-4-diene)
这是一个例子,可以给两个相互矛盾的“正确”的答案为1,根据合理化的加法课本(或老师)喜欢:“碳正离子的稳定性”或“离子配对”。这里是一些建议:如果您正在编写一个考试在这个话题,检查与你的导师和/或教科书关于这个问题,看看哪个回答他们认为是正确的。
(当然,只有一个正确答案:实验告诉我们什么?但是这些信息很难找到具体的例子)。
解释1:“更稳定的碳正离子”合理化
让我们解释这个问题首先使用“更稳定的碳正离子的框架。我喜欢这个,因为它是良好的实践应用在新的情况下熟悉的概念。
颈- 1的质子化作用的5-dimethyl hexa-2, 4-diene共轭系统的结果烯丙基的碳正离子。但看看这些两种共振形式的碳正离子在哪里!
的共振形成碳正离子是比c - 2将重要的共振形成碳正离子在c - 4,因为c - 4是一个更多的取代碳。
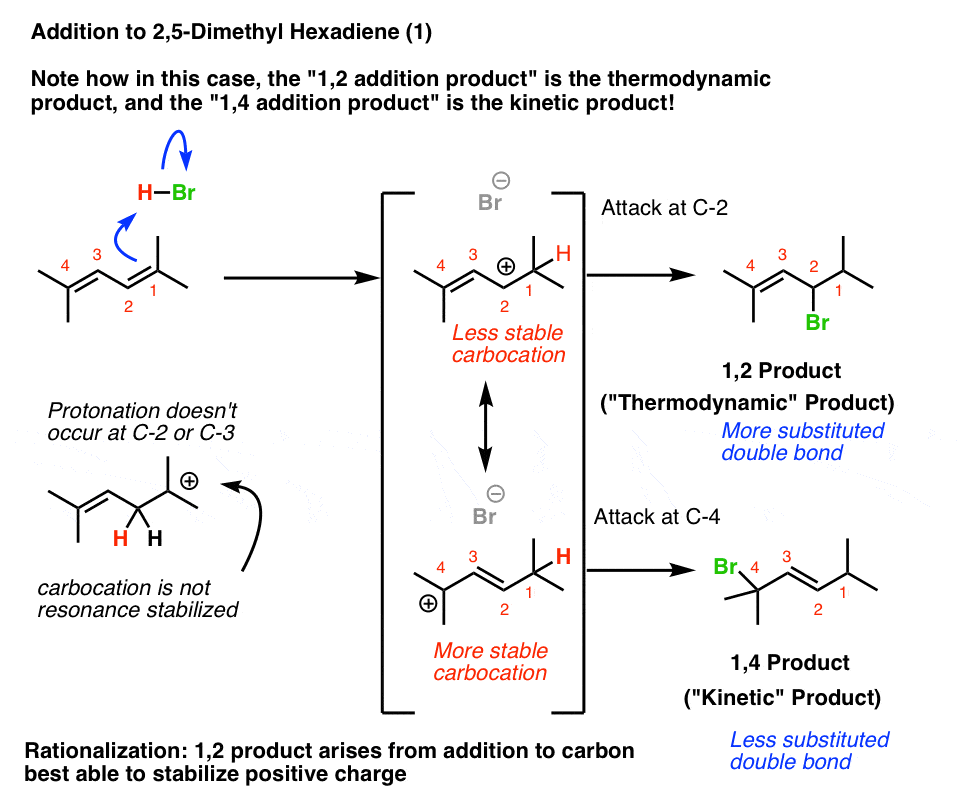
因此,我们期望,产品的动能产品。
此外,当我们观察两种可能烯烃产品,1,2-product代替越多(因此更稳定)双键!
这意味着1,2-product会热力学产品。
这里的底线是,哪个产品是产品的“动力产品”和“热力学产品”取决于结构的二烯。丁二烯和2 5-dimethyl-hexa-2 4-diene给出相反的结果,但所涉及的原则是相同的。
这是一个例子,应用概念而不是记忆支付股息。这也是我为什么发生这样的问题。
解释2:“紧离子对”合理化
Loudon和克莱因教科书(或者其他)有利的合理化,2-product总是结果在低温下由于离子配对。
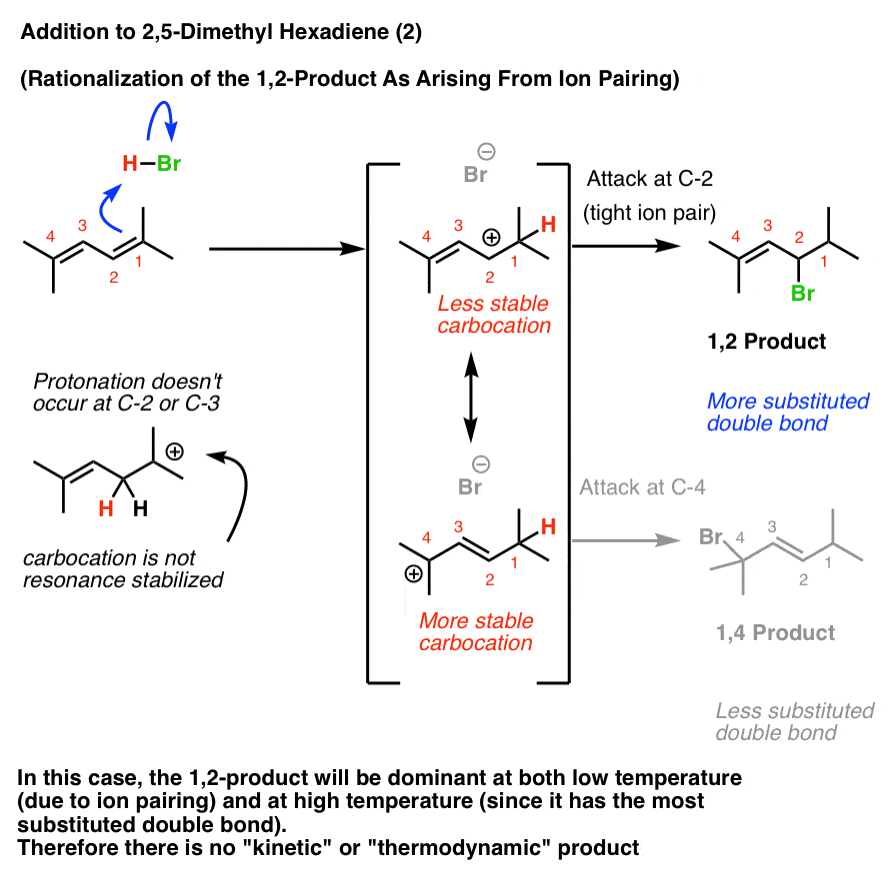
在这种情况下,1,2-product将主导在低温(由于离子配对)和较高的温度(因为它有最稳定的双键)。因此加热反应诱导逆反应不会改变产品的分布。
(实验告诉我们什么?我找不到添加盐酸或哈佛商业评论2,5-dimethyl hexa-2, 4-diene,但是与氯氯化2给出了1,2-product,支持离子对合理化在这种情况下)。
11。示例# 3:1号环己二烯
让我们看看第三(在我看来,棘手的)例子:1号环己二烯。
得到正确的答案的关键取决于选择最稳定的共轭碳正离子上可以通过质子化作用形成的。
这是一个问题,因为1-methylcyclohexadiene不是对称的!
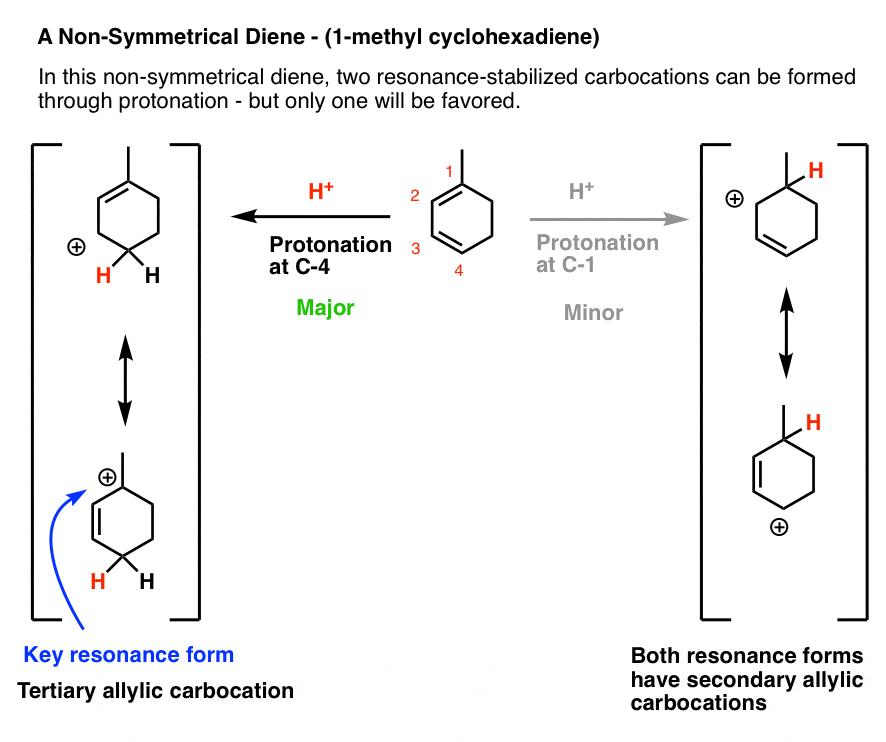
质子化作用在颈- 1导致共轭碳正离子上有两个共振形式,每一种都有二次碳正离子。这似乎是相对稳定的,对吧?
然而,质子化作用在c - 4导致共振共轭碳正离子与上两种形式,其中一个熊二次碳正离子,其中一个熊一个叔碳正离子!这将是更稳定,因此共振混合做出更大贡献。
这意味着质子化作用在c - 4是最好的答案。
如果我们继续从这两个共振形式,我们到达情况和2,5-dimethyl hexa-2, 4-diene(上图)。
如果你使用“碳可以最佳稳定正电荷”合理化,然后一个期望1,4添加产品低温将主宰(因为它将来自攻击第三颈- 1)和1,加法将主导产品在高温下(因为它有最稳定的双键)。
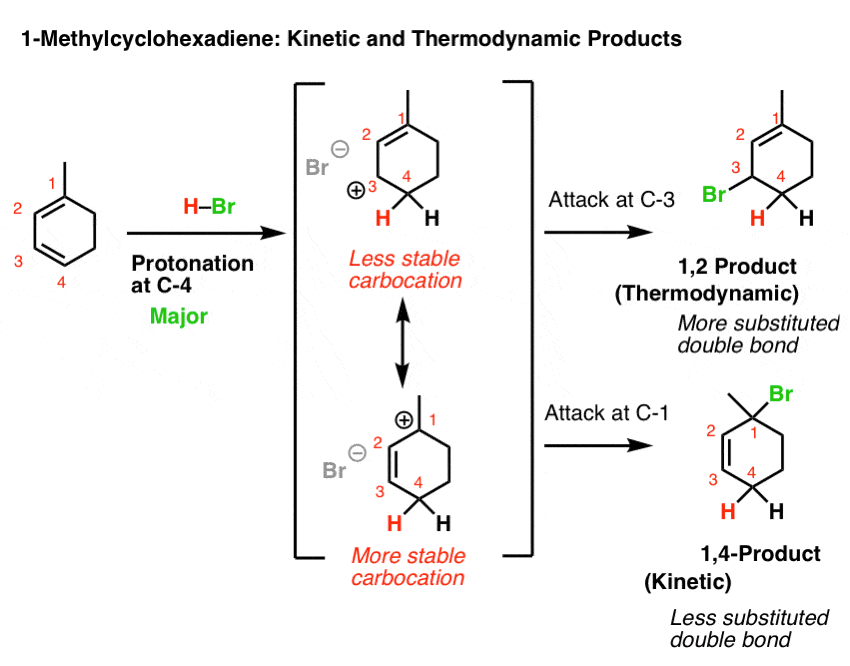
当然,如果“离子对”合理化青睐,1,2-product主导在低和高的温度,因为它有一个tri-substituted双键和1、4 -产品di-substituted双键。
又一次,查看课本/教练,他们使用的合理化。
12。结论
总之,这可能是比大多数人想知道或关心1,2 -和1、4 -二烯烃。但如果你想做好准备考试,很多人读这做!——理解背后的原则是值得这些反应在更深的层次上工作。
在下一篇文章中,我们将离极地过渡,逐步增加对一些相对二烯烃非极性,协调一致的增加二烯烃。这将使我们讨论什么是迄今为止发现最强大和灵活的反应。
感谢汤姆Struble和马特·皮尔斯这篇文章有用的贡献。
笔记
注1。这个例子的灵感来源于一个考试的问题我曾经看到从一个教练/我选择大学更不用说,这给“1 4”除了热力学产品和“加法”为动力的产品。不是在开玩笑。
(高级)引用和进一步阅读
- -Mobile-anion互变现象。第一部分的激活条件的初步研究3个碳系统,并讨论结果与除了共轭系统的模式
哈罗德•波顿和克里斯托弗Kelk英格尔德
j .化学。Soc。1928年,904 - 921
DOI:10.1039 / JR9280000904
的第一篇论文,讨论后来被称为“热力学与动力学控制”。论述了Br2丁二烯和各种取代丁二烯,1、2或1、4可以取决于替换。 - 除了共轭不饱和系统的模式。第九部分。的讨论机制和平衡,3个碳上有一张纸条prototropy
p . b . d . de la母马,e·d·休斯和c·k·英格尔德
j .化学。Soc。1948年,17-27
DOI:10.1039 / JR9480000017
这是后续论文Ref # 1,作者讨论,1,加法是卤素的动力产品丁二烯、1,产品是热力学产品,和动力产品可以重新排列的热力学产品。 - 添加氢氯丁二烯
j . m . s . KHARASCH KRITCHEVSKY, f·r·梅奥
《有机化学》杂志上1937年,02(5),489 - 496
DOI:10.1021 / jo01228a010
早期论文芝加哥大学化学家m . s . Kharasch添加盐酸丁二烯,看到的比率是否1,2,4加成反应条件不同而不同。 - 三丁基溴的机理除了1日
路易斯·f·舱口,皮特·d·加德纳和罗纳德·e·吉尔伯特
美国化学学会杂志》上1959年,81年(22),5943 - 5946
DOI:10.1021 / ja01531a025
这是一个重新调查添加溴丁二烯,假设一个中间bromonium离子的机制。 - 共轭系统的研究。诉丁二烯的准备和氯化
欧文大肠Muskat和赫伯特·e·贝蒂
美国化学学会杂志》上1930年,52(10)4043 - 4055
DOI:10.1021 / ja01373a042
早期论文讨论不仅丁二烯的氯化,而且它的合成。区域选择性解释使用“电子公式”,与亲电、亲核碳用“+”和“-”。 - 氯化环戊二烯
维克多·l·Heasley保罗·d·戴维斯·d·迈克尔炉火,克里d . Rold和基因大肠Heasley
《有机化学》杂志上1974年,39(5),736 - 737
DOI:10.1021 / jo00919a044
氯化环戊二烯为主要的独联体1,产品的加法。 - 异戊二烯氯化
e·g·e·霍金斯和m . d . Philpot
j .化学。Soc。1962年,3204 - 3212
DOI:10.1039 / JR9620003204
异戊二烯氯化很大程度上给monochlorinated产品(1-chloro-2-methylbutadiene)和1,4-addition产品(1,4-dichloro-2-methylbut-2-ene)。 - 在添加试剂过氧化效应不饱和化合物。十三。丁二烯的溴化氢
m . s . KHARASCH艾莉·t·马戈利斯,弗兰克·r·梅奥
《有机化学》杂志上1936年,01(4),393 - 404
DOI:10.1021 / jo01233a008
另一个早期的论文m . s . Kharasch他研究的哈佛商业评论丁二烯,他试图严格分开的两种模式——亲电与激进。 - Regiochemistry之外的盐酸acid-d反式1,3-pentadiene
j . Eric Nordlander菲利普·o·Owuor和杰罗姆·e·Haky
美国化学学会杂志》上1979年101年(5),1288 - 1289
DOI:10.1021 / ja00499a045
非常聪明的实验,DCl是添加到1,3-pentadiene,结果在一个对称的烯丙基的碳正离子中间体。的氘标签允许之间的比率的确定1,2 - 1,4 -产品;事实证明,1,2 -产品占主导地位。 - 溶解动力学和反应障碍的性质和离子对碳正离子反应中间体
弗拉季斯拉夫•a . Roytman和丹尼尔·a .单例
美国化学学会杂志》上2020年142年(29),12865 - 12877
DOI:10.1021 / jacs.0c06295
1、2 -和1、4 -除了教授是一个很好的概念,但这就是这个最新研究说:
“添加酸1,3-dienes通常被理解为包括离散中间体进行一个普通的后续路径之间的竞争形成了观察到的产品。结合实验、计算和动态轨迹的研究表明这种观点是错误的,而且溶解动力学中起关键作用的机制。”
你提到的经验数据添加2,哈佛商业评论的5-dimethyl-hexa-2, 4-diene未知,然后补充Cl2的事实,除了导致1,2,促进离子对理论。我的问题是不Cl2通常通过一个不同的反应机制,相应的酸(盐酸)?我认为卤素往往会形成一个halonium离子,这显然会促进1,2,将不再是共轭分子,满空的p轨道一个σ键?我不确定包括氯添加的数据是有用的,如果机制并不相同。
这就跟你问声好!好问题。的确,它经过halonium离子,但“1 4”仍然是可能的。这里将会发生什么是Cl(-)会攻击“4”的位置,和双键将占领的“2、3”头寸并发halonium离子给产品的破损Cl与1和4的位置,类似于第5部分中的示例
所以,对于异种溶解的哈佛商业评论2,5-dimethylhexa-1, 4-diene,它看起来像的能力的中间形成一个烯丙基的碳正离子的共振结构否决马氏,这将决定增加质子少代替内部碳二烯。还是我错过了什么吗?这个结果使我感到困惑,特别是在光的事实告诉我们,条件有利于kinetically-driven产品似乎导致anti-Markovnikov 1、2个产品,鉴于表明反应从未经历了烯丙基的共振形成的?或者是碳正离子共振结构形式,但它并不完全开关位置的正电荷允许1,4-addition吗?道歉,如果我不清楚。
结合1的反应速率,3-pentadiene与Br2反应速度比孤立的1,4 -戊二烯。先生你能回答这个问题吗?
反应速率与高π分子轨道的能量二烯。共轭二烯的人类是如何比较的HOMO non-conjugated二烯?
詹姆斯,
谢谢你的很好的解释! ! !您可能想要将其添加到正文——它澄清事情好。
我困惑了,因为在“离子配对”的第一个例子似乎积极bromonium离子可能仅仅作为“灯塔”指导在任何旧Br -发生在浮动的优先攻击碳(C2)直接连接到更遥远的C4 bromonium离子。
但在2,5二甲基hexa-2-4-diene例子“灯塔”效应似乎不太站得住脚的c - 4似乎带有部分正电荷高于c - 2。
感谢清理了!
詹姆斯,
为你的离子配对机制可以澄清一些关于这个词吗?第一个例子,bromonium离子形式,我可以理解为什么配对导致攻击在c - 2。
然而,2,5二甲基hexa-2-4-diene我感到困惑。首先,你被哈佛商业评论上的质子化作用C1。所以离子配对在低温度是否意味着同一Br(现在就失去了氢和Br -)不扩散,它呆在附近攻击c - 2(换句话说,H和Br的反应几乎同时)?
因为如果Br -有时间扩散,那么我认为共振将很快发挥作用,由于C4相对更多的正电荷(C2),应该吸引下一个Br -离子漂浮在(通过“离子配对”)? ? ?所以C4反应离子配对。
谢谢!
嗨,乔治,
“所以在低温离子配对是否意味着同一Br(现在就失去了氢和Br -)不扩散,它呆在附近攻击c - 2(换句话说,H和Br的反应几乎同时)?”
是的,完全正确!澄清一下,这个词“离子配对”通常意味着“紧”离子配对,相反电荷的,一旦形成,通过静电吸引粘在一起。
(最好记住,这些反应并不是发生在真空-他们包围一个shell(通常是惰性)溶剂,因此在低温下这些非常小的分子运动,周围的溶剂形成一种“笼”的每个分子都需要能量来打破。一个比喻是“球坑”,孩子们喜欢在玩。)
当形成Br -它将附近的碳正离子,会有这个碳的静电吸引。在低温下,“离子配对”可能发生如果Br -没有足够的动能离开溶剂笼,它只会“反弹”碳正离子,导致1、2的产品。
Br -可以在更高的温度,扩散,离开共轭阳离子上。然后在要么碳正离子攻击成为可能,障碍除了在“C4”少是因为它更好的稳定正电荷(和将有一个更大的部分正电荷)。
根据这一原理,1、4产品是“动态”的产品。
但是我们不做* *的反应叫Br - C2或C4在这种情况下,“离子配对”,自Br -溶剂壳的爆发。
你好,
我想知道是否在# 3例中质子化作用将发生在C2 CH3以来倾向于捐赠电子从而使C1为碳正离子和C2和C3潜力网站为亲电加成和C4网站。总体而言,我发现你的内容非常翔实和乐于助人的,谢谢!
不。质子化作用在C2和C3将导致非共轭碳正离子上。更高的活化能。
好是因为carbcation形成C2可以进一步稳定的共轭双键附近通过共振与C1在这里C2具有更稳定的碳正离子尽管C1和C2二级碳正离子吗?
完全正确!共轭碳正离子上更稳定。这就是为什么颈- 1 c - 2质子化了的优先
你好,我可以问为什么H优先加入C 1环戊二烯而不是C2形式1、2的产品?- >鉴于C1和C2形式二次碳正离子
好问题!试画出两个碳正离子。你注意到什么?共轭系统其中一个比另一个好吗?
先生你能明确一下1 - 4添加acryaldehyde格氏reagant
它会增加醛。如果你想做1,4,你应该使用一个dialkylcuprate。
哇。让这一切点击。谢谢你这么多!
很高兴听到奥斯汀。谢谢你的评论!
关于你的脚注,一些教科书,像贾尼斯史密斯的有机化学为例,武断,1,2是动能而1,4是热力学,仔细选择只显示的例子当它是正确的。
谢谢你的注意。我讨厌这一点。