消除反应
E1和E2:比较E1和E2反应
最后更新:2022年12月2日|
既然我们已经经历的机制E1和E2反应,让我们花一些时间来看看他们并排和比较。
表的内容
- 比较E1和E2反应的机理
- E1和E2反应有什么共同点呢?
- E1和E2反应有何不同?
- E1和E2:为什么一个消除“扎伊采夫”的产品,和其他消去不?
- E2反应的立体化学的关键需求
- (高级)引用和进一步阅读
1。比较E1和E2反应的机理
每个人是如何工作的:
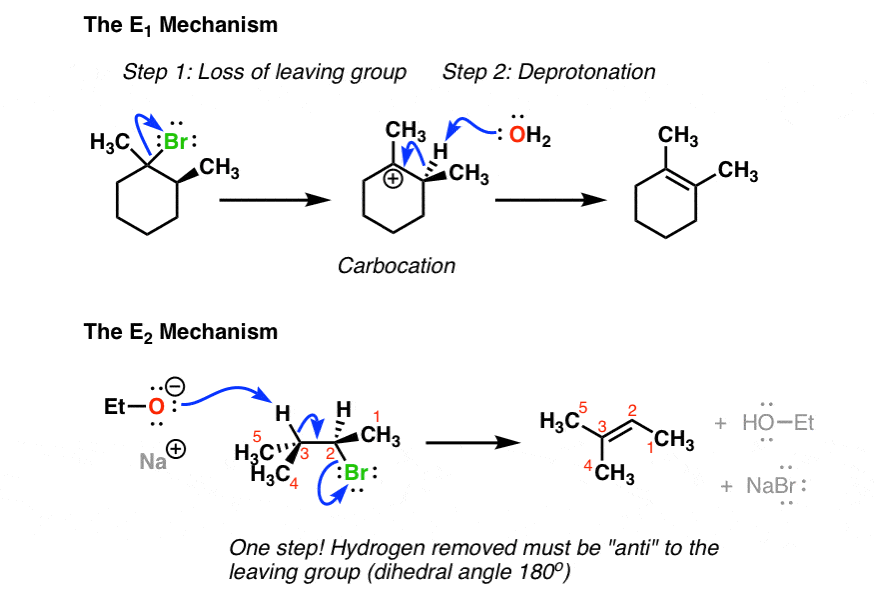
2。E1和E2反应有什么共同点呢?
这就是这两个反应每个人都有共同点:
3所示。E1和E2反应有何不同?
现在,让我们也看看这两种机制是不同的。让我们看看这个有用图表:

的速率E1反应取决于只有在底物是,因为利率限制步骤形成碳正离子。因此,越稳定的碳正离子,反应越快。形成碳正离子是“慢一步”;坚实的基础是不需要形成烯烃,因为没有离去基团这将需要取代(秒)。最后没有要求的立体化学原料;氢可以在任何方向离去基团在起始物料(尽管我们会看到交会做要求碳氢键能旋转,这样它在同一个平面上的空的p轨道碳正离子当新π键形成)。
的速率E2反应取决于衬底和基地,由于速率决定步骤双分子的(共同)。一个强碱通常是必需的,一个允许位移的极性离去基团。的立体化学氢被删除必须反的离去基团;打破碳氢键的一对电子捐赠的反键轨道C - (离去基团)债券,导致其损失离去基团。
4所示。E1和E2:为什么一个消除“扎伊采夫”的产品,和其他消去不?
现在我们能够回答一个难题,当我们第一次看着消除反应。记住这个反应——一个消除了“扎伊采夫”产品,而另一个没有。你可以看到为什么是现在?
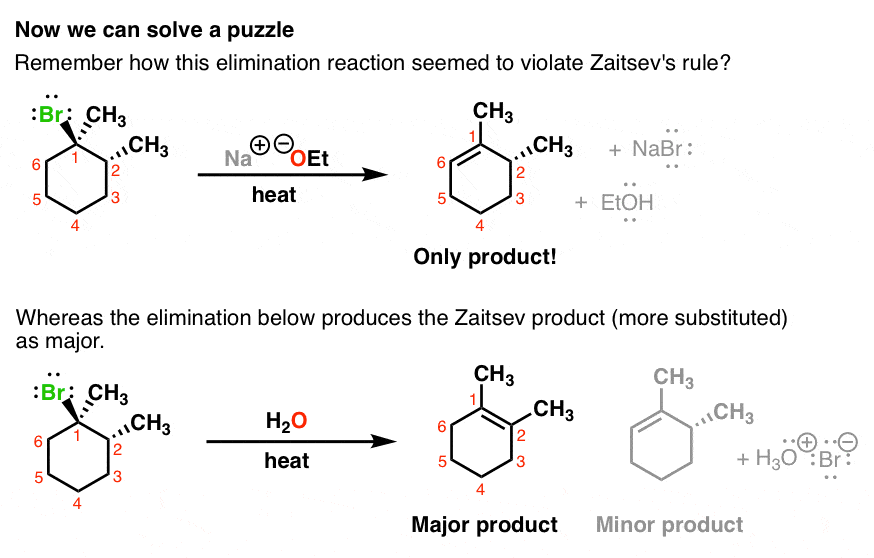
5。E2反应的立体化学的关键需求
这里发生了什么?
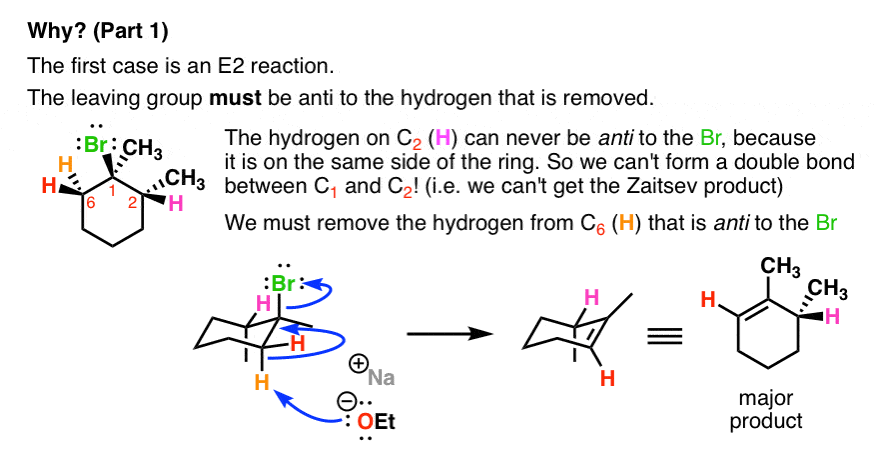
- 第二个病例是一个E1的反应。
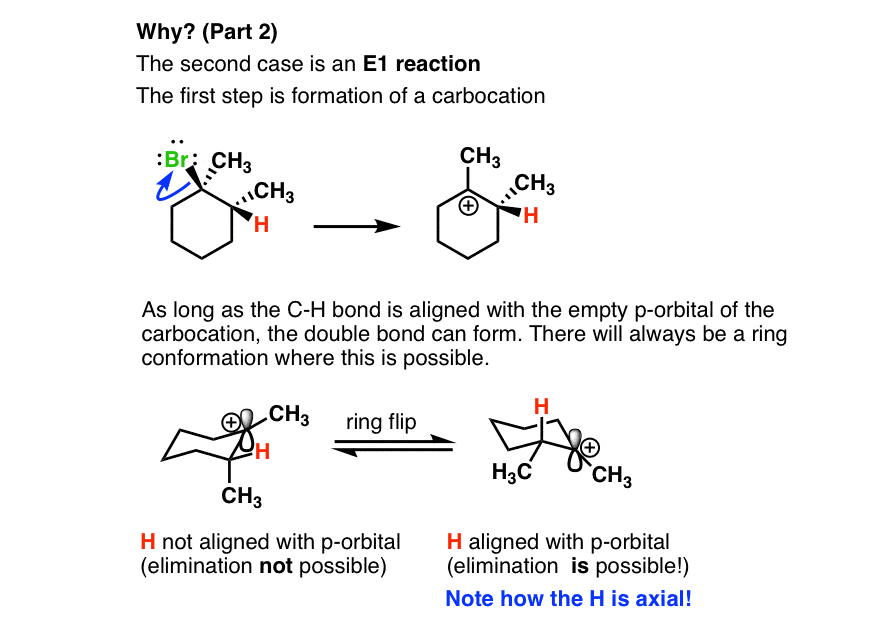
- 在我们这里的环己烷,氢轴向。这是唯一的方法,我们可以这两个碳原子之间形成一个π键;我们需要的p轨道碳正离子与碳氢键的一对电子,我们打破的去质子化的步骤。我们总是可以做一个戒指抛这个H轴向扎伊采夫的产品,所以我们可以形式。
- 去质子化步骤:
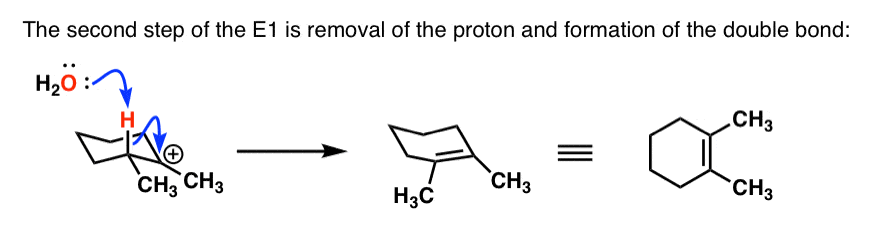
正如您可以看到的,环己烷环能导致一些有趣的并发症和消除反应!在下一篇文章我们将绕道,专门讨论E2在环己烷反应环。
笔记
(高级)引用和进一步阅读
- 消除反应的机制。习的一部分。动力学烯烃叔的消除。丁和叔。戊基溴化物在酸性和碱性酒精媒体
m·l·达·e·d·休斯和c·k·英格尔德
j .化学。Soc。1948年,2065 - 2072
DOI:10.1039 / JR9480002065
的E1综合反应不是很有用烯烃合成,因为消除的比率大大低于在替换产品E2的反应。例如,溶剂分解干燥乙醇收益率只有19%的叔丁基溴化异丁烯,而93%的收益率烯烃获得与乙醇2 m。 - 消除反应的机制。十三。基础的影响,溶剂和结构产品比率在消除反应的一些次要的甲苯磺酸盐
欧文·n·费特和威廉·h·桑德斯
美国化学学会杂志》上1970年,92年(6),1630 - 1634
DOI:1021 / ja00709a035
我在本文中显示表烯烃收益率下E1条件低于下E2条件。E2使用强碱条件可以得到,和基础力量的基地就业增加的顺序n醚<证券交易委员会醚<t醚。反应条件对产品的影响立体化学(反式/独联体烯烃)也在这里调查。 - 消除反应的机制。诉硫同位素效应在某些t-Butyldimethylsulfonium碘的反应
威廉·h·桑德斯和斯图亚特·e·齐默尔曼
美国化学学会杂志》上1964年,86年(18),3789 - 3791
DOI:1021 / ja01072a038
本文特征之间的竞争的一个例子E2和E1,强烈支持E2当强碱。在这两种情况下,反应速率随温度增加而增大。 - 消除反应的机理和动力学
d·休斯和c·k·英格尔德
反式。法拉第Soc。1941年,37,657 - 685
DOI:10.1039 / TF9413700657
回顾早期的调查E1和E2反应,休斯和英格尔德提出了“E1,E2,年代N1,年代N2”——这些现在被称为Hughes-Ingold符号。本文还总结了条件支持E1/E2反应,教本科生每年全世界。 - 取消在循环独联体量反式量同分异构体
w . Huckel博士和Priv。打。m . Hanack博士
Angew。化学。Int。。1967年,6(6),534 - 544
DOI:10.1002 / anie.196705341
非常有趣的对比的研究E1和E2之间的反应独联体和反式同分异构体在循环系统。在哪里E1和E2竞争,报纸上声明:“在订单E2反应可能青睐尽可能强烈的El反应醇盐浓度高和必须烷基集团的醇盐必须尽可能大,高度支化。因此,对于E2反应,偏好的顺序是甲醇乙醇< <异戊酯酒精≈异丙基酒精< < 2-n-butylcyclohexanol t -丁醇。”
你有1页总结pdf E1和E2机制类似于SN rxns吗?
不,不。
的刻板印象是什么反应由叔丁醇钾? ? ? ?和我们如何认识到当我们有saitzef规则当霍夫曼规则申请形成双键? ? ? ?
笨重的基地消除反应://m.deriinvest.com/2012/10/24/bulky-bases-in-elimination-reactions/
啃老代表国家资格入学考试。它是一种标准化考试,每年在印度进行确定资格进入本科课程在医学和牙科。
啃老考试是国家一级考试由中央中等教育委员会(CBSE)来测试学生的能力和智慧。2022后将可能啃老。
有很多方法可以为JEE电源考试做准备。最好的方法之一是研究和一群朋友。考试的关键在JEE电源是确保你有一个好的理解的概念。重要的是,你有一个清晰的知道你要学习和每个主题需要多少的时间和精力。有很多学习准备考JEE电源,但最好的技巧之一是确保你和你的朋友在一个学习小组。
我发现它非常有趣和方便,你新郎初学者。
这是一个最好的有机化学短音符网站提供这样惊人的内容我看过,我准备JEE和这是超级方便!我真的很想感激和谢谢你的分享! !
同位素效应是e 1中观察到的反应?是形成碳正离子的RDS e 1债券乳沟之间对RDS碳氢键没有任何影响,但我们能说,反应中间稳定同位素效应而受到影响?正如我们所知道的碳氢键很容易比c - d。http://bit.ly/2LFQNvn
没有主要同位素效应E1。反应的速率是相同的是否β碳碳氢键或c - d。在kH的E2反应一个典型值/ KD来自2 - 8。
E1的利率有显著差异的身份离去基团是改变。
谢谢,我一直在寻找它,最后我明白了…。
好的。谢谢你!
你好詹姆斯,
我已经阅读你的文章很长一段时间了。他们很容易理解的参考。你有一篇关于E1cb反应的机制?
现在还没有。在列表中,但是!
谢谢你的有用的信息。我有一个问题…E1反应能够使顺式和反式的产品类似于常见的E2反应吗?
比如4-bromo-4-methylheptane根据我的回答书说,形成3个产品,其中2看起来像一个顺式和反式但是他们不指定,与答案的E2反应在我的书中。
和澄清事情E2是唯一真正特定选择的是因为他们没有一个碳正离子中间步骤的氢可以翻到轴向位置吗?
感谢很多添麻烦很容易理解这个反应
这个网站很有帮助。谢谢你的努力让这样可怕的学习指南:)
非常感谢你们所有的人
你让我的生活如此简单! !:)thhaaannnkkks ! !
感谢您使这很容易理解。你是天赐之物! !
我需要考试作弊这像我欺骗了wife-Bruce W
“E2反应的速率取决于衬底和基地,由于速率决定步骤是单分子的(一致)。双分子的,“不应该是在桌子上吗?
哦。谢谢你,一如既往。
反应发生在单步通过高精力充沛的过渡状态通常称为一致,,,,,,单分子refferes分子状态的反应,i.e.no。的分子参与了速率限制步骤