普通化学复习
第一行元素的价电子
最后更新:2022年12月13日|
普通化学点评:第一行元素的价电子
【注:本文的目的是作为一个原子轨道上快速回顾一下学生的有机化学导论课认为普通化学。它绝不是一个完整的原子轨道的介绍。另外:这篇文章由马特·皮尔斯有机化学解决方案。问马特调度在线辅导会议在这里。]
表的内容
- 有史以来最重要的图吗?
- 图形是由电子能级的周期性填补(又名“轨道”)
- 轨道是由3个量子数n,l,米
- 参观前11的电子配置元素
- 1 s shell:电子排布的氢和氦
- 2 s Shell:电子配置锂、铍
- 2 p壳:硼、碳和氮
- 突然下降的氧气
- 氟原子的电子排布
- 最多在霓虹灯
- 3 s轨道:钠
- 尾注:一个谜。关于一个简单的分子像CH4吗?
- 笔记
1。有史以来最重要的图吗?
 报价:
报价:
“如果,在一些灾难,所有的科学知识被摧毁,且只有一个句子传递给下一代的生物,最信息最少的语句将包含什么单词?我相信这是原子假说所有事情都由原子组成——小粒子在永恒的运动,当他们是一个小的距离彼此吸引,但排斥被挤到另一个。一个句子,你会看到,有大量的关于世界的信息,如果一点想象力和思维应用。”
理查德·费曼
当然像我这样一个化学家会爱这句话赞不绝口中央化学科学知识的重要性。你可以相信一个理发师找到一个令人振奋的报价关于发型的重要性。
另外,如果有单图可以免于灾难,下一代的生物,我的投票是这个:
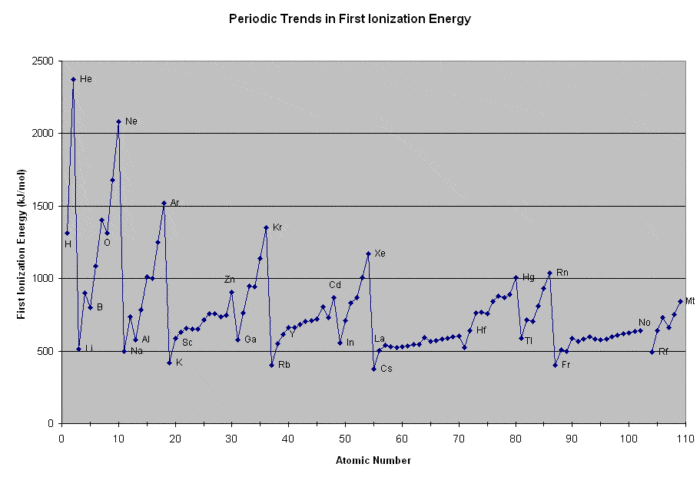
这是怎么回事?
- x轴显示的每一个元素周期表,递增的顺序原子序数。
- y轴显示的是所需的能源量电离每个中性元素+ 1(“第一电离能”)。换句话说:“有多容易完成一个电子每个元素?”。
有大量的原子结构信息嵌入在这个非常简单的情节,但这个概念本身并不是那么难以理解:“多少能量才能宰一个电子中性元素?”
两个重要的注意事项:
- 首先,请注意大趋势:一般来说,元素增加大小,拉出一个电子所需要的能量的原子会降低。我们可以对行星绕着太阳在这里画一个类比:在其他条件保持不变的情况下,越远来自太阳的行星(电子)(核),两者之间的吸引力将会有越少(衡量牛顿定律万有引力在一个案例中,库仑定律在另一个)。事实上,“行星”类比的基础波尔模型的原子。
- 第二,注意周期性规律:有某些元素(Ne,基于“增大化现实”技术,基米-雷克南,Xe)异常高的电离能,紧随其后的是元素(Li Na, K, Rb, Cs)异常低电离能。
2。图形是由电子能级的周期性填补(又名“轨道”)
请注意解释上图中自然流入讨论轨道。
是波尔首次连接(1923)的周期性原子性质可以解释定期填写的电子能级。
在早期的原子模型(1913),这是想到电子原子核周围逐步占领更远的轨道,就像行星越来越大三界围绕太阳。玻尔的“电子能级”的描述确实是现在所谓的“轨道”,比喻结束。波尔没有预料到多么weirdly-behaved电子可以,相对于行星。在1913年也没有其他人。(注1]
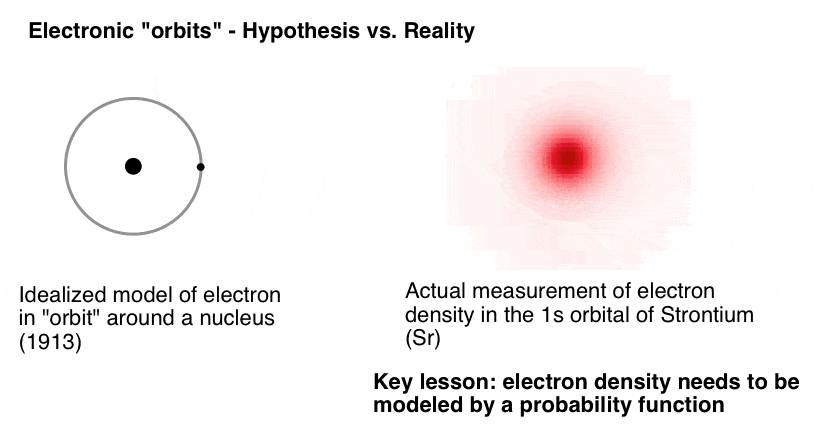
“weirdly-behaved”是什么意思?如果人知道金星的位置和动量,例如,然后一个人可以计算它的位置(如在遥远的未来倍金星凌日预测比赛是UTC时间6月10日,2498)。
海森堡发现在亚原子尺度,有限制与哪一个可以知道精度这两个粒子的位置和动量像一个电子。结果是,我们的知识的确切位置的电子是模糊的;他们必须被描述为概率函数。我们所说的“轨道”实际上是三维形状在一个电子与给定的量子数有95%的机会被发现。(注2]
3所示。轨道是由3个量子数n,l,米
这些轨道有属性定义的三个基本条件在一个特定的薛定谔波动方程的形式:
- 的主量子数n(1、2、3…),有时被称为“电子壳层”,因为它广泛涉及到距离原子核。
- ℓ(称为角量子数,但是知道的名字并不重要)。对于一个给定的值n,ℓ的可能值的范围可以从0到(n1)。所以,当n= 1,ℓ= 0。当n =2,ℓ1或0的值。
ℓ的价值决定了轨道的形状。对于ℓ= 0,轨道的形状是球形,我们称之为一个轨道s轨道。
对于ℓ= 1(这是唯一可能当n = 2或以上)轨道dumbbell-like形状,我们称之为一个p轨道。ℓ观测值就越高=2 (d轨道)和ℓ= 3(f轨道),这本身就是有趣,但在真正的有机化学的方式,我们将跳过。 - 米,这是磁量子数。的价值米取决于ℓ的价值,可以把价值观——ℓ+ℓ,包括零。所以对于ℓ=1 (p轨道),米可以有一个价值1 0 + 1。的物理解释,这是三个方向的p轨道,沿着x, y和z轴。米可以取5 d轨道的值(ℓ吗=2)和七个值f轨道(ℓ= 3)。
除了n,ℓ,和米,还有第四个量子数称为电子自旋,它可以承担价值+½或——½电子。
最后一个要点:
- 不可以有相同的两个电子的量子数(也就是说,他们不能有相同的量子态)阐明在沃尔夫冈·泡利不相容的不相容原理。粒子(电子属于一个家庭费米子拥有一个属性类似于“每个主人一个安全带”)。这是一个原子,而不是一个小丑车!

这意味着电子在原子”建立“能量水平定义良好的模式开始,1年代(可容纳两个电子,相反的旋转),紧随其后2年代(也有两个电子)2p(由于三个可能的值米,可以容纳3×2 = 6电子,然后3 s(2)电子等等。
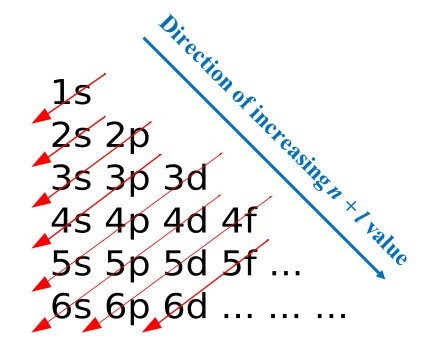
4所示。参观前11的电子配置元素
我们可以继续填满了电子,但这并不是预期的今天,这仅仅是复习前11的每一个元素的原子结构,回顾第一电离能作为指导。
所以我们旅游前11元素的电子配置,好吗?
5。1 s shell:氢和氦
让我们看一下(第一个)电离氢和氦的能量:
氢:1312焦每摩尔
氦:2372焦每摩尔
氢有一个电子在1 s轨道+ 1/2或自旋- 1/2吗(他们是相同的能量,除了一个强大的磁场)。
我们可以代表电子配置在两个方面:
- 的符号11,1指的是外壳号(主量子数n),年代是轨道的形状(其他值吗p,d,f)和上标指的电子轨道
- 另外,与一个框,显示在每个轨道电子的方向(箭头指出的方向旋转)。装轨道,旋转的方向是任意的;我要画“”,在未来所有的例子中,但它不是错误的向下而不是画。
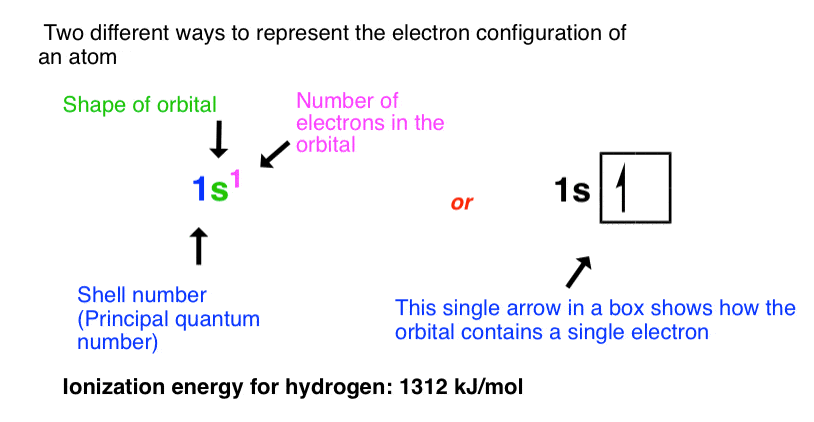
氦在1 s轨道有两个电子,每个都有反对旋转(+ 1/2和1/2),我们下面的代表。
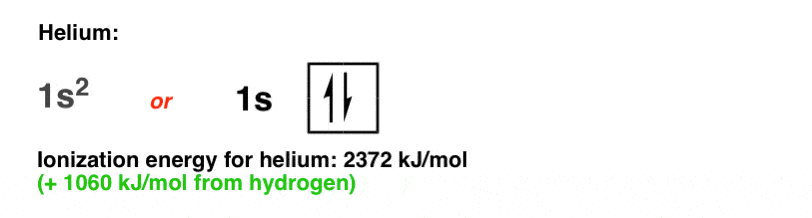
几乎是两倍难移去一个电子从氢氦比(比较:2372焦每摩尔1312焦每摩尔)。
为什么电离能高吗?因为每个电子氦现在的1 s轨道两个质子的原子核拉着它而不是一个,结果在一个更强大的吸引力库仑方程。
注意,它不是完全两倍的;我们可以合理价值较低是由于这两个电子之间的排斥力1 s轨道。
6。2 s Shell:价电子锂、铍
完整的1 s轨道,第三元素(锂)必须有它的电子放在2 s轨道,它不仅是离原子核更远,但也有吸引力的细胞核部分屏蔽的干预对电子在1 s轨道。这屏蔽电子锂只有2 s轨道的“感觉”有效核电荷(3 - 2)= + 1离原子核。
因此,这个电子尤其容易扯掉,要求只有520焦每摩尔(比较为氦2372焦每摩尔!)。金属锂会容易参与化学反应;它与水反应缓慢,例如。氦,另一方面,从未被观察到结合另一个元素。
相比之下,两个电子的1 s壳锂不参与反应。我们可以调用这些惰性电子“内壳层电子,而不是“外壳”,或“价”2 s轨道的电子。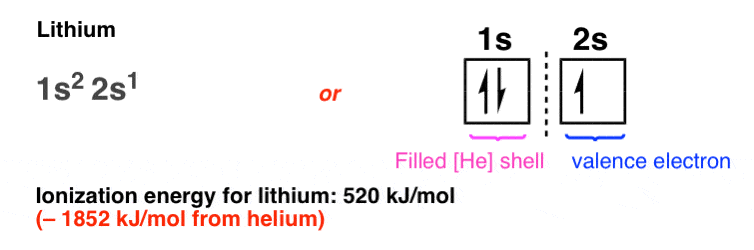 因为所有有趣的化学反应发生在2 s轨道的电子(而不是电子的“惰性”,关闭,1 s shell)一个有用的速记是画的电子配置锂(他)2 s1,这意味着锂的电子排布是氦,加上一个价电子2 s轨道。
因为所有有趣的化学反应发生在2 s轨道的电子(而不是电子的“惰性”,关闭,1 s shell)一个有用的速记是画的电子配置锂(他)2 s1,这意味着锂的电子排布是氦,加上一个价电子2 s轨道。
在第四元素,铍,2 s轨道变得完全占领了一对自旋相反的电子。注意电离能的增加(+ 379焦每摩尔从锂)与电子感到额外的质子的原子核之间的吸引力更大。
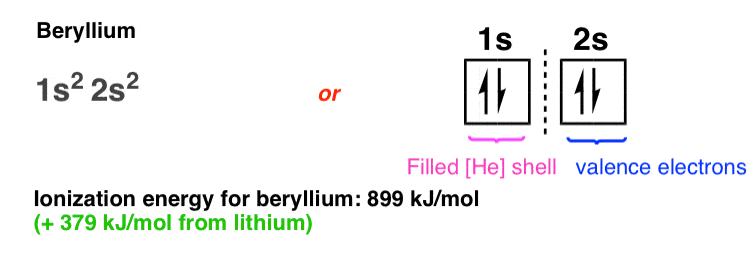
还要注意,虽然铍2 s轨道,在它表现得像一个惰性气体。铍金属容易与氧气反应生成氧化层,例如。与能源之间的差距1和2 s, 2 s轨道之间的差距在能源和最高能级2 p轨道相对较小,这些轨道,填满时,可以在一起举行的“八隅体“价电子。
7所示。2 p壳:价电子的硼、碳和氮
现在的2 s,额外电子现在必须放置在一个更高的能级,2 p轨道。
不同于s轨道,每人只能持有两个电子,每组p轨道可以容纳6。我们的解释是,每一层的p轨道(p 2 p, 3、4 p等)由三个单独的哑铃型p轨道相互对齐成直角沿着x, y和z轴。
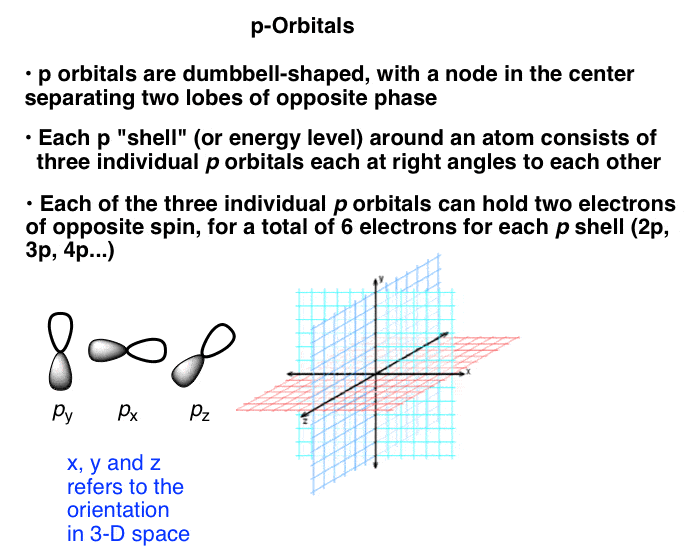
这就是电子配置的样子硼。(注意:我们也可以选择标签3 2 p 2 p轨道x,2 py,2 pz,但是对于我们的目的,所有这些轨道是等价的能量和它没有这样做的目的)。
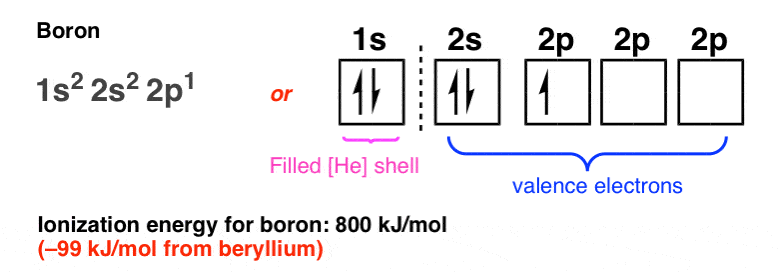
注意硼的电离能是略低(低99焦每摩尔)比铍,从中我们可以解释,2 p轨道稍微远离原子核2 s轨道。(注3]。
硼的电离能大幅进步向上碳…。(+ 286焦每摩尔)
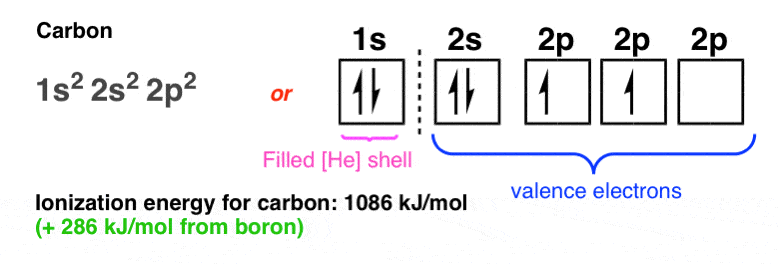
从碳…然后氮(+ 316焦每摩尔):
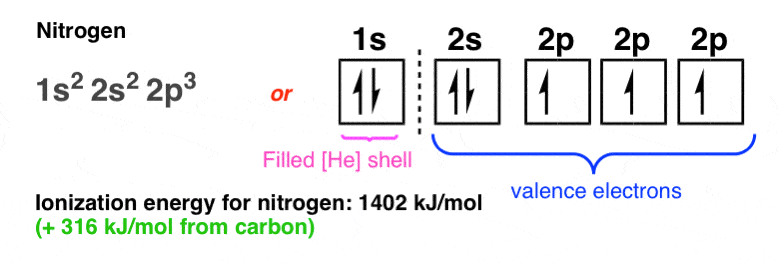
8。突然下降的氧气
然后,在氧气,电离能的突然下降(-89焦每摩尔):
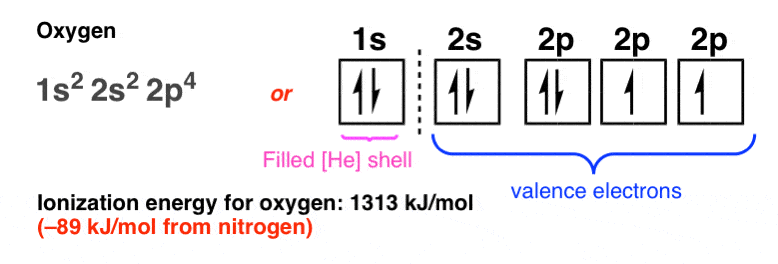
为什么?
上了一辆公共汽车来找出没有剩余的空位,你必须(恐怖)坐在一个完全陌生的人吗?
这就是这里发生了什么:每个2 p轨道(pxpypz)单独占领,任何额外的电子配对。蘸电离能反映更大的双重占据轨道之间的排斥力,使电子(稍微)更容易实现。
9。氟原子的电子排布
从氧氟电离能再次爬(+ 368焦每摩尔氧气):
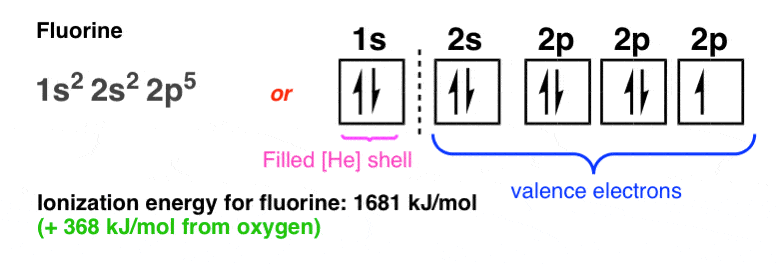
10。最多在霓虹灯
然后在霓虹灯,我们终于到达了另外一个局部最大值的电离能(从氟+ 399焦每摩尔):
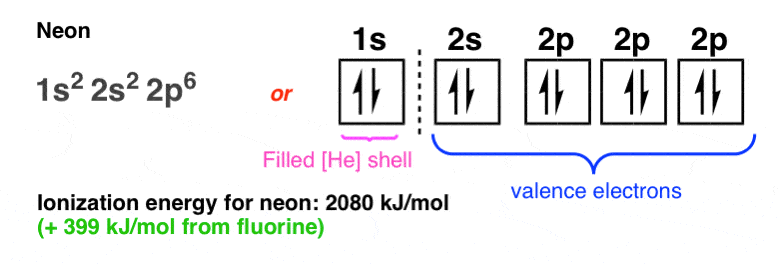
我们已经达到了最大容量的2 s和2 p轨道(代理在一起作为一个“八隅体”),其中每个电子八隅体将“感觉”的最大有效电荷离原子核。在霓虹灯,每个的八个电子价“八角”本身感觉一个+ 8的合力核原子核中的质子(10 - 2的电子干预1 s shell)和一定数量的电子之间的排斥力2 s和2 p轨道。
氖是当地最大的地方库仑吸引项是最大化,电离能。这就是产生了熟悉的“八隅体规则”,原子在哪里说“寻找完整的八位字节”等等。
11。3 s轨道:钠
让我们去一个原子进一步说明了戏剧性的钠和霓虹之间的行为差异。
有很大的差距的能量轨道在n = 2壳(2 s和2 p)和n = 3壳的轨道(3 s和3 p)。
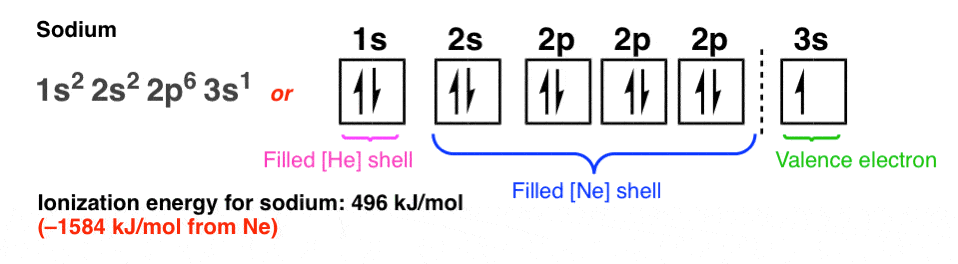
3 s轨道是远离原子核,原子核的吸引力是10个电子屏蔽的低能轨道。我们说的“有效核电荷”电子3 s轨道是钠1。(例如11 - 10 = 1)。
钠的电离能是微薄的496焦每摩尔,1584焦每摩尔不到霓虹灯。放弃其价电子容易,钠与水反应甚至(暴力);相比之下,没有其他元素观察到氖原子结合。
 我们要停止在这一点上,但你可以想象在哪里。(注意4]
我们要停止在这一点上,但你可以想象在哪里。(注意4]
12。尾注:一个谜。关于一个简单的分子像CH4吗?
这是一个问题。如果碳的原子组态[他]2 s22 p2,1 s原子氢的配置1,我们预测的结构最简单的碳氢化合物(CH4看起来像吗?
- 我们不希望看到碳氢键pxpy和pz轴(键角为90°),然后第四个碳氢键2 s轨道的尽可能远离其他电子(135°)?
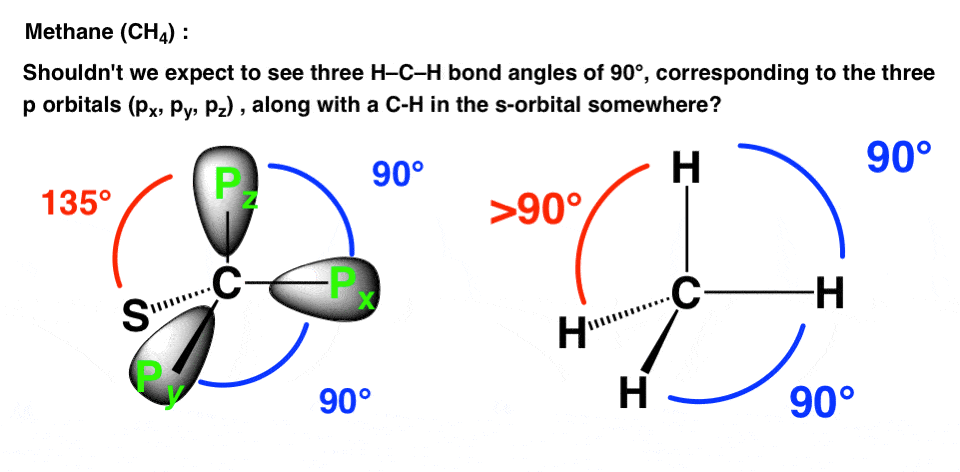
- 我们不会预测不同的碳氢键键长在p轨道(远离原子核)比碳氢键连在s轨道?
- 我们不会指望CH(小)偶极矩4吗?
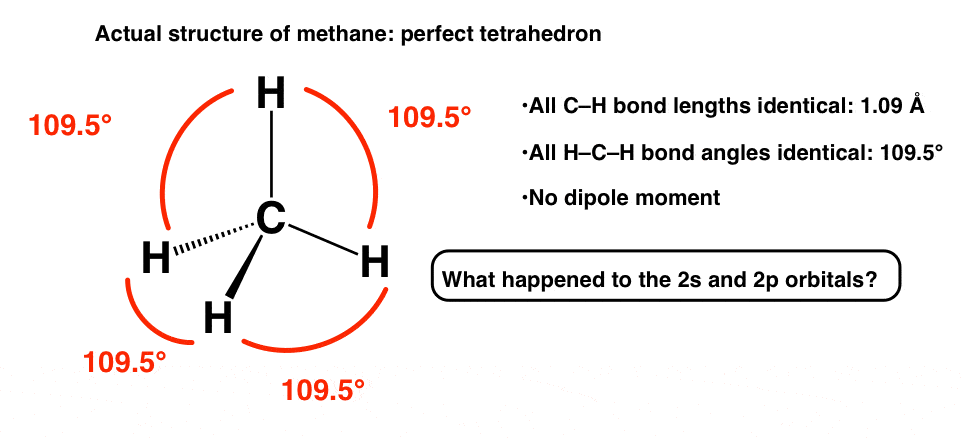
相反,这是对甲烷的观察:
- 所有的碳氢键相同的债券长度(1.09埃)。
- 所有碳氢键角都是相同的。氢是安排在一个完美的四面体,碳与所有H-C-H键角是109.5°。
- 没有偶极矩。
到底发生了什么事?这怎么可能是真的,因为我们现在知道s和p轨道的?我们如何解释这个情况2 s和2 p轨道之间的区别已经完全被湮没了吗?
那么发生了什么?我们将讨论下一篇文章。
在下一篇文章:我们怎么知道甲烷是四面体吗?
再次感谢马特与这篇文章帮助。雇佣马特作为你的导师!
笔记
注11913年:他也没有(或其他任何人)想象的高尚地时髦的形状p,d和f轨道。大自然的奇迹可以超越人类最奇特的想象力。
注2:这也产生了奇怪的现象量子隧道效应,电子有一个非零的机会出现在另一边的一个障碍。就好像金星突然出现在太阳的另一边。
注3:尽管2 s和2 p轨道的电子混合和杂交(我们会看到)2 s轨道的电子是接近原子核,它可以影响某些化学性质。例如炔烃异常强烈的酸度的碳氢键(pK一个= 25)相对于烷烃(pK一个= 50)可以被注意的合理化sp-hybridized轨道更接近原子核(50%提到),因此更稳定,相对于sp的一对电子3杂化轨道的烷基阴离子(提到25%)远。
注4:“他解决了有线吗?”
我有一个问题
“我们正在学习化学和化学反应的基础上传统的原子或假设的模型从的角度但如果我们看到一个原子的量子力学模型,所有这些反应和所有这些我们学习化学将相同或不同元素的变化什么的吗?”
和“为什么只有一些诺贝尔气体复合后形成一个完整的八隅体?为什么有必要形成稀有气体化合物,为什么只有氙和氪形成化合物不是他,Ar,相同和不喜欢他们吗?
氙和氪价电子,足够远离原子核,它们不是在“紧密”通过静电力和可以形成债券与极好的亲电试剂(如氟)。氩、氖原子的价电子太紧举行这些稀有气体化合物的形成(到目前为止)
这种材料给我留下的问题多于答案,我觉得这是一件好事。我有一个想法,是S轨道的潜在虽然是一个球体,可能在精心制作的电子旋转波但总是如上所述范围内被发现。我状态的原因是认为波/分批对偶似乎是给定的,这个兔子吹什么大脑,节点是一个不存在的位置,所有的电子,但永远不会被发现。它好像粒子是闪烁的。显然这是猜测,但我觉得自己必须如此。它产生粒子,表现得像波一样,直到节点靠近,那么短暂消失回到验证哑铃的另一边。我有这些模型,唯一的问题是问的一个问题,我希望我在早期或思考。如何带正电的粒子,即质子,留在一个原子的原子核。我玩磁铁,简而言之,斥力使它看起来像一个错误的模型。我不是一个物理学家,也不是公开的教育,而是必须添斥力,量子引力。 If there is such a thing. Newtons laws keep asserting, but in the realm of quantum, maybe everything is far from the experienced.
在细胞核中关于质子,它们在一起的强相互作用力,运营在极短的距离。
嗨。尼尔斯波尔说,“构建院系人菅直人sætte团体印第安纳州我kvantemekanik uden在blive svimmel,哈尔人ikke forstaet noget af侦破”(如果你能理解量子力学不晕,你不懂)。
至于细胞核,使带正电的质子连接在一起强相互作用力,只有运行时核非常接近对方。(它的强度随着距离的尾巴远离的6次方)。