芳香性
苯的π分子轨道
最后更新:2022年10月16日|
苯的π分子轨道
今天,让我们经历如何画出苯的分子轨道。我们将比较他们的分子轨道(线性)hexatriene。最大的结论是,从对比这两个6-electronπ分子轨道的系统,我们将打开深,神秘的谜为什么苯异常稳定。
快速的破坏者。这是苯的分子轨道是什么样子。
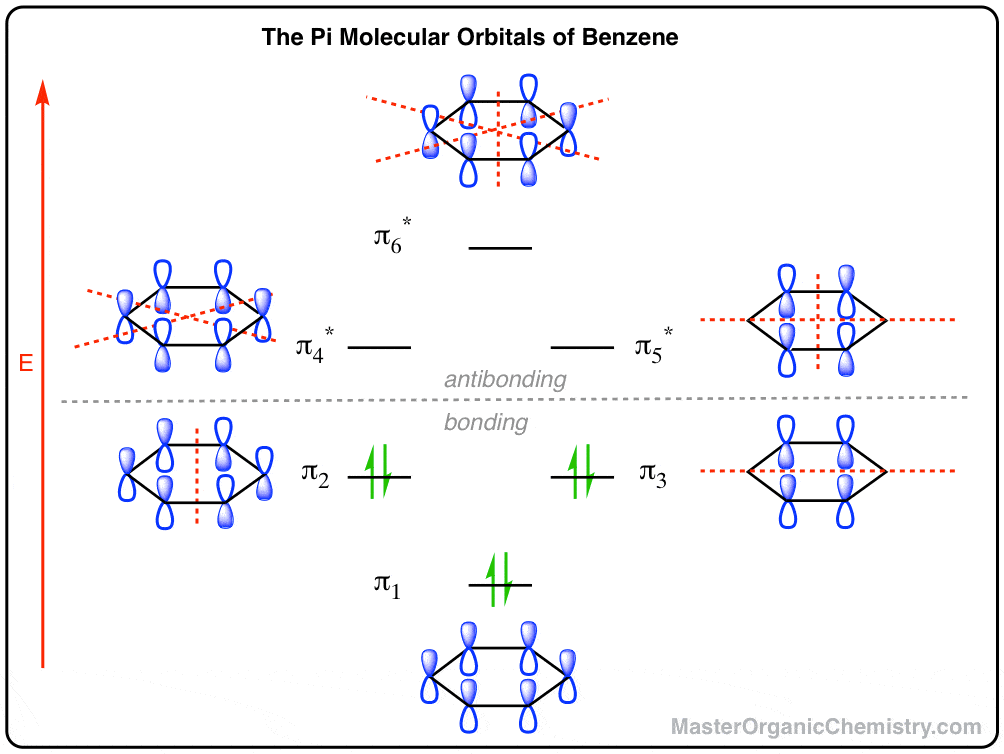
这篇文章的其余部分将描述我们想出了这幅画,这意味着什么。
表的内容
- 简短的点评:如何绘制给定ππ分子轨道系统
- 构建苯的π分子轨道图:Hexatriene和苯分别有6π分子轨道
- 最低分子轨道Hexatriene和苯的零节点
- 犯罪手法的“阁楼”图(最高能级)的最大数量的节点
- 苯有节点飞机。最大能级有3个节点的飞机
- 我们把节点中间能级的苯?
- 苯分子轨道图:把它放在一起
- 对苯填写其余的照片
- 为什么苯比Hexatriene更稳定?
- 笔记
- (高级)引用和进一步阅读
1。简短的点评:如何绘制给定ππ分子轨道系统
以前我们看了烯丙基的分子轨道系统,和的丁二烯。我们学到了一些画出的关键教训(线性)π分子轨道的系统我很快就会改变。
认为画出π轨道有点像建造一幢公寓楼,尽管一些奇怪的市政建筑规范和古怪的租户的行为。
- pi-systemπ分子轨道的数目等于原子p轨道的贡献。对丁二烯(n = 4)我们看到π的能级系统像一栋四层楼的公寓。hexatriene和苯有六个p轨道的贡献(n = 6),所以我们应该期待6π轨道。
- 节点数量的增加,每个连续的能级。一个“节点”就是相邻的p轨道之间存在相位的变化(即不能建设性地重叠)。最低的能级(“底层”,如果你愿意)所有p轨道一致相同的方式,因此p轨道之间的节点为零(不包括固有的节点p轨道,在于飞机的分子)。这提供了最大的可能的电子离域,因此是能量最低的轨道。这就是丁二烯的“底层”的样子:
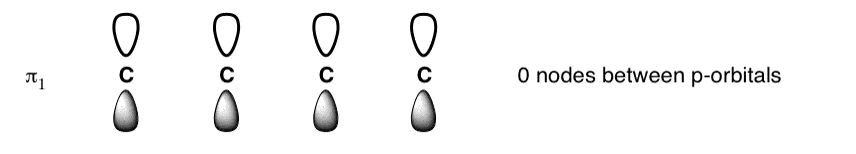
最高能级(我们建筑的“阁楼”)(n - 1)节点。我们看到,丁二烯(n = 4)最高能级轨道之间的三个节点与红线(标记)。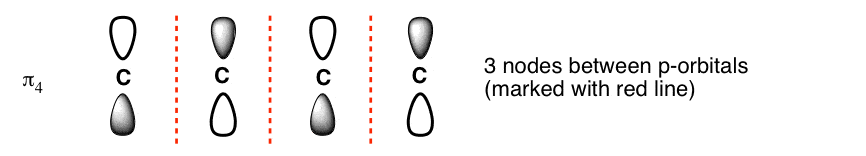
一楼和顶楼最简单的水平,因为他们遵循从简单的规则:使所有阶段,或者替代所有阶段。
棘手的部分是画中间能级的轨道,由于量子力学的市政细则,我所说的平衡节点的规则。因为(数学),节点不能被放置在任何地方;他们总是安排对称与轨道的中心。
- 单个节点必须穿过中心的分子轨道。
- 两个节点都必须放在一个平等的距离中心(即,它们平衡对中心)
- 每个连续的能级增加了一个额外的节点。注意,轨道与奇数节点将总是有一个节点的中心。
分子轨道的最后一项任务是填满我们的建筑与租户使用熟悉的(电子)构造原理:从一楼开始,每个单元(轨道)填满一个电子,最高占用两个。(注1]
现在让我们用这个框架hexatriene和苯。
2。构建苯的π分子轨道图:Hexatriene和苯分别有6π分子轨道
希望简单的!6 p轨道的pi系统苯和hexatriene将产生6π分子轨道。
水平在堆栈hexatriene像一个六层楼高的建筑。苯有不同的安排,我们很快就会看到下面的原因。
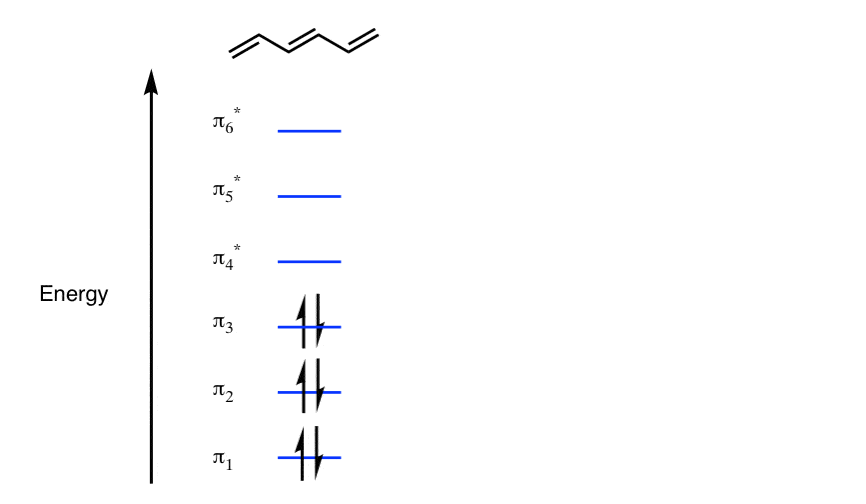
注意,下面三个轨道都是成键轨道和三大反键轨道。只有底部的三个“层”是中性hexatriene占领。(如果在这栋大楼每一层完全注满租户(电子)建筑很快就会毁灭。谈论一个混乱的建筑)
3所示。最低分子轨道Hexatriene和苯的零节点
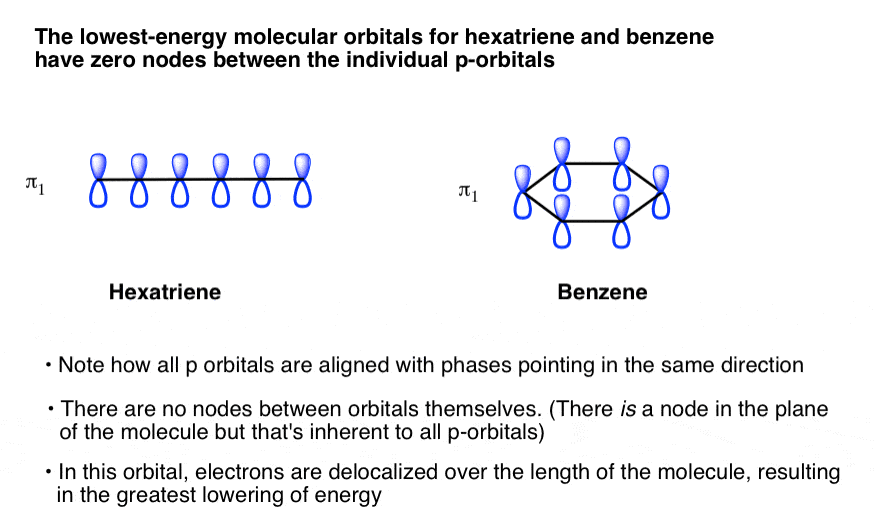
对丁二烯上面描述的模式后,我们首先画出“底层”,所有p轨道的阶段相同的方式保持一致。没关系如果你画“阴影”或“白”叶向上或向下,只要他们都以同样的方式。
这就是它们看起来像hexatriene和苯:
4所示。犯罪手法的“阁楼”图(最高能级)的最大数量的节点
最高的能量分子轨道与完全交替阶段p轨道。
像一楼,高能分子轨道(π体系的“阁楼”)也是简单的画。
画出所有的p轨道交替阶段。没有任何两个相邻的p轨道应该叶相同的阶段。
对于线性系统,我们看到这给最高能级(n - 1)节点。hexatriene (n = 6)这意味着最高能级将有5个节点。
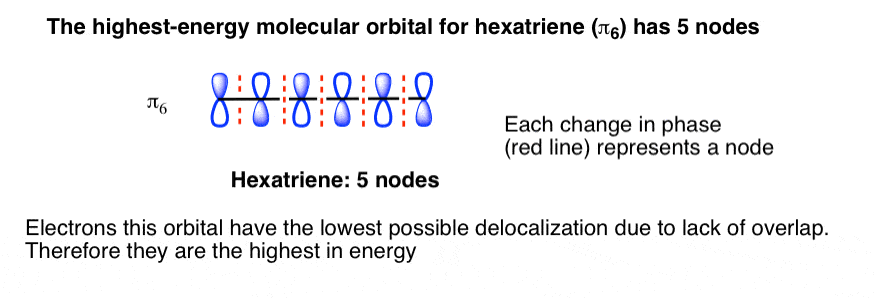
苯呢?这正是事情变得有趣。
5。苯有节点飞机。最大能级有3个节点的飞机
在循环系统中,(n - 1)规则失败。画一个分子轨道的苯与5节点就像解决5魔方的脸:不可能的。meelion美元如果你能证明我错了:试一试!(注2]
然而,我们可以轻松地画出另一个轨道,所有的阶段。不过,在这种情况下,我们可以计算六个阶段变化的地方。与其看着这些作为单独的节点,它是把这些三也许更有帮助节点的飞机,穿过分子在不同的点。
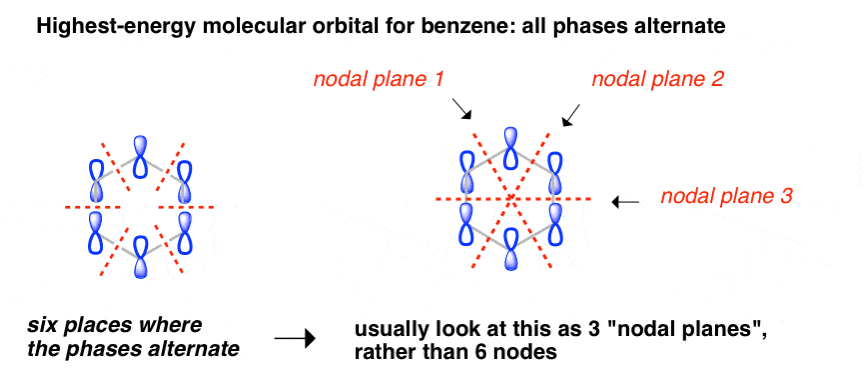
这个轨道是零重叠相邻p轨道,因此电子轨道有最低可能的移位。因此他们最高的能量。
6。我们把节点中间能级的苯?
正如我们上面所说的,棘手的问题在构建π分子轨道是知道把节点的中间水平。
hexatriene,二楼(一个节点)相当乾脆:我们把节点的中心,是这样的:

画一个环pi系统是不可能的一个节点,但我们可以画一个系统有一个节点飞机。在这里,例如,我们画一个节面穿过两个单一债券:

但是等等!实际上第二个方法。我们也可以画一个节面通过原子,像这样。

这两个分子轨道(π2和π3)具有相同数量的节点平面,因此有相同的能量。我们通常的方式描述这个化学说轨道简并。
这是关键的区别在分子轨道的图片循环系统和一个非循环系统:两个单位可以共存于同一层。对苯、结果在降低的能量。
7所示。对苯填写其余的照片
这是第三、第四和第五的“地板”hexatrieneπ体系,两个,三个,四个节点,分别。
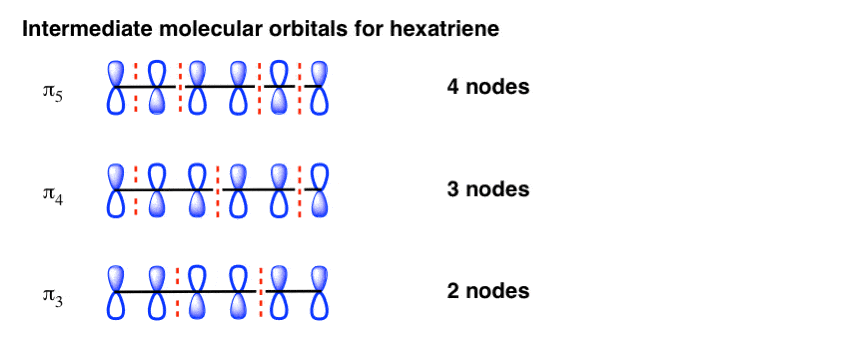
苯,下一层有两个节点的飞机。再一次,有两种方法可以做到这一点:穿过债券,或穿过原子。再一次,这些是相同的能量。
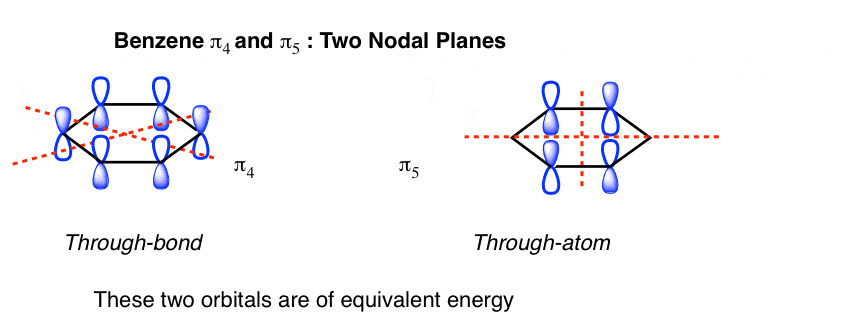
8。苯分子轨道图:把它放在一起
最后一步是安排一起π轨道(通过“层”),然后填满每一层电子(“承租人”)。
这是完整的分子轨道hexatriene图片:
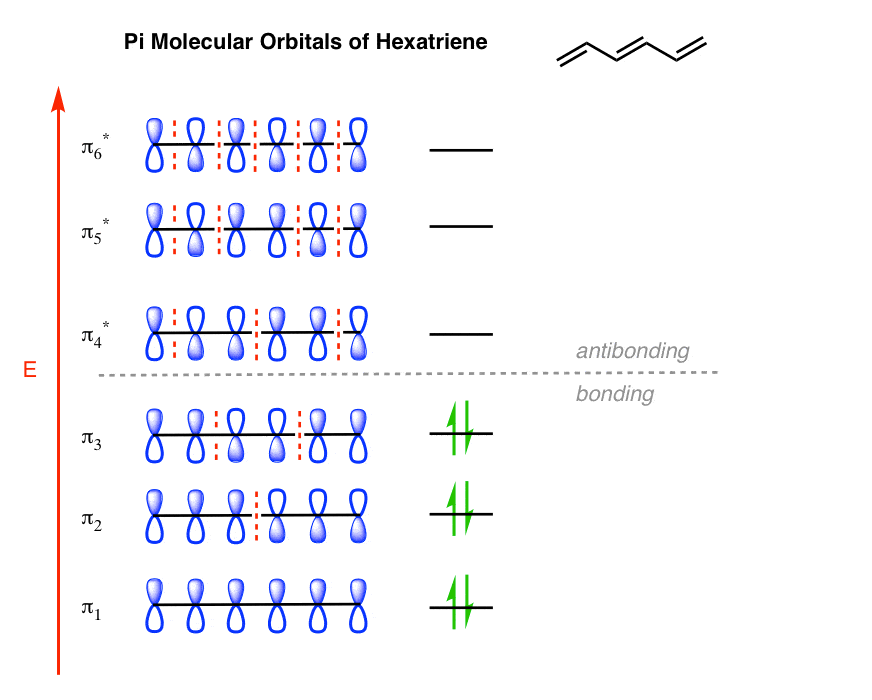
完整的苯分子轨道图是画的顶部,但在这里又为非滚动的快乐:
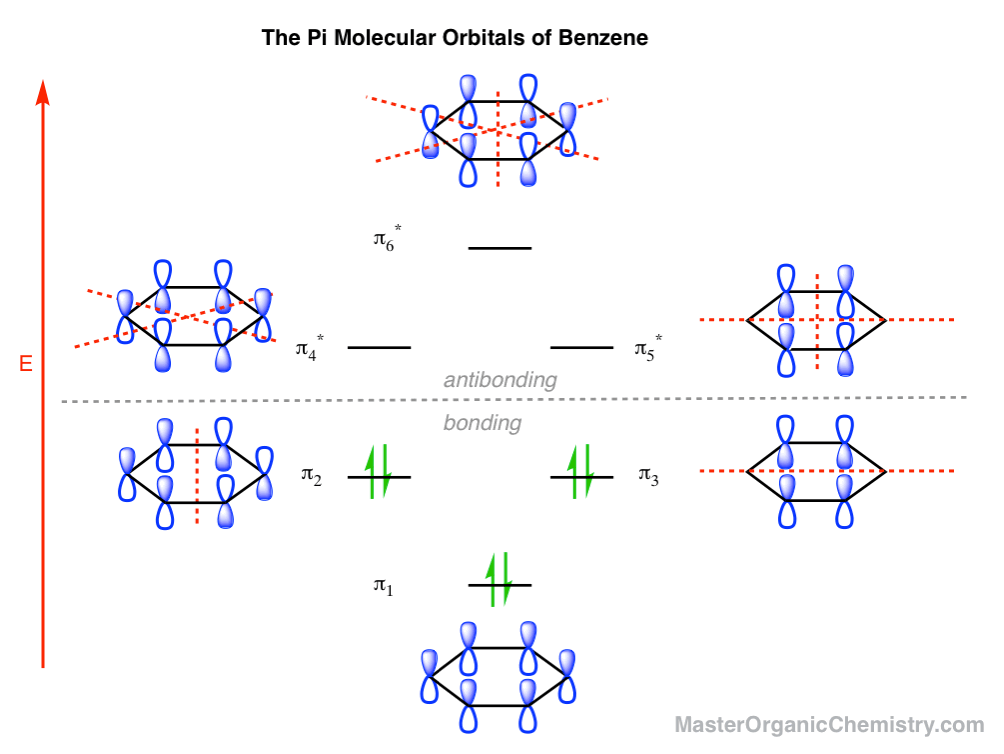
看到关键的区别吗?称其为“一个更高效的能量水平叠加”并不遥远。
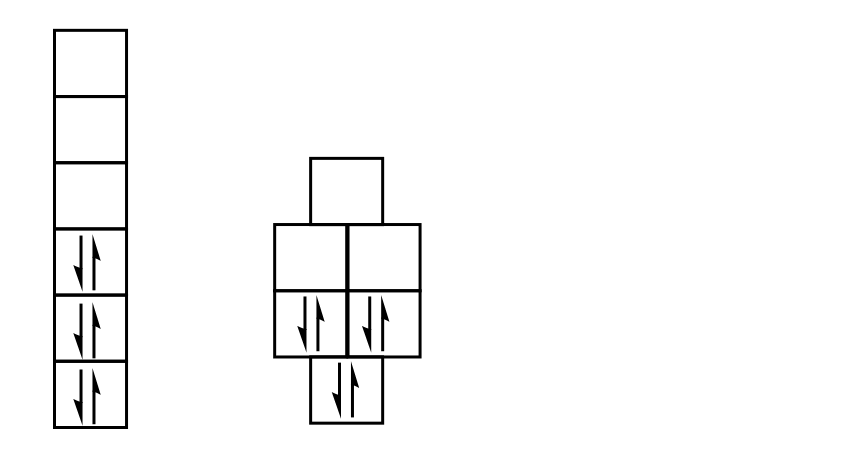
9。为什么苯比Hexatriene更稳定?
环pi系统允许两种方式将一个节面:通过债券,或者通过atom。在苯中,这意味着第二个和第三个“层”各有两个单位相同的能量——它们是“堕落”。
按照我们有些粗糙的类比,两座建筑有六个“租户”,但在苯,租户不高离地面,从而减少潜在的能量。
在化学方面,最高占据分子轨道(HOMO)苯比最高占据分子轨道能量较低(HOMO) hexatriene。对于我们的目的,低能量的π电子转化为较低的反应活性。(注3]
这是一个不完美的比喻,但是对于我们的目的,它会做。
在接下来的帖子,看看我们可以检查的分子轨道anti-aromatic环丁二烯同样获得洞察其不寻常的不稳定。
由于汤姆Struble对本文的贡献。
笔记
注1。电梯的发明之前,办公室在地面层的建筑是最令人垂涎的。构造原理回归本源那些日子“阁楼”层的建筑是最不可取的,因为它涉及跋涉了楼梯。
注2。开始π6苯的分子轨道,有六个网站的阶段变化。翻转其中任何一个p轨道的阶段给你一个分子轨道与4个节点(两个节面)。同样可以证明,苯的分子轨道只能有偶数个节点。
(高级)引用和进一步阅读
- Quantentheoretische Beitrage zum Benzolproblem
死Elektronenkonfiguration des粗苯和学会Verbindungen
Erich Huckel
Zeitschrift毛皮物理学1931年,70年,204 - 286
DOI:10.1007 / BF01339530
Erich Huckel实现识别的详细说明,以及彼得·德拜理论强电解质在1923年,后来通过应用一个简化版的量子理论中p电子共轭分子,这被称为Huckel分子轨道(HMO)理论。虽然他从来没有明确制定一个“4 n + 2规则”,这是明显的从他的工作。Huckel表明单环系统连续接合有6、10、14等p电子受益于额外的稳定和芳香。但它是更准确的指“Huckel 4 n + 2 p,电子规则,”而不是“休克尔规则”。 - 分子轨道能量的记忆技巧
阿瑟·a·弗罗斯特和鲍里斯Musulin
j .化学。理论物理。1953年,21,572年
DOI:10.1063/1.1698970
“冰冻圈”的起源助记手段确定的莫electrocyclic系统。 - 克罗克,不是Armit和罗宾逊,生六芳电子
Alexandru t . Balaban和亨利·保罗·v . r . Schleyer Rzepa
化学评论2005年,105年(10)3436 - 3447
DOI:1021 / cr0300946
回顾历史上的一些非常著名的化学家的芳香性理论提供证据表明,苯的起源是6 p电子一直mis-cited文献中!一个很好的阅读那些对化学的历史很感兴趣。
非常感谢,我发现这个地方真的很有帮助
为什么p轨道的第一和第三个碳苯不ψ3和5中流离失所的?
你能解释为什么环戊二烯基阳离子anti-aromatic吗?我知道这4 nπ电子,但莫图表明它不占据任何反键帽,它只是不补键帽,它很不稳定吗?是因为不配对电子π2π3 MOs ?非常感谢。
构建莫图,我将使用一个冰冻圈一个五角大楼顶端向下。你前两个π电子在最底部水平(顶点),但是接下来的两个能级简并,装。这就是问题所在:分子与两个装轨道双游离基字符相同的能量,一种非常不稳定的情况。
我们能说简在苯是反映在休克尔(4 n + 2)芳香性的规则吗?
不,(4 n + 2)只是一个系列的代数表达式2、6、10、14…。它没有物理意义。
非常感谢你
Hayder高兴你发现它有用。
最左边的苯pi-6分子轨道的轨道应该颠倒,不应该吗?
固定的。再一次谢谢你。