自由基反应
开始,传播、终止
最后更新:2022年12月7日|
初始化、传播和自由基反应终止
在前面的帖子自由基取代反应我们谈论为什么需要光或热在自由基反应(看到帖子:自由基反应——为什么光或热是必需的)。在这篇文章中我们要通过自由基取代反应的机制,它有三个主要类型的步骤:初始化、传播和终止。
表的内容
- 自由基的机制替代与氯烷烃2
- 一步有净增长自由基的数量被称为“启动”
- 一步没有净收益或损失的自由基被称为“传播”
- 当心这个常见的错误在图纸自由基机制
- 有两种传播步骤自由基卤化烷烃
- 哪里有一步净减少自由基被称为,“终止”
- 烷烃的自由基取代反应机理
- 摘要:自由基取代反应
- 笔记
- (高级)引用和进一步阅读
1。自由基的机制替代与氯烷烃2
你可能记得看到这个反应在先前的自由基氯化后与氯甲烷2。
这是一个替代碳因为碳氢键的断裂和新C-Cl债券形式。副产品盐酸。
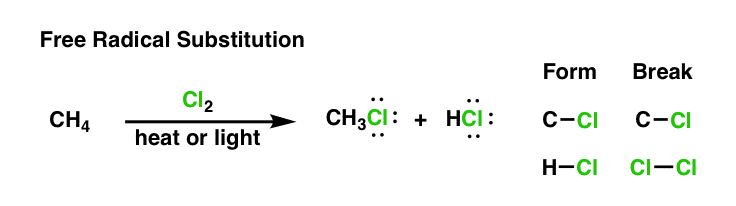
现在,我们更了解什么是自由基及其关键属性,今天我们将回答,“这个反应是如何工作的呢?”。
我们要通过这个反应的关键步骤和学习,他们是由三个关键阶段:初始化,终止,传播。
2。哪里有一步净增加自由基的数量,“启动”
自由基反应通常需要热或光应用。这是因为这两种能源可以导致相对较弱的键均裂像Cl-Cl给自由基(即。Cl•]
每一个自由基反应开始于一个自由基创建的步骤,因此这最初的一步启动。
这是起始阶段的方程。两个注意事项:
- 反应是一个平衡——在任何给定的时间只有一个小浓度的自由基存在(但这就足够了,我们将看到)
- 请注意,有自由基的净增长在这个反应。我们要从零(反应物)两个(产品)。
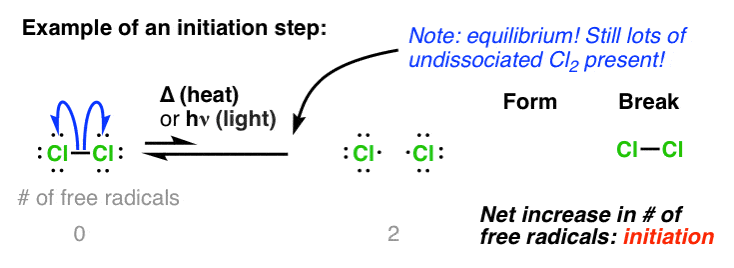
3所示。一步没有净收益或损失的自由基被称为“传播”
只有一次我们的衬底(CH自由基的存在4在我们的示例中)。氯自由基具有很高的活性,并能结合氢从甲烷甲基,•CH3
如果你计算自由基的数量在这个方程,您会注意到,有一个在反应物和一个产品。所以有没有净增加自由基的数量。
这种类型的步骤被称为“传播”。
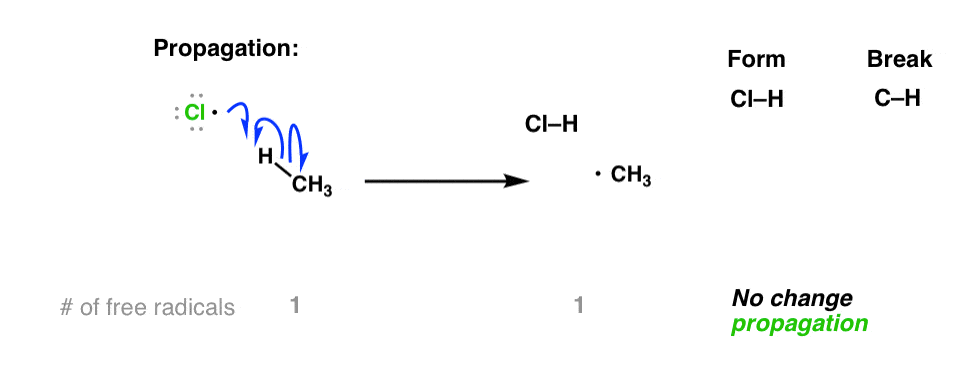
如果你记分,这一点你应该能看到,只有一个键形成反应之前完成。我们需要做的就是C-Cl债券。
4所示。当心这个常见的错误在图纸自由基机制
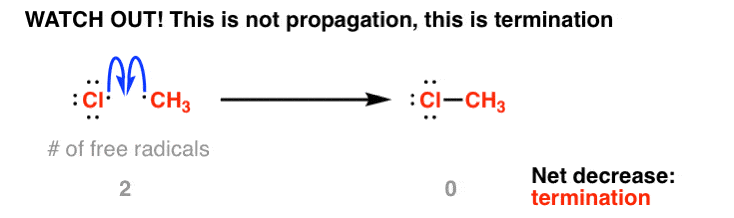
在这儿,很容易让一个小错误。看到有两个氯自由基形成的起始步骤,似乎自然汇集氯甲基和激进的CH3cl。对吧? ? ? ? ?
Nooooo !
注意自由基的数量减少在这里,不保持不变。不能传播!(实际上终止,我们将讨论在一分钟内)。
5。有两个自由基传播步骤替换
事实上,我们可以做适当的“传播”步骤:将甲基,与氯反应2仍然存在。这给了我们CH3Cl和氯激进。请注意,没有净改变自由基的数量,这仍然是一个“传播”。
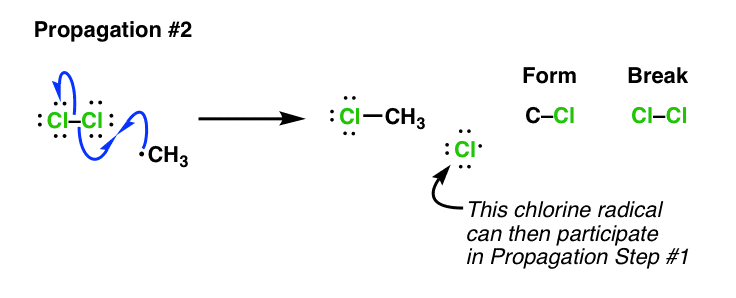
请再次注意,我们正在形成一个氯激进!有什么重要的呢?这是至关重要的,因为这个氯自由基可以执行传播步骤# 1新分子的衬底(CH4),持续的过程。这是一个连锁反应——一旦生成,氯激进催化。这就是为什么我们只需要少量的氯自由基反应进行。这不是不寻常的104或多个周期终止发生之前进行。(看到这个参考下面)
6。哪里有一步净减少自由基被称为,“终止”
这连锁反应永远持续下去吗?不。
让我们考虑两个极限情况。如果Cl的浓度2相对于低CH4(换句话说,Cl2是我们限制试剂)传播第二步的速度就会慢下来的浓度降低。没有任何Cl2反应,我们•CH3激进分子可以结合另一个自由基(如•Cl)给CH3例如,Cl。这个反应的本质上没有障碍。注意,这里的自由基数量从2降低到零。这就是所谓的终止。
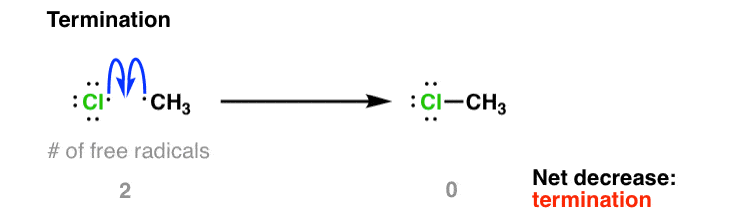
也有可能两个甲基结合CH3ch3;这也是终止!
7所示。烷烃的自由基取代反应机理
让我们一起把所有这些步骤我们可以清楚地看到开始,传播,和终止步骤。
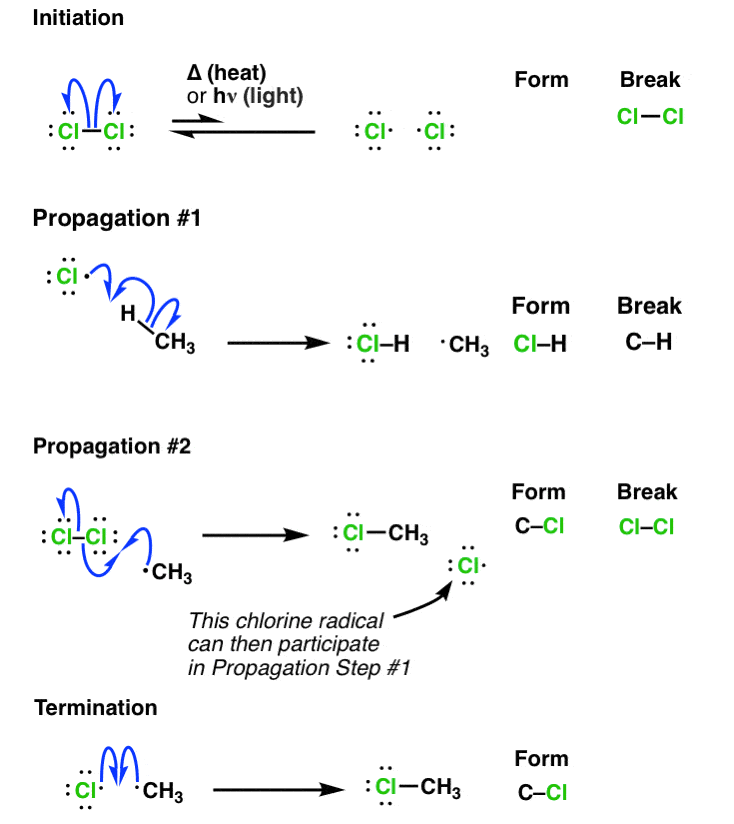
8。摘要:自由基取代反应
这三种类型的步骤中遇到每一个自由基反应。
这里的底线是,通过计算自由基创建或销毁的数量在每个步骤中,您可以确定步骤开始,传播,或终止。
- 层- >净自由基的形成
- 传播- >自由基的数量没有变化
- - >终止自由基的破坏
我们把两个难题留给未来的职位。
第一次…请注意,这里我们使用CH4,每一个碳氢键都是相同的。会发生什么,如果我们用烷烃,所有碳氢键不相等…像丙烷或戊烷,例如?
其次,这个反应不引人注目当Br2是用来代替Cl2CH的反应4。然而,我们会发现Br2可以在某些特殊情况下工作。
更多的很快!
在下一篇文章:同分异构体的自由基反应
笔记
额外的材料。
我们刚刚谈论的情况一个相当于氯(Cl2使用)。当我们使用多个等价物,甚至是一个巨大的过剩?
想想一秒钟。想象我们有多个等价物的Cl2在CH的存在3Cl。你认为会发生什么?
一个原子的Cl•与CH反应3Cl给•CH2Cl (HCl),可以与氯反应2给CH2Cl2!
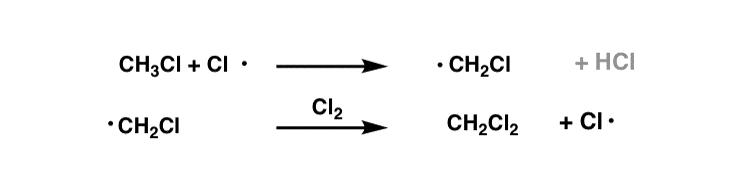
同样地,如果我们仍然有过多的Cl2,然后我们将观察CH转换2Cl2对CHCl3。
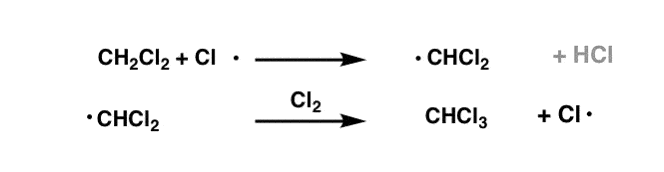
最后,给予足够的Cl2我们可以想象CHCl的转换3CCl给4。
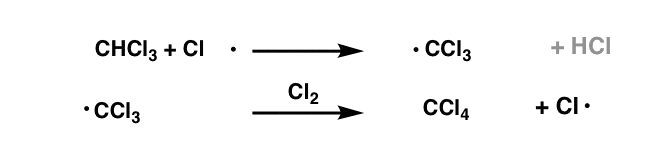
在这一点上没有进一步的碳氢键与氯自由基发生反应,因此我们的反应最终将终止。
这里的底线是,烷烃,给定一个足够大的Cl2,最终将他们所有的氢氯取代。
这个途径实际上是二氯甲烷(CH2Cl2-共同的实验室溶剂)氯仿(CHCl3CCl)和四氯化碳(4)工业生产。几十年来,三地4生产规模mega-ton用作制冷剂,干洗溶剂,直到研究涉及和其他氯氟化碳的吗臭氧层的消耗。
(高级)引用和进一步阅读
- 墙体,c。自由基在溶液中威利和儿子,纽约1957 p。352
- 氯化甲烷
t . McBee h·b·哈斯c . m .内尔和h·斯特里克兰
工业化学与工程化学1942年,34(3),296 - 300
DOI:10.1021 / ie50387a009
本文表明氯化甲烷可以控制给任何所需的氯甲烷的高收益。这是重要的,因为CH3Cl, CH2Cl2,CHCl3CCl,4都是重要的原料或溶剂,这是他们如何生产工业。 - 动力学的热氯化甲烷
罗伯特·n·皮斯和乔治·f·Walz
美国化学学会杂志》上1931年,53(10)3728 - 3737
DOI:10.1021 / ja01361a016
本文提供了动态证据表明氯化甲烷是2nd甲烷和Cl顺序(一阶2)。 - 环己烷的溴化甲基环己烷和异丁烷
威廉·m . s . KHARASCH她和弗兰克·r·梅奥
《有机化学》杂志上1941年06(6),818 - 829
DOI:10.1021 / jo01206a005
自由基链反应机理的本质在烷烃的替换是不能完全解决,直到1940年代。在这种开创性的1941年的报告,Kharasch提出连锁机制我们现在读教科书:
2)Br2 +高压- > Br•(启动)
b) rh + Br•- > R•+哈佛商业评论(传播步骤1)
c) R•+ Br2 - > R-Br + Br•(传播步骤2)
Kharasch报道,自由基取代的环己烷Br2反应非常缓慢地在黑暗中,或在缺乏氧气。在低浓度、氧气可以作为自由基引发剂(从Br2形成Br•自由基)但是这里Kharasch还观察到,在高浓度氧气可以抑制自由基反应。Br•反应的选择性与碳氢键的顺序三级>二级>主也指出。
非常感谢,真的很有帮助。
你好!谢谢你所有的信息,该网站是真正伟大的。
如果我可以,我有一个问题。首先为什么Cl *激进”采取“氢,例如,甲烷?是甲烷的·hc·邦德弱于Cl-C债券?我应该问Cl *激进或者至少比H3C *彻底稳定吗?哪一个是正确的问题吗?和其他基本的考虑吗?
谢谢你!
看它的方法是比较键焓变和计算能量的差异从原料到产品。
八氯键的强度约为106 - 107千卡每摩尔的键的强度而H-CH3大约是104千卡每摩尔。因此“获得”的能量约为3千卡每摩尔的氯化甲烷。
(C-Cl债券不考虑到这个反应,作为一个可能的终止阶段除外)。
至少让你知道是否会积极有利的整体过程。
我们不涉及自由基氟化,因为氟键比碳氢键更强,而且反应放热,燃烧往往发生。
另一方面自由基碘化通常失败,因为设定h债券非常弱,相对于碳氢键。
因此,在总结:债券的优点是一个很好的指南。
它是如何工作的
氯氟化碳?
这是自由基卤化烷烃,尽管氟氯化碳与臭氧的反应也通过初始化,传播和终止的步骤。
提出一个2-methylpropane光化学氯化的机制。标签开始,传播和终止的步骤
你能做到。用这个作为模板。
嘿。我不明白为什么它是第二繁殖所必需的步骤。为什么不能直接甲基和氯自由基结合给氯甲烷?
氯甲基和激进的出现在非常低的浓度(相对于甲烷和氯),应该为大多数的低反应速率与浓度成正比。如果这些激进分子见面,他们会反应当然,只是很不可能的。
与氯烃基的反应更青睐是因为氯的浓度,大大高于Cl的激进。
当丙酸与氯反应紫外线照射下,为什么2-chloropropanoic酸形成的而不是3-chloropropanoic酸?为什么氯附着在碳羧基旁边?马氏规则不能被应用,因为它不是亲电加成。
检查激进的形成通过C2碳氢键均裂,而激进的形成通过C3碳氢键均裂。你注意到它的邻居?
虽然这不是最好的例子,你可能会发现这个有趣的:https://en.wikipedia.org/wiki/Captodative_effect
我不能正确理解烷烃的反应过程
我可以请丙烷的氯化的自由基反应吗
写在这里一样,只是用丙烷代替甲烷。复杂的是,你将有两个不同的工程产品。1-chloropropane 2-chloropropane。
这确实存在
嘿有任意两个氯自由基可以结合在终止?
是的!尽管Cl•在任何给定时间的浓度很低,所以它往往是缓慢,直到物种参与传播的浓度是耗尽。
嗨,Cl如何激进的“拉动”氢原子从甲烷?
不要谈论electroneg。差异,因为甲基不能够打破Cl-Cl债券。
未配对电子的Cl与氢和s轨道的相互作用存在一个过渡态之间有部分债券Cl和H和碳。八氯债券相当强度(102千卡每摩尔)·hc·邦德的甲烷(105千卡每摩尔)过程是相当有利的。由此产生的碳基激进然后用剩余的氯反应。在甲烷碳氢键离解能量相当高相对于其它烷烃,所以在其他烷烃将更加有利。
在二氯甲烷的形成如果一个原子的Cl激进与CH3Cl互动传播的第一步,你怎么还在第二步中氯吗?难道你只有一个Cl激进左派?
氯和2 Cl•之间有个平衡。它严重到左边,所以实际上是一个大量的氯现在和Cl•很少
我有两个问题。
首先,为什么溴大多未能做这些步骤?是因为溴的天性吗?
第二,如果我们丙烯反应而不是甲烷?氯的位置是哪里?
我在这篇文章中讨论溴。基本的热力学不太有利,因为弱H-Br债券形成。
//m.deriinvest.com/2013/09/23/selectivity-in-free-radical-reactions/
二氯丙烯会与氯反应给附近的(氯化),而不是通过激进的途径。
坦克你的信息,真的很有用。
但是我有一个问题。
当甲烷与氯气反应,产品随氯的混合物。所以当使用等量的氯和甲烷时,会发生什么?请帮帮我!