有机金属化合物
吉尔曼试剂(Organocuprates):他们的用途
最后更新:2023年7月6日|
那么什么是吉尔曼试剂用于呢?
上次我们谈过如何使吉尔曼试剂(organocuprates)。在这篇文章中,我们将讨论他们的实际使用。
吉尔曼试剂有一些有用的对比格氏试剂。
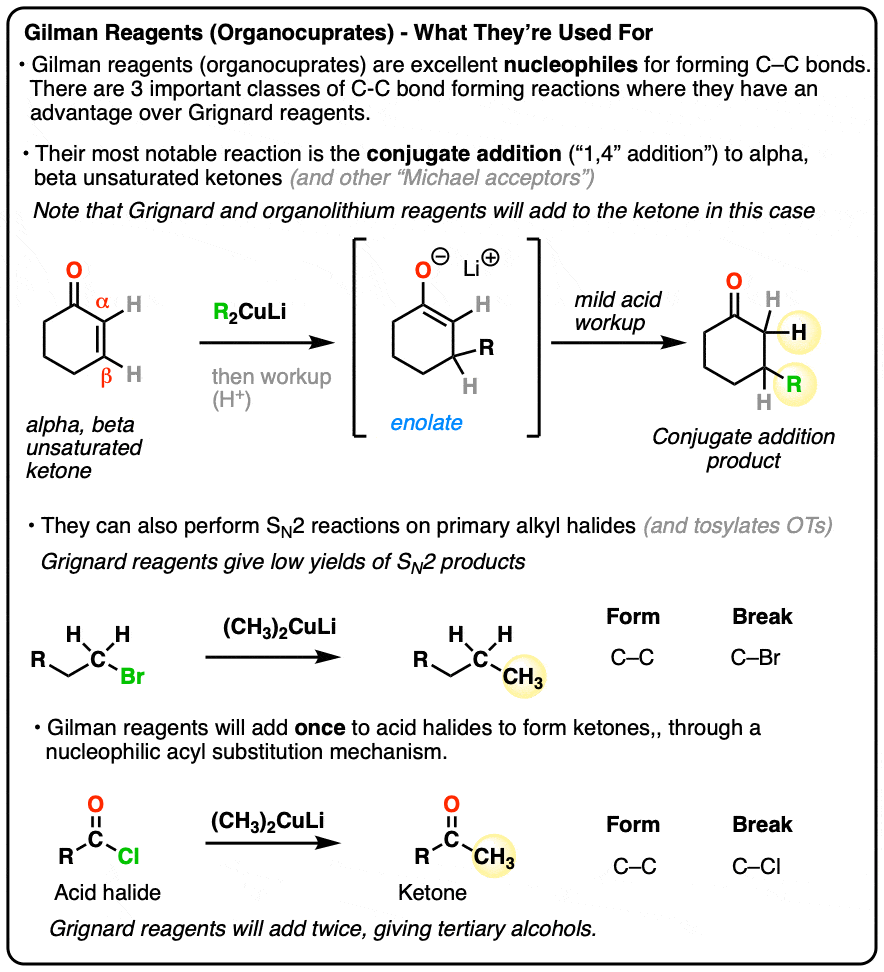
- 首先,他们可以用来执行共轭加成反应(1,4-addition)α,β不饱和酮。相比之下,格氏试剂只倾向于增加羰基碳。
- 其次,吉尔曼试剂的亲核试剂,是有用的SN2与主反应,形成碳碳键烷基卤化物和磺酸盐(如甲苯磺酸盐、甲磺酸)
- 第三,吉尔曼试剂将通过亲核酰卤化物酸转化为酮替换。格氏试剂将增加两次酸卤化物给叔醇。
表的内容
- 吉尔曼试剂与格氏试剂
- 共轭加成:吉尔曼的关键反应试剂
- 你怎么知道是否“正常”或“共轭”除了会发生?
- 共轭加成机制
- 吉尔曼试剂是年代伟大的亲核试剂N2反应
- 结论:吉尔曼试剂
- 笔记
- (高级)引用和进一步阅读
1。吉尔曼试剂与格氏试剂
正如我上次暗示,吉尔曼格氏试剂提供了一个有趣的对比和organolithium试剂。
记住所有这些例子格氏试剂添加醛、酮酯类吗?嗯,吉尔曼试剂通常不这么做(他们将增加酸性氯化物,但我跑题了)
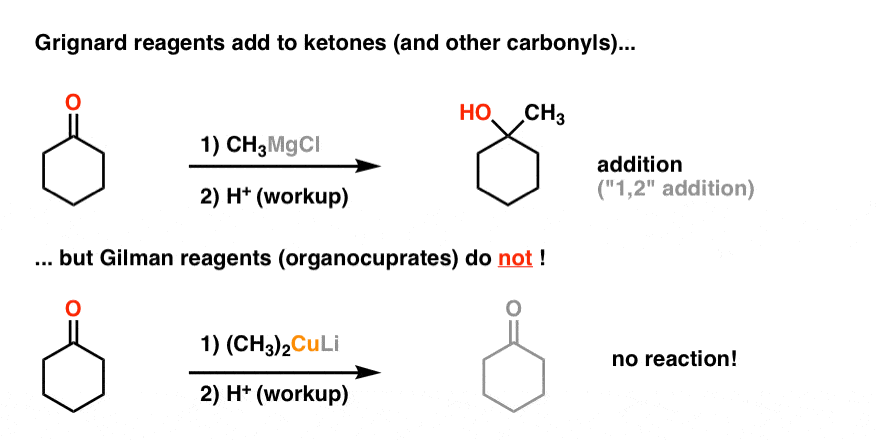
你可能会发现自己在想,“那又怎样?”。为什么我们要去学习这些东西如果他们甚至很被动?
嗯,亲爱的读者,让我填补你第二个例子。我们将改变一件小事,一切都变了。
让我们把一个双键的旁边酮并再次运行反应。
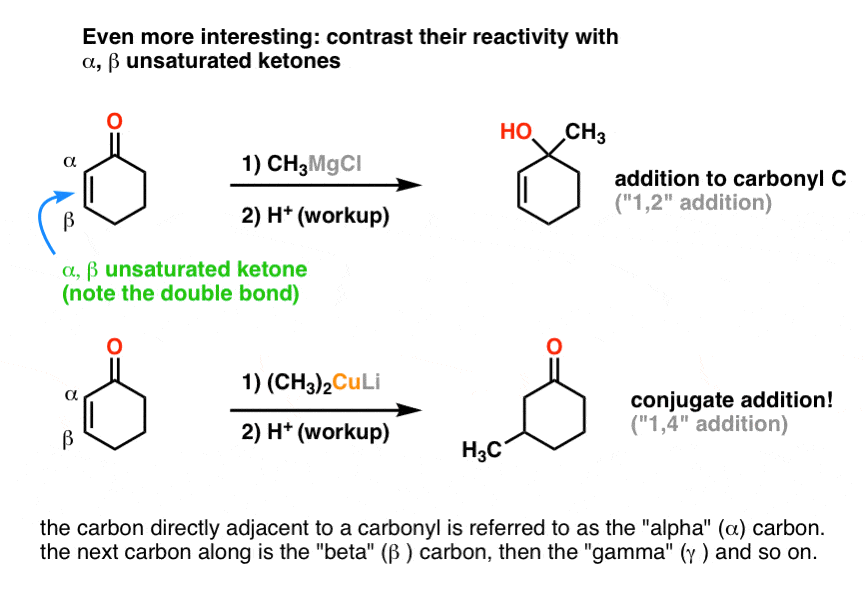
哇。刚刚发生了什么事?
2。共轭加成:吉尔曼的关键反应试剂
格氏试剂的反应(一样羰基organocuprate),但是,看到我们打破了碳碳π键(双键),形成新的碳碳键吗?
如果你,看上去有点怪异,它应该!孤立的烯烃,如环己烯例如,不要做这个反应。
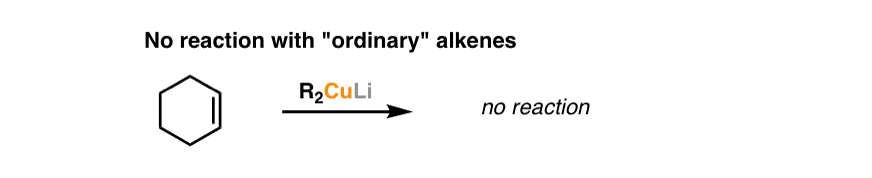
所以一定有什么重要的事实烯烃旁边是一个羰基。为什么这很重要吗?
看看共振形式,你会看到一个线索。
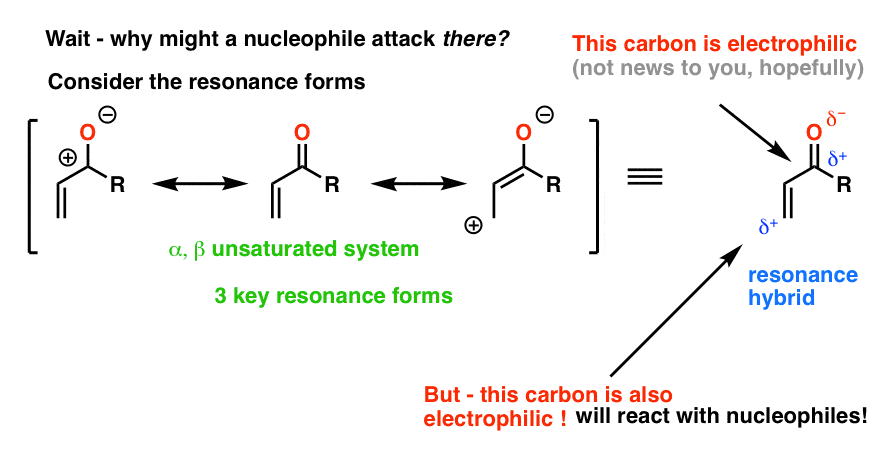
有一个重要的共振形成的碳两个碳原子从羰基碳(我们称之为“测试版”(β)位置)熊一个正电荷。因此,在共振混合碳熊部分正电荷。
换句话说,碳亲电。它能与亲核试剂反应!(如organocuprates)。
这与普通的对比烯烃共振的形式与碳轴承负电荷不是一种重要的共振。电荷被放在这一事实氧气在共振的一个α,β不饱和系统共振形成的相对重要性的关键。(比较醇盐的碱度(RO)和alkyllithiums (R),这将给你一个想法的相对稳定性]。
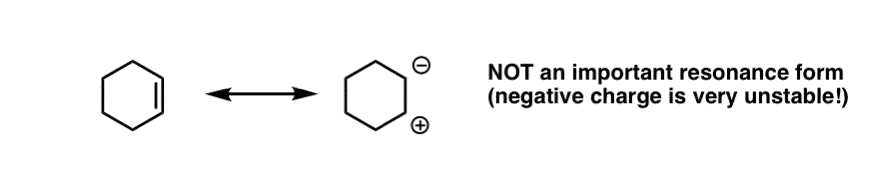
(更多信息,见文章)迈克尔加成和共轭加成]
3所示。等等,你怎么知道是否“正常”除了“共轭”除了会发生吗?
这引出了一个重要的问题:你怎么知道是否亲核试剂将攻击羰基碳增加(有时称为“1、2”在我们的行话)或β的位置(“1 4加法”或“共轭加成”)。
简单的问题。很难回答简洁,太大这篇文章的主题。
简短的回答:记住那格里纳增加金属羰基合物,而organocuprates做共轭加成。
(鸭子,而人们乱扔东西在屏幕上)
我只说“记住”,因为为了充分理解这一现象,我们必须进入一些分子轨道理论的关键概念”硬软酸碱理论(HSAB)”,在这一点上,我们不会支付它。
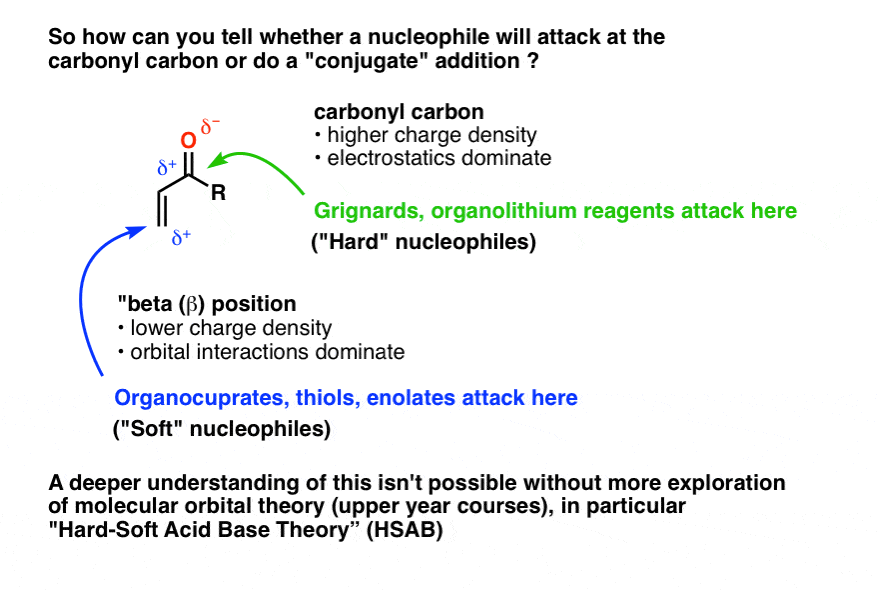
反应的机制呢?现在这是我们可以覆盖。
4所示。共轭加成机制
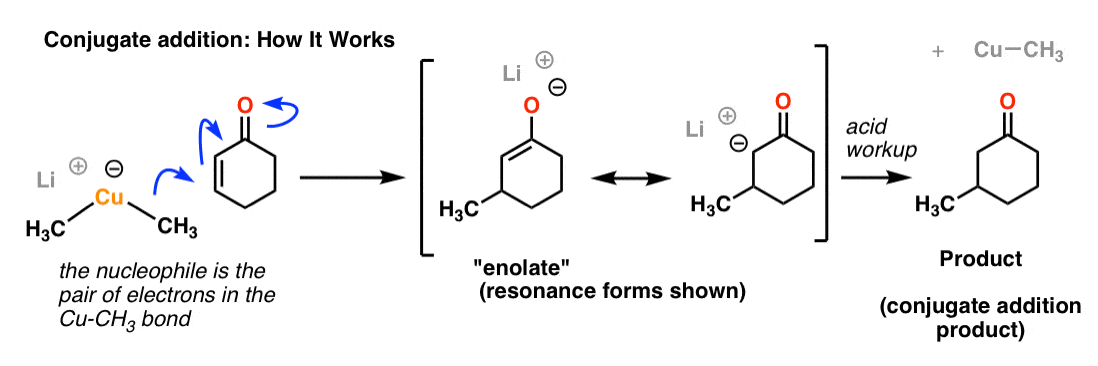
在第一步中,亲核试剂(这是Cu-CH一对电子3债券,不负电荷在铜!)形式与β的位置酮。碳碳π键断裂,形成一个负电荷α碳。我们可以走得更远,画一个共振形成我们形成新的碳碳π键和地点上的负电荷氧气。你会看到这个化学物种很多在随后的章节——它被称为一个烯醇化物,这是非常重要的。(见文章:烯醇化物)
现在,关键是负电荷的氧气更稳定的(基本)碳比拥有一个负电荷。
添加酸会使质子化烯醇化物(这是一个基础,毕竟),导致我们的最终产品。
5。吉尔曼试剂是年代优秀的亲核试剂N2反应
但是等等!共轭添加不organocuprates所能做的。
如果你有一个敏锐的眼睛在本系列的其他文章,您可能已经注意到,SN2反应是没有出现在列表中,格氏反应是有用的。(为什么?好问题。简短的回答是,我们观察到很多副反应发生,比如去质子化和还原。用格氏试剂做一个年代N2反应形成碳碳键通常不是一个伟大的过程]。
然而,一旦我们切换到吉尔曼试剂,SN2工作良好。这是一个方便的反应形成碳碳键的工具箱。
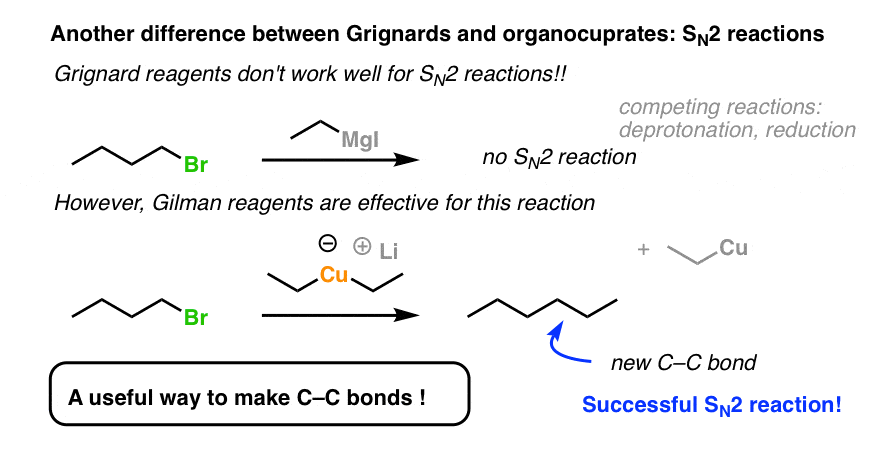
汇总而已,现在吉尔曼试剂。我们可以添加,他们可以使用酮酸的卤化物我犹豫,在目前,鉴于这篇文章足够长。(一般的机制是本文中涉及亲核酰取代。]
6。结论:吉尔曼试剂
吉尔曼格氏试剂(organocuprates)执行两个反应试剂(organolithiums)不:
•他们执行共轭添加α,β不饱和酮。
•他们是有效的亲核试剂N2反应。
在下一篇文章中,我们将换一个更有争议的话题——过渡金属催化反应。
在下一篇文章:H艾克,铃木和烯烃复分解反应
笔记
这是一个小测试。更好的是什么亲核试剂吗?有机铜试剂或organocuprate试剂吗?
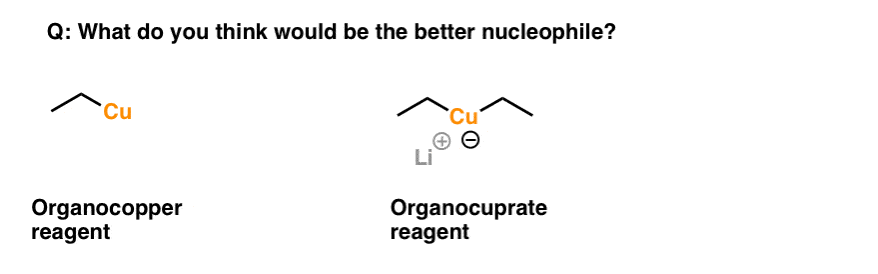
思考这个问题的时候,分析离去基团。线索就在于此。
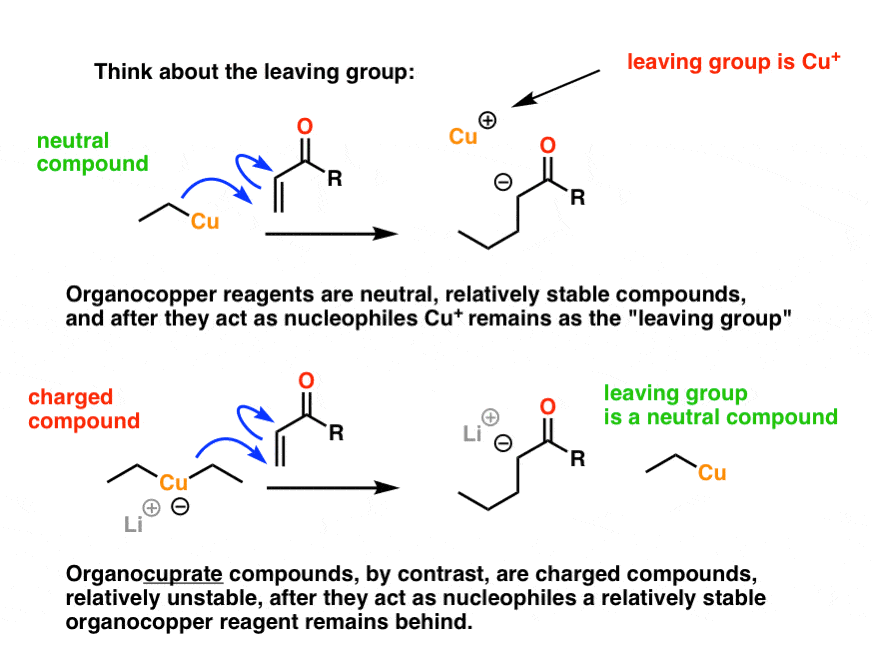
当有机铜试剂的亲核试剂,他们从中立的,相对稳定的化合物离子铜+。尽管这是一个全面的概括,费用最小化通常是有机化学中带来更大的稳定性。我们将从一个中性化合物(有机铜)带电离子(铜+)。(我也可以添加铜+,是一个柔软的离子,在绑定到O -不是很有效,但这是一个非常先进的点]。
相比之下,organocuprates。在那里,我们开始作为一个相对不稳定带电物种,我们最后的铜产品中性有机铜试剂。这绝对是下坡的稳定。合理的期望,organocuprate会更被动,因此成为一个更好的亲核试剂。
同样的原则可以用来解释为什么NaBH4是一个更好的还原剂比黑洞3,LiAlH4是一个更好的还原剂比AlH3。
(高级)引用和进一步阅读
吉尔曼试剂或锂organocuprates (R2CuLi),非常有用的亲核试剂在有机合成。这些从格氏试剂和organolithiums有不同的反应,因为吉尔曼试剂是柔软的。
吉尔曼试剂形成:
- Methylcopper的准备和一些观察有机铜化合物的分解
亨利·吉尔曼,鲁本·g·琼斯和洛杉矶森林
《有机化学》杂志上1952年17(12),1630 - 1634
DOI:1021 / jo50012a009
的第一篇论文,教授亨利·吉尔曼(美国爱荷华州)“吉尔曼试剂”——diorganocopper化合物。在这种情况下他描述dimethylcopper的准备。
吉尔曼的共轭加成试剂: - 负碳离子的化学反应。第十七章。添加甲基有机金属试剂cyclohexenone衍生品
赫伯特·o .房子和小威廉·f·费舍尔。
《有机化学》杂志上1968年33(3),949 - 956
DOI:1021 / jo01267a004 - 共轭加成反应的有机铜试剂
加里·h·波斯纳
反应。1972年,19,1 - 114
DOI:10.1002/0471264180. or019.01
有机反应维护的是一系列的评论ACS的有机化学和波斯纳教授这篇评论,铜酸盐的化学专家,涵盖了所有你想知道的关于共轭添加铜、1972年。到最后也给出了详细的实验程序。酮可以通过添加吉尔曼合成试剂酰卤化物: - 甲基,烷基酮的羧酸氯化物和有机铜试剂
g·h·波斯纳,c, e·威顿
四面体。列托人。1970年,11(53),4647 - 4650
DOI:10.1016 / s0040 - 4039 (00) 89398 - 3
这个反应最初的论文之一。波斯纳教授所做的大量的工作研究有机铜化学在他的职业生涯。 - 有机铜化学。晕,青紫羰基代替酮从相应的酰氯化物和有机铜试剂
加里·h·波斯纳、查尔斯·e·威顿和保罗·麦克法兰
美国化学学会杂志》上1972年,94年(14),5106 - 5108
DOI:1021 / ja00769a066
前面的纸的延伸,扩大反应的底物范围。的年代N2吉尔曼的反应试剂烷基卤化物也称为Corey-Posner-Whitesides-House反应: - 选择性碳碳键的形成与组之间使用有机铜试剂
伊莱亚斯·j·科里和加里·h·波斯纳
美国化学学会杂志》上1967年,89年(15),3911 - 3912
DOI:1021 / ja00991a049
诺贝尔奖得主e·j·科里教授首先描述了吉尔曼的反应试剂CH3李(CH3)2CuLi)烷基和芳基卤化物形成新的碳碳键。 - 碳碳键形成的选择性耦合n-alkylcopper试剂和有机卤化物
伊莱亚斯·j·科里和加里·h·波斯纳
美国化学学会杂志》上1968年,90年(20),5615 - 5616
DOI:1021 / ja01022a058
科里扩展这个方法来教授n -丁和乙基(从n -BuLi和EtLi)。 - 二烷基锂的反应——和diarylcuprates有机卤化物
乔治·m·怀特赛兹教授威廉·f·费舍尔,约瑟夫·圣菲利普·Jr . Robert w . Bashe,赫伯特·o .的房子
美国化学学会杂志》上1969年,91年(17),4871 - 4882
DOI:1021 / ja01045a049
经典论文g·m·怀特赛兹教授(麻省理工学院,现在哈佛)的耦合吉尔曼试剂(R2与芳基碘化CuLi)。这个反应是详尽研究,功能全面机械的调查,这就是为什么他的名字是包括在反应。
如果已经有一个R组β碳?
还是工作!大量的例子在这卷:https://onlinelibrary.wiley.com/doi/abs/10.1002/0471264180.or041.02
除了酸性氯化物,吉尔曼试剂会增加alkylsulfonyl氯化物MsCl吗?我没有访问SciFinder或Reaxys,我很难检查是否这将是一个有效的反应。
主要烷基磺酸盐工作做好。吉尔曼之间的SN2反应试剂和仲烷基磺酸盐不工作。就此而言并没有太多的好例子organocuprates反应二次烷基卤化物或甲苯磺酸盐。
https://pubs.acs.org/doi/pdf/10.1021/ja00804a039
嘿,首先令人惊讶的内容。我从印度Tirth为JEE做准备。我有这个疑问离去基强度的比较,你说。如果organocuprate是从更稳定更稳定,不会倾向于演奏这个反应。然后不应该亲核性较弱?
我想我不明白你的问题。与organocuprates反应你在想些什么?
DOI是正确的但超链接是错误的
固定的,谢谢
参考4链接到错误的URL,这是正确的:
https://www.sciencedirect.com/science/article/abs/pii/S0040403900893983
谢谢你!
哪个更被动的吉尔曼还是organolithium ?为什么? ?
具体来说,反应到什么?
你好先生,gilmann试剂能与酸反应衍生品. .R2Cd怎么样的反应?
谢谢你,先生。
吉尔曼试剂能与酸反应卤化物、酐和硫醇酯(有时)。一切忘记它。我相信是镉反应更少。看到的:https://pubs.acs.org/doi/pdf/10.1021/jo00134a015
你好,詹姆斯,
吉尔曼试剂可以作为亲核试剂与乙烯基卤化物反应生成烯烃高吗?
排序的。例如锂dimethylcuprate将与乙烯基卤化物的反应,你可以用甲基取代卤素。我不知道它是如何工作与其他吉尔曼试剂。
这不是SN2反应,铜插入C -(卤素)债券得到瞬态铜(III)物种经历还原消除取代烯烃。
你所描述的是通常最好通过交叉耦合反应(如查看铃木,根岸英一和Kumada反应)
负电荷在铜?还是吉尔曼试剂有限公司任命复杂? ? ?
对铜有一个正式的负电荷,但说碳比铜的电负性,实际的负电荷驻留主要是碳。因此,这是一个亲核的碳源。
你好!
(Br-CH2) 2 culi可以用于共轭加成?我在确定碱度r基团。
谢谢你!
不,它不会稳定。Br与负碳离子反应。
为什么organolithium和格氏试剂容易增加酮,但diorganocopper锂试剂不?
这是一个非常好的问题。一条线索是铜的电负性比李和Mg,所以Cu-C债券更多的共价的性格。
例子CH3MgCl与环己酮反应,不会退出酸性h在α碳,形成甲烷?
提前谢谢!
你描述了格氏试剂作为基础。这可以发生在某些情况下,例如当一个酮相当位阻,但在正常情况下加成反应会更快。
一个微妙之处的去质子化反应是碳氢键只有合理酸性排队接近90°时相对于C = O键,它允许为稳定的孤对共振。
这是C = O的π*轨道稳定孤对吗?
是的,这是捐赠的碳氢键的一对电子π*轨道C。
我认为organocuprates可以添加到一个酰卤和取代卤R组?
是的,他们可以。谢谢你指出这个遗漏,需要更新。
是的,他们当然可以,形成新的酮。
问候!在第二和第三个例子计划你有吉尔曼R2CuBr试剂。这是不同于R2CuLi吗?为什么一个卤素在物种吗?谢谢!
固定的。谢谢!
organocuprate化合物中的R可以任何类型的化合物?例如(CH2NO2) 2 culi可以使用吗?NO2的部分会改变或影响反应吗?
非常感谢你的时间。
嗨,珍娜-铜酸盐是很好的选择R组强碱性时,由于铜有助于减少碱度。对于CH2NO2(-)父分子(硝基甲烷)已经很酸和共轭碱通过去质子化。你可能只是deprotonate硝基甲烷与强碱(如LDA),看看这是如何工作的!
HSAB理论不足以解释为什么在非结合的环己酮没有添加吗?我理解为什么1,4比1,2,但对于一个亲电碳,和一个基本上是一个负碳离子的亲核试剂,甚至“软化”,没有其他可行的攻击网站,“不反应”似乎有点极端吗?
再次感谢你的时间。