醇、环氧化合物和醚
醇的酸度和碱度
最后更新:2022年11月4日|
酸碱反应的醇
醇是轻微的酸。典型的脂肪族(即。”烷基”)醇如乙醇,异丙醇,t丁醇有pK一个大约16,比水略酸性更强。
- 醇的动词的词形变化π键或芳环酸性更强自共轭碱共轭系统。一个主要的例子是苯酚(C6H5哦)。(pK一个= 10)。
- 附近的吸电子集团将稳定的负电荷共轭碱通过感应效果。例如,2,2,2-trifluoroethanol (pK一个= 12)是更多比乙醇酸(pK一个= 16)。
醇也弱基地。他们能与强酸反应氧鎓离子有pK一个约2。
醇的反应的一个关键是我们前进的共轭酸是一个更好的离去基团和共轭碱是一个更好的亲核试剂。
表的内容
1。四个要点回顾酸碱反应
- 每一个酸碱反应有4个组件:一个酸,一个基地,一个共轭酸和一个共轭碱当酸失去一个质子,它变成了共轭碱。当基地获得一个质子,它成为它共轭酸。以前的文章中提到,共轭bas的酒精被称为一个醇盐。的共轭酸一个酒精被称为一个氧鎓离子。(看到帖子:在有机化学酸碱反应)
- 我们通常描述酸碱反应作为一个平衡。在酸碱反应更强的酸和平衡将有利于方向产生一个较弱的酸碱性强和弱的基础当您添加盐酸氢氧化钠,暴力发生酸碱反应,导致H的形成2O(弱酸性比盐酸)和生理盐水比氢氧化钠(一个较弱的基础)。毫无疑问你会发现当添加食盐(氯化钠)水,这个反应没有进行任何重要程度在相反的方向。
- 我们测量使用一个术语叫做pK酸度一个。这是一个衡量的平衡常数一个物种放弃一个质子形成的共轭碱。pK一个在规模约-10到50。六十数量级!pK越高一个酸性越少。较低的pK一个(负面)=酸性更强。
水(pK一个14.0)是一个较弱的酸比盐酸(pK一个8)。(见文章:如何用pK吗一个表) - 酸性越强,越弱共轭碱。较弱的酸,就越强共轭碱。的共轭碱盐酸的强酸(pK一个8)是无害的氯离子(Cl -),一个非常弱碱。的共轭碱弱酸性的H2O (pK一个14)是强碱性氢氧离子(HO)。
2。酸碱反应的醇类的例子
这里有一个例子有利的酸碱反应的醇。注意我们从更强的酸和强基础较弱的酸和较弱的基础(pK一个值确定的告诉我们)
去质子化是非常有利的。请注意,共轭碱一个酒精被称为一个醇盐。
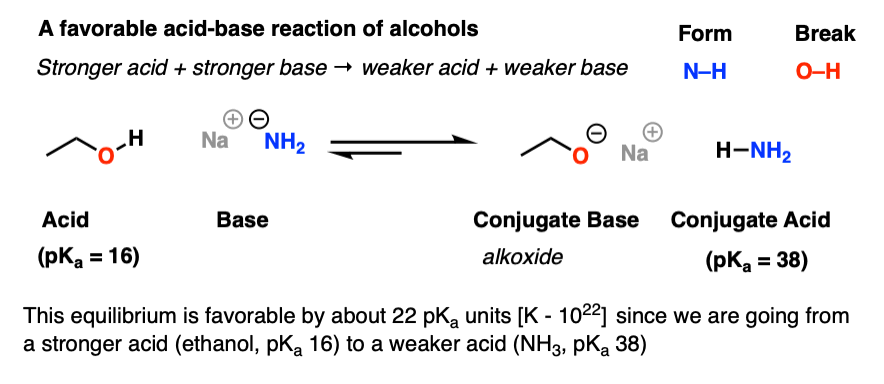
这里有一个例子(非常)不利的酸碱反应的醇类:质子化作用的酒精在北半球3。最重要的原因是不利的,是因为我们要从一个较弱的酸(pK一个38)和较弱的基础更强的酸(pK一个2)和更强的基础。平衡常数约40个数量级错误的方向!
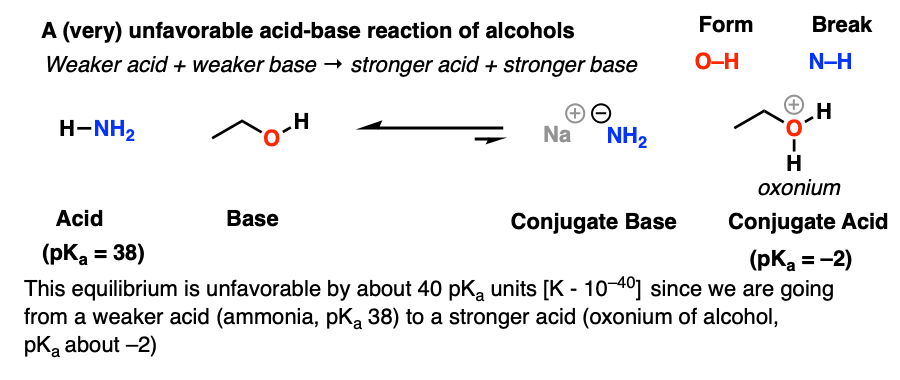
3所示。审查的关键因素,确定酸度
是什么决定了酸性分子呢?
的关键因素决定酸度是稳定的共轭碱。这使得任何因素共轭碱更稳定的将增加酸的酸度。(看到帖子:5个关键因素影响酸度)
这是什么意思,到底是什么?通常,这意味着稳定负电荷自共轭碱永远都是一个单位的“负面”比酸。(看到帖子:7因素稳定负电荷)
负电荷稳定吗?两种方式。
- 首先,通过将电荷接近带正电的原子核(“相反电荷吸引”,记住)。在一行例如,元素周期表的碱度降低我们从H3C- - - - - -到H2N- - - - - -到何- - - - - -到F- - - - - -因为原子的电负性在增加。负电荷是接近原子核,因此更加稳定。一个好的经验法则是,“孤对更稳定,基本就越少。这也是为什么某些物种是由酸性相邻吸电子集团。
- 第二,通过将费用分配在一个更大的体积。扩散比集中收取收取更稳定。下一行的元素周期表,例如,碱度降低为我们从F- - - - - -对氯- - - - - -对溴- - - - - -都给我- - - - - -因为这负电荷被分散到一个更大的体积(更大的原子)。更大的原子更“极化”。(注意,这个效应占主导地位而不是电负性。这也是为什么共振提供稳定的指控;分布在多个原子电荷,因此减少个人的电荷密度。(看到帖子:总之,共振)
4所示。将这些原则应用于醇的酸性
这些原则与醇怎么样?实际上很简单。因为我们永远是比较相同的原子(氧气)我们不需要担心周期性规律,我们只需要关注共振和相邻的吸电子集团。
醇的共轭碱是共振稳定将更多的酸性。典型的例子是环己醇和苯酚。
环己醇有pK一个一个典型的酒精(16)。的pK一个然而,苯酚10。我们来看看:
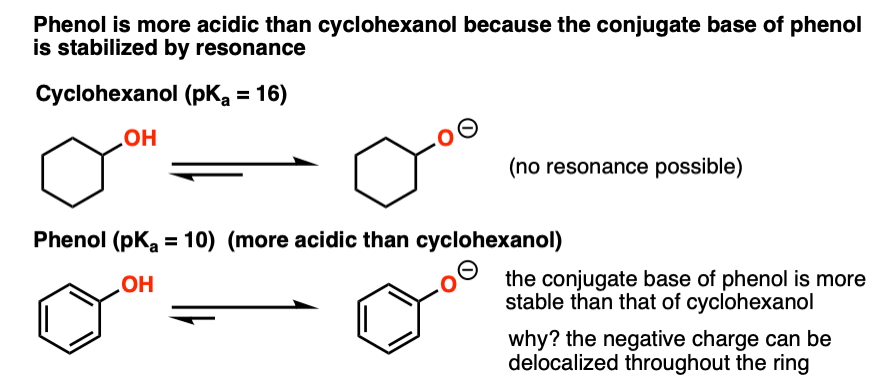
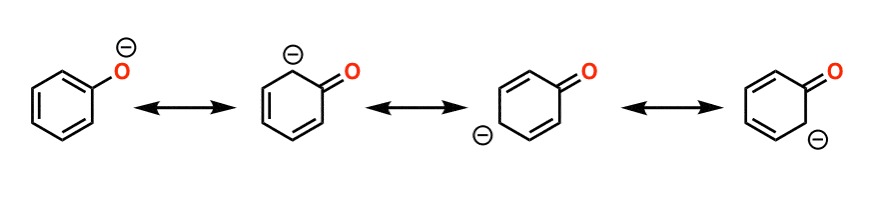
看看,负电荷的氧酚可以“离域”回戒指吗?这意味着收费可以分散在整个分子中,稳定。稳定的任何因素共轭碱会增加酸度。
这是另一个例子。比较乙醇(pK一个16)2,2,2-trifluoroethanol (pK一个12)。你为什么认为trifluoroethanol酸性更强吗?
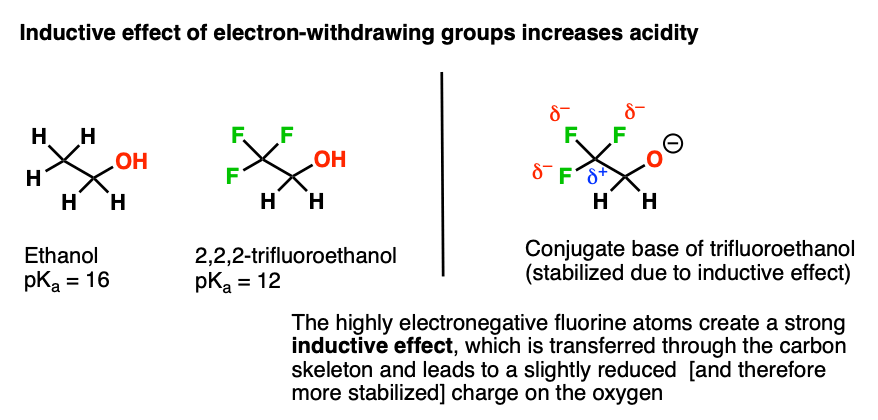
比较他们的共轭基地。氟在这里做的是什么共轭碱更稳定?
这是一个一个的例子诱导效应。氟,电子密度高电负性,把邻近的碳。碳,目前电子差,隔壁的碳的电子密度。碳,有点电子差,可以把一些电子密度远离氧气。
最终的结果是,氧的电子密度较低,稳定。再一次,稳定共轭碱- >增加酸度。
(年代情感表达:酸性越强,较弱的共轭碱)
如果我们比较这同样适用酒精变化,改变哦和氟原子之间的距离。
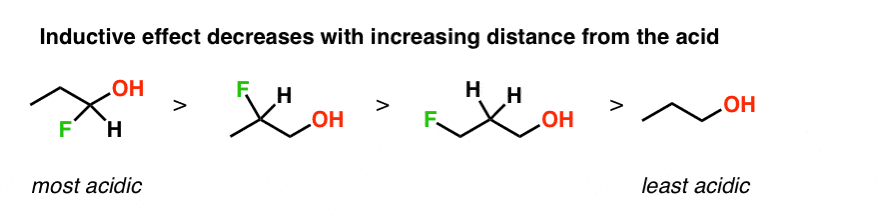
这是因为诱导效应减少大小越远我们从原子的电负性。
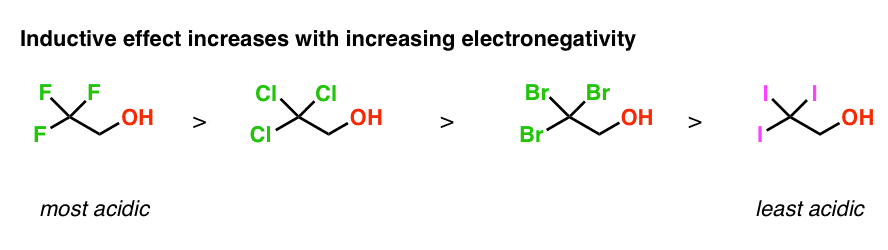
我们还可以使用电负性的趋势来确定在这些分子的酸度。因为氟原子的电负性比氯比溴电负性更强的电负性比碘、CF的诱导效应将最高3和最低的词3。
5。一个实践的问题
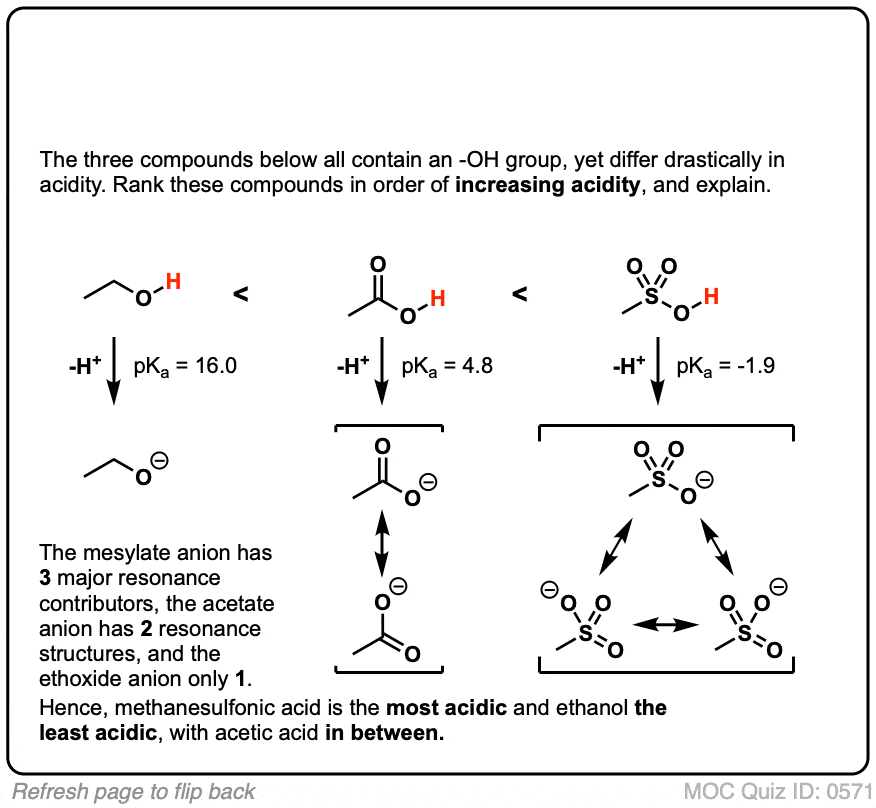
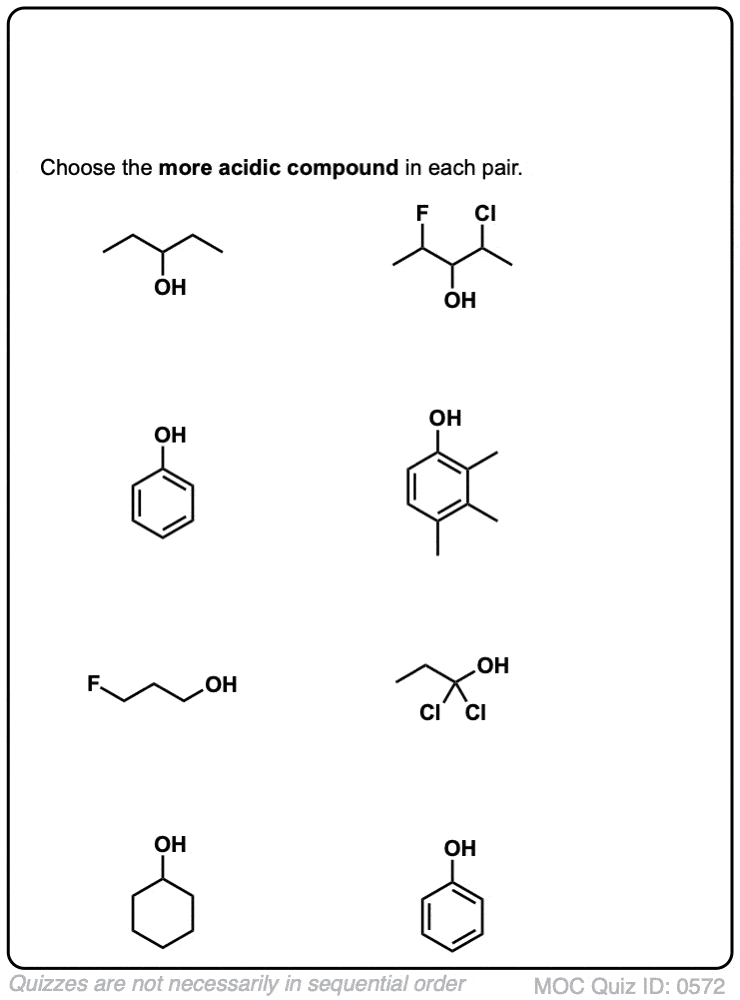
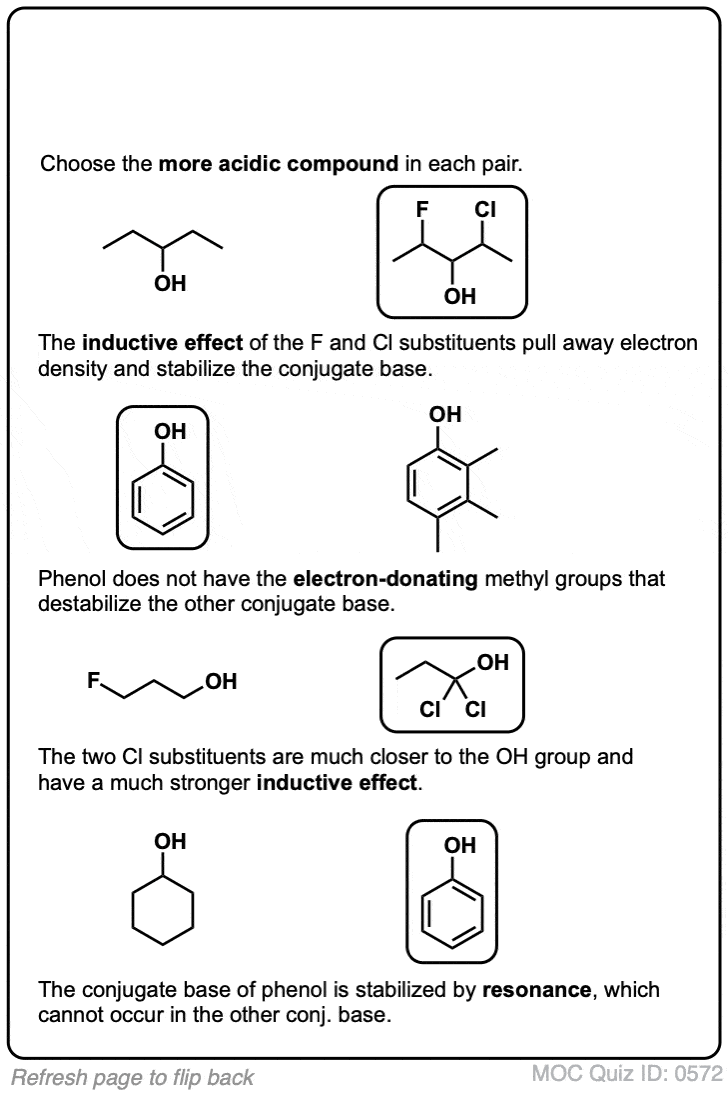
最后,最后一个例子。我们甚至可以想到的例子,这两个效果相结合:
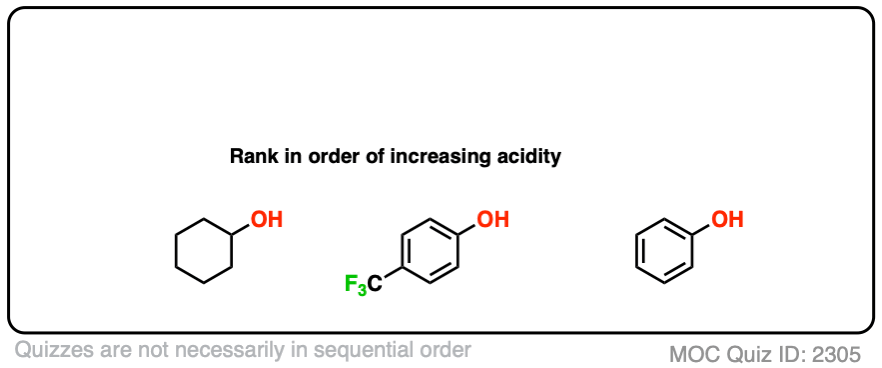 点击翻转
点击翻转
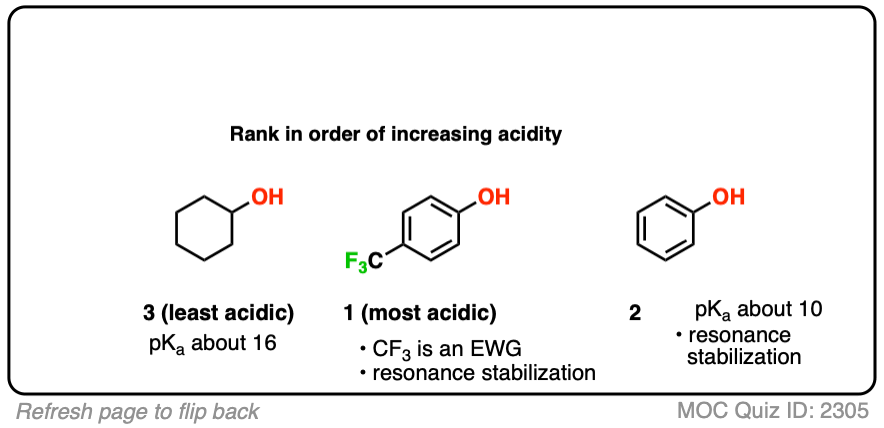
你认为哪个可能是酸性最强吗?
6。摘要:酸性醇
现在我们已经介绍了醇酸的管理的关键因素,我们更准备的细节他们不同的反应。在下一篇文章我们将讨论的酸度和碱度如何影响我们可以使用的反应条件。
醇类,因为我们总是处理氧气,这里唯一的相关因素共振和电子撤回组。
在下一篇文章- - - - - -威廉姆森醚合成
笔记
测试你自己!
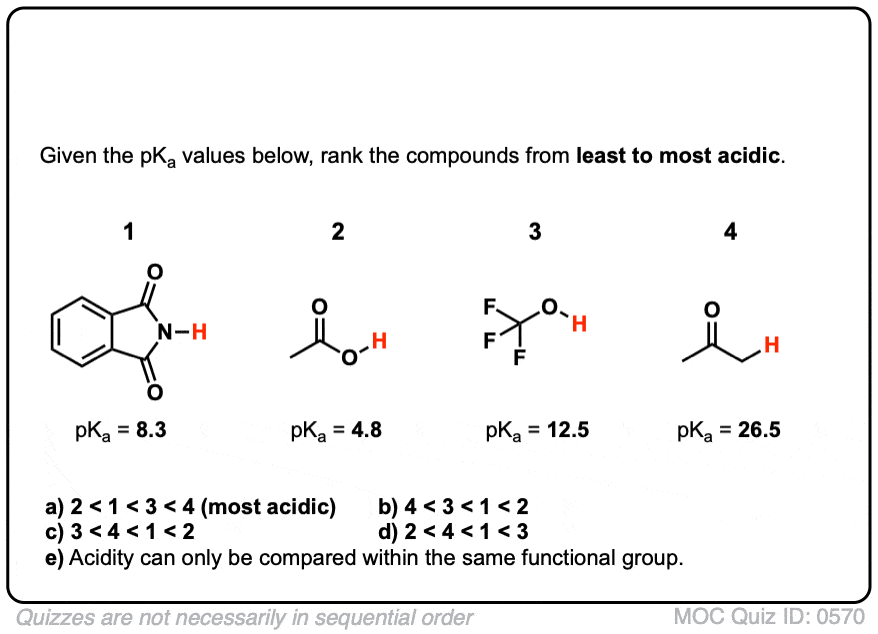 点击翻转
点击翻转
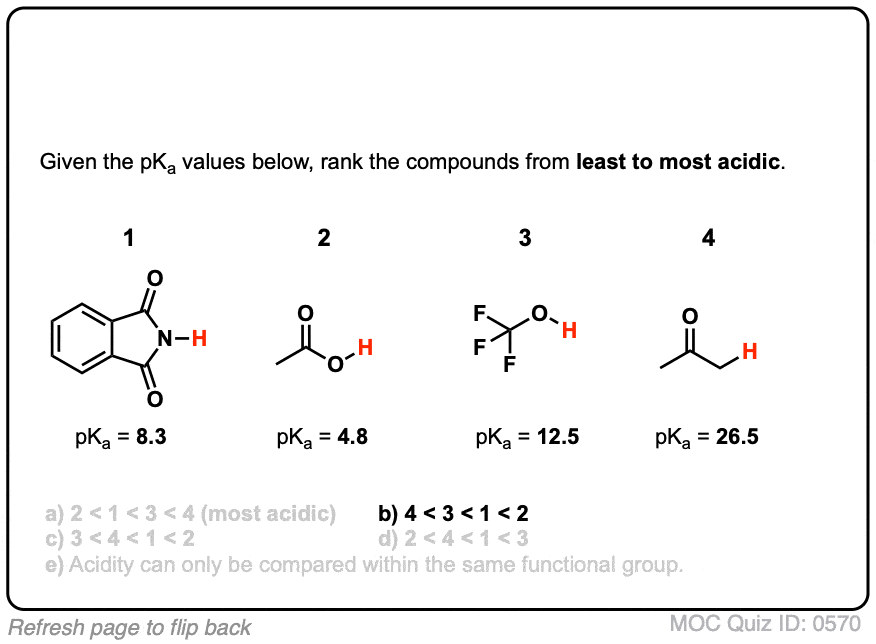
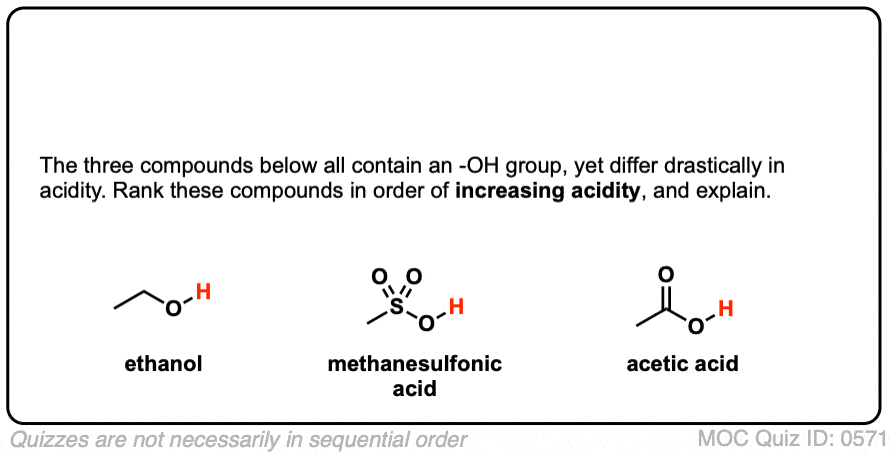 点击翻转
点击翻转
 点击翻转
点击翻转
(高级)引用和进一步阅读
1。Acidity-Basicity收集数据
这个网站大学的爱沙尼亚有大量策划的研究各种有机化合物的酸度和碱度。
这是一个领导参考。这些pK一个价值观是指乙腈作为溶剂,因此将大大不同于以水溶液,尽管总体趋势将是相同的。
2。酸的优势乙腈
a . Kutt s Tshepelevitsh j .个味儿,m . Lokov·卡,,塞尔伯格(s . Selberg)如此Leito
欧元。j . Org。化学。2021年,2021年,1407年。
DOI:doi.org/10.1002/ejoc.202001649
(开放)
虽然有些人可能认为的不同酸度trichloro v trifluoroethanol是微不足道的,我认为这是一种常态。谁能给我一个例子的氟取代基是一个更好的电子比氯弃权者,除了简单介绍酸。如果您希望将简单介绍酸,那么请解释代替乙酸的取代基的酸性酸类。
纠正我如果我有错误的人,但是我相信你已经10多年来评论这个话题。你有一篇文章,你会建议我可以直接我的读者,这样他们可以更全面地了解这一点。谢谢你!
这是伟大的概念网站给适当的guidness和理解的反应。大大感谢先生.excellent工作
Esterification-hydrolysis绝对是一个平衡。如果你不开车的反应你在中间。
我认为它不是一个纯粹的酸碱反应,但绝对是一个酸碱成分在里面,这就是为什么你需要一个酸或碱至少开始。
但是我明白你的意思,如果你有一个简单的酸碱反应在关闭容器,它是正确的。
我有一个更严重的问题(我不是一个化学家)。
费歇尔酯化反应中,第一步是氧气的羰基质子化作用。我认为这一步是非常不利的。它移动量平衡一个烯醇,或考虑的pKa RCO2H2 +这将是一个非常强大的酸。
我的第一个问题是:
我们为什么不先做亲核试剂进攻,和质子化作用后的O -。它看起来更有利。
我的第二个问题是:
化学家们似乎没有问题做一个烷氧基负离子离开四面体中间,但它似乎是一个巨大的错误进行羟基阴离子离开。为什么?
他们的共轭酸的酸度系数是相同的。
注意:你的网站是美妙的。
我不相信我们应该学习:
更强的酸+基地- >弱酸性+基地
这取决于其他因素。
例如:
酯的水解。你开始与水(pKa = 16)和一个与羧酸酯,最终(pKa = 4)和酒精。
或者你留下一个不错的周五晚上一杯酒醋周六上午。
酯水解(和它的反面,费舍尔酯化)不是酸碱平衡。这篇文章是关于简单的酸碱反应,氢的只有债券形成和破坏。
更重要的是酸性烯烃或酒精?
你认为,基于pKa表吗?
你说,在醇的酸性;更稳定的醇盐离子形成(通过感应效果等),意味着更多的酸性是酒精。
确定,但你会得到的趋势并不是类似于数据发现在气相反对数据发现的解决方案。
醇的酸性主要是因为polarizibility和溶剂化作用。
来源:https://chem.libretexts.org/Textbook_Maps/Organic_Chemistry/Supplemental_Modules_ (Organic_Chemistry) /醇/ Properties_of_Alcohols / Acidities_of_Alcohols
和
有机化学(第六版)由罗伯特·桑顿莫里森博伊德和罗伯特·尼尔森(Pg。228]
嗨——我假设我们正在处理液相化学气相。任何引用pKa值引用水和/或DMSO溶剂。
问题. .除了溶剂影响电负性到底如何突然优先于极化率在稳定负电荷和增加的酸性羟基功能? ?对此我很困惑。我了解极化率优先由于分布式的大原子的稳定性,可以进一步证明极化率和这里的稳定的影响通过事实电子所需的时间环游较大的原子创建一个更大的偶极矩,因此更大的部分。然而,开始一个新的句子,电负性越高(由于更高的吸引力通过closness反对指控)产生较小的卤化物主要问题可以b合理的电子撤回碳和氧因此稳定阴离子从这两点电负性,和极化率。然后我想回答我的问题,但引发了极化率实际上优先于哪里? ?
任何有意义的方式来分散电荷密度(例如共振或“极化率”)优先。
例如,苯酚(最右边的分子在问题上面的结论),由于共振结构的pka 10。数百倍的酸性比2,2,2-trifluoroethanol,酒精3氟原子作为一个例子用于上面的诱导效应。恶的感应能力,但共振仍是更重要的。
极化率的另一个例子:主要醇(集团)四处pka 16虽然主要硫醇(SH组)10 -一百万倍左右的pka酸性更强。
只是小心如果你“电子云的极化率”指的是稳定,如烷基链(我敢肯定这是超共轭现象),而不是“极化率”稳定碘或硫化共轭碱(很确定这只是一个shell或尺寸效应)。前者效果弱(+ 1 pka)及其趋势反转在水与气相(例如水>甲醇>乙醇),因为溶剂效应对其进行压制。趋势从后者的效果(如氢卤酸强度或水和硫化氢)之间得不到扭转,水,气相。
订单在你的第二rank-the-acidity是不正确的。这将是正确的如果电负性是唯一的球员排名酸度,但事实并非如此。卤素也因素的大小在这里…蔓延出电荷增加…即酸度。为什么高频弱酸盐酸…< <哈佛商业评论<嗨…因此,排名2,2,2 trifolorethanol应该逆转…2,2,2 trifolorethanol(弱)< 2 2 2 tricholor等等…pka triflorethanol是~ 12.46 . .pka tricholorethanol ~ 12.02
这里我很好奇. .我发了一个关于电负性与极化率问题。我能理解极化率较大的卤素产生较强的酸通过创建较大的偶极矩或小卤素的事实,高电负性(相反电荷的亲密)撤回电子更强烈,但是条件(如溶剂)很可能会决定反应性物种的问题? ?我看到它说,极化率需要管理然而,正如你所说,他反对酸度趋势在示例中显示。有环境条件我俯瞰,不是说为了证明这个吗? ?或者特征哦双保税氧气贡献? ?
你回答正确的人在一个点和错误的一切。2,2,酸性2-trichloroethanol确实比2,2,2-trifluoroethanol。
然而,很小的区别:12.24 vs 12.46 pka,分别。
此外,除了2,2,2-trichloroethanol,模式实际上是正确的。它不应该完全逆转喜欢你回答的人。2,2,2-tribromoethanol时钟在12.7 pka,按照模式,和2,2,2-triiodoethanol没有测量到我能找到。
最后,这里的机制在起作用的极化率无关上下文你习惯或任何与氢卤酸,高频,HCl,哈佛商业评论,你好。较大分子的极化率是相关的为你解释分子间作用力(诱导偶极吸引力)。卤素阴离子的稳定性(共轭碱的氢卤酸)与电荷密度。氟很小,所以携带负电荷本身集中负电荷在非常小的空间与其他电子,导致排斥和不稳定的交互。在碘,单一的额外的电子分布在一个更大的体积,减少不稳定交互。这与轨道重叠(HSAB理论-传统上覆盖着你的第一个无机化学课程)应该或多或少占氢卤酸pka的差异。
老实说,顺着这页的建议和忽略的专门性2,2,2-trichloroethanol。0.3 pka的差异非常小,它会涉及到复杂的多种变量分析查明原因,所以没有办法出现在考试中,期望你知道除了2,2,2-trichloroethanol。
谢谢你,布莱斯!
积极影响的效果是什么类型的归纳影响酒精的酸度和碱度胺
很神奇的。重新打开我的心灵的有机化学。
我有一个问题。你认为酸性/碱性是相关的1 h NMR化学位移?专门为质子化了的氨基酸。
谢谢。
关于苯酚和环己醇的例子,因为大多数共振破环的芳香性,形式电荷离域仍然足够重要,使其更稳定的共轭碱吗?
对不起,但是我有一个问题为什么主>二级>三级>醇在酸性秩序
谢谢你!
思考如何影响酒精的electron-richness烷基组,相对于氢。他们是电子给体和电子受体吗?他们更富电子或少电子富有吗?的关键影响因素之一的酸度是共轭碱的稳定性,在这种情况下将是一个醇盐(O)。氧气已经有一个负电荷。负电荷将电子给体做什么?让它更大或更小的?你认为更稳定,更大的费用,或一个较小的费用?如果电荷不太稳定,这意味着共轭碱会更基本,这意味着父酸性酒精会减少。
这是一个优秀的写。我有机化学教材甚至不是这么详细。
很高兴你发现它有用的克拉伦斯!
thanku !这是真的帮助我度过我称MCAT:)
只是一个词这样非常棒!真的有用!你救了我的人:-)
谢谢你分享这篇文章。这是非常有趣的。我想听到你更多的消息。
我很抱歉如果我说错了,但不是乙醇的pKa接近16(15.9是最引用值)?
也“原子核的电负性是提高”和“带负电荷的氧气trifluoroethanol将有氟原子的电荷重新分配”本科生可能有点难以理解。也许一点点的细化和/或描述可能在秩序。
再一次谢谢你。固定的。我在你的债务为你优秀的建议。
谢谢mamid……我本科,老实说我还是听不懂的一些短语被用来解释
对酸度的影响是什么积极作用的酒精(哦)