烯醇、烯醇化物
动力学和热力学烯醇化物
最后更新:2023年5月25日|
动力学和热力学酮的烯醇化物
烯醇化物有很多共同点烯烃。他们是公寓,有一个碳碳π键。
- 扎伊采夫规则提醒我们,烯烃稳定增加而增加碳原子直接相连烯烃(即“替换”烯烃更稳定)。
- 烯醇化物形成强大时,(如氢氧化钠或NaOCH non-bulky基地3)的倾向更多的代替烯醇化物形成。当烯醇化物与亲电试剂反应,这意味着亲电试剂将添加到更多的代替α碳。
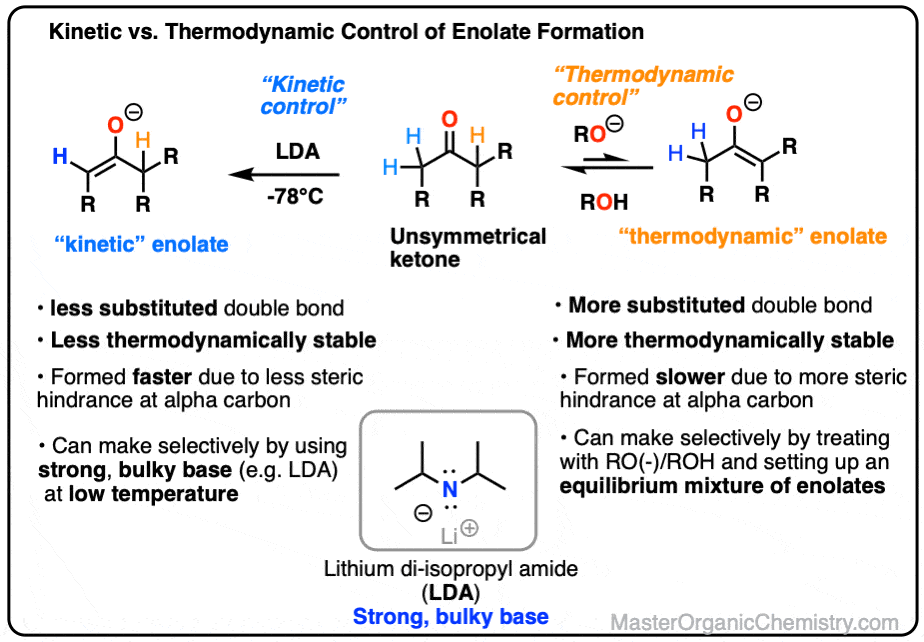
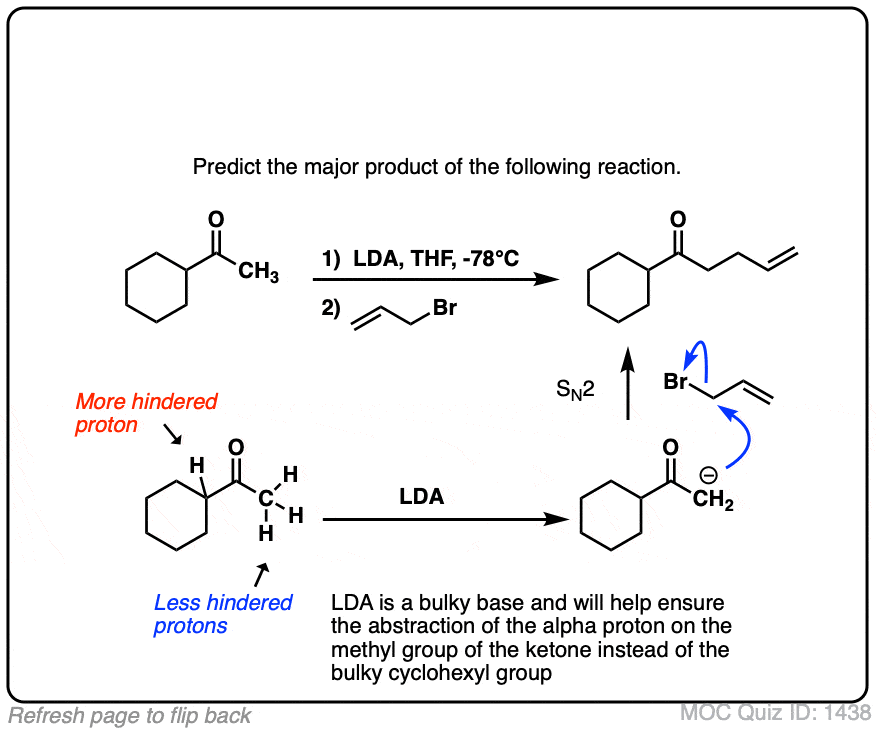
- 我们可以克服这种倾向的烯醇化物通过使用一个强大的、笨重的基础等乔治。(锂di-isopropylamide)与位阻越少质子反应速度比它更多的位阻质子。
- 这种“替换”烯醇化物被称为“动能烯醇化物”。
表的内容
1。热力学烯醇化物形成
如果你不熟悉烯醇化物和需要更多的背景,回过头去看以前的文章在烯醇化物。(参见:烯醇化物]
许多酮能够形成两个不同的烯醇化物,这取决于α碳deprotonated。
问题是,会喜欢哪一个?
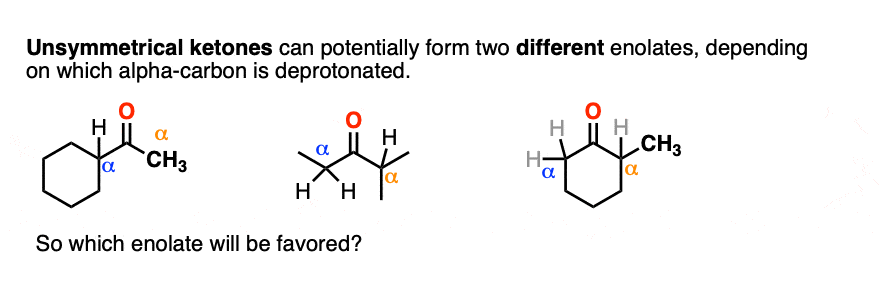
通常烯醇化物平和可以被认为是类似的烯烃,即使他们倾向于与亲电试剂反应负碳离子。
回到扎伊采夫规则,我们看到很多例子烯烃增加稳定性的数量H直接连接到环原子减少。(或者相反,附碳原子数量的增加)
这也适用于烯醇化物。碳氢键越少的烯烃,越热稳定。
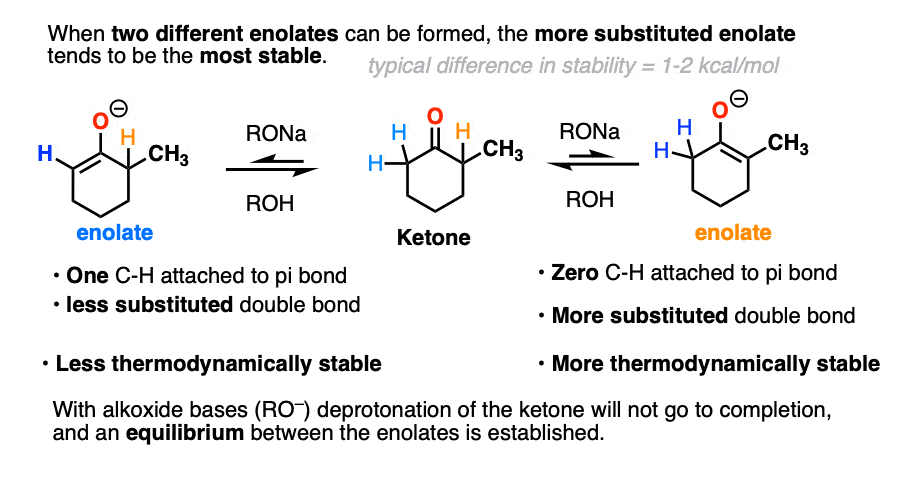
酮发生去质子化能与强碱(如醇盐RO(-)给烯醇化物。
醇盐不是基本一样酮烯醇化物,所以酸碱平衡倾向于开始酮。然而,他们仍然是建立一个足够强大的基地平衡之间的开始酮和两个不同的烯醇化物。
热力学平衡的位置,将有利于最稳定烯醇化物(即最代替),即使它有点慢形成由于碳氢键是更多的位阻。
因为这个原因我们调用更多的替代烯醇化物的热力学烯醇化物因为它更大的稳定性。
我们也说这的形成烯醇化物正在热力学控制。
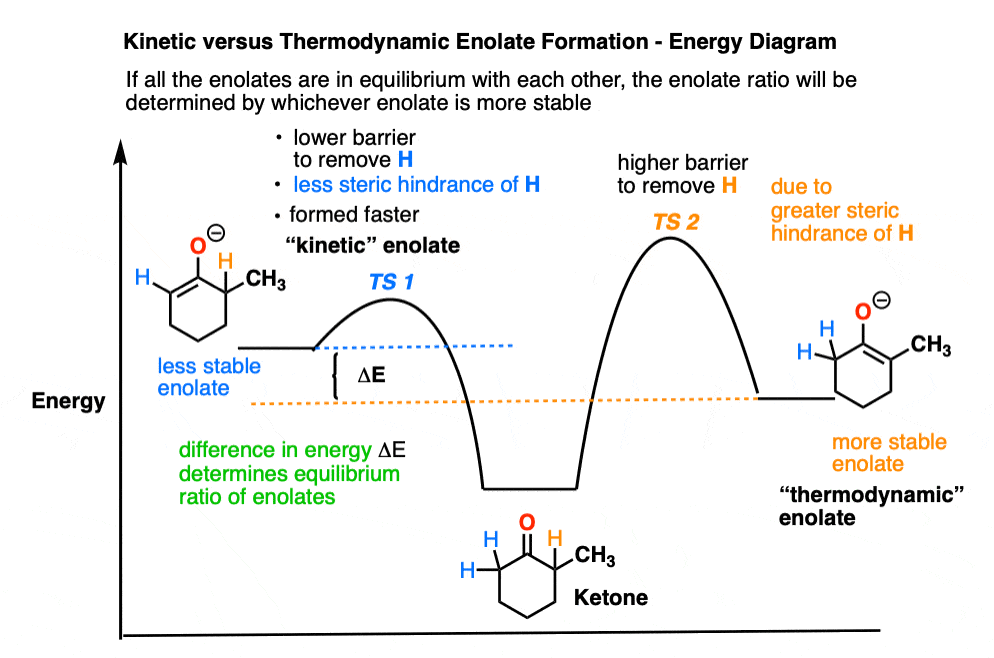
烯醇化物的平衡率将取决于能量的生成热之间的差异(通常是1 - 2千卡每摩尔)。作为一个粗略的经验规则,4:1是个好大概的数量,但可能会有很大差别。(注2]
2。反应热力学的烯醇化物
这些“热力学”在不同的烯醇化物可以作为亲核试剂反应。
任何时候我们形成一个烯醇化物热力学控制,我们应该期待主要产品将会出现的反应更多的代替烯醇化物与亲电试剂,比如在这卤化反应。(注3]
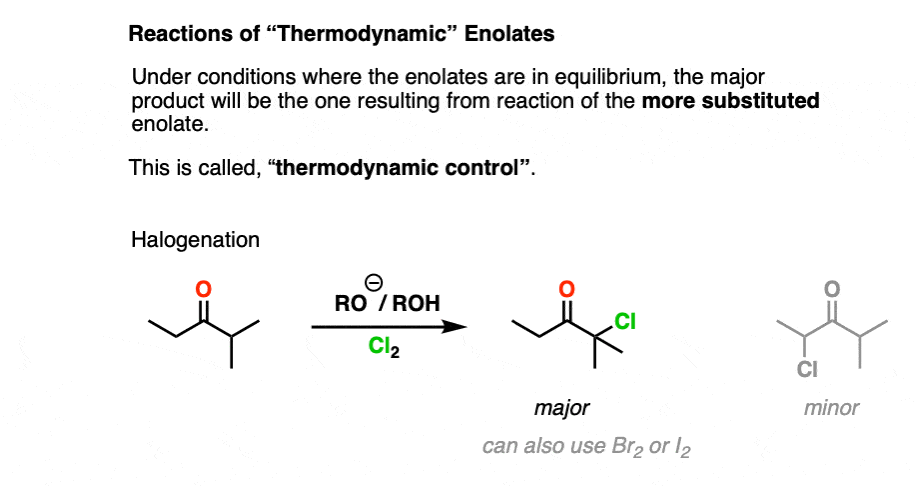
同样的,这种情况也会在这些例子中醇醛的反应,烯醇化物烷基化和共轭加成。(注意4]
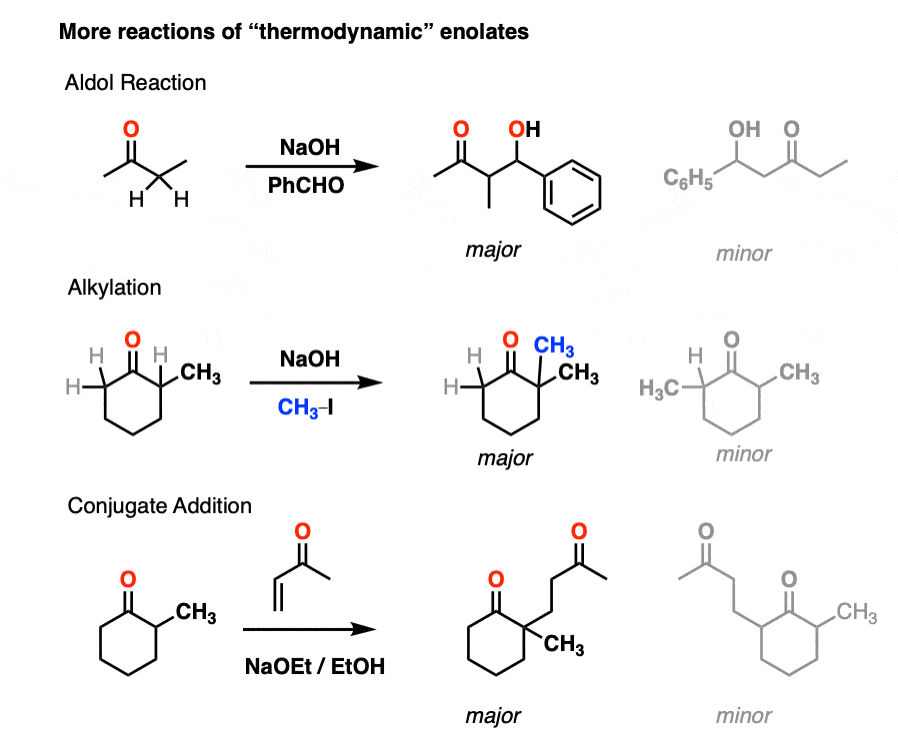
你可能会问,“是它吗?”
我们注定了热力学的偏好吗烯醇化物来从来没有能够形成其他代替烯醇化物,只是因为它尖叫。”从热力学角度来看,我不想!”。
没有!有一个解决方案!
3所示。选择性动能烯醇化物的形成
有很多时候我们可能希望less-substituted烯醇化物。这里是如何使它的策略。
首先要注意的是,氢取代基更多的一面更难以访问由于的存在额外的烷基集团。
这就是为什么有一个更高能量势垒去质子化的能量图(见上图)。
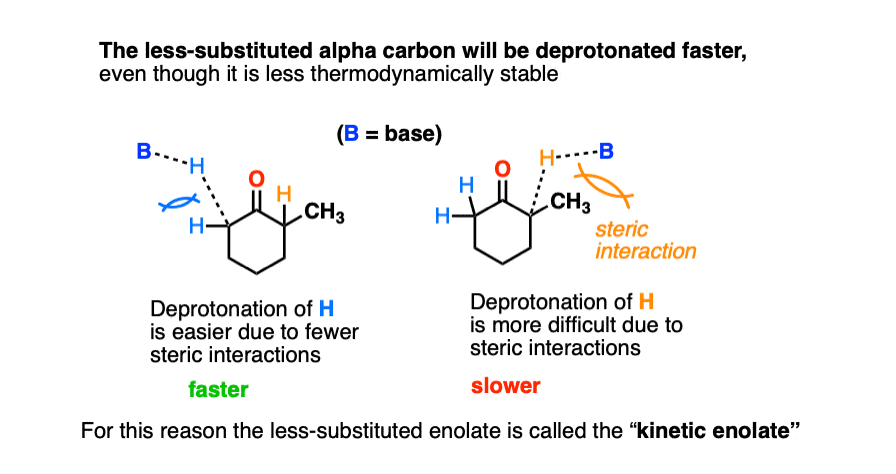
所以如果我们使用基础十分位阻吗?
在这种情况下的反应位阻质子应该非常慢和反应少位阻质子在另一边快。
一个不错的选择,这是一个强大的笨重的基础,di-isopropyl锂酰胺(乔治。)。
乔治。有两只又大又笨重的吗异丙基组织在一个非常基本的侧面酰胺基地。的pK一个的共轭酸是38,所以deprotonating酮α碳(pK一个16日至18日)是没有问题的乔治。。
同时,与醇盐基地RO(-),去质子化去完成。只要使用过多的基础,没有不同的烯醇化物之间的平衡。(注5]
乔治。是如此强大,去质子化可以在极低的温度下发生。这帮助我们,因为我们可以用低温慢下来,更不受欢迎的酸碱反应。
所以,当我们酮是处理乔治。在较低的温度下得到优惠less-substituted的形成烯醇化物。我们叫这个。”动力学控制”。
请注意,没有什么魔法-78°C。这恰好是方便和便宜的温度干冰丙酮冷却槽。
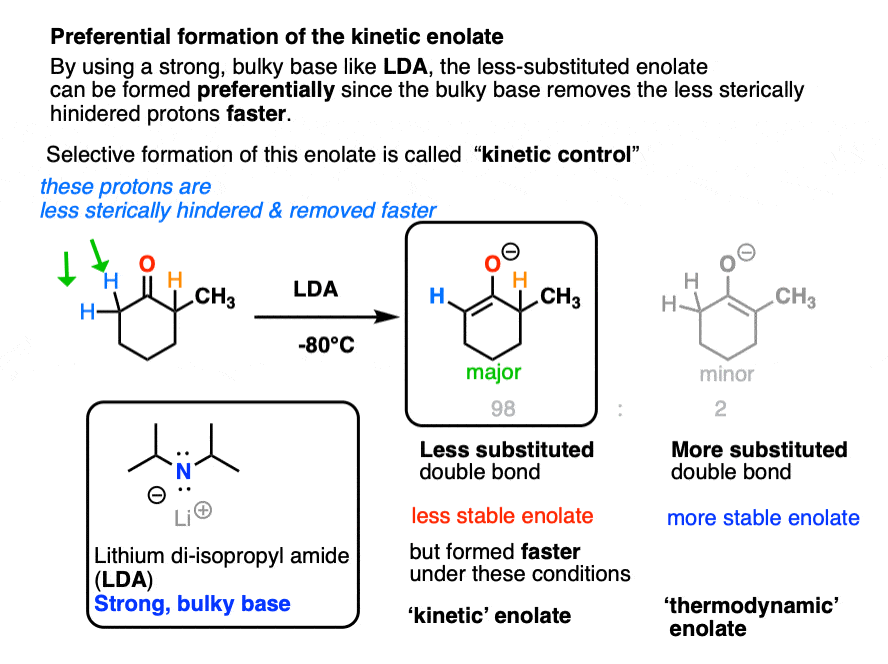
我们称之为代替越少烯醇化物“动能烯醇化物“因为我们是根据反应速率的差异(“化学动力学”还记得选择性?)给我们。
请注意,烯胺还可以用于执行less-substituted反应α碳。(注6]
4所示。反应动力学的烯醇化物
动能烯醇化物可用于相同反应的烯醇化物我们之前提到的,如烷基化、醇醛反应,卤化。
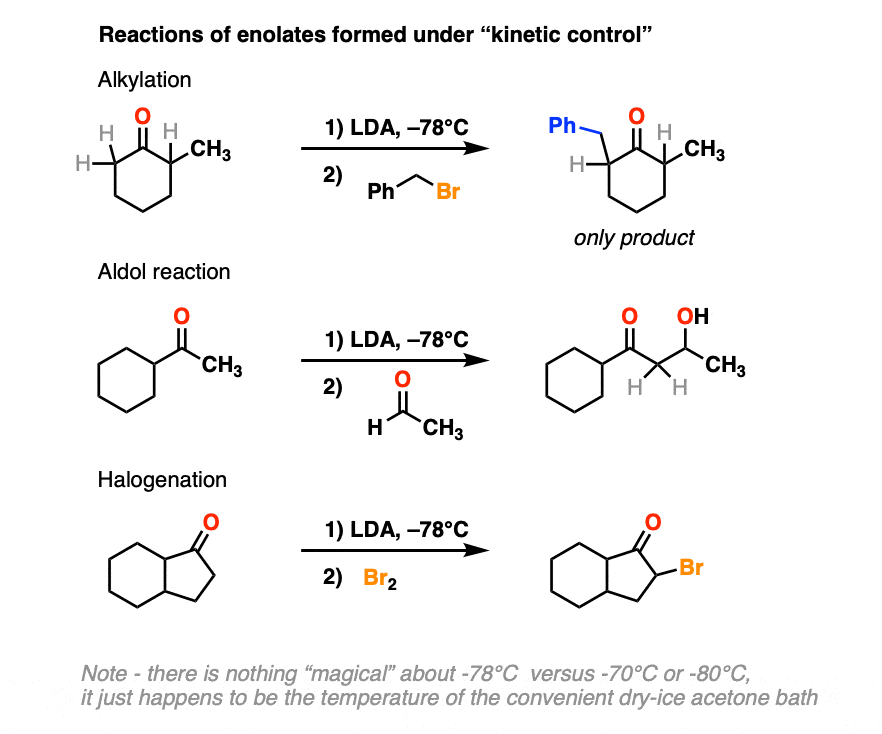
5。LDA的进一步冒险
还有另一个优势乔治。。自乔治。是这样一个强大的基础,我们可以使用它的一些更不容易烯醇化物的羧酸衍生品等酯类、酰胺和腈。
这些烯醇化物可以执行相同的类型的反应正如上面那些我们已经看到的,如烷基化和共轭加成。
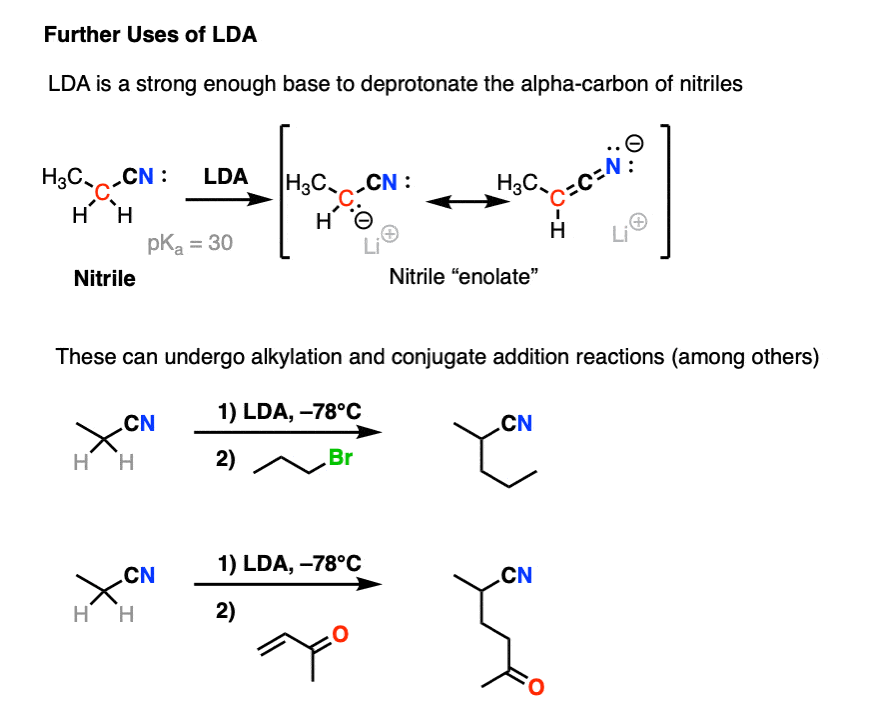
简而言之,乔治。是一个非常有用的强碱,能形成任何烯醇化物你需要的,提供的碳氢键不是位阻。(请注意7]
6。总结
我们学到了什么?
- 不对称酮能够形成两种不同的烯醇化物
- 当醇盐使用基地(RO - /卢武铉)有不完整的去质子化。因此,一个平衡之间存在的起始酮和两个可能烯醇化物
- 平衡通常更喜欢更多的代替烯醇化物因为你可以把它作为一个多取代双键。因为这个原因代替烯醇化物被称为热力学烯醇化物。
- 通过使用强大的笨重的基础,更多的去质子化的替代率烯醇化物只能放缓,less-substituted吗烯醇化物形式。这被称为动能烯醇化物。
- 乔治。(锂二异丙基酰胺)是一个强大的、笨重的基础,可用于酮的去质子化,酯类酰胺,腈,等等。
笔记
注1。一个粗略的经验法则是,每个碳氢键代替碳碳让你额外的1千卡每摩尔的稳定。这可能听起来不算很多,但即使是1千卡每摩尔足以给你关于80:20平衡率。
注2。“它可以相差很大”。典型的热力学的比例:动能烯醇化物在“热力学条件”(NaOR /卢武铉)约为4:1,但可以明显大于。碱金属的身份抗衡离子可以有巨大的作用。第二页的这篇文章在形成热力学烯醇化物提供了一个很好的概述。
注3。这反应很难控制!在热力学条件下一个问题与卤化酮(RO(-) /卢武铉)卤化产品是酸性更强比开始的酮。这很可能导致多个卤化,如卤仿反应。
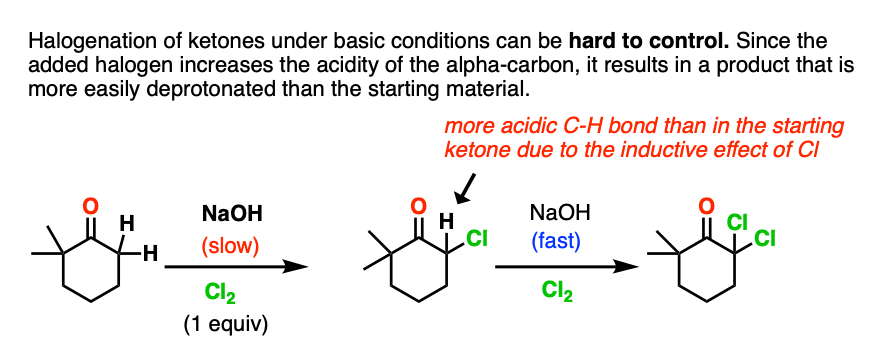
注4。更多的烷基化酮在热力学条件下,明白了这个经典的研究。原来的反应酮NaOR / CH3我确实把CH3的替换烯醇化物(在41%的收益率),但是由于over-alkylation有很多副产品。对这门课的目的,这就是为什么程序一样乙酰乙酸酯合成是首选烯醇化物烷基化。
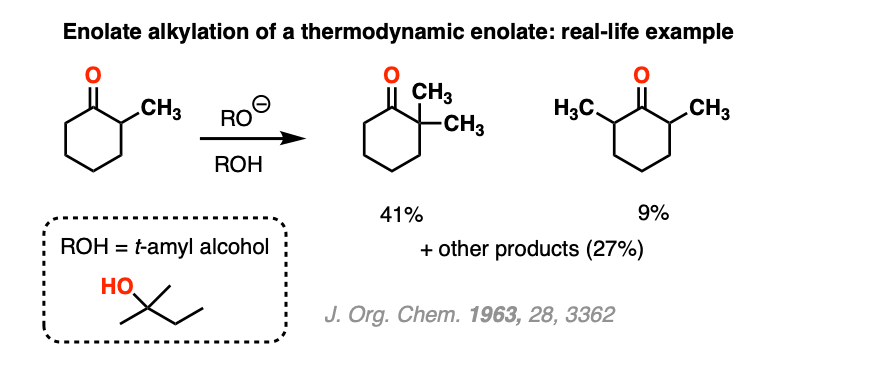
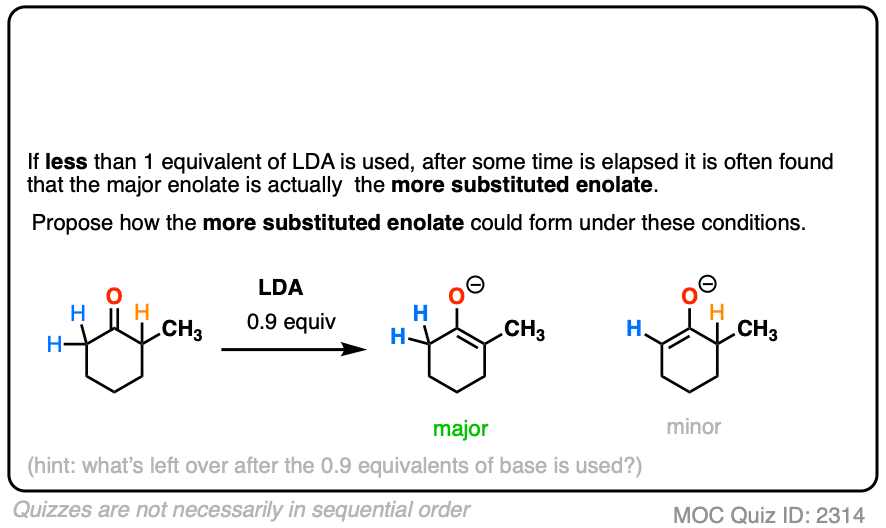
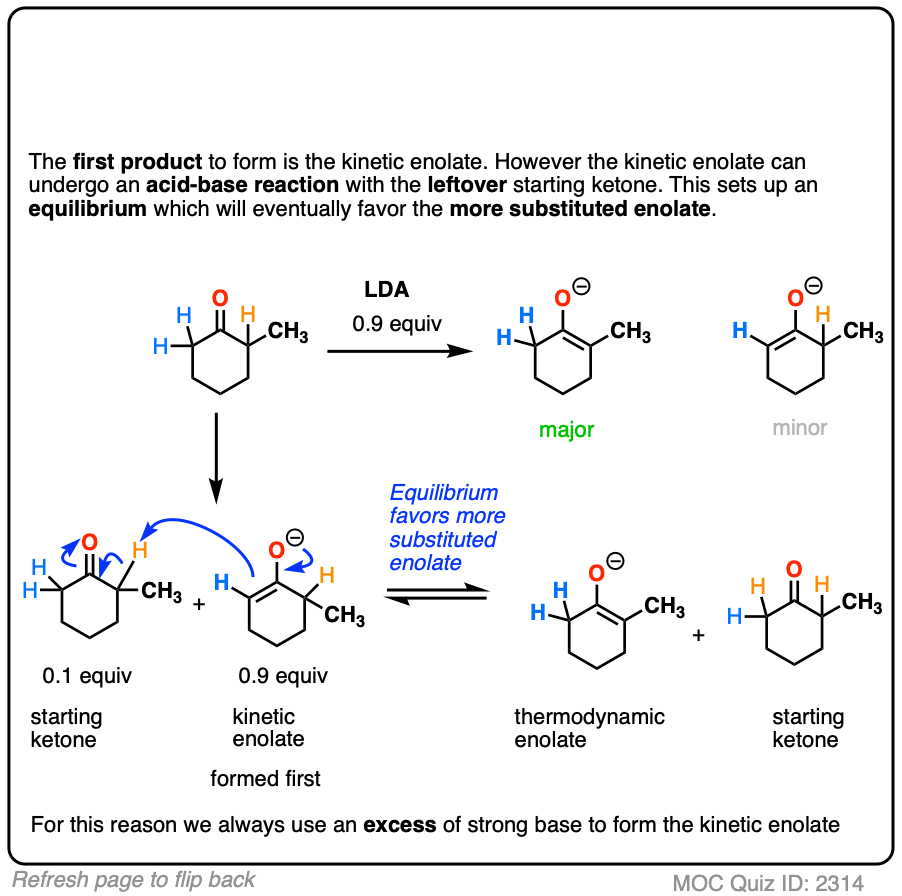
注5。烯醇化物之间的“不平衡”。如果小于1相当于使用强碱,最终有可能与热力学烯醇化物过了一段时间已经流逝。
 点击翻转
点击翻转
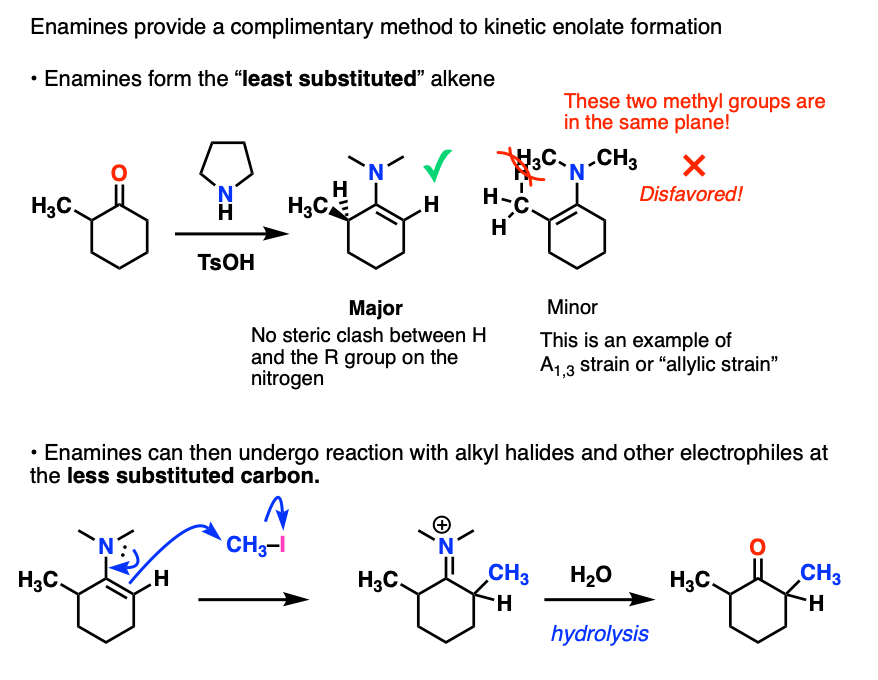
注6。动能的替代品烯醇化物是形式形成烯胺往往倾向于less-substituted烯烃。
请注意7。乔治。对醛的去质子化并不是特别有用。它会执行亲核加成相反。
测试你自己!
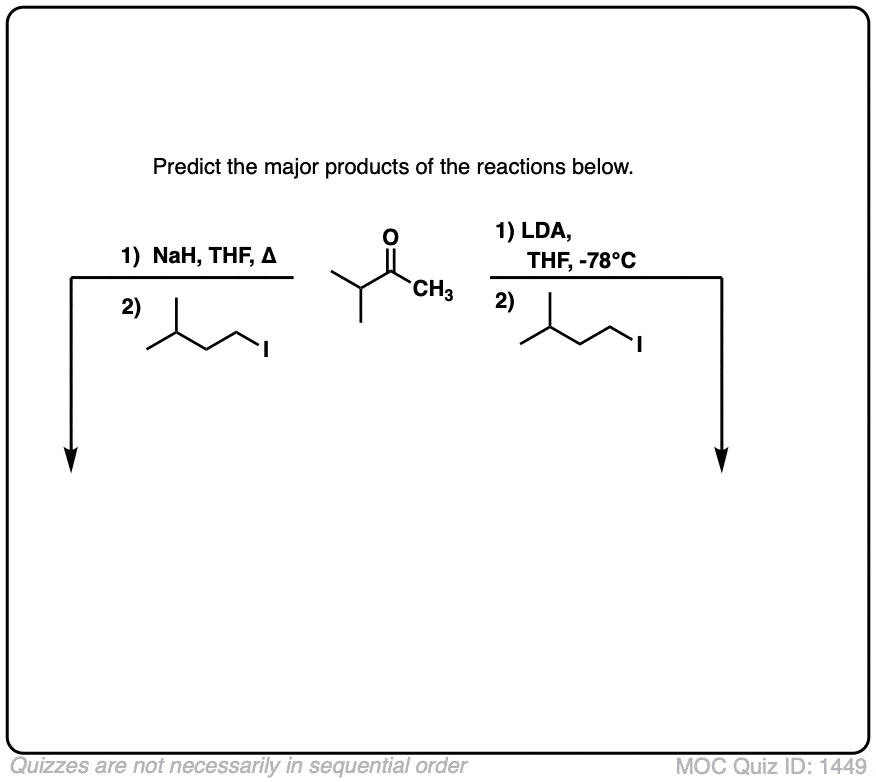 点击翻转
点击翻转
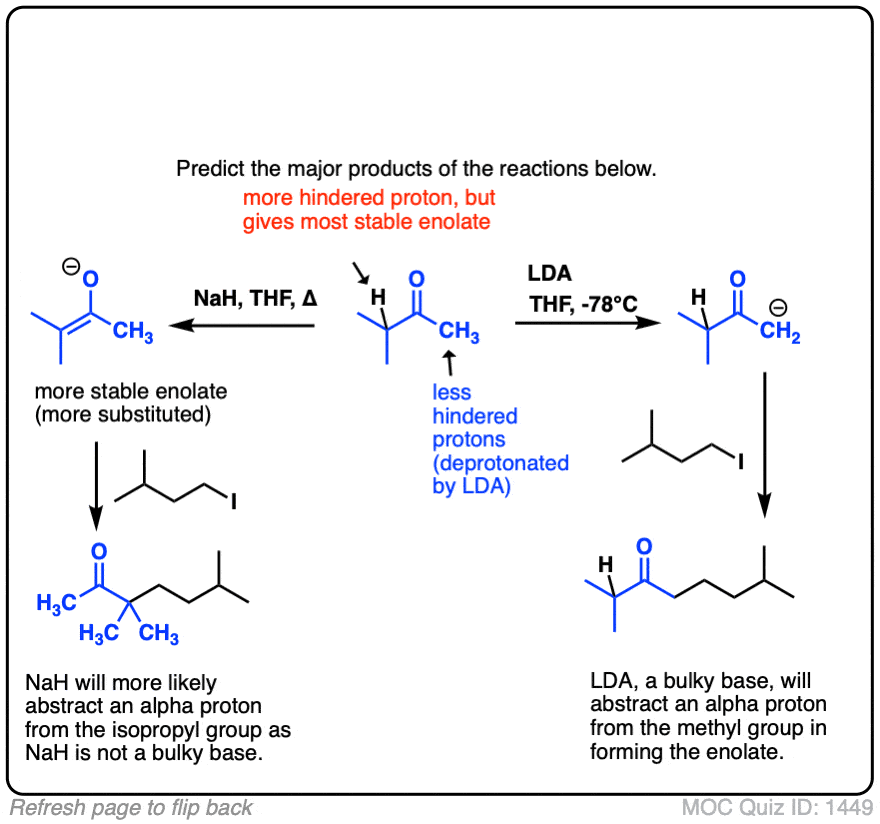
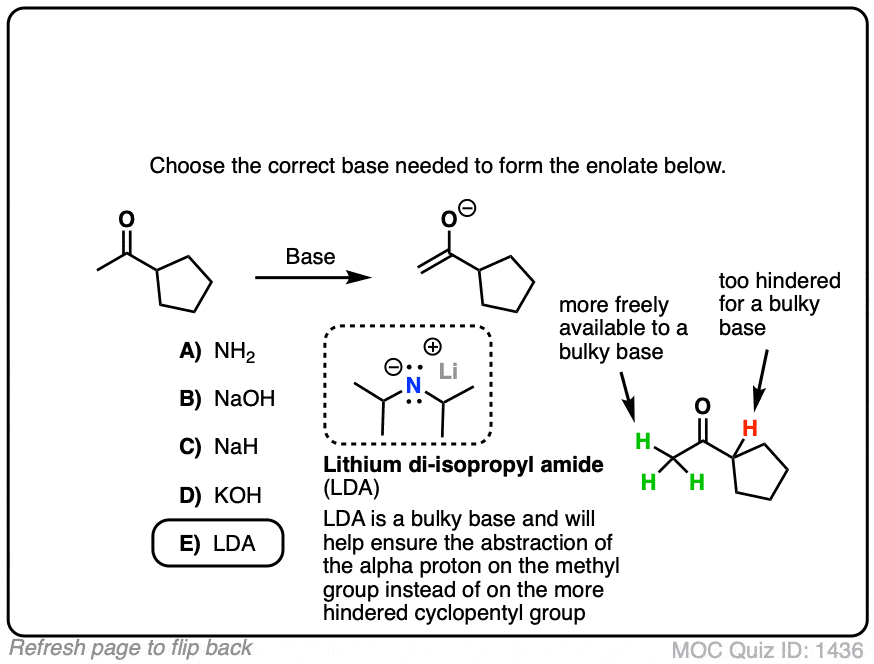 点击翻转
点击翻转
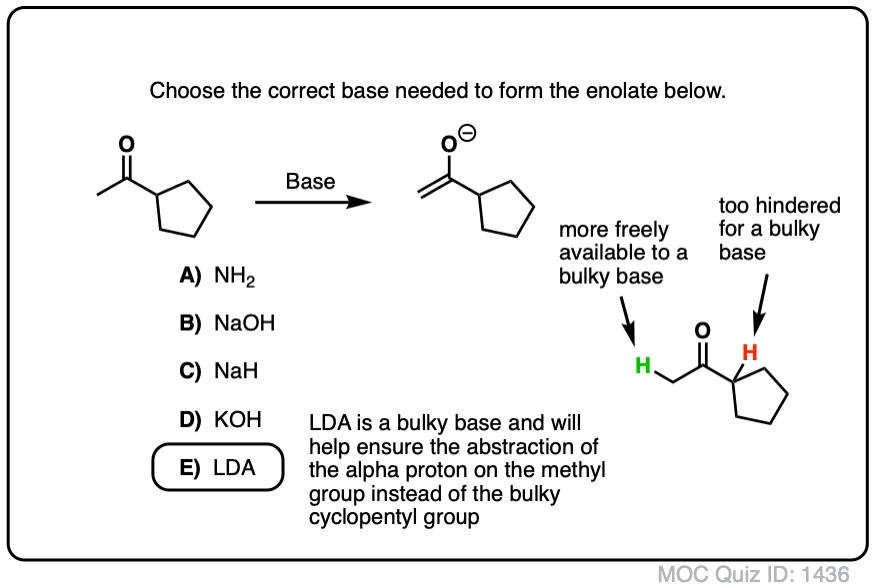
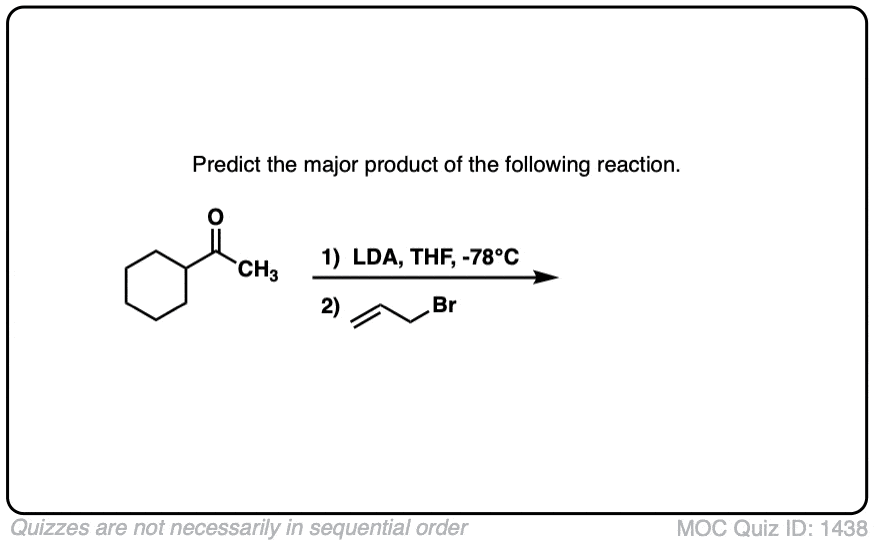 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
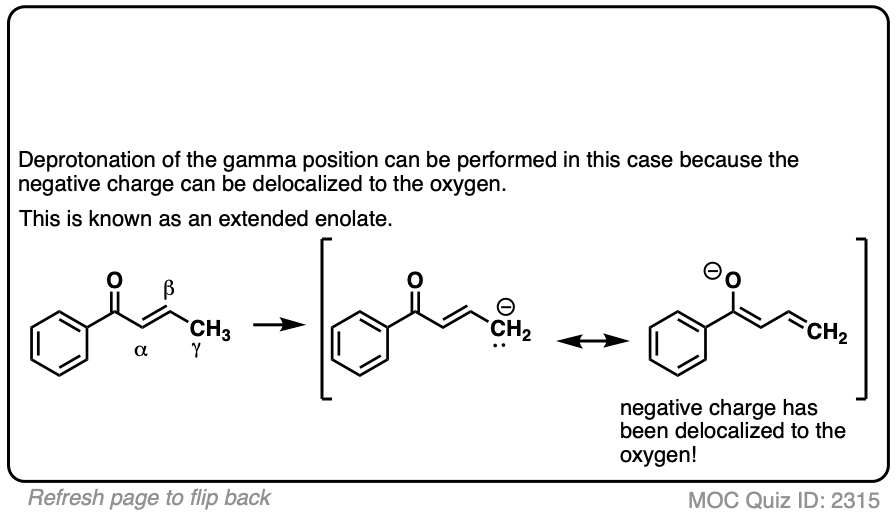
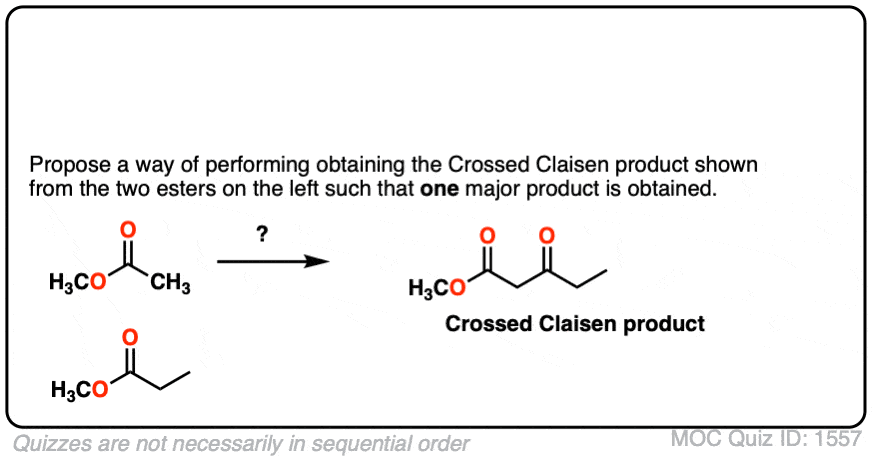 点击翻转
点击翻转
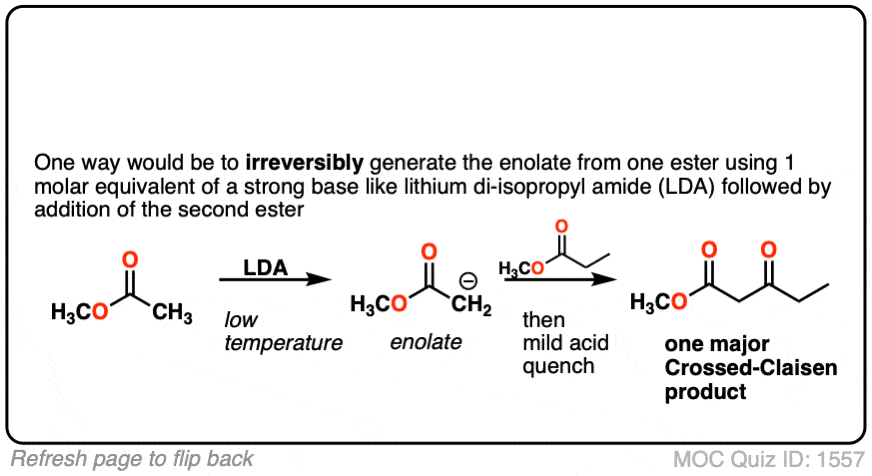
(高级)引用和进一步阅读
引用
- 具体的形成和烷基化烯醇化物阴离子的不对称酮:2 -苄2-methylcyclohexanone和2 -苄6-methylcyclohexanone
马丁胆和赫伯特·o .的房子
Org。Synth。1972年,5239岁的
DOI:10.15227 / orgsyn.052.0039
这个过程从有机合成有不对称的特定选择的烷基化的详细实验条件酮通过动能和热力学烯醇化物形成条件。 - 的烯醇化物α-ALKYLATION LITHIUM-AMMONIA还原α,β-UNSATURATED酮
吉尔伯特鹳,佩里罗森和诺曼·l .高盛
美国化学学会杂志》上1961年,83年(13),2965 - 2966
DOI:10.1021 / ja01474a051
本文的第一个动力的描述烯醇化物在文献中形成——“成功的捕获烯醇化物离子IV取决于烷基化反应速度比最初产生的平衡烯醇化物第四通过质子转移一些更稳定II最初形成中性的烷基化酮。” - 四面体报告25号:酮烯醇化物:regiospecific制备和合成的用途
吉恩·d天使
四面体1976年,32(24),2979 - 2990
DOI:10.1016 / 0040 - 4020 (76)80156 - 1
本文综述了各种方法烯醇化物形成,组成各种数据酮- - - - - -烯醇化物混合动力学和热力学条件下形成的 - 热力学和动力学控制的烯醇化物:一个项目面向问题的实验课
奥古斯汀对峙Jr .)迈克尔·a . Knopp和Jhong金姆
《化学教育1998年,75年(1),78
DOI:1021 / ed075p78
论文从j .化学。艾德。包括如何展示的概念动能和热力学烯醇化物在本科实验室会话。 - 负碳离子的化学反应。诉不对称酮的烯醇化物派生
赫伯特·o .房子和维拉Kramar
《有机化学》杂志上1963年,28(12),3362 - 3379
DOI:10.1021 / jo01047a022 - 负碳离子的化学反应。第九。钾离子和锂烯醇化物来自环酮
赫伯特·o .和Barry m . Trost房子
《有机化学》杂志上1965年30.(5),1341 - 1348
DOI:10.1021 / jo01016a001 - 动能烯醇化物形成锂Arylamide:碱度对选择性的影响
Keith Vanlandeghem Linfeng谢,库尔特·m·艾森伯格和伯尼尔卡洛琳
《有机化学》杂志上2003年,68年(2),641 - 643
DOI:10.1021 / jo0263465
本文的主题烯醇化物形成和检查的立体化学烯醇化物形成不同的性质取决于Li-amide基地。 - 一个立体选择合成(±)-gymnomitrol总额
史蒂文·c·韦尔奇,他Chayabunjonglerd
美国化学学会杂志》上1979年,101年(22),6768 - 6769
DOI:1021 / ja00516a057
这个总数的第一步合成的烷基化烯醇化物2-methylcyclohexanone,由去质子化乔治。在-78°C,紧随其后的是平衡的热力学更稳定的替代烯醇化物阴离子在室温下4 - 5小时。 - 伪麻黄碱作为一个实际的合成手性辅助光学纯度高羧酸、醇、醛、酮
安德鲁·g·迈尔斯,科比h·杨,侯,莉迪亚,麦金斯(David j . Kopecky和詹姆斯·l·格里森
美国化学学会杂志》上1997年,119年(28),6496 - 6511
DOI:1021 / ja970402f
的烯醇化物来自N-acylation伪麻黄碱可以有选择地从脸部烷基化。它是容易诱发选择性很大在一个反应比构型,和一个办法是使用手性辅助——你一个手性的支架上,附着在基板上,然后删除在你烷基化。这是一篇论文,说明实际化学——当时,更容易获得比现在,伪麻黄碱和迈尔斯(现在哈佛大学)教授广泛记录的反应和程序,以使其可再生的,健壮的,可靠的。 - 不对称烷基化反应的手性酰亚胺烯醇化物。一种实用方法拆分.alpha.-substituted的综合羧酸衍生品
d·a·埃文斯·m·d·埃尼斯,d . j . Mathre
美国化学学会杂志》上1982年,104年(6),1737 - 1739
DOI:10.1021 / ja00370a050
这是一个里程碑式的论文,埃文斯教授率先使用手性助剂和展示了他们可以用于不对称醛醇反应。这里使用的辅助是一个手性oxazolidinone,这种化学被称为“埃文斯不对称醇醛”或“埃文斯手性辅助”。
评论
评论部分