自由基反应
债券的优点和激进的稳定
最后更新:2022年9月28日|
债券的优点和激进的稳定
最后两个帖子讨论了因素稳定,破坏自由组成。那么,我们如何量化自由基稳定?需要一些谨慎看到这个请注意——但如果我们保持足够的变量不变,碳氢键的强度(“键离解的能量”,或12)是一个很好的指南碳自由基的稳定性。
表的内容
- 量化自由基稳定
- 为什么水比CH4键离解能更高吗?
- 键离解能与自由基的稳定性
- 因素1:稳定增加的顺序甲基< <二次<三级。键离解能量(12)
- 因素# 2:自由基是由共振稳定。
- 因素# 3:免费的组成是由相邻的原子稳定
- 因素# 4:在元素周期表,自由基稳定性随增加电负性
- 因素# 5:元素周期表,自由基稳定的原子尺寸增加而增加
- 因素# 6:自由基的稳定性下降的轨道接近原子核
- 因素# 7:电子撤回组织破坏自由基
- 摘要:量化自由基稳定性与邦德离解能量(12)
- 笔记
- (高级)引用和进一步阅读
1。量化自由基稳定
在最后两个帖子我们已经经历的因素影响自由基的稳定性。
底线是缺电子的激进分子帮助,任何因素捐赠装轨道电子密度,或者传播,未配对电子在一个更大的体积(a.k.。一个“delocalize” it) will stabilize the radical.
我们讨论了总共有六个因素。最初你可能会觉得很难跟踪我们提到的因素。没关系,因为有趣的是,有一个测量可以帮助我们保持所有这些因素。【编辑:我们只提供在此提供一些简单的示例)
它被称为键离解能[12]。你可能对它已经很熟悉!有可能一个表的键离解的能量在你的课本,通常在100页左右。
许多人需要一些时间才能意识到的是,12是一个测量所需的能量均裂债券乳沟,正如我们前面所讨论的,均裂债券乳沟导致自由基的形成(异种溶解的债券乳沟有机化学中更为常见,导致物种的形成至少一个带电离子[]]。
因此,12本质上是一个衡量的自由基的稳定性。(编辑:Wenthold教授指出,从分子的稳定性也是一个因素需要考虑。在本帖里,我们交易债券的简单例H不牵强附会的,但在这种情况下紧张的债券,债券被显著削弱电子排斥,或债券原子的电负性,必须改正这些因素来确定定量自由基稳定性)
这篇文章的目的是帮助连接键裂解键能的概念与自由基稳定性。
2。为什么水键离解能高于甲烷吗?
让我们来看一个快速代表例子。两个分子-甲烷(CH4)和水(H2H O)。这有较弱的债券?回想我们前面谈到的化学,如酸碱反应,难免会想说地是较弱的比碳氢键,因为我们可以把许多强大的基地将deprotonate水(pK一个= 14],但很少deprotonate烷烃(pK一个= 50)。
但是当我们看12的,我们看到HO-H 118千卡每摩尔和H3碳氢键是104千卡每摩尔。碳氢键是弱吗?到底发生了什么事?
如果你考虑12和酸碱反应,你使用错误的思维模式。
酸碱反应涉及异种溶解的乳沟,12是衡量均裂乳沟。
而不是稳定的离子(异种溶解的乳沟!)我们需要看看自由基的稳定性(均裂)。
这是一个例子,我们需要看看在这种情况下:
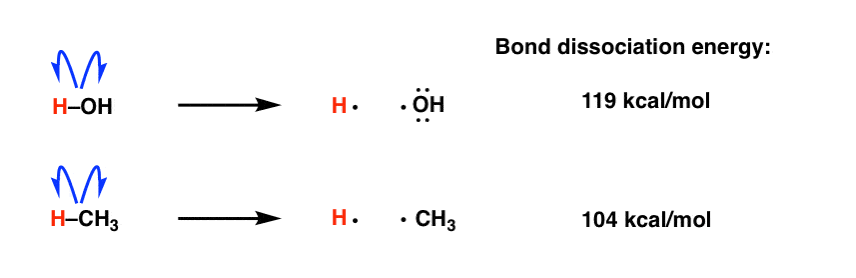
注意我们如何形成一个H激进的在这两种情况下。有什么不同的身份其他激进。
使我们比较稳定的H3HO•C•和我们以前学过(其他所有条件都相同)自由基的稳定性减少我们在元素周期表中从左到右,因为O比C和部分空轨道电负性被带正电的原子核更紧密地合作。可以更低。
3所示。键离解能与自由基的稳定性
这篇文章的底线b核能开发局离解能与自由基稳定。
低债券裂解键能反映稳定自由基的形成,和高键离解能反映不稳定的自由基的形成。
(编辑:警告适用于扩展时讨论超出本文讨论的范围。看到注1]
如果我们保持一个变量恒定和其他不同的变量,我们可以分析结构在自由基稳定性的影响。
这里我们将继续H的变量是相同的,和通过检查趋势影响自由基稳定在一个新的光。
让我们看看这七个因素:
- 稳定增加的顺序甲基(不稳定)< <二次<三级(最稳定)
- 自由基是稳定的共振
- 自由基是稳定的相邻原子的孤
- 自由基在稳定增加电负性原子的减少
- 自由基增加稳定性下来元素周期表(更大的规模,更可极化)
- 自由基稳定性下降从sp3对sp2对sp杂化
- 相邻电子撤回组减少自由基的稳定性。
4所示。因素1:稳定增加的顺序甲基< <二次<三级
注意,12的碳氢键减少我们从甲基主要二级到三级。他们更容易打破均裂以来债券乳沟的结果更稳定的激进。
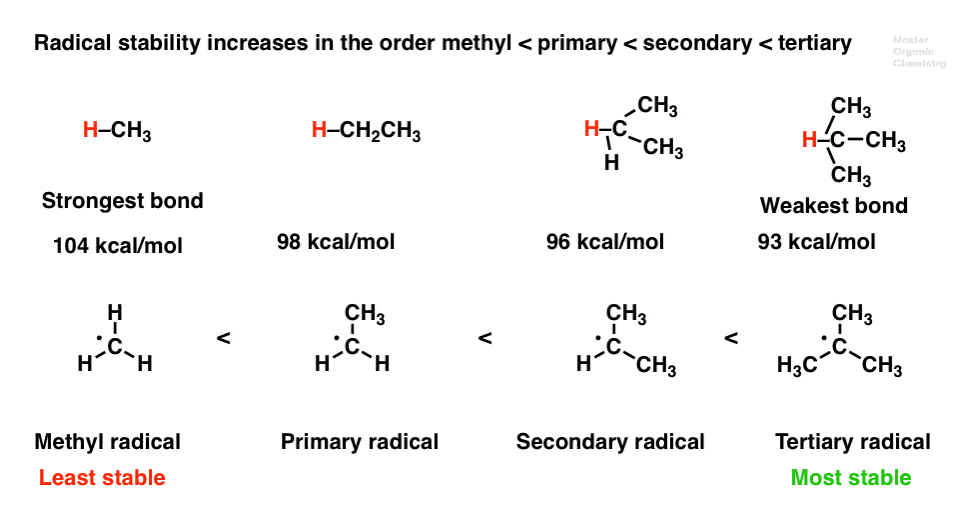
5。因素# 2:自由基是由共振稳定。
注意区别在债券之间的优势(主要)碳氢键的丙烷和丙烯的烷基碳氢键。相当大的区别(~ 13千卡每摩尔)是反映了更大的共轭烯丙基”上激进的稳定性。
虽然没有直接的可比性,看看碳氢键强度时,相邻两个烯烃(76千卡每摩尔)。这种“双烯丙基的”碳氢键就更不行了,反映了这一事实更多的共振形式可用于激进的物种。
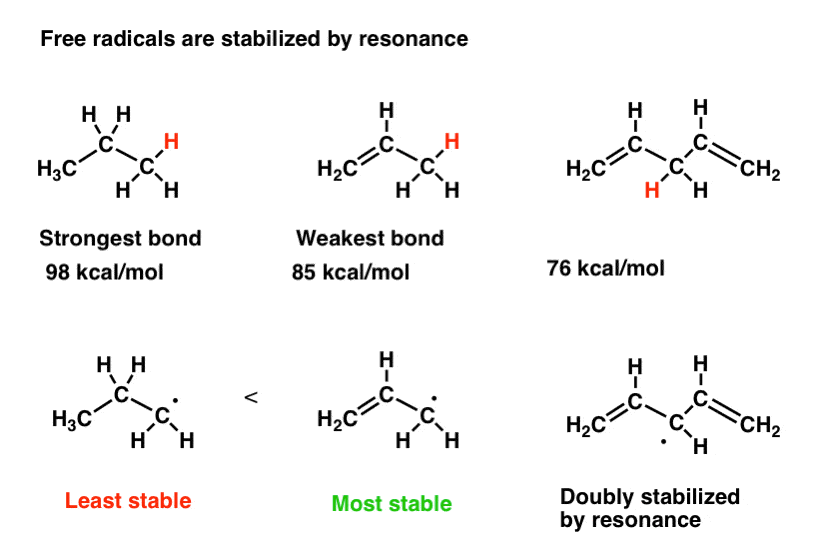
6。因素# 3:自由基是由相邻的原子与稳定。
[这是一个微妙的一点!]。注意区别在甲烷碳氢键之间的粘结强度(104千卡每摩尔)和甲醇(95千卡每摩尔)。之间的碳氢键氟代甲烷(101千卡每摩尔)。
注意,即使氟原子的电负性大于H,孤独的存在对F实际上是稳定相对于H。
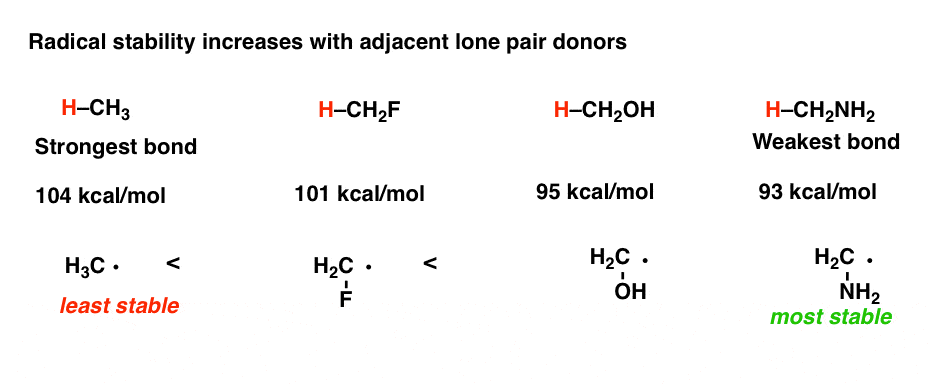
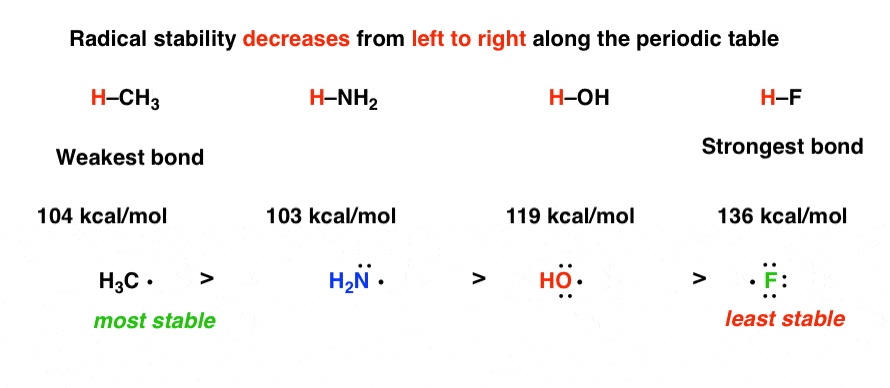
7所示。因素# 4:在元素周期表,自由基稳定性随增加电负性。
注意H-CH之间的区别3键H-OH[104],[119]和[136]。
的电负性最强的元素至少稳定的自由基,这反映在键的强度就越高。
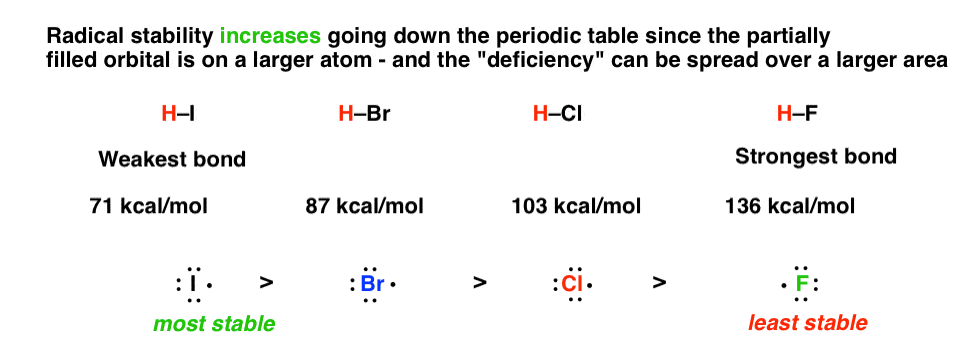
8。因素# 5:元素周期表,自由基稳定的原子尺寸增加而增加。
看12减少作为氯从氢氟键[136][103],H-Br[87]来设定h [71]。现在,我们应该期待的碘化激进是最稳定的,因为大的规模和轨道因此“分散”更大的体积。离原子核更远,因此“感觉”有效核电荷比原子更小。(感谢评论者二甲苯这种建设性的建议。
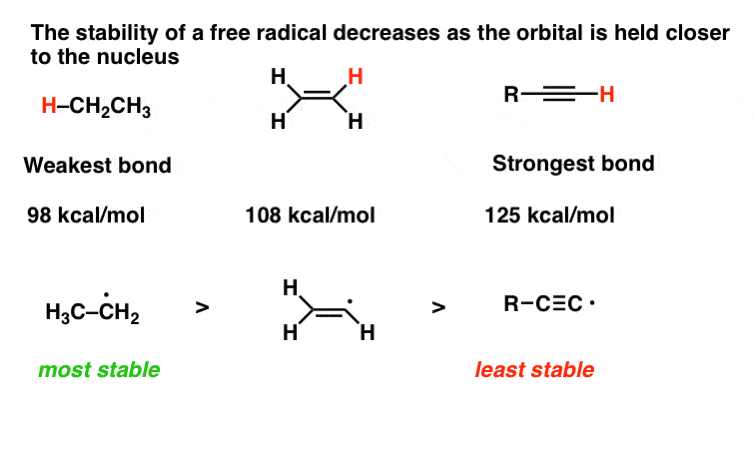
9。因素# 6:自由基的稳定性下降的轨道接近原子核。
看看发生了什么键的强度,我们从乙烷,sp3杂化(98千卡每摩尔)乙烯(sp2109千卡每摩尔),乙炔(sp, 125千卡每摩尔)。
这在很大程度上同样的效果如上# 5——远离原子核装轨道,越稳定。
10。因素# 7:电子撤回组织破坏自由基。
隔离这种效应是很重要的看例子吸电子集团不能捐献的孤对激进的(见因素# 3)。一个很好的例子是乙烷与trifluoroethane比较碳氢键的强度。

11。摘要:量化自由基稳定性与邦德离解的能量
希望现在很明显,碳氢键,通过检查键离解的能量,我们可以辨别自由基稳定性的趋势。
这将是最重要的理解选择性在自由基的反应:“哪个自由基形成?”。
一个微妙的观点是,同样重要的是在质谱分析理解分散模式,但我们没有。
在下一篇文章:激进的反应——为什么需要光或热?
笔记
注1。需要更多的谨慎比我先前表示关于这篇文章的主要论点——自由基稳定性仅反映在债券的优点。他们依靠的稳定性这两个反应物和试剂。

编辑内联表示。更多的讨论见底部分。TL;博士——将军趋势在这篇文章中是有效的,因为我们讨论债券H,但注意当比较氢以外的任何其他类型的债券。由于保罗Wenthold教授(普渡大学)的输入。
利用债券的优势(12)不牵强附会的债券氢是一个合理的方法激进的稳定性的趋势,在这篇文章中讨论。
然而,12的本身不可靠的绝对激进的情况下稳定性债券可能削弱了应变,对孤电子之间的排斥力,或其他因素。
例如过氧化氢的12是51千卡每摩尔,这不暗示何氏•激进是稳定的,而是oo的债券不稳定由孤之间的排斥力。
注2。在观察粘结强度数据经常有2 - 3千卡不同来源之间的差异。这里的重要部分,与其说是绝对数字,但是趋势。这两个文件帮助当编译这篇文章编号为:
(高级)引用和进一步阅读:
- 缺点以激进的稳定能量债券分离烷基组氢的能量
安德烈亚斯•a . Zavitsas唐纳德·w·罗杰斯,尼基塔Matsunaga
《有机化学》杂志上2010年,75年(16),5697 - 5700
DOI:1021 / jo101127m
激进一些教科书,包括一些高级的,提供稳定的能量,并论述了为什么,可能不是最好的方法量化自由基的稳定性。 - 烃自由基稳定能源的优点基于R−H键离解的能量
马修·d·Wodrich w·麦基乍得和保罗·冯·Rague Schleyer
《有机化学》杂志上2011年,76年(8),2439 - 2447
DOI:1021 / jo101661c
本文地址的一些缺点上面Ref # 1中使用的方法。末Schleyer教授是一个很有影响力的人物在有机化学中,并使用计算方法解决的先驱在有机化学感兴趣的问题。 - 激进的稳定能源的替代Carbon-Centered自由基取决于取代基的功能和Ordinality激进
马文·l·Poutsma
《有机化学》杂志上2011年,76年(1),270 - 276
DOI:1021 / jo102097n - 一个激进的普遍规模稳定的能量并不存在:全球债券离解能量和激进的热化学结合描述两个普遍的尺度
安德烈亚斯•a . Zavitsas
《有机化学》杂志上2008年,73年(22),9022 - 9026
DOI:1021 / jo8018768 - 键离解能量动力学方法
答:克尔
化学评论1966年,66年(5),465 - 500
DOI:10.1021 / cr60243a001
本文描述了实验测量均裂bd的技术。 - 第三,键能
西德尼·w·本森
《化学教育1965年,42(9),502年
DOI:10.1021 / ed042p502
介绍了实证测量均裂键离解的能量。本文作者是本森教授在斯坦福研究院(现在SRI国际),一个非盈利的斯坦福大学研究中心很近。1978年,本森教授加入了南加州大学教授乔治Olah并帮助建立了物料间烃研究所。 - 从平衡酸度激进的稳定的能量
弗雷德里克·g·博德维尔和西安人
的化学研究1993年,26(9),510 - 517
DOI:10.1021 / ar00033a009
本文试图将质子的酸度与相应的碳氢键或12 x h键。 - 从头开始计算的相对能量共振稳定烯丙基苄激进分子
David a . Hrovat和韦斯顿撒切尔波登
《物理化学》杂志上1994年,98年(41),10460 - 10464
DOI:1021 / j100092a014
乙烯基的稳定能源集团(烯丙基自由基)和苯基(苄激进)被计算15.7千卡/摩尔和12.5千卡/摩尔,分别。 - 相邻的受体和捐赠者对carbon-centered自由基的稳定性
g·博德维尔、张Xianman和米哈伊尔·s . Alnajjar
美国化学学会杂志》上1992年,114年(20),7623 - 7629
DOI:10.1021 / ja00046a003
表我在这篇文章中包含稳定的能量甲基自由基与不同取代基(例如·CH2X)。
嘿,你提到的部分(8),碘自由基是最稳定的。但如果我不是错误的烷基碘化不准备使用这种机制作为自由基形成(碘)形式I2分子。谢谢你! !
是的,你是正确的,烷基碘化不准备直接通过自由基卤化因为设定h债券比碳氢键弱得多。
谢谢您,先生。但是我和f, 36个千卡/摩尔和38千卡/摩尔,12的分别。显然,他们的激进分子具有相同的行为,但事实证明,他们不喜欢。氟自由基更有选择性,但碘与任何氢反应。我错了吗?为什么会这样呢?
你在哪里得到氟激进更有选择性?运行与氟自由基反应不是一颗卑微的心…
为什么比因子4氨基甲基自由基更稳定吗
更高的氮和碳由于电子亲和能更大的电负性。
有人能帮我稳定的秩序tertairy碳水化合物自由基。
如:3
甲基三乙基vs
大概是一样的。微不足道的差异。
詹姆斯,我有2个问题
首先:降低自由基稳定我们减少杂交?这似乎完全反直觉;你希望sp会稳定得多,因为激进接近原子核是由于50% s轨道…这是为什么呢?
其次:邻孤稳定激进?哇,这完全出乎我的意料;你期望电子斥力/电子密度增加破坏激进?
谢谢,很高兴你喜欢这个助记符(我创造了明天我的物理有机试验:/
1)稳定增加的顺序甲基< <二次<三级
2)自由基是由共振稳定
3)自由基由相邻原子的孤对稳定
4)在稳定自由基增加原子的电负性减少
5)自由基增加稳定当我们沿着周期表(大)
6)自由基稳定性下降,当我们从sp3 sp2 sp杂化
7)相邻电子撤回组减少自由基的稳定性
4和7说同样的事情,所以我们只需要1提醒我们关于电负性。
一个好的记忆是S H R E S:
替换
杂交
相邻的孤
共振
电负性
大小
感谢蒂姆!
只是觉得我添加在我们的课程教ewg和EDGs稳定自由基,因为增加稳定的电子轨道。更喜欢如果两组——captodative。比较CH3CH2 F3CH2并不适合作为甲基。
你会注意到我选的EWG *不是* captodative(正是出于这个理由:-))。我的观点是,比CF3CH2 CH3CH2更稳定。
这里,通常是一个电子撤回原子(如F,哦),孤在激进的稳定。也就是说,它是通过感应电子捐赠的。
但在处理酸性时,这些类型的原子连接相邻的负碳离子说甲基conj.基地会稳定过剩负电荷。
如何在这种情况下,自由基,F通过捐赠与孤稳定激进但撤回电子密度稳定一个负电荷吗?
再保险:你的第一段是不通过感应电子捐赠。
Re:第三段,真正讨论这个问题,我们会用分子轨道理论来说明捐赠一个孤对装轨道是一个稳定的现象,降低了能源的激进。事实证明,捐赠的孤对电子密度比的稳定通过归纳。
第二段最后,这种现象不会发生在阴离子,因为没有空(或半空)轨道接受负电荷。这就是为什么稳定在负碳离子负电荷的电子撤回原子如F是纯粹的一种感应现象。
我认为4 C和N之间的影响因素是由于几何松弛杂交结果的变化。碳和氮从sp3的封闭外壳sp2的激进分子。碳有三个氢原子重新排列而氮只有两个。如果甲基的能量和氨基酸激进分子在固定计算几何图形(仍然sp3杂交)我认为氨似乎有更高的12。
我认为我有一个原因为什么H-NH2异常。同样的解释N接近零的电子亲和能,而不是积极的。.NH2激进的形成时,由于自由基亲电,你会得到一个电子形成氨基-离子。然而,电子不希望与另一个电子,因为它会增加它们之间的静电排斥,所以.NH2不是特别反应,因为有这能量势垒。至于O开始,质子增加电子的吸引力,使其不再是问题。
的电子亲和能趋势自由基CH3 <氨基<哦< F NIST化学Webbook上可以看到。N -电子亲和能的原因是它有一个半闭壳层结构。
# 5:关于因素是它完全正确地说,激进的更稳定,因为它是更分散?毕竟,越接近原子核的轨道(较低的量子数或增加有效核电荷),降低其能量(即其稳定性越高)。技术上来说,这将意味着,在其他条件保持不变的情况下,一个激进的孤独的电子在一个大型轨道(离原子核更远)会比一个激进的更不稳定的一个孤独的电子在一个小轨道(接近原子核)。
我相信真正的原因在这里工作有相同的基础。碘具有更大的轨道,从而形成弱债券本身只是因为重叠并不是那么有效。较弱的键被破坏,形成更稳定的自由基(相对于反应物)。绝对规模,我认为氯自由基会比一个更稳定的碘激进——它只是相对于氯更加不稳定。
一个类似的观点可以为因素# 6:sp和sp2碳氢键只是比sp3碳氢键。激进和sp2轨道电子sp或可能会比一个激进的更稳定和电子sp3轨道,绝对规模,但相对于反应物,秩序是正如你所说。
这是一个更好的解释,减少潜在的能量。我将重新编辑。谢谢你!
嗯…实际上回想起来我不太确定有多少“绝对反应性”问题。毕竟,化学平衡都是基于能源* *变化,即相对能量。因此氯自由基反应仍然是比一个碘激进(假设攻击另一个氯原子)因为氯自由基之间的能量差和dichlorine高于碘激进和diiodine(当然,忽略动能因素)。
中固有的问题,氯激进并不总是攻击另一个氯原子,和碘激进也是一样。但是我想你可以使用的力量Cl-Cl或我债券作为一个粗略的衡量Cl和另一个原子之间的键能(如氢气)或在我和另一个原子之间。
(其实我想说的是,绝对稳定有点红鲱鱼在这里——这是一个有效的但没有太多影响“真正的化学”)
绝对稳定有点红鲱鱼,我想说的是,没有一个1:1的差异之间的相关性债券焓变和激进的稳定性差异。然而,就像你说的,这当然是一个粗略的(定性)计,配不上我们的目的。
你好,我是觉得有点困惑在阅读这篇文章,你的评论。所以是Cl激进更稳定或碘激进?还是在很大程度上取决于反应环境?
我将感激如果你能更详细地解释这个。谢谢!
设定h键较弱,所以碘激进的更稳定。八氯键更强,所以Cl激进更不稳定。这说得通吗?