SN1 SN2 / E1、E2的决定
决定SN1 SN2 / E1 / E2(1) -底物
最后更新:2023年5月25日|
- 判断一个反应是SN1 / SN2 /E1/E2首先需要了解债券的形式,打破这四个反应和关键特性的机制(检查在这里- - - - - -SN1/SN2/E1/E2)
- 一级,二级,三级和甲基碳原子连接到离开团体(如好烷基卤化物和磺酸盐)是良好的基质N1 / SN2 /E1/E2反应。如果这是不清楚,检查在这里
- 如果烷基碳是主空间位阻,缺乏年代N2可能和碳正离子稳定性的缺乏使得年代N1,E1不太可能的。主要的例外是强大的,庞大的基地(E2)。
- 如果烷基碳是三级,它将不是年代N2。需要更多的信息来确定哪些反应将会发生。根据基地的身份(强弱)可能是年代N1 /E1(弱碱)或E2(强碱)
- 二次烷基卤化物可以接受所有四个反应和需要分析亲核试剂/基地。(在这里看到的)以及溶剂和温度。
- 醇也可以基质的年代N1 / SN2 /E1/E2反应,但需要酸性条件哦,转化为好离去基团(哦2+)。基本条件醇转化为醇盐(RO- - - - - -),是很好的亲核试剂。
表的内容
1。首先:确定基质是初级,二级或三级
第一步是什么在决定是否反应经过年代N1,年代N2,E1或E2吗?
- 的第一件事是确定的好离去基团如氯、溴、我或OTs / OMs !(复习,之前看到这个后如何知道替换和消除反应会发生什么)
- 另一个需要注意的关键是,除了极少数的例外,替换和消除反应只有发生在烷基(即sp3杂化碳原子。
所以对于我们的目的,为了SN1/SN2/E1/E2,我们通常需要看到一个烷基卤(或烷基磺酸盐,如甲苯磺酸盐和甲磺酸-见阿宝圣:甲苯磺酸盐和甲磺酸)。
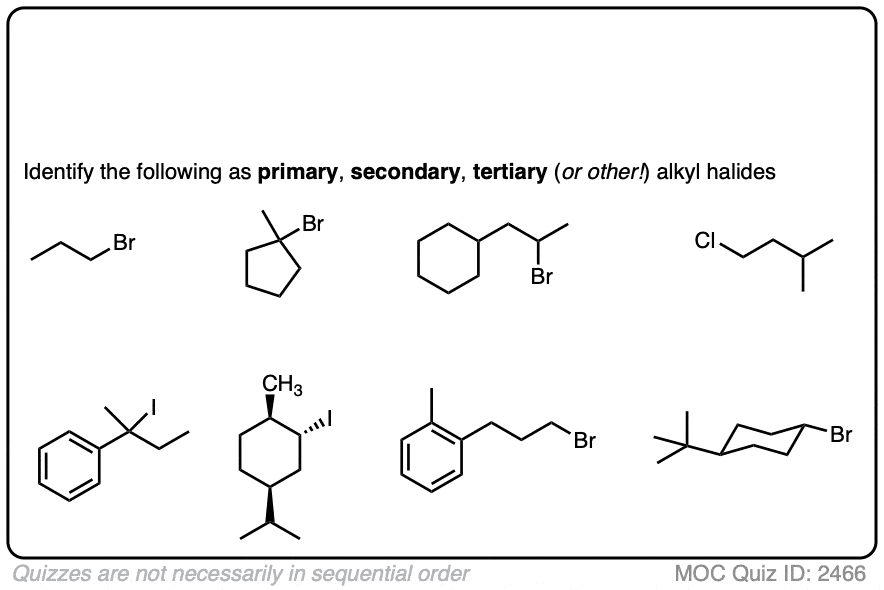
一旦你确定了一个烷基卤,下一步是确定主,二次,或三级。
试着自己这个快速测试!
 点击翻转
点击翻转
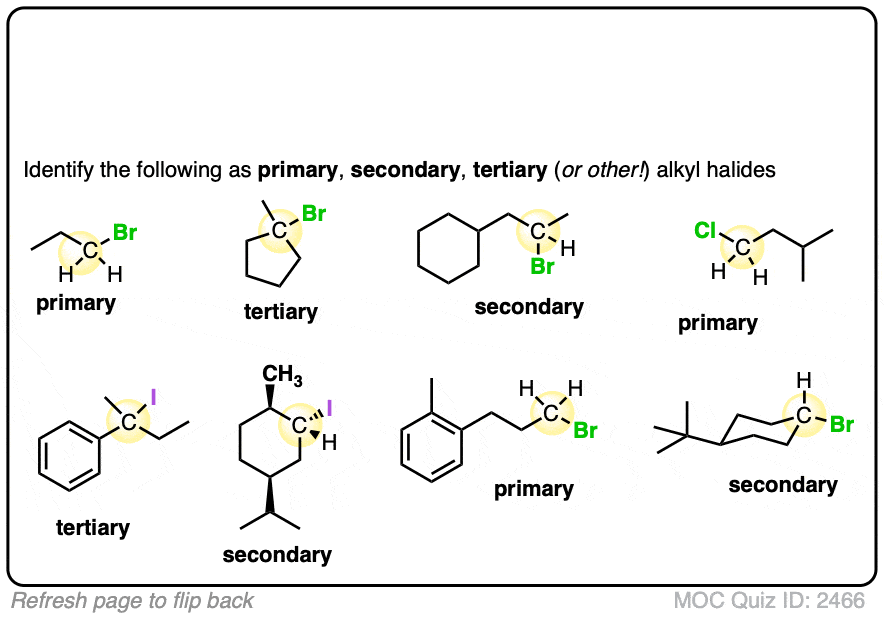
如果这些对你是困难的,那么备份和另一看这篇文章(见文章-一级,二级,三级,四级在有机化学)
如果这是太简单了,那么这是一套(稍微)更加困难。
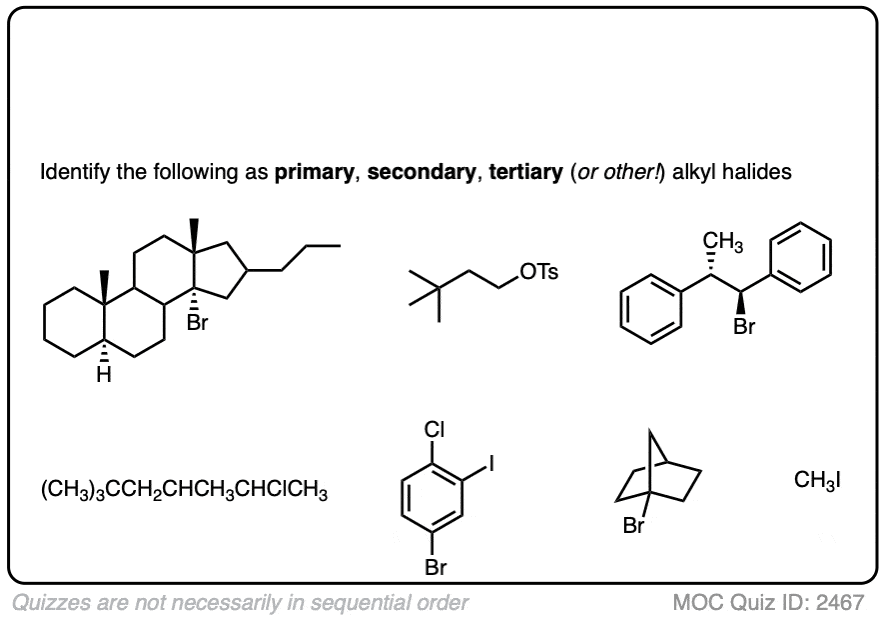 点击翻转
点击翻转
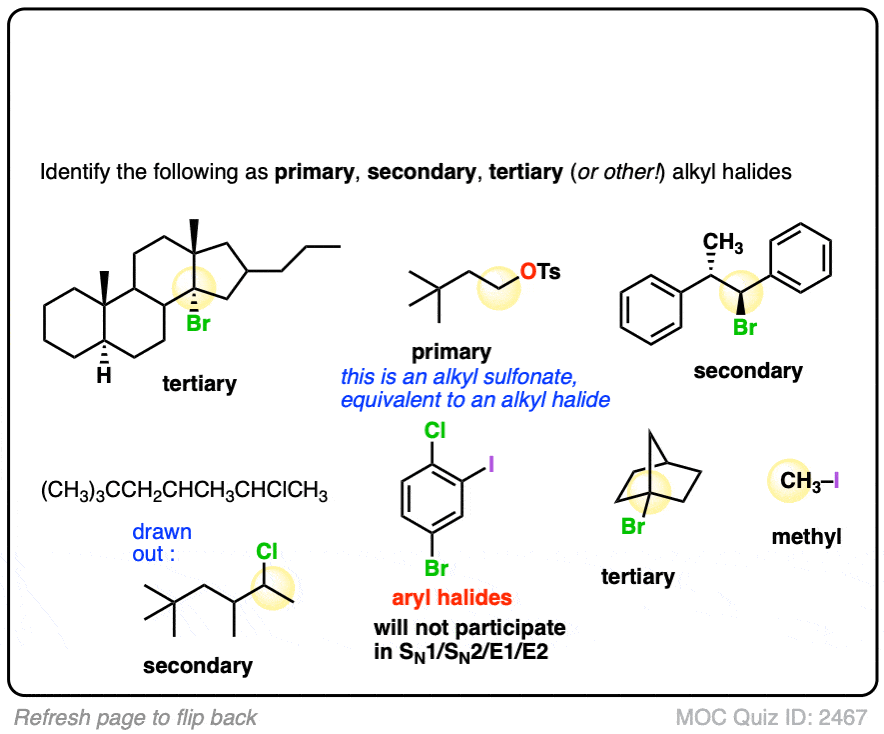
吸引注意,有时这些反应与反应,不能工作。为了测试你的理解机制。如果你看到一个问题涉及一个烯基卤,你的工作是找出如果是放在那里一个技巧问题,或者把它视作一个(罕见)例外情况”烷基碳”规则。(主要的例外是形成炔烃通过消除——看到的两倍文章)
2。看一些反应
一旦你能分类烷基卤化物作为初级,二级、三级(或甲基!)下一步是上下文中的几个反应,它是件司空见惯的事情有点异常地。
问任何问题之前,看看下面的反应,看看是否可以识别潜在的基板的年代N1 / SN2 /E1/E2反应。
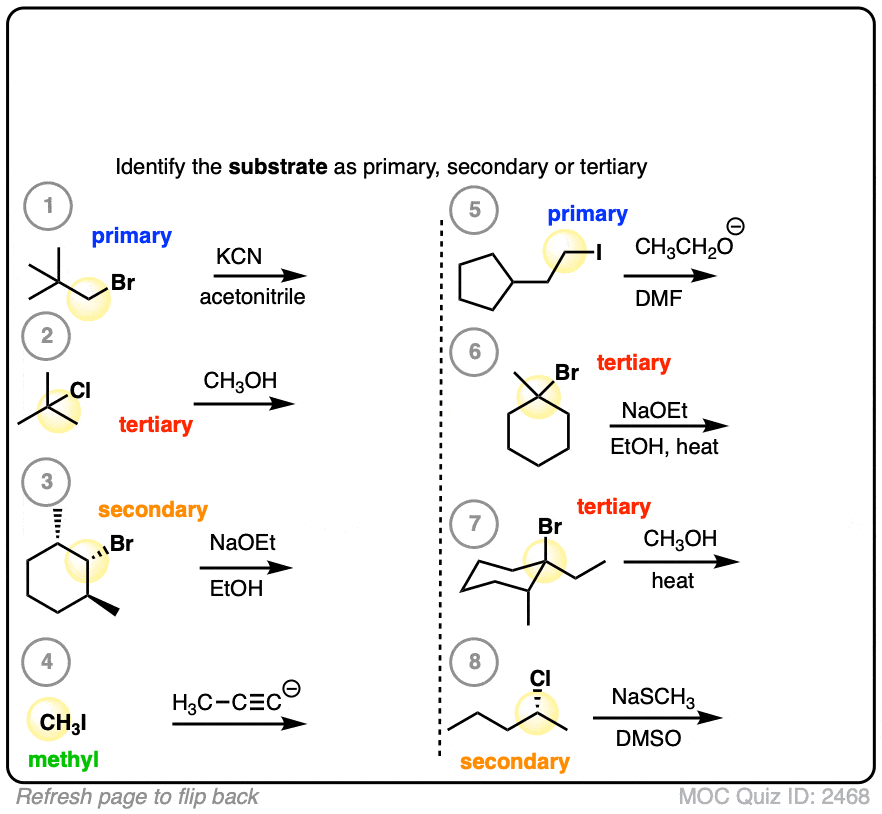
让我们先从一个相当简单的。确定小学,中学,和三级:
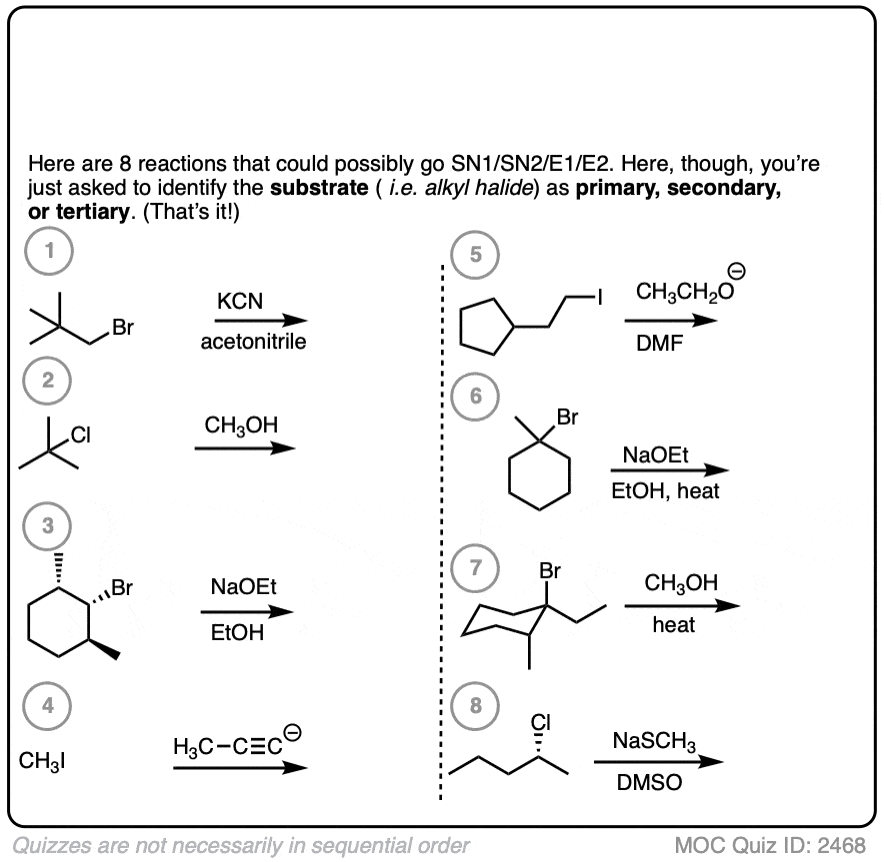 点击翻转
点击翻转
这一个是更困难的。
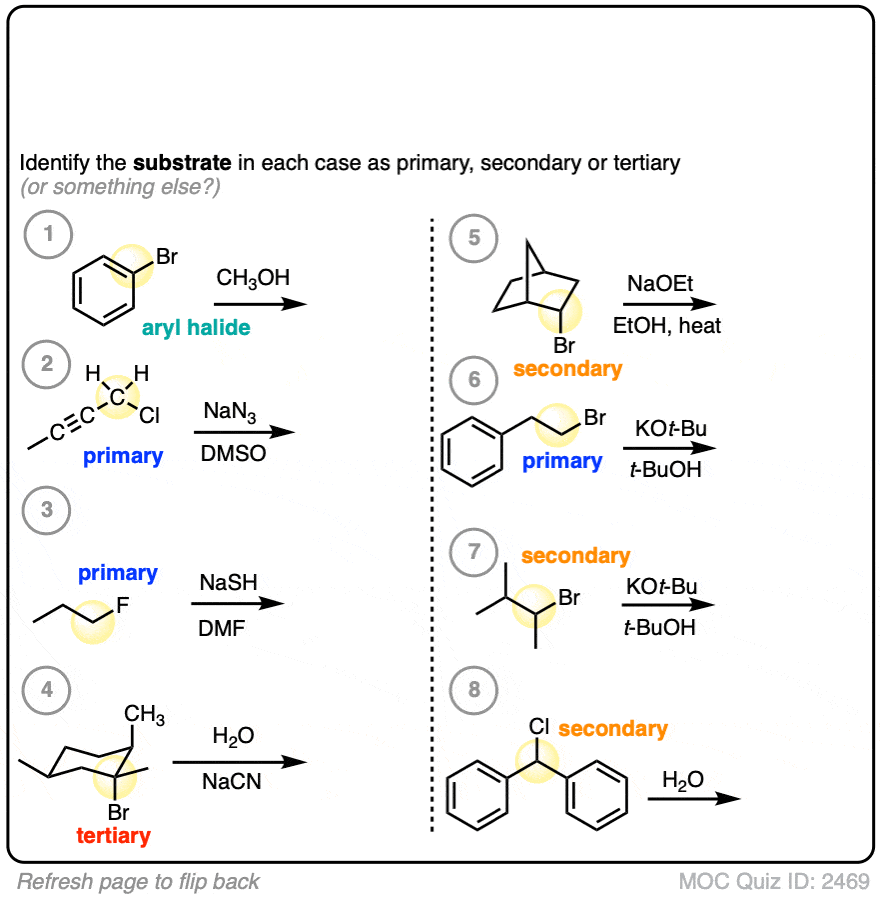 点击翻转
点击翻转



最后,这有一些困难的例子。
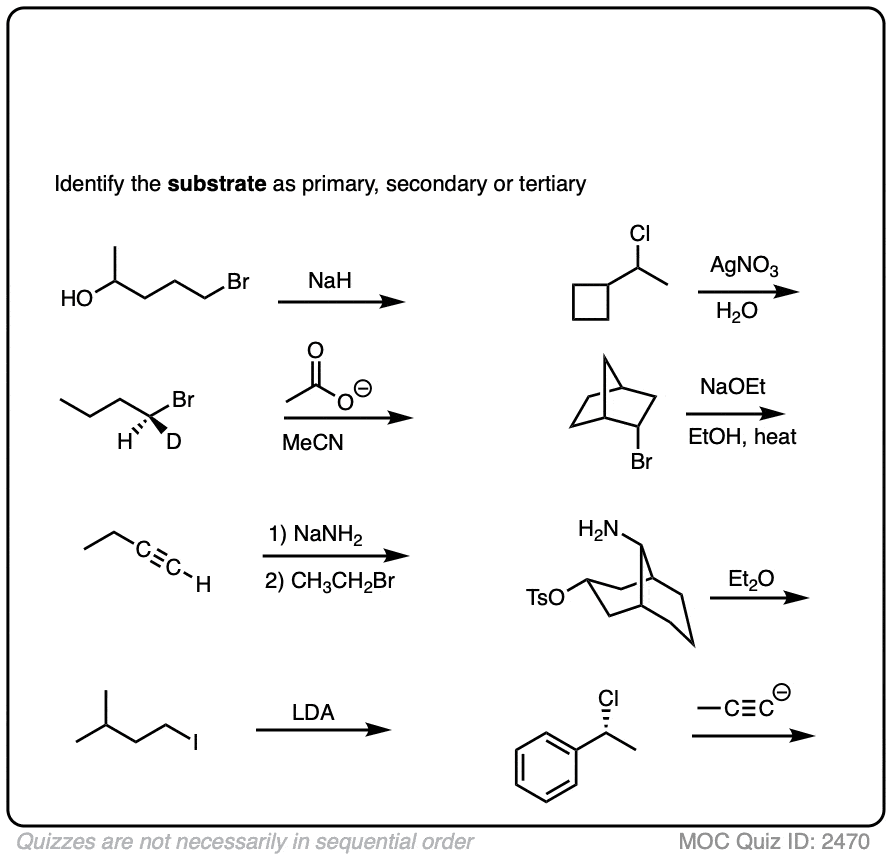

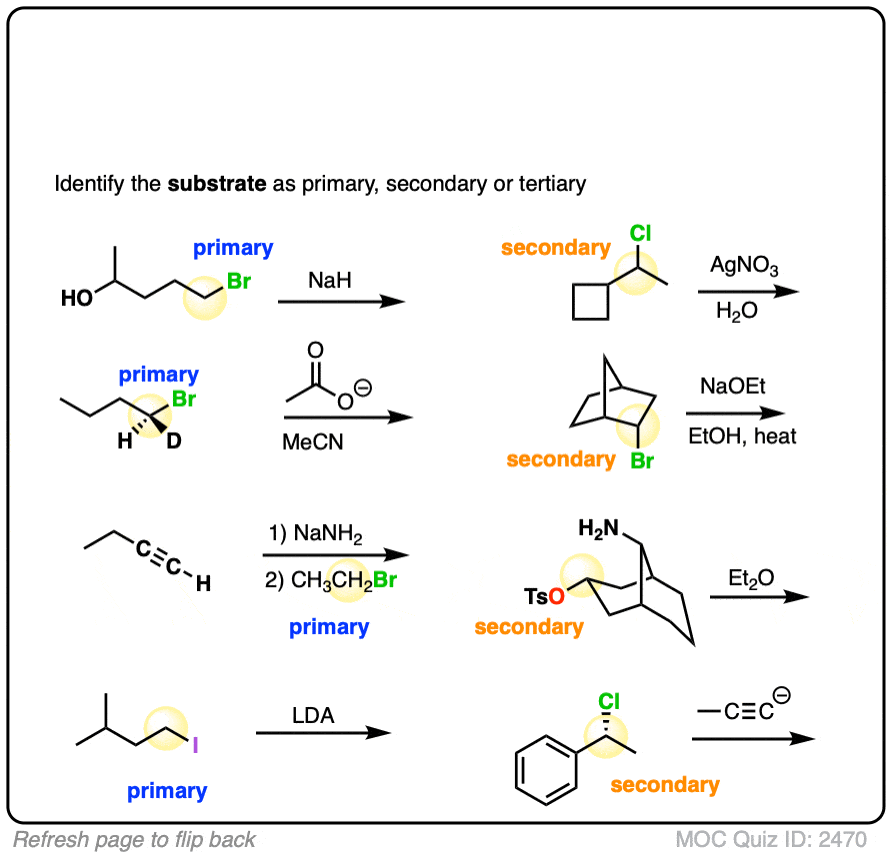

如果你看着反应,发现一个初级,二级、三级或甲基卤化物(或甲苯磺酸盐/甲磺酸盐,但是不氟化),那么你可能看一个替换或消去反应。
3所示。卤代烷是主-现在什么?
好吧。假设我们已经确定了烷基卤,主。
现在我们怎么做?
我们可以做一个自信的预测。当底物主(或甲基),期望的年代N2
这些反应几乎可以肯定不是年代N1或E1。(注1这是因为年代的第一步N1 /E1是亏损的离去基团形成碳正离子,主要碳正离子会不稳定。(见文章:碳正离子的稳定性)
下一步是预测产品。要做到这一点,我们:
- 找一个好亲核试剂,然后
- 应用关键模式的年代N2反应(C-Nu形式,打破C-LG)
- 反如果有一个手性中心(主要罕见)
此外,它可以帮助回忆的身份共同的极性非质子溶剂等DMF,DMSO溶液,乙腈(MeCN)。这些会影响但它们替换率的反应不的亲核试剂。(见文章关于溶剂)
现在,让我们把它付诸行动。假设这些反应N2,画出产品。
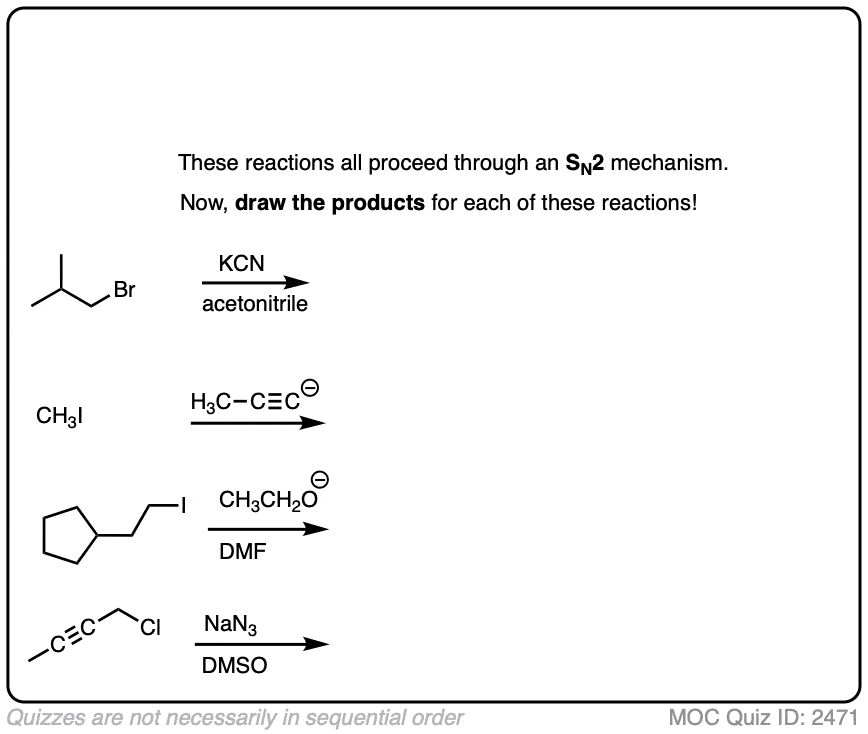

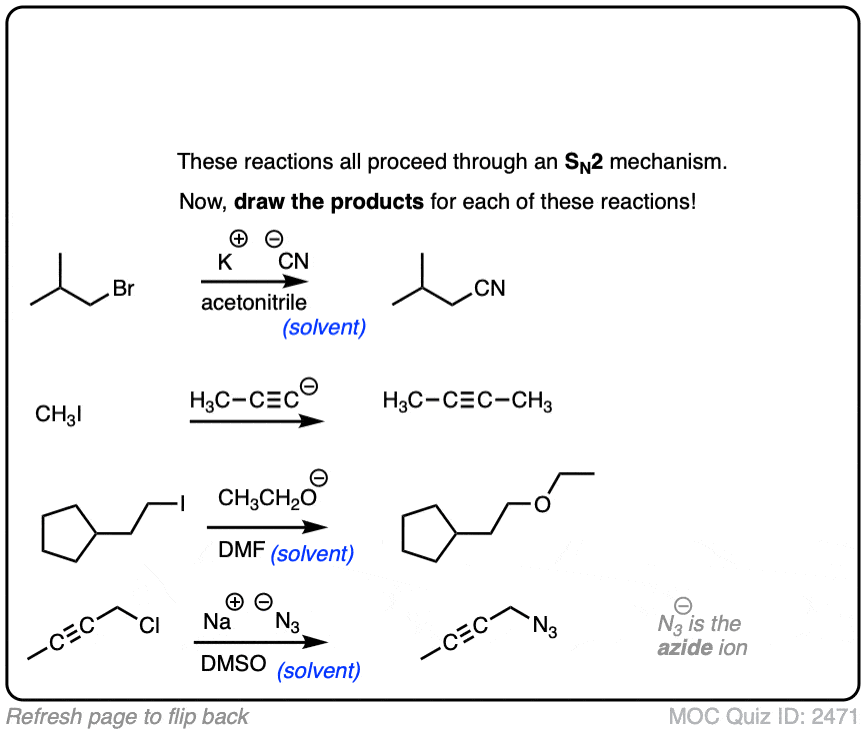

这些例子都要简单。如果你发现,那些主要的例子烷基卤化物过于简单,那么看看下面这些棘手的例子。(并不是所有的这些一定会N2)
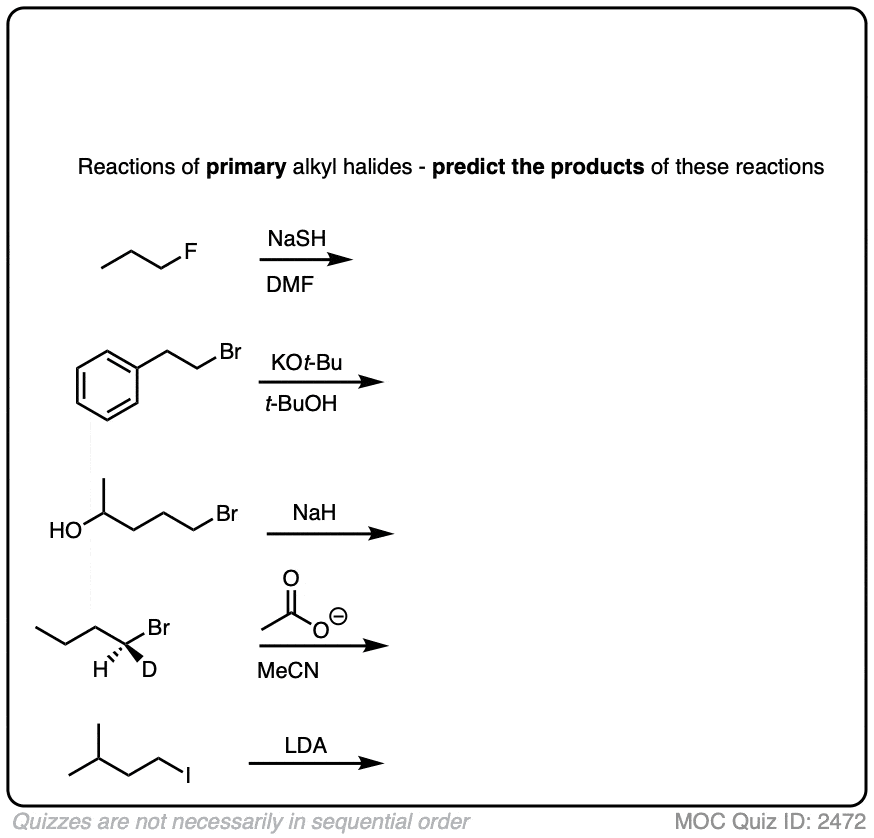





一些额外的注意事项:
- 烷基氟化物一般不接受替换或消除反应在正常情况下由于强烈的氟键。
- 氢化钠(不)是一种强基地但一个贫穷亲核试剂。它不攻击碳取代离去基团,但它将deprotonate醇给醇盐(RO (-))是优秀的亲核试剂。(永远不会忘记,共轭碱总是更好的亲核试剂!]
- 只有一种情况,另一个反应可以竞争的年代N2主烷基卤,那就是当一个强,笨重的基础如t醚离子(如。KOt布鲁里溃疡)或锂二异丙基酰胺(乔治。使用)。在这些情况下,SN2是低于正常由于空间的亲核试剂和消除(E2)可能开始与年代竞争N2。(注2]
4所示。卤代烷是三级-什么?
二次烷基卤化物有点棘手,我们跳过它们一会儿,直接搬到三级。
如果衬底三级,你可以排除年代N2。为什么?
年代N2反应一般不发生在第三烷基卤化物,因为年代N2通过背后攻击(C-LG西格玛*轨道),三级的背后烷基卤化物太位阻N2反应发生在任何有意义的。(看到后位阻就像一个脂肪守门员)
年代以来N2是不相干的,我们试图离开之间做出选择N1,E1,E2。
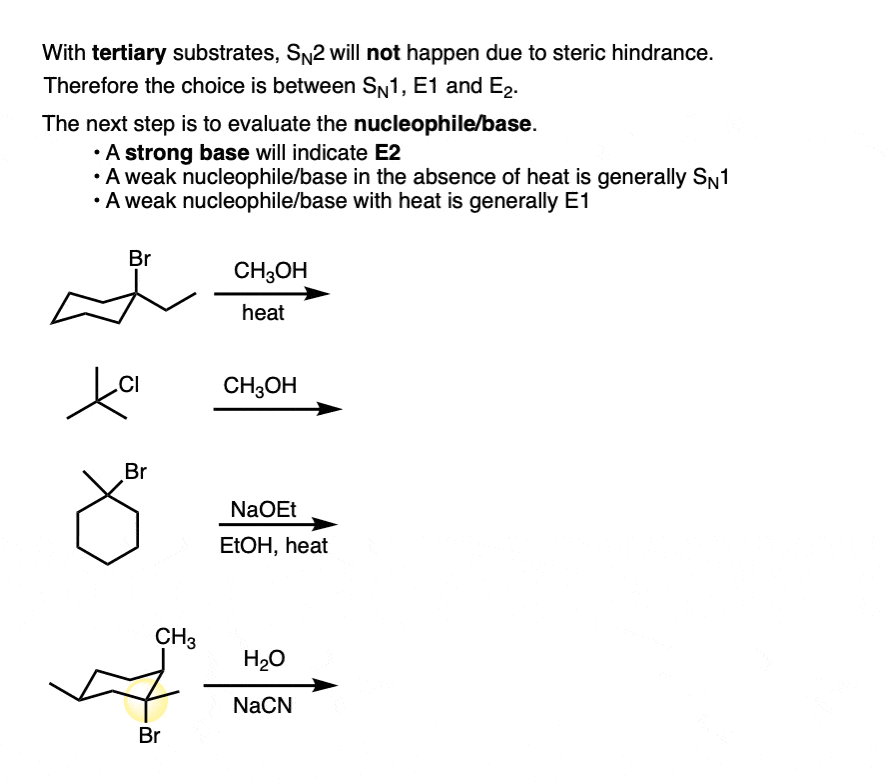

那么什么?
我将介绍在以下的这篇文章,但我不认为我破坏说下一步是什么寻找良好的基础。(看到下一篇文章,决定SN1 SN2 / E1 / E2 -亲核试剂/基地]
通过“基地”好,我通常指带电种类至少有基本的醇盐(RO- - - - - -)或更大。(虽然我也包括三级胺注3]
看到“热”或δ象征“Δ”也是一个很好的线索消除。(见文章-消除反应的热量]
在没有一个强大的基础,期望年代N1 /E1与三级烷基卤化物。
当然,只是打开了另一个问题。如何区分年代N1或E1吗?
这也将覆盖另一个后续的文章(见文章-决定SN1 SN2 / E1。E2- - - - - -的Role of Temperature),但简短的回答是,“热”。如果热应用,那么期望的反应E1。
在下面的测试,收集从上面的例子中,我已经做过的工作确定最可能的反应途径。你的工作是画的产品。
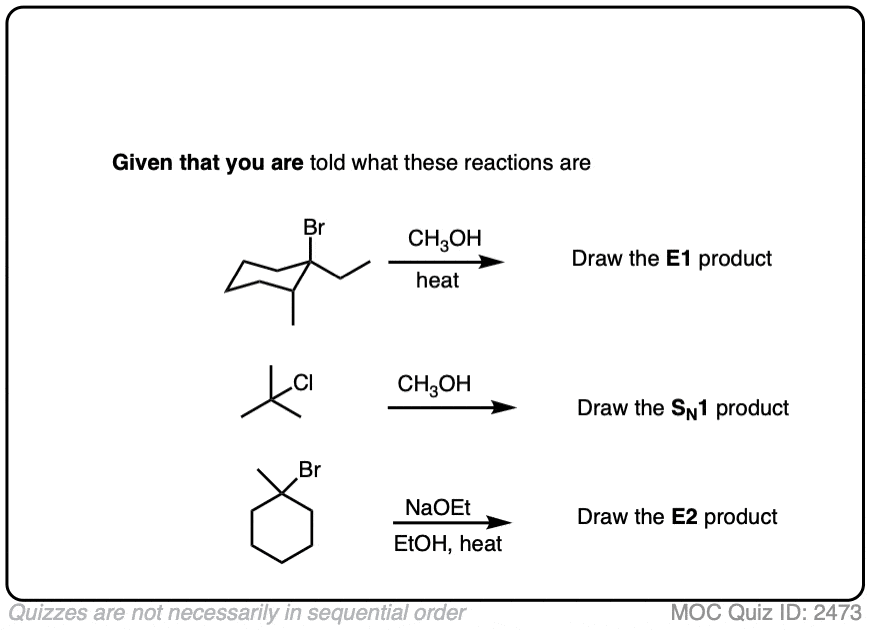

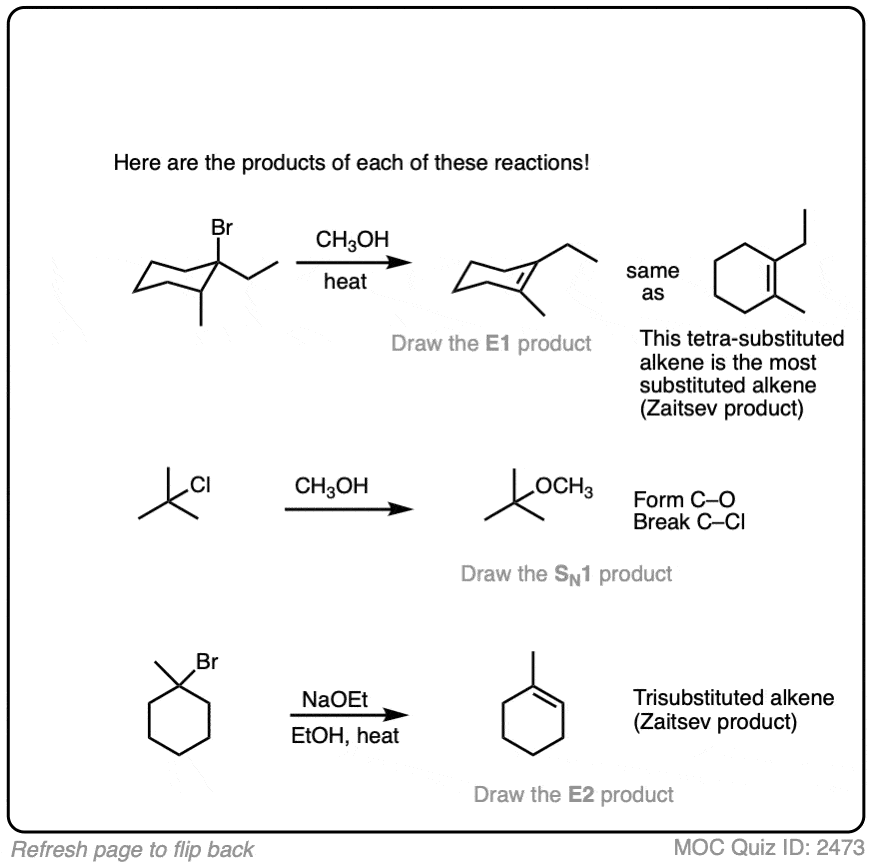

看到这个注意4更困难的例子。
5。二级-现在什么?
最后我们到达“有趣”的部分:次要的烷基卤化物。(注意:你对“快乐”的定义可能不同)
的短消息是次要的烷基卤化物,我们不能排除任何可能性。根据条件,四种反应模式可能会观察到。
我不会能够总结整个范围的可能性在一个段落,但下一个将是关键问题检查基础/的身份亲核试剂。
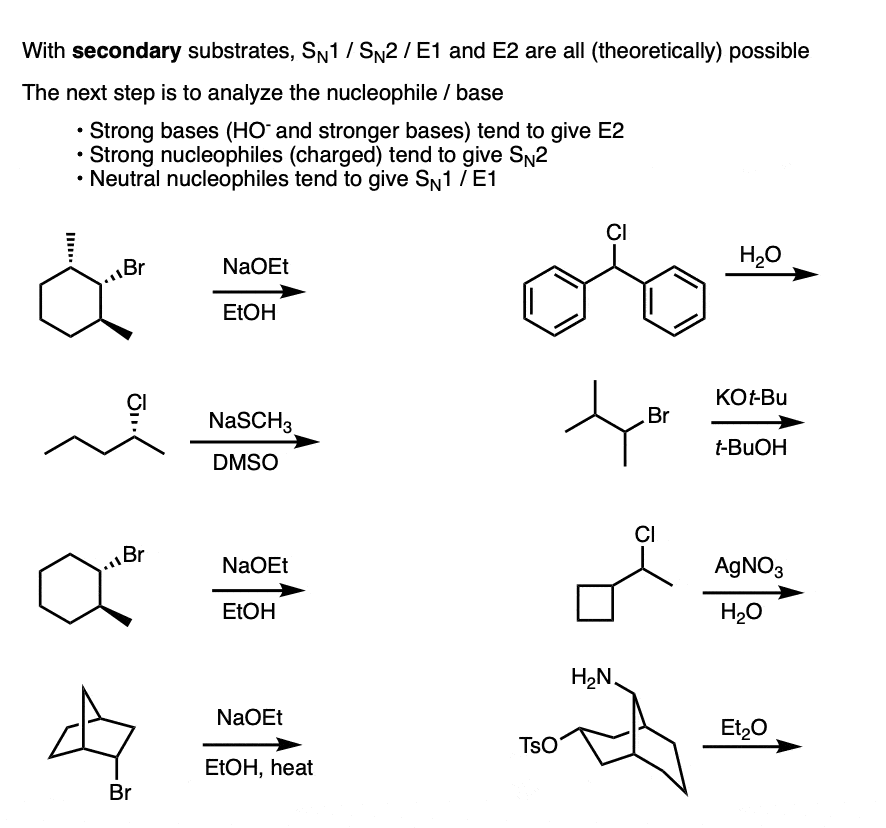

年代的区别N2对E2在第二个烷基卤化物值得自己另外撰写一篇文章。
现在,让我们注意E2需要一个强大的基础,而SN2需要一个强大的亲核试剂。
“强大的”我建议氢氧根离子(HO -共轭碱的水,pK一个= 14)作为一个良好的分界点。
- 硫醇盐,硫醇的共轭基地(pK一个10)倾向于对二次进行置换反应烷基卤化物,那么基本的物种,如N3CN(-)(-),卤化物,羧化物。(良好的亲核试剂列表,见后为什么这个年代N2是强大的)
- Ssecondary烷基卤化物醇盐处理是一个特别棘手的情况,因为这是年代之间的边界地区N2,E2。一段美好的时光,问问你的老师什么他们认为将会发生的事情。(我个人的观察是,极性非质子溶剂等DMSO溶液,DMF,乙腈表明年代N2而极性质子溶剂表示E2,但也有例外)。
- 的亲核试剂,比醇盐基本倾向于给予E2与二次烷基卤化物。乙炔化物,终端的共轭基地炔烃是一个典型的例子。(注5]
下面是一些简单的例子。更复杂的下面我将介绍在笔记中。
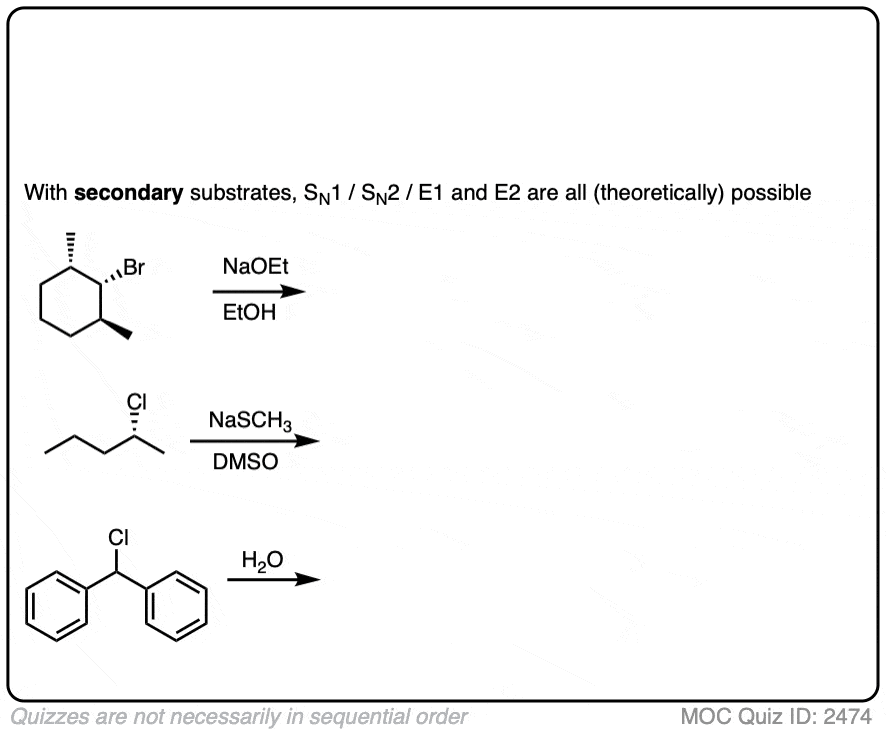

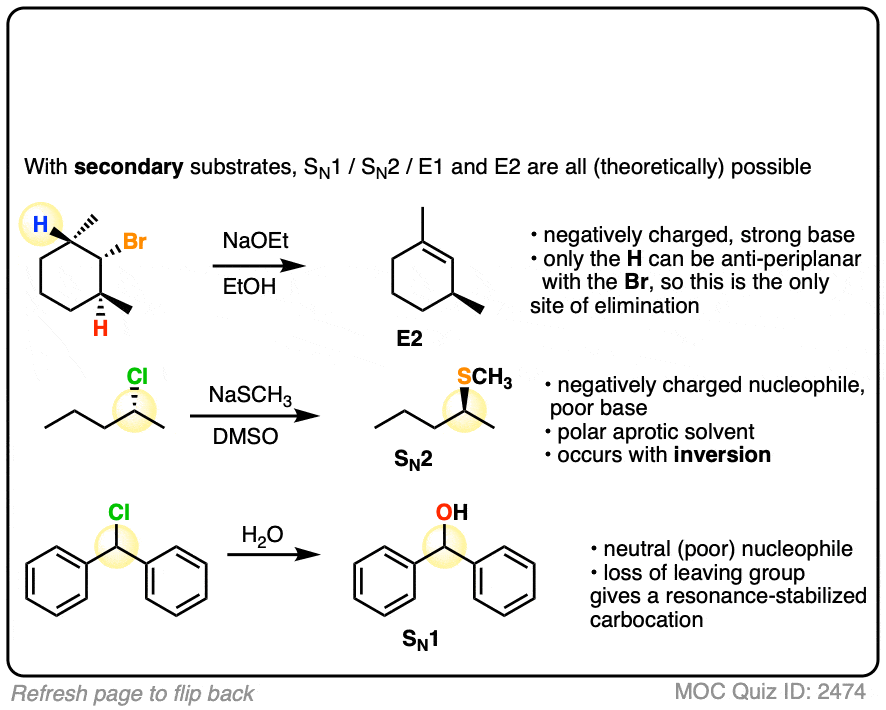

我将处理一些更复杂的次要的烷基卤化物在表格下面的备注。
6。一看前面
虽然这是为了只是一篇文章在一个序列,走过决定的过程SN1/SN2/E1/E2,我意识到不是每个人都会经历这个顺序。
这是一个思考过程的概述:
- 衬底的作用(这篇文章)
- 的作用亲核试剂/基地(下一个!)
- 溶剂的作用(年代N2对E2仲卤代烃)
- 温度的作用(年代N1对E1)


7所示。一些例子与醇
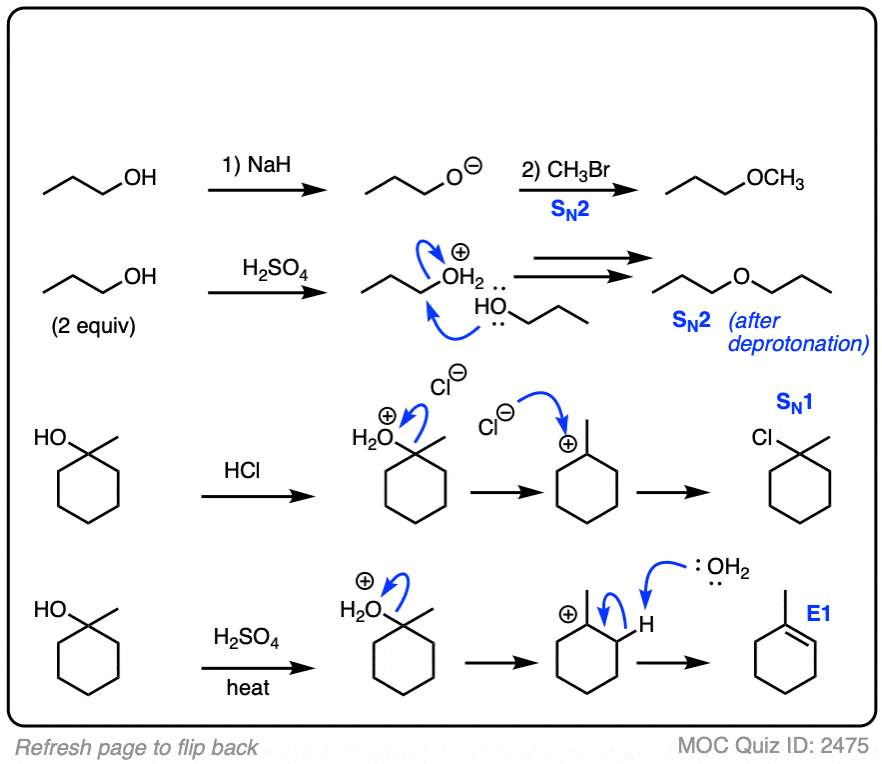
我们一直在谈论的反应烷基卤化物,但是这些反应可以发生醇。
中性形式醇贫穷的亲核试剂,也可怜的基质N1 / SN2 /E1/E2氢氧化反应自组(HO)- - - - - -)是一个穷人离去基团。
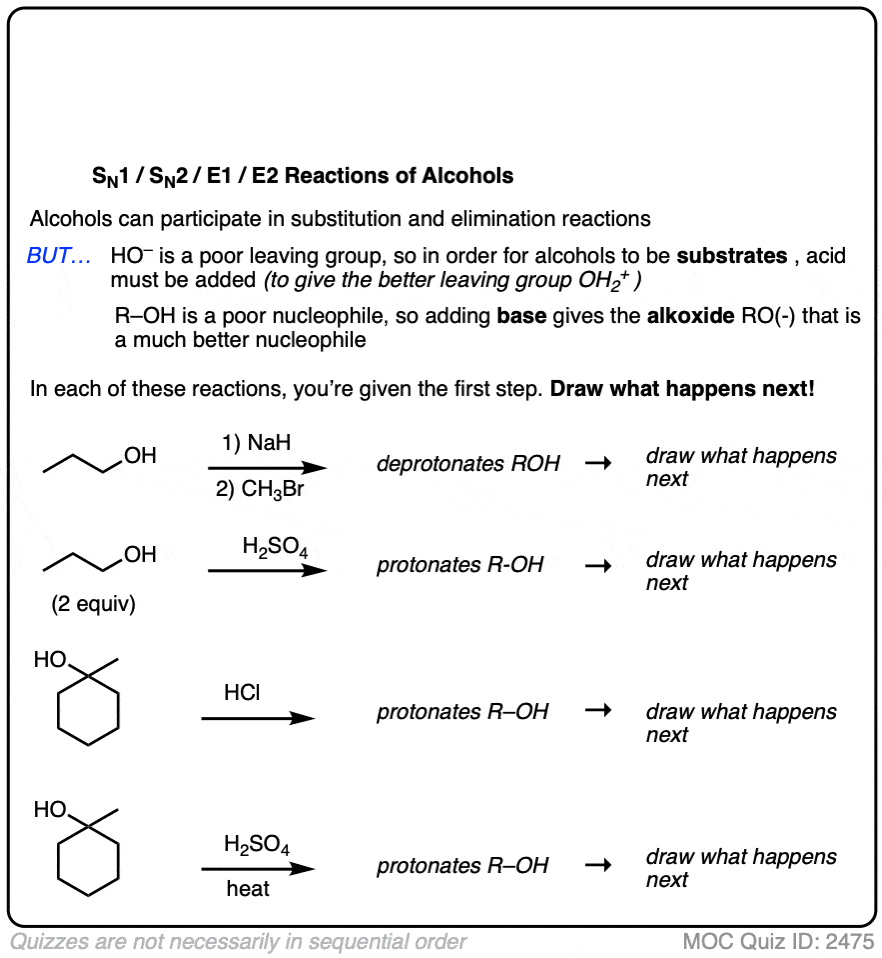
然而,添加一个酸或者一个基地可以改变酒精急剧的个性!
- 对待一个酒精与一个基地使酒精成一个醇盐,这是一个更好的亲核试剂比一个中立的酒精。
- 对待一个酒精与一个酸使质子化的羟基R-OH R-OH2(+)这是一个更好的离去基团比(-)。这意味着使质子化醇可以亲电试剂N1 / SN2 /E1反应(但一般不E2,因为强酸不兼容强烈的基地!)


8。总结
- 识别类型的衬底(一级、二级、三级或甲基卤化物)是识别反应的第一步N1 / SN2 /E1/E2。
- 我个人认为更有利于从的角度执政的事情而不是逆。
- 如果烷基卤是初级,可以排除SN1和E1,排除E2除非亲核试剂是一个非常庞大的基地。
- 如果烷基卤是三级,可以排除SN2。
与二次烷基卤化物,你不能排除任何途径在某些情况下没有看亲核试剂/基地。
这就是下一个!
笔记
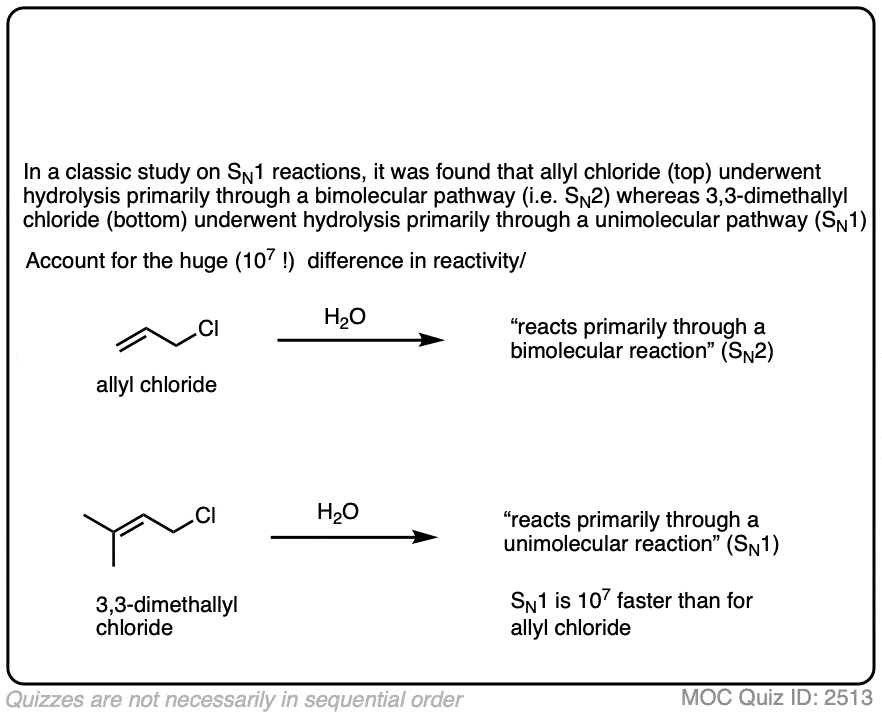
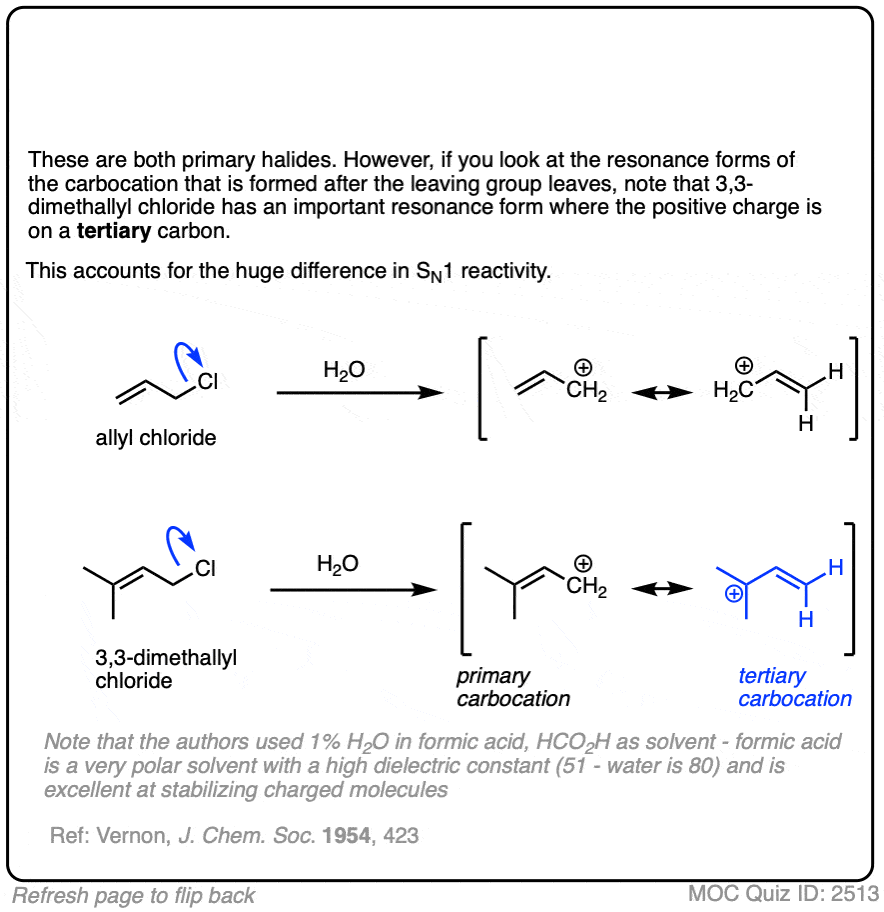
注1。也有可能的N1途径和主要操作烯丙基的能够形成非常稳定的碳正离子的卤化物,尤其是非常极性溶剂水和酒精的混合物或甲酸等。
一个经典的例子是γ,γdimethylallyl氯,SN1通路是主导。


注2。请注意,我不是说在这里E2将会是独家(100%)产品的比例E2产品将开始增加相对于SN2。在有机化学混合物的产品相当常见。
注3。三级胺(右3N)是一个例外的经验法则的一个例子,因为他们是中性的物种还能干的基地。
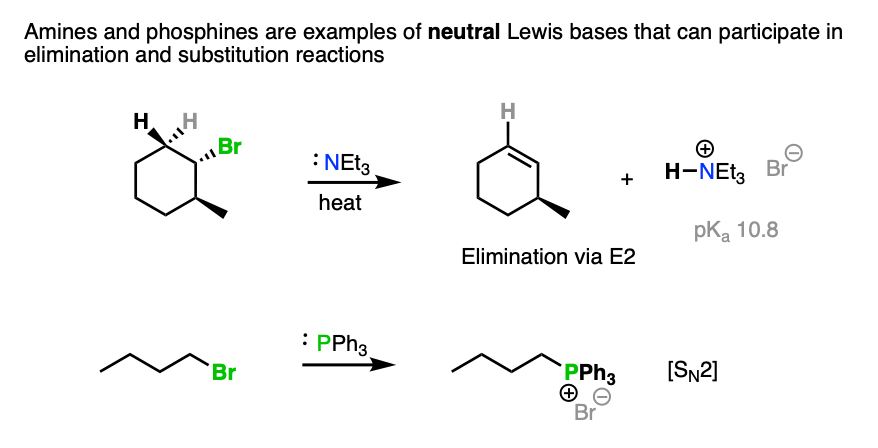

膦类化合物(如三苯基膦、产后大出血3)可怜的基地,但优秀的亲核试剂N2反应。
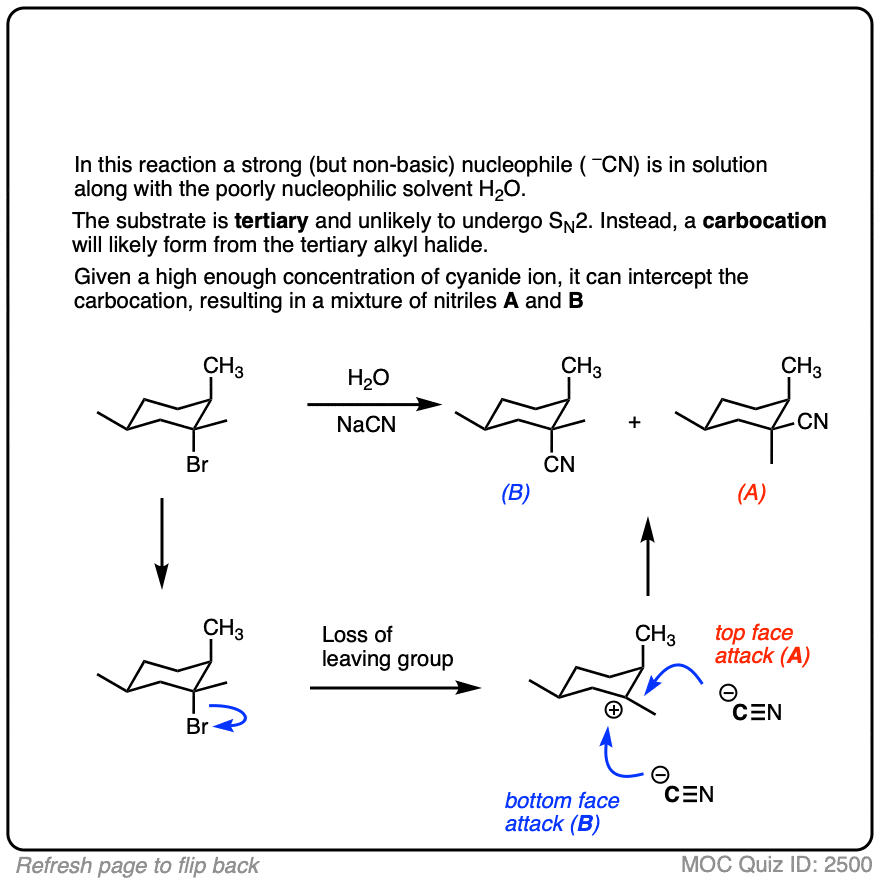
注4。如果碳正离子形成一个物种的存在,是一个很好的亲核试剂但一个贫穷的基础,如氰化物或叠氮化离子,那么这些良好的亲核试剂可以“拦截”碳正离子反应的溶剂。
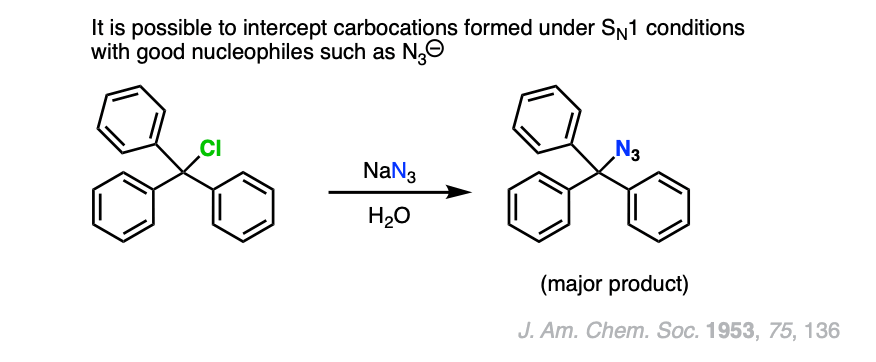

注5。当二次烷基卤化物与乙炔化物治疗,往往是主要的产品消除而不是替代产品。
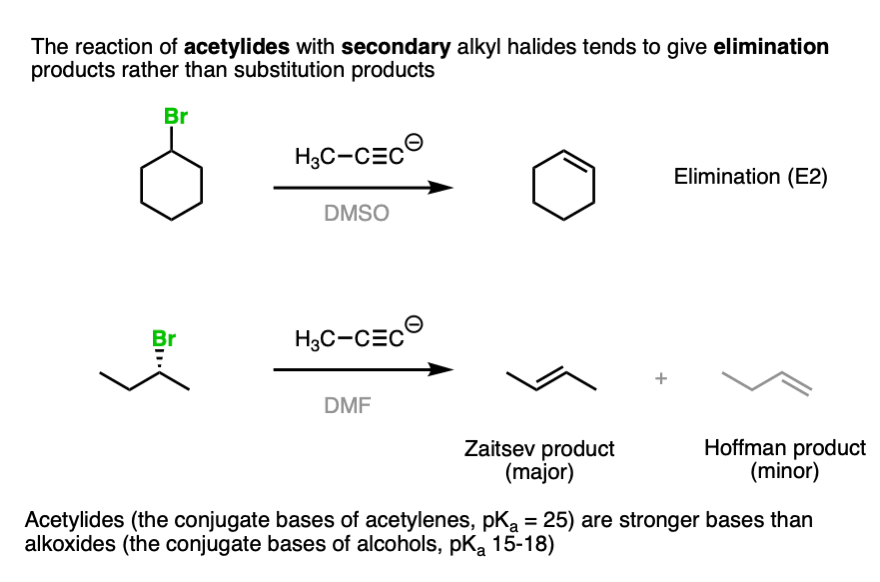

有关示例,请参见参考。
注6。这是一个方便的表为各种相对利率烷基卤化物与卤离子置换反应。
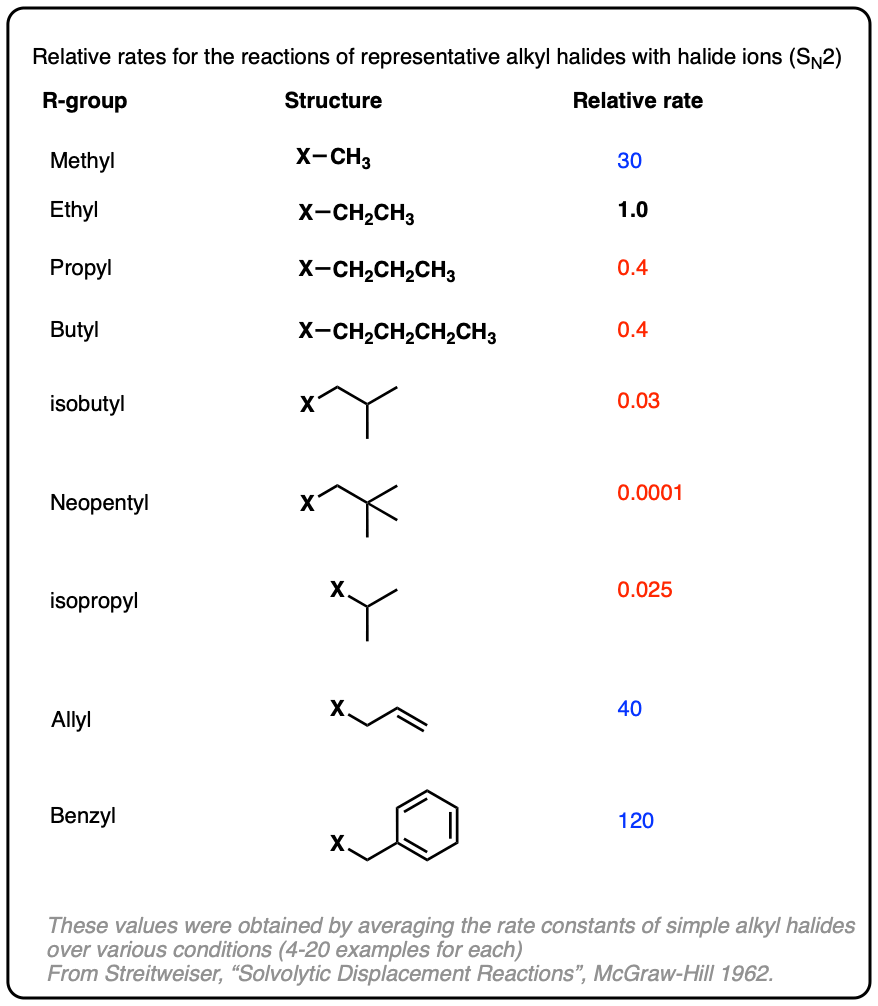

测试你自己!
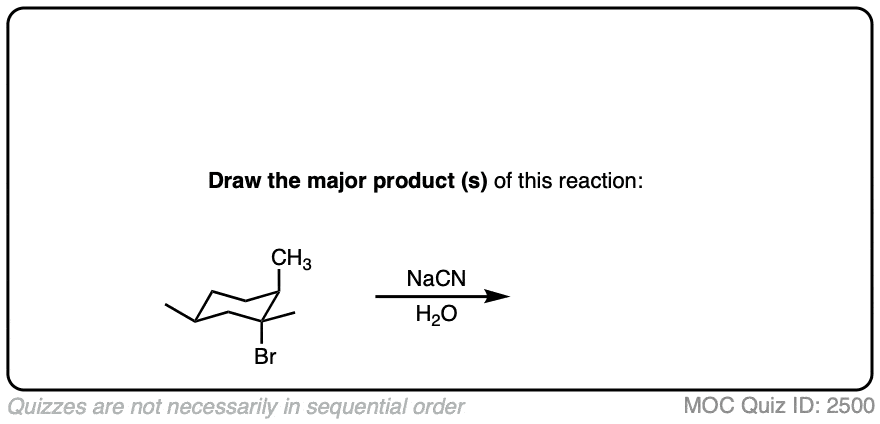






(高级)引用和进一步阅读
一个关键的参考理解之间的相互作用SN1/SN2/E1和E2反应是一个老,但非常有价值的评论教授Andrew Streitweiser(伯克利)”溶剂离解作用位移反应”(麦格劳-希尔,1962年,纽约)总结了数以百计的出版物在1960年之前。bdapp平台这本书的大部分内容是早期的再版审查通过Streitweiser轴承相同的标题。(化学评论,1956年,571年56岁)
- 的亲核位移的动力学机制烯丙基的系统。八世。的反应活性烯丙基的没有重排氯化物对双分子的替换
c·a·弗农
j .化学。Soc。,1954年,4462 - 4470
DOI:10.1039 / JR9540004462 亲核位移的动力学机制烯丙基的系统。诉反应部分烯丙基的卤化物的年代N1水解机制
c·a·弗农
j .化学。Soc。,1954年,423 - 428
DOI:10.1039 / JR9540000423
研究SN1通路(溶剂分解)数主烯丙基的氯化物。的SN1通路的水解γ,gamma-dimethallyl氯甲酸尤为重要,相对于烯丙基氯。- 的制备炔烃Dialkynes Monohalo反应-和Dihaloalkanes锂Acetylenide-Ethylenediamine复杂
史密斯w·诺维*o . f . BEUMEL Jr。
合成,1974年,441 - 443。
DOI:10.1055 / s - 1974 - 23341
研究SN2与不同的主反应的锂乙炔化物烷基卤化物(主烷基碘化和陈词滥调都快,初选烷基氯化物是缓慢的,次要的烷基卤化物给消除) - SN2与SN2′竞争
托马斯•汉森帕斯卡染色体,Lea德容,f . Matthias Bickelhaupt和特雷弗·a·哈姆林
《有机化学》杂志上2022年87 (14),8892 - 8901
DOI:10.1021 / acs.joc.2c00527
最近的论文SN2(和SN2′)反应的烯丙基卤化物与主要引用。
所以我有一个问题关于如果区分SN1或SN2反应假设衬底是6碳单链第二碳的楔形H和梯子相同碳Cl和攻击亲核试剂的Br -。你能告诉这是SN2如何?
Sn1想象5碳链和碳2楔Br和梯子H与亲核试剂的Cl -你怎么能告诉如果一个Sn1反应。这样我有问题。请尽快让我知道我有考试在周四!
这里是思维过程:
1)二次碳。在这个阶段不能排除任何可能性。
2)亲核试剂的身份/基地:Br (-)。良好的亲核试剂(带负电),弱碱。排除E2因为E2需要一个强大的基础。排除SN1 / E1因为他们操作(一般中性)基础薄弱。这使得SN2。
3)所以画产品的SN2反转配置。
你好,我只是想知道如果一个复合(R) 2-bromopropan-1-ol与NaCN进行取代反应,它导致的(R)配置产品的溴取代氰化物,其反应机理做吗?SN1还是SN2 ?
可以通过任何化合物进行进料侧攻击机制,因为它是一个次要复合?
您可能想要查看的主题“双反转”:-)特别是在基本条件。bdapp平台
先生我该什么产品预计在治疗ethylbromide t醚。顺便说一下好创建这样一个令人难以置信的博客
主要的烷基卤化物。几乎可以肯定的SN2反应。
above-given反应中形成的产品是什么?
你必须在快速前进N '发现肮脏的指南。
对于例外,主要碳正离子是可能的烯丙基的或苄基的…因为共振?感谢分享这些信息。
是的,正电荷在空的p轨道的主要碳正离子可以通过更大的离域pi-system。
在注意部分,它也可以解释为部分双键特性在乙烯基卤素和芳基卤化物吗?
卤素不会有显著的π键的字符。答案是,生成的碳正离子会非常不稳定。
如果有一个因素有利于Sn2赞成Sn1但另一个因素。
就像如果它是一个主要基质弱亲核试剂,还是三级底物在极性非质子溶剂?
好了,这些东西你必须权衡在评估这些问题。阅读部分2和3。
你好詹姆斯,你写你的文章的底部”例如,下面的烷基卤化物(“新戊基氯”)确实是主要…”但是图像显示新戊基溴。仅供参考。
噢,是的,谢谢杰西卡。固定!
有一个机会,一个主要卤代烷经历SN1反应吗?昨天在大学我这个例子:Hydrolisis(溴乙基)环戊烷。
第一个主要的碳正离子形成,后来氢化物发生转移到形成一个叔碳正离子。是可能的吗?我担心的是:第一个主要碳正离子中间体形式即使是后来迅速稳定吗?但我也认为,关于烯丙基的观众主要和第一主碳正离子形成并迅速稳定. .谢谢提前
主要的烯丙基的,是的。主要卤代烷,形成主要的碳正离子的中间是不可能的。可以有共同的重排反应,邻近组织的迁移伴随位移离去基团,通常这些类型的事情发生。
你能解释一下* * SN2为什么青睐/ E2主要卤代烃?我一直以为酸碱反应是最快的…
谢谢你非常宝贵的资源!
酸碱反应*杂原子*是快,但经验法则并不适用于E2反应,你打破了碳氢键伴随改变碳杂化的…
我不理解的东西,哪里有人费心去解释它。
当有一个主要的碳正离子,它可以通过重排为什么不会呢?然后你不能排除Sn1。
环己烷的例子,主要是连接CH2Cl起初但重排可以成为teritary…这是非常稳定。那么会发生什么呢?
谢谢。
环己烷环不会因为稳定环本身是如何重新排列。
形成机制涉及carboction总是更喜欢稳定的碳正离子重排形成的,可以通过氢化转变,甲基转移或环扩张除了HydroborationOxidation rxn和Oxymercuration Demercuration rxn carboction不能接受任何形式的重组
如果它会自动反应SN1 E1吗?
不会自动,但E1反应可以陪SN1反应。有时E1反应是不可能,比如在溴化苄的情况下在水中。
你没有给的例子
谢谢你这非常有用! !确保每个人都检查文章2和3。
你好,这是SN2发生在主酒精吗?我知道,一个主要的碳正离子是不稳定的,但如果一个甲基氢化/转变是可能的吗?它会形成一个二级碳正离子比小学更稳定的碳正离子?
对不起,SN1 *
是的,你必须使质子化酒精给共轭酸,然后离去基团是水。一个例子是蛮力形成的乙醚加热乙醇酸。
在溴丙烷的例子,为什么我们可以不考虑碳正离子重排吗?
我相信碳正离子重排可以考虑,但反应会更喜欢SN2 / E2 /重排+ SN1 / E1。如果我错了,请纠正我
在“现实生活”SN2途径更有利但教科书/试题并不总是代表了现实生活。通常情况下与二次烷基卤化物教师测试重组的机会,等等。这就是为什么重要的是要意识到这些类型的情况。不过你是对的——它可以依赖老师。
我的老师总是强调互换发生时,我一直在想:在多大程度上)
对于例外,主要碳正离子是可能的烯丙基的或苄基的…因为共振?
是的!
carboctaion秩序稳定Triphenylcarbocation > tropilium > biphenylcarboction > cylopropenylcarb > 3°C > phenylcarb > Allylcarb > 2°> 1°> methylcarb > doublebondedcarb > benzylcarb > tripplebondedcarb一般prensence苯、分支和饱和度增加稳定的碳正离子平面sp2指控物种
你能告诉如何当一个化合物被共振稳定,而且它只重要Sn1或E1反应机制而不是另外两个?
化合物是由共振稳定如果共振结构的形成是可能的碳正离子。这SN1和E1才重要,因为只有这两个反应,形成碳正离子。例如看isoprenyl溴他上面了。如果你删除Br离去基团上留下一个正电荷碳之前。如果你移动双键在右边,共振结构,正电荷的叔碳,使它更稳定的碳正离子。如果反应是SN2或E2不要担心共振,因为它发生在一个步骤,不形成碳正离子。
简单:寻找π-conjugated系统。在这些结构共振是可能的。
对不起!我得到了答案经过第2部分,3、4 . .
产品形成在上述给定的反应是什么?