胺
斯特合成的氨基酸
最后更新:2023年2月9日|
斯特氨基酸合成
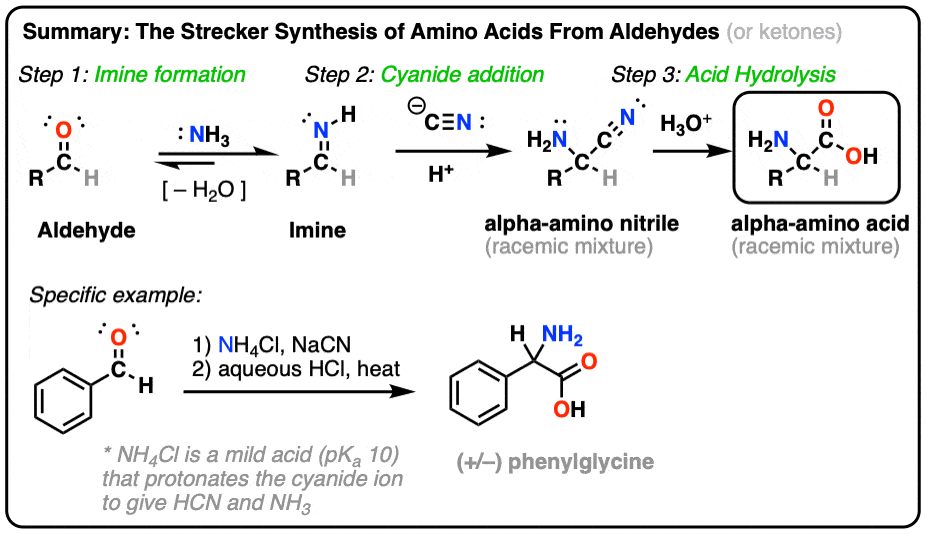
- 的斯特合成的合成是一个两步的过程吗氨基酸。
- 它的开始氰根离子亚胺,形成一个alpha-amino腈。然后水解与强酸(如)给一个alpha-amino酸。
- 通过改变R组亚胺,各种各样的氨基酸这样可以。
表的内容
1。斯特合成的氨基酸
不喜欢氰根离子是什么?
好,好,这是一个致命的毒药,在实验室里就应该十分认真对待它。
但除此之外,这是一个优秀的亲核试剂可以和各种各样的亲电试剂发生反应,导致一个新的碳碳键终止官能团(腈),可以在许多不同的方式阐述了。
下面是三个例子氰根离子的行动。当添加到烷基卤化物,它提供了腈。它攻击酮和醛,氰醇。同时也攻击醛和酮的含氮的表亲,否则称为亚胺。这导致alpha-amino腈。
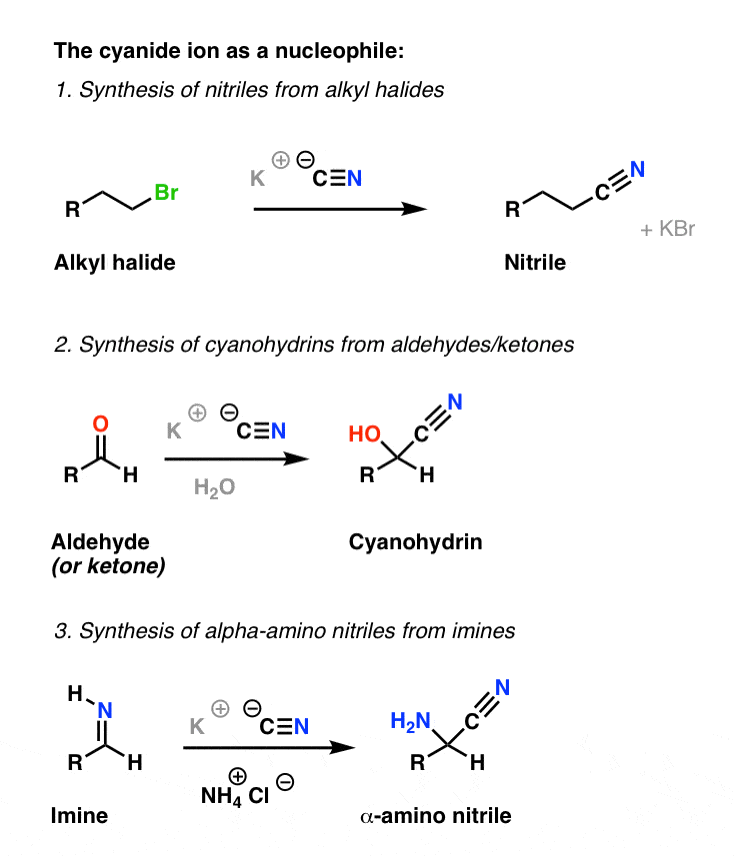
现在,也许“α氨基酸腈”不是一个名字,很容易卷舌头。
但也许你已经听说过…氨基酸?
我们说过,腈可以转换成各种各样的物种:胺(通过减少)酮(通过添加格氏其次是水解),最重要的是为了我们的目的,羧酸(通过酸性水解)。(看到帖子:酰胺的水解)
所以“alpha-amino的水解腈“水酸应该会给一个alpha-amino酸(简称“氨基酸”,)。
事实上它!
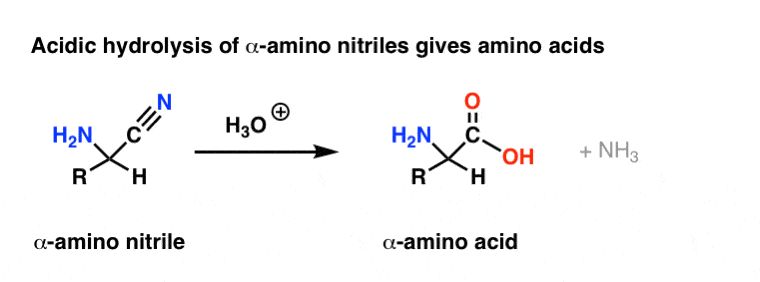
醛和酮的过程使氨基酸(通过亚胺)被称为斯特合成的氨基酸。
根据“R”组的亚胺,各种各样的氨基酸可以使用这种方法合成。
举例来说,这里的苯丙氨酸的合成,20”proteinogenic”(即。来合成)氨基酸编码在信使核糖核酸(mRNA):
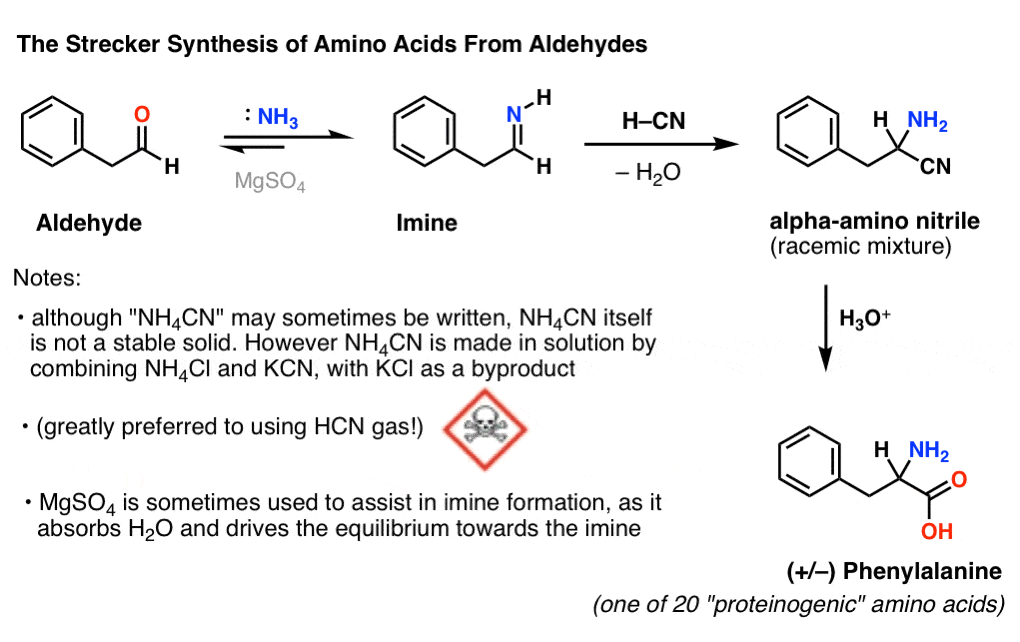
最初的斯特协议(1850)采用NH3和氰化氢(HCN)。
鉴于大多数化学家不到热衷于使用氰化物气体,(注1)安全协议利用轻松处理固体NH4Cl (铵氯)和KCN(氰化钾)通常采用对NH注24CN]。这里的想法是,在弱酸性(pK一个9)铵离子使质子化的醛对攻击与解放NH,激活它3。NH攻击后3、质子转移和消除水,然后氰根离子攻击合成亚胺(或者,更有可能的是,共轭酸亚胺,称为“iminium”)。这导致α氨基酸腈。
添加盐吸水MgSO等(干燥剂)4经常帮助形成的亚胺,因为它有助于推动平衡向亚胺。
2。斯特合成的机制分为两部分
斯特的第一部分涉及alpha-amino的形成腈途中,proteinogenic氨基酸缬氨酸(通常缩写为Val或者V)。
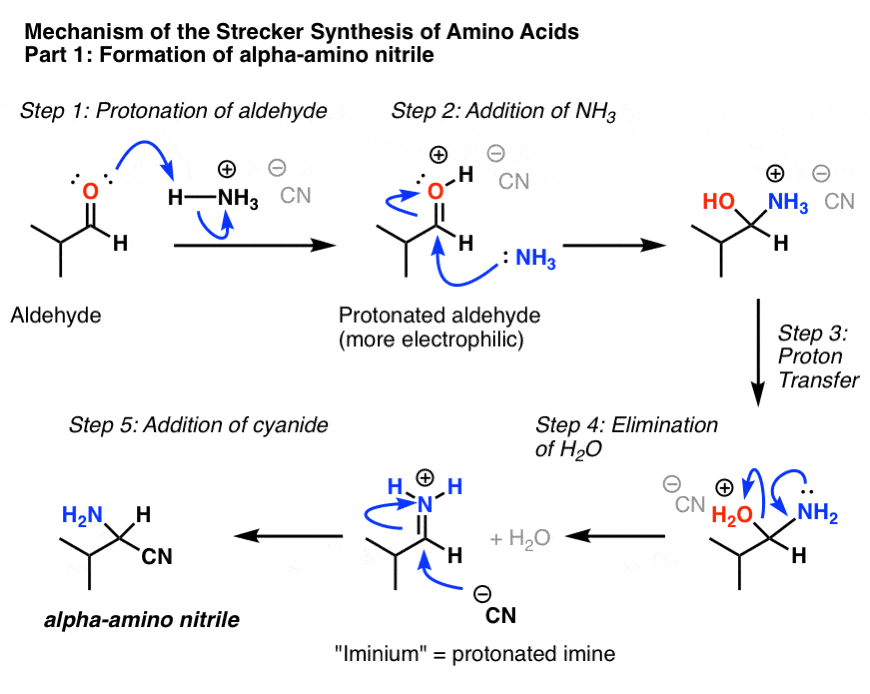
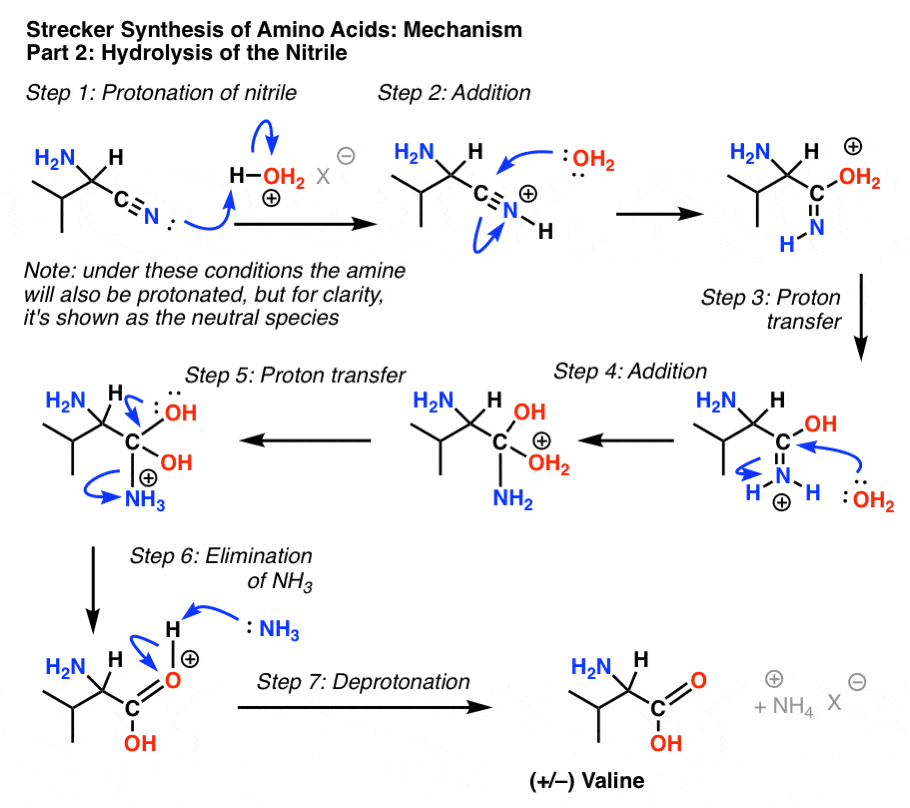
下一步是水解腈与水酸。这是描述为H3与反离子不明O + X。
质子化作用的腈(注意:北半球2也会使质子化在这些条件下,但是为了清楚起见,描绘成中性的物种)紧随其后的是攻击的水(步骤2)。质子转移到氮(步骤3)其次是增加水碳(步骤4),而另一个质子转移到氮(步骤5)带正电的结果铵,这是消除NH(步骤6)3。去质子化的羰基氧气(步骤7)完成的过程,给予缬氨酸作为外消旋混合物的对映体。
3所示。Non-Proteinogenic氨基酸的合成:左旋多巴
你可能会问:那又怎样?
蛋白质(例如从大豆或乳清)是现成的,天然的氨基酸可以廉价和容易从水解蛋白质的分离。由于自然提供了他们丰富的供应,为什么要让他们?
原因有很多。这里有一个:proteinogenic氨基酸通常以多种方式修改在活的有机体内,一个方法来访问这些少见,氨基酸变成了必要的修改。一个例子是左旋多巴,一个重要的治疗帕金森病(在体内转化为多巴胺和肾上腺素)。
在体内酪氨酸的,左旋多巴是由羟基化,但有机化学家还没有完全掌握了如何执行这个反应在实验室里。另一种方法是通过特建立左旋多巴反应。从3开始,4-dihydroxyphenylacetaldehyde NH(下图)治疗”4CN”(NH相结合制成的4Cl和KCN解决方案)酸性水解导致紧随其后外消旋混合物L - D -二羟基苯丙氨酸。纯左旋多巴可以通过手性决议。(注意,DL-DOPA是一样的(+ / -)多巴。只是不同的描述方式外消旋混合物)(注3]
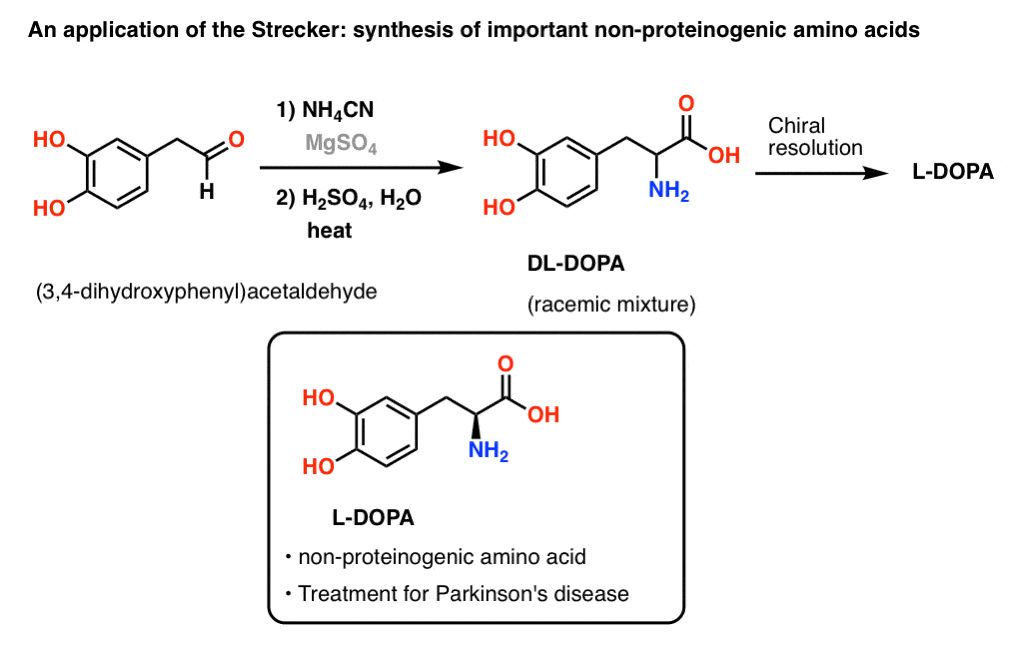
斯特还可以应用于构建非天然的氨基酸有不自然的立体化学,荧光标记、叠氮化(“点击”化学的应用程序),和许多其他属性。这不是一个“边缘”的反应。斯特是很重要的。
一个警告:如图所示,特提供外消旋氨基酸与自然使用光学纯氨基酸。
所以只能特被修改,使其产生主要是一个对映体?
简短的回答是肯定的。的第一个应用程序之一手性辅助(1963)在斯特的反应原田。在过去的几年中,各种催化不对称方法已经开发出来,这不在我们的讨论范围。我提到你的工作雅各布森和首歌为进一步阅读。
具有讽刺意味的是光学纯的左旋多巴是解决这个问题不是通过斯特,但通过催化氢化作用,由诺尔斯教授和他的团队在杜邦公司在1970年代。这种获得的份额2001年诺贝尔化学奖不对称催化。
笔记
注1。这1941年的论文建议在实验室吸烟(在昔日的一个普遍习惯)在处理HCN,因为它给了香烟口味特征。
注2。而不是使用NH4Cl和KCN使用NH似乎更有效4CN。唉,NH4CN不是一个稳定的固体,不幸的财产给了HCN气体。这是使它的解决之道原位与北半球4Cl和KCN。
注3。如果你覆盖碳水化合物化学,你可能会认识到斯特是一个表哥的Kiliani-Fischer方法糖链延伸。这是同样的想法!
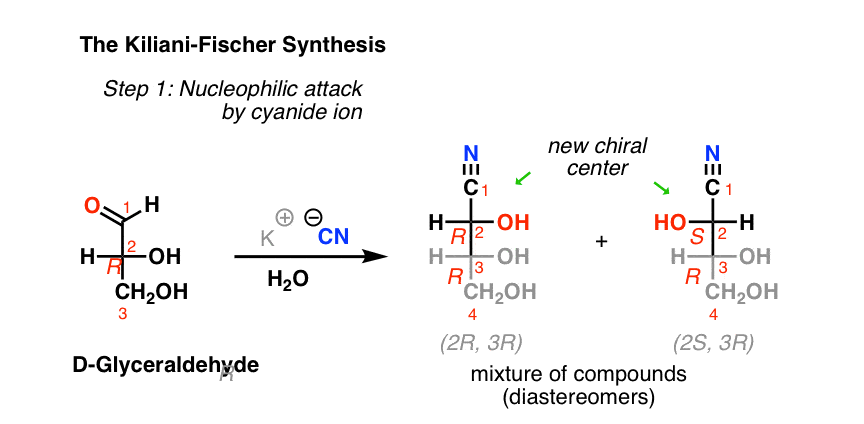
现实生活的例子
现实生活中的例子:
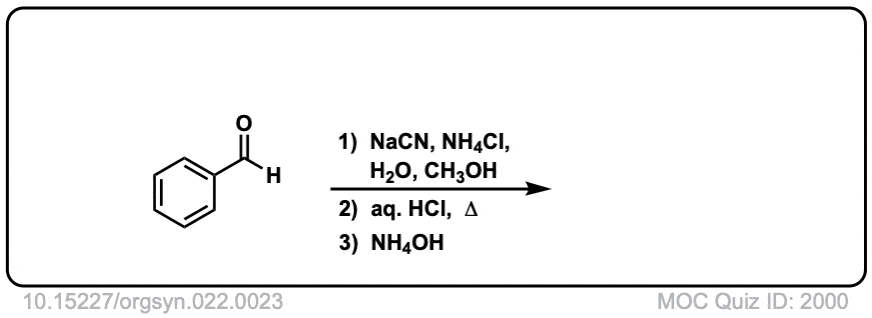
Org。Synth。1942年,22、23
链接DOI: 10.15227 / orgsyn.022.0023
 点击翻转
点击翻转
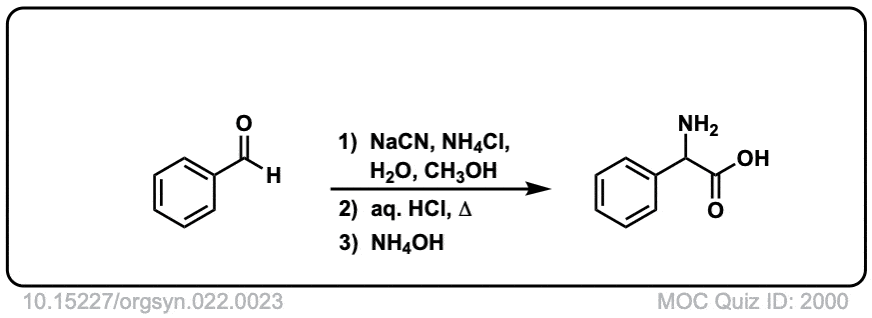
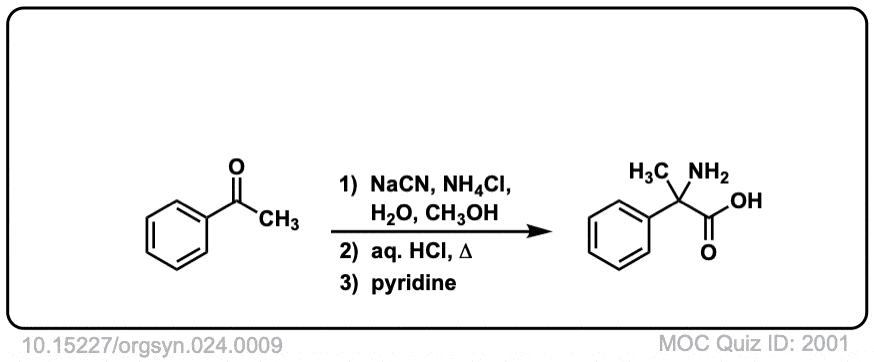
Org。24岁的Synth。1944 9
链接DOI: 10.15227 / orgsyn.024.0009
 点击翻转
点击翻转
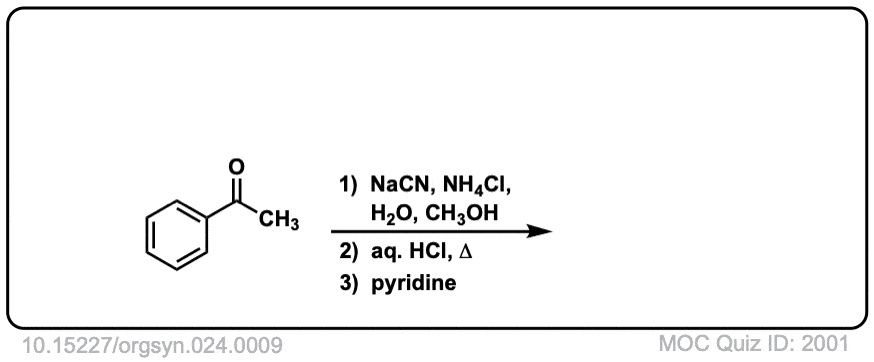
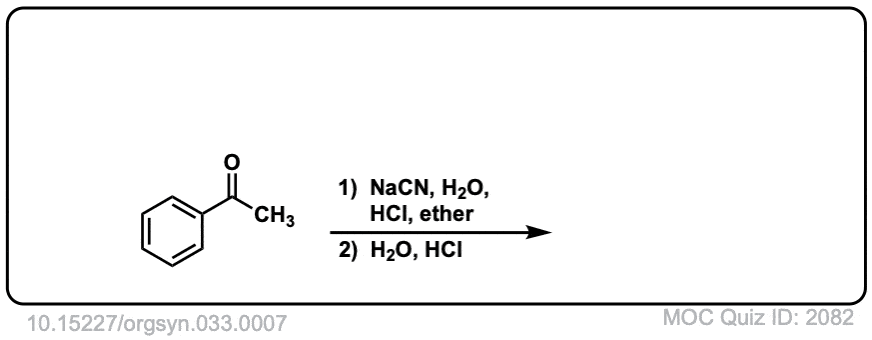
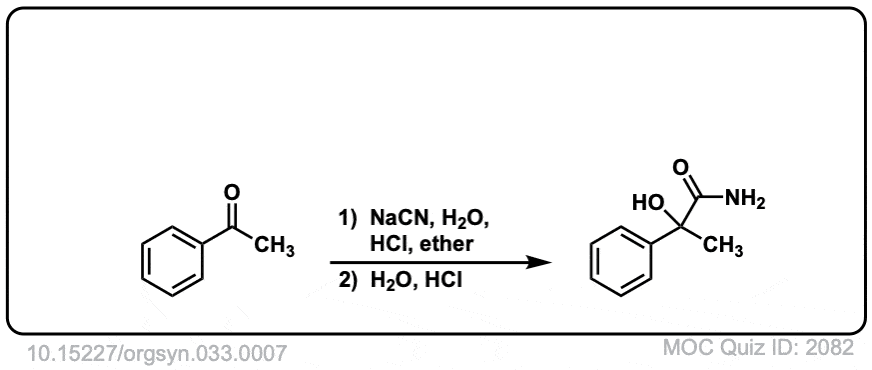
Org。Synth。1953年,33岁的7
链接DOI: 10.15227 / orgsyn.033.0007
 点击翻转
点击翻转
(高级)引用和进一步阅读
这是一个非常简单但强大的反应,将三个组件:一个醛/酮、氰化物和一个胺。该产品是一种a-aminonitrile可以水解氨基酸。
- Ueber死kunstliche陶冶der Milchsaure和杯neuen,民主党氢氨乙酸homologen Korper
阿道夫·斯特
而已。Lieb。安。化学。1850年,75年(1)27-45
DOI:10.1002 / jlac.18500750103
我认为这是斯特的原始论文反应(不幸的是我不能读德语)。但它有150多年的历史了,说明这个反应很简单和鲁棒性。 - dl-ALANINE
c·肯德尔和b·f·麦肯齐
Org。Synth。1929年,94
DOI:10.15227 / orgsyn.009.0004
一个古老的但可再生的过程通过斯特合成外消旋丙氨酸。 - 拆分催化添加HCN Ketoimines。第四纪的催化合成氨基酸
切赫Vachal和埃里克·n·雅各布森
有机的信2000年,2(6),867 - 870
DOI:10.1021 / ol005636 +
不对称反应特克。注意,这个使用HCN作为氰化物的来源,这是值得庆幸的是不习惯整洁或气体,但之前在溶液中生成的反应TMSCN +甲醇(见注10)。
你好,我想知道为什么会发生质子转移哦和NH3 +第一部分第3步的机制?如果O电负性大于N,岂不是更不可能承担积极的形式电荷当它变成水吗?是因为水是更好的比NH3(基本)LG吗?非常感谢!
到的所有步骤的NH3离开平衡状态。但一旦氨基质子化了的NH3和NH3的叶子,酸会把它变成NH4 +和反应本质上是不可逆转的。
这就跟你问声好!
我很好奇关于现实生活中的例子# 3。
为什么腈转化为酰胺基取代羧酸像其他例子吗?
感谢你的阅读!
酸的酰胺是一个中间的途中。如果使用了足够的条件温和,酰胺可以孤立。
你如何准备二羟基乙醛二羟苯。
与boronic酸亚胺芳基氨基酸没有钯和基地
在氨基酸合成莫泽酸可以使用
氰醛和莫泽酸铵instu准备手性纯氨基酸骨干。
叠氮化反应的咪唑和丙二酸给diazido复合,可以减少氨基功能。酯可以funtiinalized
我不知道我想问的问题或建议我给输入。
我可以对酶反应制备氨基酸。
嗨. .我只是想知道什么是中间体在这个过程. .都是3,即亚胺,imminium离子和α氨基腈的中间体或只是其中两个吗?
你好,伟大的解释!我只是想知道为什么氨添加到醛,而不是直接氰化物?因为我知道氰化物比氨亲核的?
氨被添加到醛因为之前,首先需要形成亚胺氰化物的攻击。如果添加了氨添加氰化物后,该产品将氰醇。不是我们想要在这种情况下,:-)