焊接、结构和共鸣
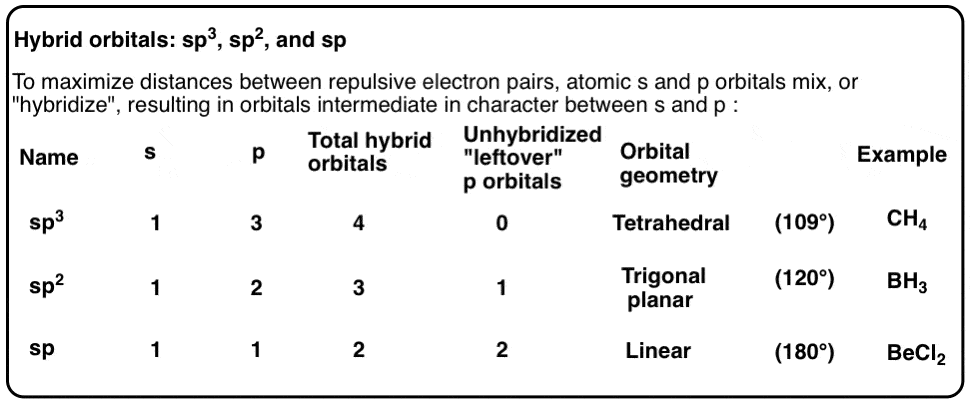
杂化轨道和杂交
最后更新:2022年12月13日|
今天的文章杂化轨道。这里有一个快速的总结:
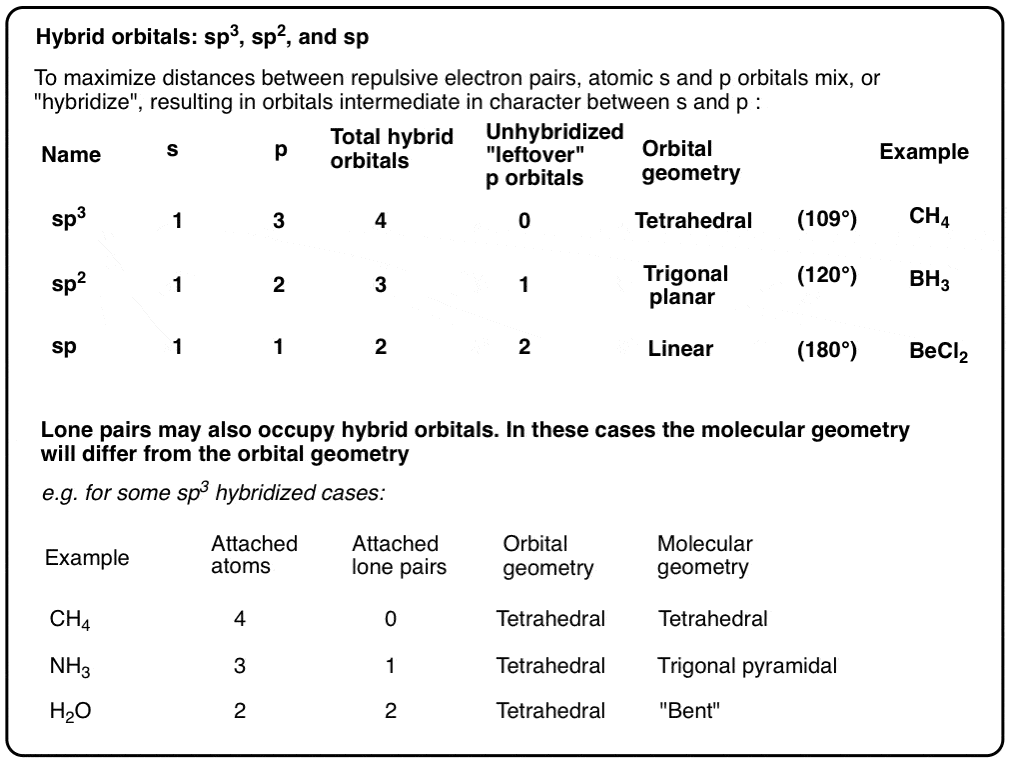
【注:这篇文章由马修·皮尔斯有机化学解决方案。问马特调度在线辅导会议在这里。]
表的内容
- 轨道所参与碳氢键的四面体排列碳甲烷(CH4)?
- 结合在碳杂化轨道:一个解释
- 一个流行的类比:混合苏打水
- sp3杂交准确描述中的原子排列(板凳)元素连着四个原子…
- …的数量以及情况(原子+孤)= 4
- sp2杂交
- sp杂化
- 总结- - -杂化轨道
- 笔记
1。轨道所涉及的四面体排列的甲烷(CH4)?
在过去的文章甲烷的结构我们问我们如何知道甲烷是四面体(见文章:我们怎么知道甲烷是四面体吗)。
基于碳的轨道(2 s和2 p)我们可能会天真地期望的三个碳氢键排列沿着x, y,和z轴,分别和另一个在任意角度(如135°左右)
但是,这种事情在中国经常发生在科学、我们美丽的直观的假设被一些恼人的实验事实:
- 甲烷没有可衡量的偶极矩(我们的“合理的”结构,在左,将会有一个可衡量的偶极矩)
- 金刚石的晶体结构是四面体,相同碳原子间键的长度和角度为109.5度。这不是我们希望如果我们处理债券之间的“纯”2 s和2 p轨道!
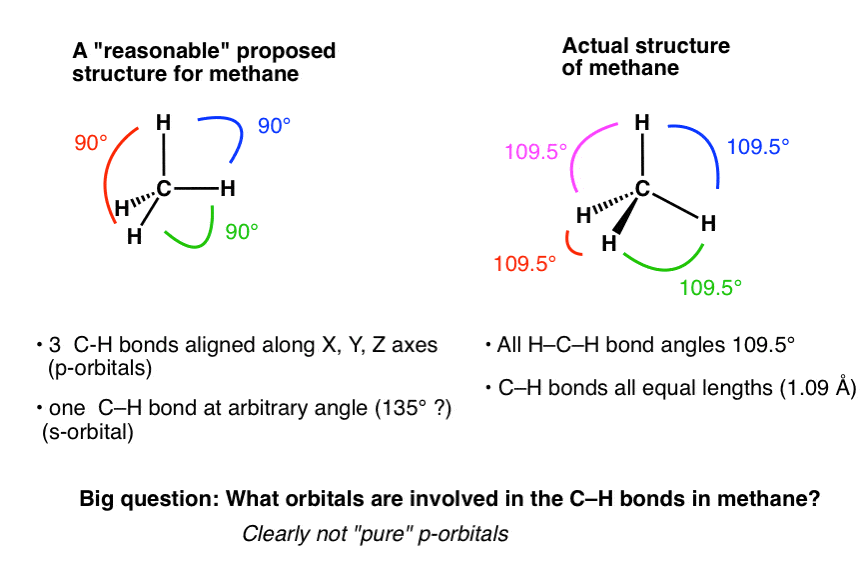
回想起来,几何意义。碰巧109.5度是最大化的方向的四个键对之间的距离,从而减少他们的排斥相互作用。换句话说,几何是直接结果的“相反电荷的吸引,同种电荷相互排斥”。
但是我们如何描述轨道用于给,键角吗?
这是一个真正的chin-scratcher。他们不可能是纯2 s轨道(只有一个2 s轨道,)。他们不可能是纯粹的p轨道,自从p轨道在90°是一致的。
什么见鬼的轨道是他们吗?
2。结合在碳杂化轨道:一个解释
莱纳斯鲍林问同样的问题在他的经典著作,化学键的性质(1931)(pdf这在很大程度上赢得了1954年诺贝尔化学奖。
鲍林的解决这个难题,我们今天仍然适用,是以下:
- 没有一个成键轨道在甲烷100%或100% p。相反,他们是杂化轨道每个插件都有部分年代性格和部分p的性格。
- 3 2 p轨道和单一的2 s轨道杂交(即。,mix) to create four hybrid sp3轨道,四面体地排列在中心碳原子。
- 的四个杂化轨道两个提到25%和75%。
- 对于甲烷,这些sp3杂化轨道与氢的1 s轨道重叠形成碳氢键
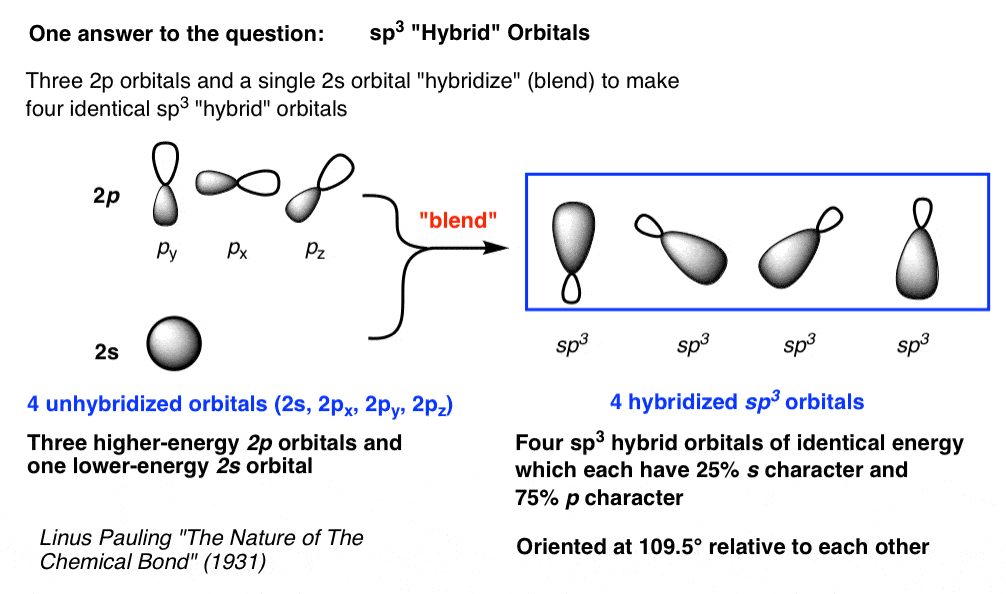
我将诚实的在这里。许多学生不喜欢这个解释。
当然,这是令人困惑的。为什么?
我认为当我们最初学习轨道,我们凭直觉认为容器-有点像原子特百惠举办电子发生各种可爱的形状。

电子,然后,可以想象到像“水果”,使在这些容器(严格的限制:每集装箱2 !)。不是很惊讶我们的直觉当我们学习,他们可以从容器,容器内原子甚至彻底离开原子。
什么是令人惊讶的是,当我们打开冰箱,发现可爱的小球体,哑铃型特百惠容器改变他们的形状和相互合并它们的属性!这违反了我们的直觉如何容器的行为!

这是量子世界,人!如果这不使迷惑你…它f *王应该!
展望未来,我不要求你理解甚至“相信”杂交在深的数学或理论水平。这不是我们的目的所必需的(鲍林是一个伟大的老师。你可以阅读原始鲍林纸,在这里,如果您选择]
我只是建议你试一试暂停你的怀疑,因为使用这个杂交将帮助我们提供一个合理的模型很多的分子结构、几何结构和行为。
3所示。一个流行的类比:混合苏打水
之前我们在任何进一步的潜水,这是我认为是一个有用的比喻(谢谢,史蒂文),可以帮助获得的观点。
- 想象你有四瓶流行:一瓶雪碧(S)和三瓶百事(P)。
- 现在想象一下涌出来,混合在一起,然后re-filling每个瓶子的混合物。
- 守恒定律流行说,你还有四瓶的液体。但是现在流行既不是纯粹的百事可乐雪碧或纯;这是一个两者之间的混合。
- 具体地说,现在每个瓶雪碧25%和75%百事字符。
- 我们可以称之为“混合”流行,如果你喜欢,sp3
![]()
这有点像发生了什么我们2 s和2 p轨道。通过混合2和3 2 p轨道,我们现在有四个轨道有25%和75% p字符。(尽管如此,重要的是,它的瓶子的形状改变,不仅内容)。
最后一步是安排这四个轨道在四面体的角落,它允许四个电子对之间的最大距离(同性相斥!)
这是如何合理化帮助我们吗?
- 它解释了甲烷的四面体分子几何,4相同H-C-H键角(109.5°)
- 它解释了4相同的碳氢键的长度(和债券的优势)的甲烷
- 它解释了缺乏甲烷的偶极矩,由于电子的四面体排列对允许部分费用取消(即向量总和为零)
- 模型甚至有助于理顺某些反应如何发生,我们现在不会(如。背后攻击的年代N2反应发生在空的“反键轨道180°碳氢键轨道成键,如果你一直读下去)
4所示。sp3杂交准确描述中的原子排列(板凳)元素连着四个原子…
这并不仅仅适用于甲烷。它适用于任何情况(板凳)元素是连着四个原子。显然四面体碳是最显著的例子,我们将探索,但它也适用于四面体(如氮。NH4(+)]甚至四面体(如硼。男朋友4(-)]。
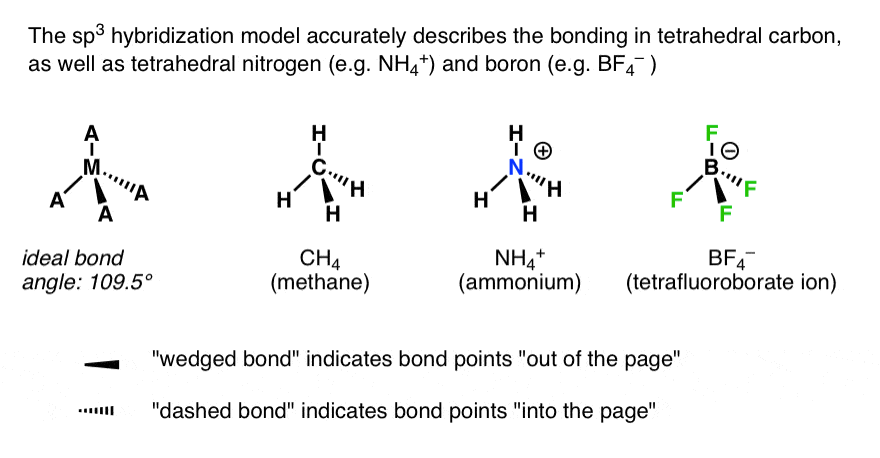
5…。以及情况的数量(原子+孤)= 4
轨道的四面体排列甚至当一个或多个双是一个非键孤对电子(如果你遇到VSEPR理论,大多数人都有有机化学,他们抵达的时候,这不该是一个震惊。)
例如,氨(NH)3),“甲基阴离子”(CH3-),水合氢离子(H3与4 O +)都有一个中心原子对电子:3对成键电子和一对非键电子。正如我们所看到的,理想的几何安排四双电子是四面体,使杂交中心原子的sp3。这使得分子的“钢琴凳”对中心原子的原子排列,我们称之为“三角形金字塔”几何。
另一种方法是,中心原子四面体轨道几何(sp3)和三角形的平面分子几何。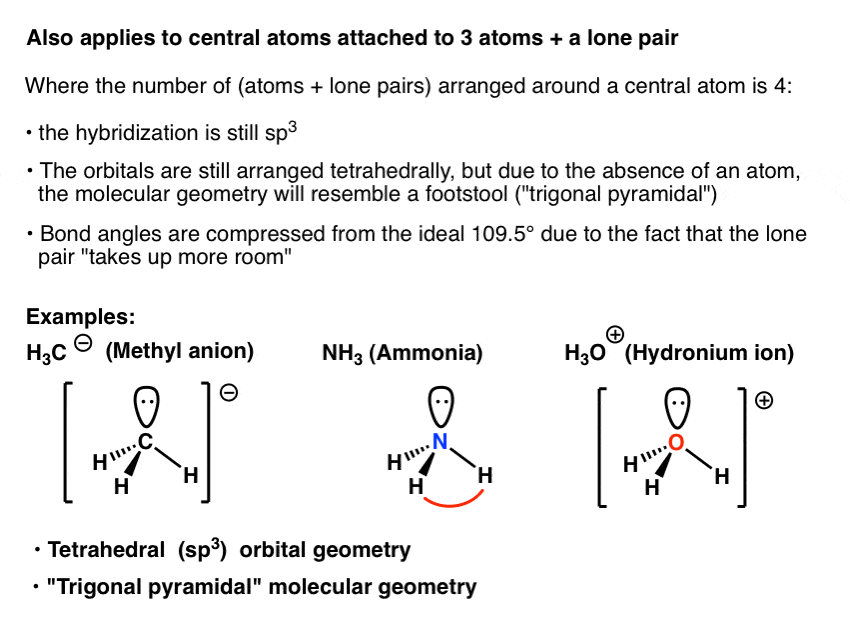
一个有趣的事实是,这些被压缩的键角从理想的角度为109.5°。在氨H-N-H债券角度,例如,是107度。我们合理化,这是由于这一事实非键孤对排斥比一双“正常”键,可能因为它是接近原子,产生一个更强的影响力。
这种偏离“理想”在H键角更大2有两个孤对O(水)。的杂交仍然是sp3,轨道几何仍然是四面体,但形状(“分子几何”)产生的分子是“弯曲”。

的确,鲍林的引人注目的成就之一杂交模型是正确占水的偶极矩。如果水是完全“线性”,很多人可能会天真地认为之前我们学过化学,偶极子会彼此抵消。
“弯曲”几何的另一个例子是在酰胺阴离子NH找到2- - - - - -两个孤氮。
快速表可能有助于总结我们建立的所有关于sp3杂交:

6。sp2杂交
让我们回到我们的瓶子类比。说我们只有混合和两瓶百事可乐雪碧,不是三。
这留给我们什么呢?
![]()
这给了我们三个混合瓶流行一个剩下的unhybridized瓶子。
以此类推,如果我们把2 s轨道有两个2 p轨道,我们获得三个sp2杂化轨道,和一个剩下,unhybridized p轨道。
当这三个sp2轨道充满了电子对,键角最大化他们的距离是120°。
这给了我们一个“三角形平面”sp的安排2unhybridized p轨道的轨道,直角的平面。它像一个奔驰的象征。
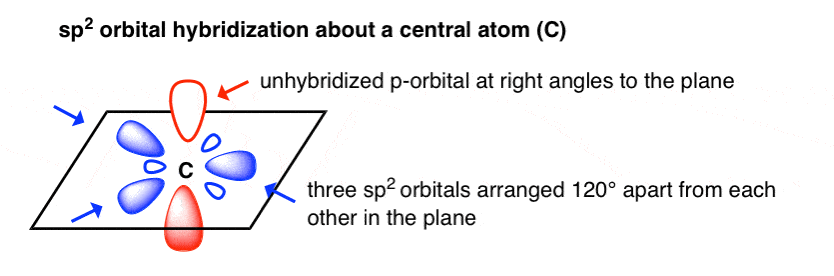
一个经典例子三角形平面几何是硼烷,黑洞3三对成键电子,安排在120°。三角形平面几何是碳正离子还发现,如甲基阳离子,CH3+。

你可能会想:unhybridized p轨道在哪里?
在平面直角。回想一下,这三个p轨道相互成直角。所以无论两个p轨道杂化,第三(剩余的)p轨道将成直角的平面形式(就像z轴垂直于xy平面)
在BH3和碳正离子,的unhybridized p轨道是空的。
还有一个很常见的情况,sp2然而,几何是观察。如果相邻原子有单电子unhybridized p轨道,如果这些p轨道可以重叠,债券可以结果。这一现象被称为“pi-bonding”。(我们将有更多的关于它。)
π键——通常称为,“双键”——需要一个unhybridized p轨道,以形式。
碳,氧,氮原子在下面的例子中,所有有π键(双键)sp2杂化。轨道分离的角度大约120°。
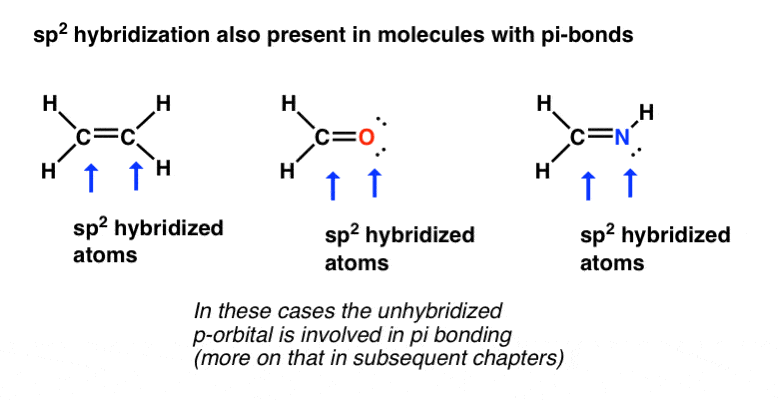
注意,可以在sp孤2杂化轨道,就像我们看到在北半球3和H2O在sp的情况下3杂交。还需要注意的是,在midde分子(甲醛),氧各有两个孤对(sp2杂化轨道),在右上角分子氮有一个孤对sp2杂化轨道。
当孤对存在时,键角将略低于120°的孤对可以被认为“房间”。
7所示。sp杂化
让我们看看最后一个可能的情况下。如果只有一个p轨道与s轨道?
这给了我们两个混合“sp”轨道被分开的最大角度:180度。我们称这样的安排,“线性”。每个混合sp轨道有50%和50% p字符。
![]()
这两个unhybridized p轨道都在直角sp杂化轨道。
例如,这里的轨道是什么样子在氯化铍(BeCl2)Cl-Be-Cl键角为180°。如果我们认为Cl-Be-Cl债券是沿着x轴,两个(unhybridized) p轨道将沿着y和z轴,分别。
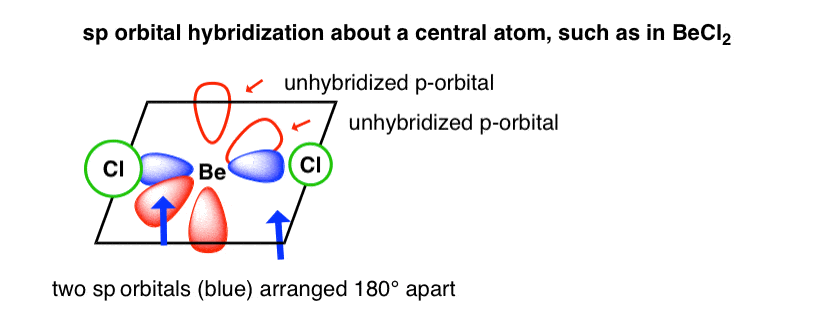
sp -杂交通常情况下观察到的有吗两个对单个原子π键。最突出的例子是“三键”,见炔烃,腈,一氧化碳(CO)。在这些情况下,不仅是碳原子sp-hybridized,但氮(也是如此腈原子)和氧(一氧化碳)。
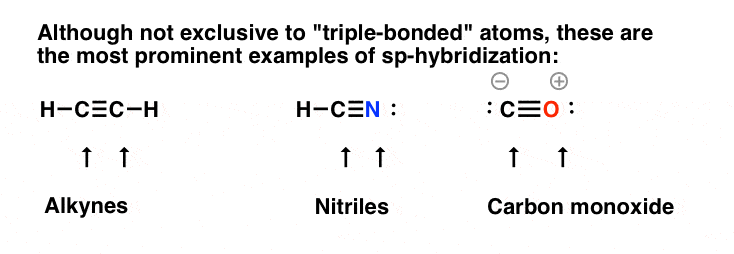
还请注意,孤可在sp-hybridized轨道,见腈和一氧化碳。
sp -杂交不是独家三键原子——例如,中央碳丙二烯和乙烯酮参与两个π键,因此sp-hybridized——但三键是最立即识别的例子。
8。总结- - -杂化轨道
好的。这是无意中很长的文章的要点:
- 电子对相互排斥。在没有轨道杂交,周围的键角CH4将局限于p轨道的几何形状(90°)。这是积极有利的s和p轨道杂交形成sp3轨道,结果在一个更大的电子对的分离和键角为109°(即在四面体的顶端)。这也适用于中心原子的孤对电子与电子对NH等3和H2O。
- 当只有两个p轨道参与杂交,三个sp2杂化轨道的结果,采用三角形平面轨道几何。剩下的(unhybridized) p轨道,在直角三角形的平面上,可以是空的(如黑洞3)或独占(如分子含有π键)。
- 当只有一个p轨道参与杂交,结果是两个sp杂化轨道和一个线性轨道几何。剩下的两个p轨道可供pi-bonding(如triply-bonded有机化合物等炔烃和腈),或者可以是空的(如BeCl2)。
- 注意,中心原子周围的轨道总是4所示。轨道是创建和销毁杂交;他们只是改变了。
在下一篇文章我们将只提供迅速确定一个超级简单的方法杂交中心原子。
再次感谢马特与人合写。问马特调度在线辅导会议在这里。
谢谢你伟大的解释。
我想知道是什么决定了有多少用于杂交p轨道。例如,CH4使用3三个p轨道杂化,而BH3只使用两个。
谢谢你!
的数量(单键+孤)中心原子
- 4(单键+孤)- - > sp3杂化——一个s轨道,3 p轨道
- 3(单键+孤)- - > sp2杂化——一个s轨道,2 p轨道
- 2(单键+孤)= - > sp杂交- 1 s轨道,1 p轨道。
CH4共有4个中心原子周围的单键和零。sp3杂化——一个s轨道,3 p轨道
BH3共有3中心原子周围的单键和零孤。sp2杂化- 1 s轨道,2 p轨道
目前的工作显示了不适用的化学键的泡利不相容原理,和一个新的化学键的理论模型提出了基于海森堡测不准原理。
看到第104 - 88页。回顾。苯三电子债券的基础上。(泡利不相容原理,海森堡的不确定性原理和化学键)。http://vixra.org/pdf/1710.0326v1.pdf
泡利不相容原理和化学键。
泡利不相容原理,这是量子力学的基本原理,它声称,两个或两个以上相同的费米子(与半整数自旋粒子)不能同时出现在相同的量子态。
沃尔夫冈·泡利,一个瑞士的理论物理学家,1925年制定这一原则[1]。在化学完全泡利不相容原理通常视为禁止三电子债券存在的多样性为1.5,但它可以表明,泡利不相容原理并不禁止三电子债券的存在。为此,详细分析了泡利不相容原理。
根据泡利不相容原理相同的费米子组成的一个系统,两个(或更多)粒子不能在同一个州[2]。波函数的相应公式并给出行列式的引用(这是一个标准的费米子体系的考虑),但我们将我们的注意力集中在推导:“…当然,在这个配方,泡利不相容原理只能适用于系统的弱相互作用粒子,当一个人能说(至少大约在单个粒子的状态)”[2]。泡利不相容原理,只能适用于弱相互作用的粒子,当一个人可以谈论单个粒子的状态。
但是如果我们回想一下,两个原子核之间的任何经典形成化学键(这是原子轨道的根本区别),它以某种方式“拉动式”电子一个在另一个,这是合乎逻辑的假设形成的化学键,电子不再被视为弱相互作用粒子。证实了这种假设是化学键的概念引入的早些时候作为一个单独的semi-virtual粒子(自然组成部分粒子“部件”不能弱相互作用)。
表示化学键的章节中给出“海森堡的不确定性原理和化学键”断然拒绝关于化学键的语句作为一个系统的弱相互作用电子。相反,它遵循从上面的描述,在化学键,电子“失去”他们的个性和“占领”整个化学键,也就是说,化学键的电子“尽可能多的互动”,直接表示不适用泡利不相容原理的化学键。此外,动量的量子力学的不确定性和协调,事实上,严格表明化学键的电子系统的“最大限度”强烈相互作用的粒子,和整个化学键是一个单独的粒子中,没有一个“个人”电子的概念,它的速度、协调、能源、等,描述。这从根本上是不正确的。化学键是一个单独的粒子,称为“semi-virtual粒子”,它是一个复合粒子,由单个电子(强烈相互作用)和核之间的空间位置。
因此,引入一个三电子债券多样性为1.5从化学的角度来看是合理的(简单地解释了苯分子的结构,芳香性,结构的有机和无机物质,等等)证实了泡利不相容原理和化学键的逻辑假设系统的强相互作用的粒子(实际上一个单独的semi-virtual粒子),结果泡利不相容原理不适用的化学键。
1。泡利w .超级窝Zusammenhang des Abschlusses der Elektronengruppen在原子麻省理工学院der Komplexstruktur der Spektren - z phy。765 - 783,1925,31日。
2。A.S.达维多夫。量子力学。第二版。出版社“科学”。莫斯科,1973年,p . 334。
海森堡的不确定性原理和化学键。
化学键的进一步分析,让我们考虑一个电子的康普顿波长:
λc.е。= h / c(我*)= 2.4263 * 10 ^ (-12)m
电子的康普顿波长等于波长的光子的能量等于电子的静止能量本身(标准的结论如下所示):
λ= h / (m * v), E = h *γ,E =我* c ^ 2, c =γ*λ,γ= c /λ
E = h *γ,E = h * (c /λ)=我* c ^ 2,λc.е。= h / c(我*)
路易德布罗意波长λ,我是电子的质量,c,γ是光的速度和频率,h是普朗克常数。
更有趣的考虑会发生什么在一个地区一个电子线性尺寸小于电子的康普顿波长。根据海森堡测不准在这个领域,我们有一个量子力学的不确定性至少势头m * c和量子力学的不确定性的能量至少我* c ^ 2:
Δp≥mе* c和ΔE≥我* c ^ 2
这是足够的虚拟正负电子对生产的。因此,在这样一个地区电子可以不再被视为一个“对象”,因为它(电子)花部分时间在“电子+一对(正电子+电子)”。由于上面,一个电子在距离小于康普顿长度是一个有无限个自由度系统及其交互应该描述量子场理论的框架内。最重要的是,转换到中间状态“电子+一对(正电子+电子)”进行每一次~λc.е. / c
Δt =λc.е。/c = 2.4263 * 10^(-12)/(3*10^8) = 8.1*10^(-20) s
现在我们将尝试使用所有上述描述化学键使用爱因斯坦的相对论和海森堡的不确定性原理。要做到这一点,让我们做一个假设:假设一个电子的波长在玻尔轨道(氢原子)是电子的康普顿波长相同,但在另一个参照系,因此有一个137倍康普顿波长(由于相对论的影响):
λc.е。= h / c(我*)= 2.4263 * 10 ^ (-12)m
λb。= h /(我* v) = 2 *π* R = 3.31 * 10 ^ (-10) m
λb. /λc.е。= 137
玻尔半径R = 0.527Å,。
由于氢原子的德布罗意波长(根据波尔)是137倍电子的康普顿波长,很合乎逻辑的假设将弱137倍的能量交互(光子波长越长,频率越低,因此能量)。我们注意到1/137.036是一个精细结构常数,基本物理常数描述电磁相互作用是引入科学的力量在1916年由德国物理学家阿诺德·索姆费尔德相对论修正的测量在描述框架内的原子光谱的n·波尔的原子模型。
描述化学键,我们使用海森堡测不准原理:
Δx *Δp≥ћ/ 2
考虑到137倍的能量交互弱化,海森堡测不准原理可以书面形式:
Δx *Δp≥(ћ* 137)/ 2
根据最后一个方程,电子的量子力学动量的不确定性在化学键必须至少我* c,和量子力学的不确定性在能源不小于我* c ^ 2,这也应该是足够的虚拟正负电子对生产的。
因此,化学领域的结合,在这种情况下,一个电子不能被视为一个“对象”,因为它(电子)将花部分时间在“电子+一对(正电子+电子)”,因此它的交互应该被描述在量子场论的框架。
这种方法可以解释,对于多电子化学键(两电子、三电子等),电子间的斥力是克服:由于化学键实际上是一个“沸腾的质量”的电子和正电子,虚拟正电子“帮助”克服电子之间的排斥力。这种方法假定化学键实际上是一个封闭的空间袋(一种潜在的能源意义上的),“沸腾”的真实电子以及虚拟正电子和电子发生,和潜在的“体积”袋实际上是一个“量”的化学键和量子力学的空间测量电子的位置的不确定性。
严格地说,这样的考虑,电子不再有一定的能量,动量,坐标,并不再是一个“质点”,但实际上占用化学键的“卷”。可以说,在化学键单个电子是没有人性的,失去了个性,事实上,它不存在,但真正有“沸腾的质量”的电子和虚拟正电子与电子的波动变化。即化学键实际上是一个单独的粒子,如前所述,semi-virtual粒子。此外,这种方法可以扩展到基本粒子的结构如一个电子和正电子的:一个基本粒子在这个考虑是一个脉动真空封闭在一定空间袋,这是一个潜在的对这些波动。
尤其值得注意的是,在这个考虑,电子是强烈相互作用的粒子,因此泡利不相容原理并不适用于化学键(更多细节,请参阅部分“泡利不相容原理和化学键”),不禁止存在相同的三电子债券多样性为1.5。
上面是很容易证明的例子1长度的化学键。德布罗意的波长是书面形式(化学键的长度L = 2 *Δx):
λ= 2 *π*Δx
和海森堡的不确定性比的形式:
Δx *Δp≥(ћ* 137 * 2 *π)/ 2
从中我们得到:
L *Δp≥ћ* 137 * 2 *π
L是化学键的长度,和Δp每个电子的动量的量子力学的不确定性在给定的化学键。
那里,我们得到一个公式来决定在化学键动量的不确定性:
Δp≥(ћ* 137 * 2 *π)/ L
有必要的计算为1的长度,我们得到:
Δp≥(ћ* 137 * 2 *π)/ 10 ^ (-10)
Δp≥9.078 * 10 ^(-22)公斤* m / s
也就是说,脉冲的不确定性比我大* c
(我* c = 2.73 * 10 ^(-22)公斤* m / s)
(很明显,电子速度的不确定性将大于光速),应根据我们的假设。
看到第104 - 88页。回顾。苯三电子债券的基础上。(泡利不相容原理,海森堡的不确定性原理和化学键)。http://vixra.org/pdf/1710.0326v1.pdf
苯三电子债券的基础上:
审查。苯三电子债券的基础上。(泡利不相容原理,海森堡的不确定性原理和化学键)。http://vixra.org/pdf/1710.0326v1.pdf
1。苯分子结构的基础上,三电子债券。
http://vixra.org/pdf/1606.0152v1.pdf
2。实验确认存在的三电子债券和理论依据它的存在。
http://vixra.org/pdf/1606.0151v2.pdf
3所示。一个简短的分析化学的债券。
http://vixra.org/pdf/1606.0149v2.pdf
4所示。补充三电子债券存在的理论依据。
http://vixra.org/pdf/1606.0150v2.pdf
5。three-electrone债券理论在四个使用简短的评论。
http://vixra.org/pdf/1607.0022v2.pdf
6。审查。苯三电子债券的基础上。http://vixra.org/pdf/1612.0018v5.pdf
7所示。量子力学方面的l·鲍林的共振理论。
http://vixra.org/pdf/1702.0333v2.pdf
8。MO方法和VB的量子力学的分析方法从pq的位置。
http://vixra.org/pdf/1704.0068v1.pdf
9。审查。苯三电子债券的基础上。(泡利不相容原理,海森堡的不确定性原理和化学键)。http://vixra.org/pdf/1710.0326v1.pdf
Bezverkhniy之上(viXra):http://vixra.org/author/bezverkhniy_volodymyr_dmytrovych
谢谢詹姆斯(Matt)也为另一个说明性的文章。
另一件事一直困扰着我,这也是与这个话题有关,是氧气的杂交(特别是解释104.5°的键角水)。
我交谈过的很多人,教授和意见似乎是很分裂。
一方面,人们说,氧气与像碳一样,两对孤电子将从109.5°角到104.5°。
另一方面,人们认为s和p轨道的氧气也大力远杂交和这个模型只是一个简单的但不准确的解释。
根据这两个氢债券两个p轨道的角度90°,但由于排斥不完全坐在p-axes但略(104.5°),导致贫困轨道重叠(有利不利,但比杂交)。
我听到的第三种方法是弯曲的规则(亨利·弯曲),这表示,在一个sp ^ n杂化轨道,n不需要一个整数。所以孤的轨道会有更多提到(因为接近原子核)和氢更两个(因为离原子核更远)。
也许有一天,如果你有时间和资源可以讨论这个话题。
我很感兴趣你的承担。
最好的祝福来自奥地利。