自由基反应
烯丙基溴化
最后更新:2022年12月7日|
烯丙基溴化和苄基的溴化:它是什么,它是如何工作的呢?
激进分子在前面的博文中,我们已经看到了溴可以选择性地与叔碳氢键反应(键的强度93千卡每摩尔)二级(96千卡每摩尔)和初级(100千卡每摩尔)碳氢键。
如果你回想一下,债券离解的能量是一个很好的指南预测激进的稳定,那么你不会惊讶“苄基的”和“allyllic”碳氢键也可以有选择地溴化。这些碳氢键尤其弱因为激进的形成通过碳氢键均裂破坏是由共振稳定。
表的内容
- 烯丙基的和苄基的溴化:例子
- 自由基是由共振稳定
- 苄基的机制与溴溴化2而光/热
- Br2不是一个合适的烯丙基溴化试剂,因为它形式附近的二溴化
- 使用N-Bromo琥珀酰亚胺(国家统计局)确保Br的低浓度2
- 笔记
- (高级)引用和进一步阅读
1。烯丙基的和苄基的溴化:例子
那么,什么是烯丙基的和苄基的卤化呢?这里有一个例子。
以甲苯和治疗与Br2在光的存在,按照这个过程或N-Bromosuccinimide (国家统计局)在一个激进的发起者+热(或光)和苄基的碳氢键之一是C-Br所取代。
(注意,苄基的立场是苯环碳相连;苯环碳氢键的本身是“苯基”碳氢键)。
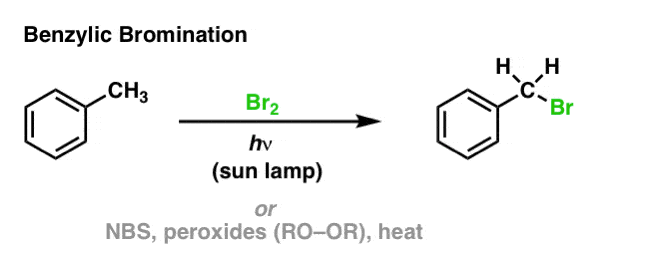
这里有一个例子烯丙基溴化丙烯,这次使用国家统计局和过氧化物(或加热)
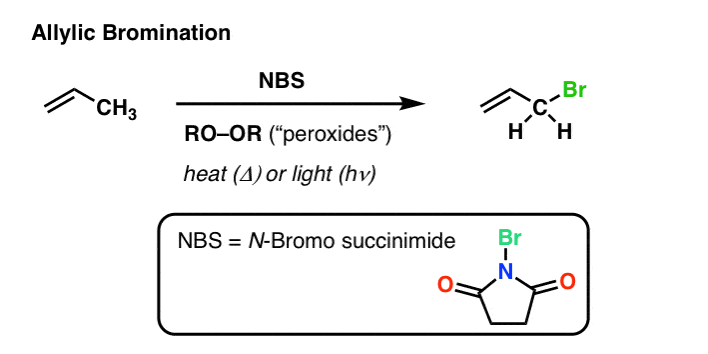
我们花了大量的时间讨论自由基的稳定性尤其不稳定,尤其是初级自由基。
所以在这种情况下有什么不同呢?这是什么”国家统计局“东西?
2。自由基是由共振稳定
回想一下,自由基是由共振稳定,和债券离解能量(12)又名“债券的优点”措施均裂债券乳沟。
因此,甲基(上图)并不是普通的甲基-由共振产生的自由基非常稳定!
因此当我们看键离解为苄基的和能量烯丙基的碳氢键不应该令人惊讶的发现,这些债券的优势很弱(89 - 90千卡每摩尔的初选烯丙基的或苄基的激进)相对于叔碳氢键(93千卡每摩尔)。
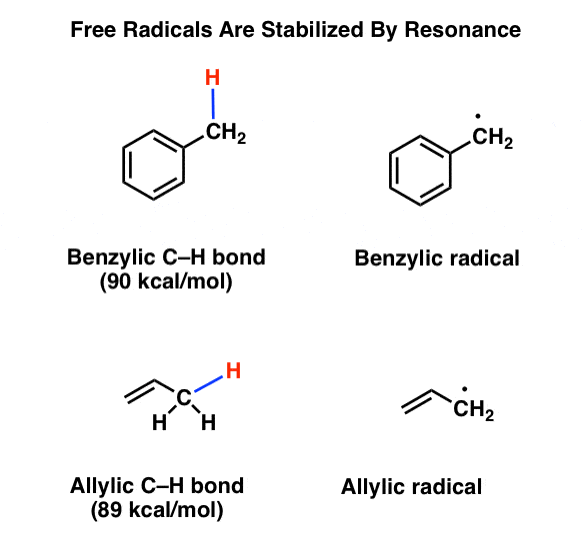
怎么可能烯丙基的或苄基的溴化工作吗?
3所示。苄基的机制与溴溴化2而光/热
对苄基的溴化,希望想象机制非常简单:初始化(通过光或热),溴彻底打破了碳氢键(形成苄基的激进)[传播步骤# 1)和溴苄基的激进的攻击2重新生成溴激进(传播步骤# 2]。这两个步骤重复直到Br的浓度2运行低,于是激进的链终止将会发生。
(见开始,传播、终止]
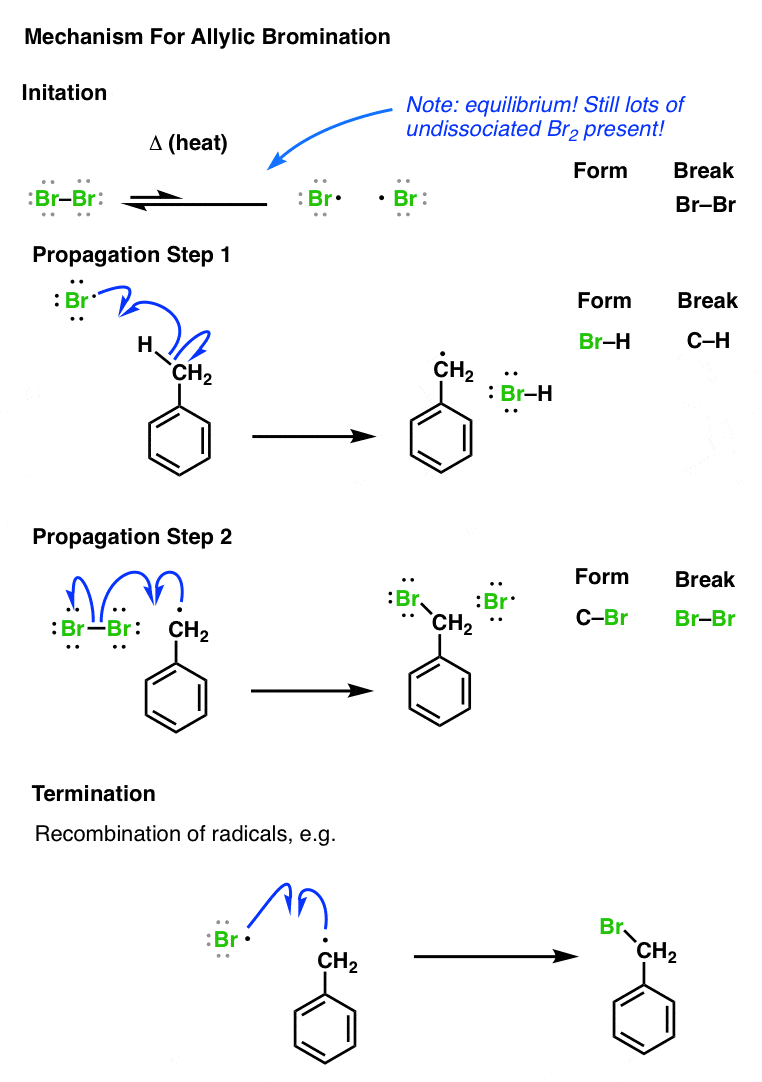
4所示。Br2不是一个合适的烯丙基溴化试剂,因为它形式附近的二溴化
让我们转向烯丙基溴化。你看到任何原因治疗和Br分子下面吗2可能导致的问题?
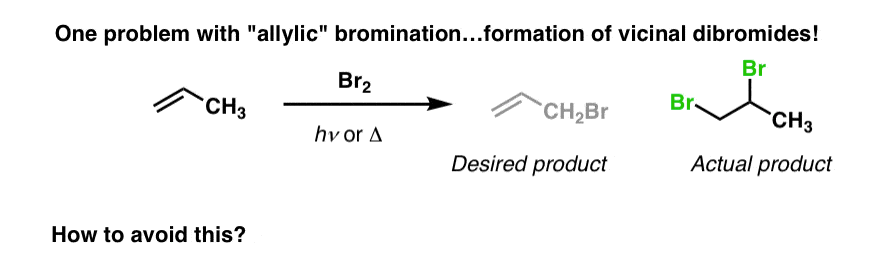
您可能还记得,烯烃与溴反应2形成本地的二溴化,实际上是将会发生什么如果我们将1相当于Br2与一个烯烃。
问题在于这样一个事实:我们有1相当于Br2游泳,其中只有一小部分在任何给定的时间会存在溴激进的(由于起始步骤)。
我们如何解决这个问题和支持激进的替换dibromination吗?
想象一下,如果你愿意,我们有一个非常低的溴的浓度2。如果Br的浓度2保持低,不仅dibromination率会降低,溴激进的相对浓度相对于Br吗2将会增加。因此,碳氢键的速度相对于dibromination抽象会增加,这将允许我们的烯丙基溴化产品形成更高的收益率。(注1]
当然,这将创建一个新的问题:我们如何生成一个低,常数Br的浓度2吗?
5。使用N-Bromo琥珀酰亚胺(国家统计局)确保Br的低浓度2
事实证明,有一种方法。如果bromonium离子源N-bromosuccinimide(国家统计局)存在与一个跟踪数量的酸(哈佛商业评论),哈佛商业评论会做出反应国家统计局琥珀酰亚胺和Br2。(注2]
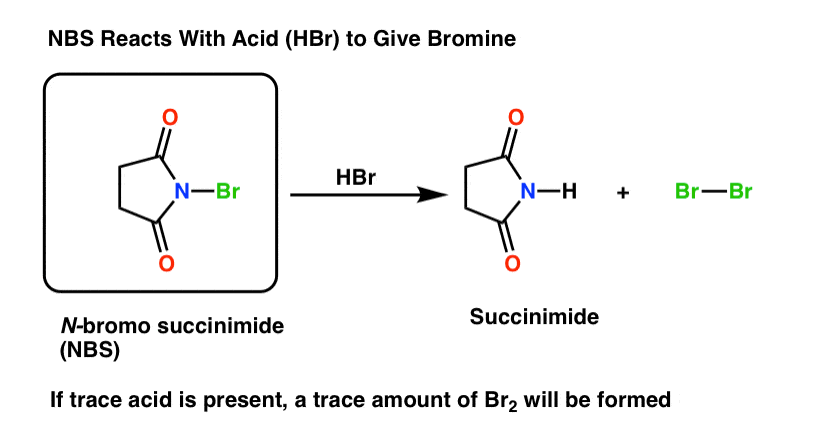
因为一个相当于哈佛商业评论生成一个相当于Br2、溴2完成后将生成唯一的吗传播步骤# 1。注3]。这使溴的浓度2低,允许自由基反应竞争烯烃加成反应。
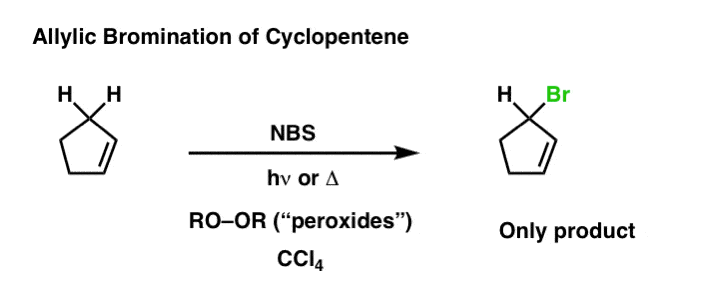
在所有其他方面烯丙基溴化反应是与上面所示的苄基的溴化反应机理。然而在一些* *的情况下有一个额外的转折烯丙基的重排,我们将简要讨论在接下来的帖子。
在下一篇文章:烯丙基的重排
笔记
注1。如果这个解释听起来有点不满意,你的东西。毕竟,没有这种减少的浓度Br•吗?一个额外的并发症是理论研究表明强有力的证据的怪兽分子形成的速率决定步骤bromonium离子(即参与的烯烃和两个Br分子2)。减少溴的浓度2因此大大减少的速度吗bromonium离子形成(因此dibromination)相对于自由基卤化。
注2。碰巧,国家统计局已经离开一段时间通常会含有微量哈佛商业评论(以及Br吗2,给它一个黄色或橙色)。出于这个原因,如果做一个激进的反应国家统计局这是常见的避免再结晶之前使用,因为它会移除跳开始的微量酸的反应。
(高级)引用和进一步阅读
- 死综合des斑蝥素。
齐格勒,K。Schenck, G。Krockow,已经Siebert。Wenz a和韦伯,h (1942),
贾斯特斯李比希安。化学,551:1 - 79。
DOI:10.1002 / jlac.19425510102
齐格勒的报告使用国家统计局为烯丙基溴化,从1942年。 - 溴化N-Bromosuccinimide和相关化合物。沃尔齐格勒反应。
卡尔。Djerassi
化学评论1948年43(2),271 - 317
DOI:10.1021 / cr60135a004
早期的但有用的评论烯丙基溴化卡尔教授Djerassi(斯坦福大学),类固醇化学做出了许多重要的贡献。 - 添加和替换定律在卤素原子反应
亚当,J。、GOSSELAIN p &金手指,p。
自然171年,704 - 705 (1953)。
DOI:10.1038 / 171704 b0
“金手指机制”烯丙基溴化提出的,国家统计局Br2服务提供一个低浓度。早些时候提出的机制succinimidyl激进链载体,这是不正确的。应该注意的是,除了Br•烯烃* *发生在某种程度上,但反应是可逆的,如果Br2和哈佛商业评论浓度低,除了产品将恢复到开始烯烃。 - 的高温氯化烯烃碳氢化合物
弗雷德里克·f .防锈、威廉·e·沃恩
《有机化学》杂志上1940年05年(5),472 - 503
DOI:10.1021 / jo01211a002
早期,关键观察。生锈,沃恩和发现Cl2来烯烃是喜欢在低温下,而在更高的温度吗烯丙基的替换占主导地位。 - 替换的比例添加氯的反应烯烃在稀释四氯化碳溶液
t·d·斯图尔特,肯尼思•国防部和乔治·Stenmark
美国化学学会杂志》上1937年59(9),1765 - 1766
DOI:10.1021 / ja01288a507
找出一个重要拼图的机制烯丙基的卤化,从1937年。烯丙基的替换被看好在除了低浓度的卤素(氯)。 - 机制的苄基的溴化
格伦·a·罗素查尔斯。DeBoer,凯瑟琳·m·德斯蒙德
美国化学学会杂志》上1963年85年(3),365 - 366
DOI:1021 / ja00886a040
苄基的溴化遵循相同的机制烯丙基溴化本文解释了。国家统计局(N-Bromosuccinimide)是一种方便的自由基溴化试剂,和机械的研究包括以下文件国家统计局: - 苄基的机制与N-Bromosuccinimide溴化
e·皮尔森和j·c·马丁
美国化学学会杂志》上1963年85年(3),354 - 355
DOI:10.1021 / ja00886a029
这些论文教授j·c·马丁(伊利诺斯)在他职业生涯的早期,他做这工作之前最著名(研究“hypervalent”分子,包括开发的“Dess-Martin Periodinane”)。 - Chain-Carrying物种的身份与N-Bromosuccinimide:溴化的选择性取代N-Bromosuccinimides对甲苯代替
e·皮尔森和j·c·马丁
美国化学学会杂志》上1963年85年(20),3142 - 3146
DOI:10.1021 / ja00903a021 - N-bromosuccinimide。的机制烯丙基溴化和相关的反应
h . Incremona马丁和詹姆斯·卡伦
美国化学学会杂志》上1970年92年(3),627 - 634
DOI:10.1021 / ja00706a034 - 激进的溴化环己烯亚兰的溴:添加和替换
w·麦克米伦和John b . Grutzner
《有机化学》杂志上1994年59(16),4516 - 4528
DOI:10.1021 / jo00095a029
介绍小心动力学研究表明,Br的低浓度2(如提供的不洁净的国家统计局在极地)将支持激进的替换加成反应。 - 4-BROMO-2-HEPTENE
l·格林伍德·m·d·Kellert和j . Sedlak
Org。Synth。38卷,p。8 (1958)。
DOI:10.115227 / orgsyn.038.0008
一个可靠的程序烯丙基溴化与国家统计局在有机合成。 - 二溴化o-XYLYLENE
艾米丽·f·m·斯蒂芬森
Org。Synth。34卷,p。100 (1954)
DOI:10.15227 / orgsyn.034.0100
一个可靠的过程与溴苄基的溴化2在有机合成。 - 在芝加哥自由基化学的发展
弗兰克·r·梅奥
《化学教育1986年63年(2),97
DOI:1021 / ed063p97
对于那些感兴趣的历史科学,这种回顾性梅奥讲述了他如何和Kharasch发现了“过氧化效应”,从而有机化学的一个新领域。
为什么你不能使用Br2和过氧化物苄基的情况下?
你可以在这个过程:http://www.orgsyn.org/demo.aspx?prep=CV4P0984
如果您正在使用国家统计局是明显污染的哈佛商业评论/ Br2,那么可以添加多个溴吗?
这是标准程序在许多反应添加一个轻微的摩尔过剩(如10%)的试剂来确保完成反应。我没有见过的“坏”国家统计局分析量化Br2内容可以有多高,但我不希望它是超过10%。
所以我的简短的回答是不,不是任何重要程度,将影响收益率超过10%。
如果* *很多Br2在场,两件事可能发生。首先,如果不洁净的国家统计局是添加到解决方案和溶解,在不增加烯烃第一,的Br2解放可以re-combine琥珀酰亚胺(毕竟,这是国家统计局如何形成)。
如果相对高浓度的Br2持续下去,然后更有可能的是,一开始看到dibromination烯烃(如添加Br2)在双键,溴化倾向于3日以来订单总体和低浓度Br2避免这个副反应。
在这种情况下,又有较低的收益率将所需的产品,但不是双溴。
如果添加一个大过剩的国家统计局,是的,它可能是一个问题。
时将产品3 -亚甲基环己烯与哈佛商业评论反应吗?解释
你需要确定的动力学和热力学的产品是什么。//m.deriinvest.com/2017/03/22/reactions-of-dienes-12-and-14-addition/
我有点困惑。似乎你的解释实现低浓度的反应避免dibromination Br2是哈佛商业评论的痕量与国家统计局Br2少量,然后Br2反应溶剂的存在和与光与烯丙基溴化产品。为什么我们不能只是从少量开始Br2和反应与光的地方吗?为什么我们必须从哈佛商业评论和国家统计局开始吗?
如果在产品3溴环戊烯进一步增加Br2,做的产品是什么?
溴化是可能的吗?
是的,如果你添加Br2 3-bromocyclopentene,你将溴化双键。
嗨,詹姆斯
我只是想知道为什么我们使用亚兰作为溶剂?
高沸点。如果需要热启动反应是有用的选择有一个相对较高的沸点的溶剂。还有没有碳氢键可能与自由基反应。
嗨,詹姆斯
我一个关于对位ethyltoluene问题,(4-ethyltoluene)与哈佛商业评论反应时,会发生什么我不明白bromation将,
如果氯苯与KI反应会怎样?有什么反应?如果有地方发生吗?我一个orgnic反省,我真的不知道如何处理这些类型的反应。
谢谢
使用哈佛商业评论作为试剂溴化不会发生。在这种情况下会发生的是,你会(是暂时性的)使质子化的戒指。
氯苯+ KI(非常)迫使条件下可能产生通过亲核芳香取代碘苯,但有更好的方法去做。
怎么能一个一个选择性溴化苄型的网站的两个不同的网站……说如果我想slectively溴化的苄基的ch2 -群p-ethyltoluene取代苄基的甲基组?
二级激进应该更加稳定,所以你至少应该得到一些选择性的位置。
如果你有一个分子与叔丁基取代基、甲基取代基,与集团将Br激进更有可能做出反应?
特定的分子是1-methyl-3-tert-butylbenzene提出这个问题。
甲基。没有苄基的碳氢键氢的叔丁基溴彻底删除。
嗨,詹姆斯
为什么不Br•攻击vinylic碳取代烯丙基的碳就像在过氧化效应吗?
和你给的原因为什么会不适用于过氧化效应?
应该νγ。
是的,固定的,谢谢!
你好,詹姆斯,
对烯丙基溴化同样的推理应用于烯丙基氯化吗?
是的。
你好,
我可以使用DCM (dichlormethan)作为溶剂而不是PhCl ?激进的反应往往不是很挑剔。为什么溴化无论如何选择性在benzylposition而不是别的地方呢?
许多人认为
通常你想要一个合理的高沸点溶剂,由于起始步骤需要热量。二氯甲烷沸点很低。你可以去二氯乙烷。(83°C和40°C)
嗨,詹姆斯-
我理解,烯丙基的意味着分子两个双键,没有直接连接,vinylic意味着它是附着在双键。因此不会彻底第三碳1-propene vinylic吗?
vinylic激进会直接连接到双键——即sp2杂化。例如一个激进的1或2碳1-propene vinylic。邻烯丙基的碳(碳3)。如果有一个4碳位置将被称为,“homoallylic”。
亲爱的詹姆斯,
你能告诉我是什么产品3甲基环己烯与国家统计局/ br2反应。
谢谢你!
至少有两个不同的烯丙基溴化产品是有可能的。
詹姆斯,
还有其他溶剂的亚兰除了可以用于苄基的卤化吗?
非常感谢
我试着氯仿或者1,二氯乙烷。
不会Br•攻击vinylic碳就像在过氧化效应和由此产生的自由基将进一步Br2开始连锁反应通过攻击
乙烯基碳氢键的键离解能约111千卡每摩尔和烯丙基碳氢键的键离解能约90千卡每摩尔所以很容易打破了烯丙基碳氢键和激进的形式。
嘿,詹姆斯,
我会在假设是正确的,除非采用严格的条件,如1相当于国家统计局,第二个溴加成将?溴化还是第一个EWG的本质影响第二个补充?
物理的学生我想指出,光是由h(ν)h(γ)。很简单我知道。
Bromonium离子形成可逆的只要打开它没有很强的亲核试剂,可以摆脱过多的国家统计局。经常发生的是,你需要不断增加激进的发起者(AIBN或过氧化物等)随着时间的推移,如果反应停止。
谢谢你的更正!
詹姆斯,
烯丙基溴化,起始步骤后,溴自由基形成。他们有一个电子低于他们的要求,所以他们想要选择一个电子。那么他们为什么不叫π键,松散束缚电子,并把它吗?
你描述的是添加溴激进的π键,也就是当你对一个烯烃与过氧化物和哈佛商业评论。在这个反应,一旦Br•增加了π键,您获得一个激进的碳。如果存在大量的哈佛商业评论,那么激进的攻击哈佛商业评论的H和周期仍在继续。
然而在烯丙基溴化的情况下,反应(理想情况下)一个死胡同。一旦Br•彻底addd双键,碳基自由基的形成,(理想情况下),不需要它有反应,因为我们没有添加哈佛商业评论和我们保持Br2低的浓度。因此将回复到双键和Br激进,并最终Br•将抽象的氢从烯丙基的位置。
今天在课堂上提出同样的问题,快速键能的计算表明,添加在双键Br2可能更有利。烯丙基的H抽象的传播步骤略有吸热,而“竞争”的传播一步激进的C = Cπ键有点放热。
这让我很困惑,但去我的老研究生物理有机文本(Lowry &理查森,1981,页717 - 726)认为,抽象的阿伦尼乌斯碰撞取向因素是pi-addition比这更有利,即使活化能有点少。最终的结果是速率常数的差异在300 K ~ 5倍。在典型的反应温度(回流亚兰,~ 350 K)约为13倍的差异。
谢谢你戴夫。L&R指向原始文献的参考吗?