醇、环氧化合物和醚
SOCl2机制醇烷基卤化物:SN2和SNi
最后更新:2022年11月12日|
SOCl会2机制与醇,有或没有吡啶:亲核取代N与内部返回(2)与亲核取代N我)
- 大多数时候,醇与亚硫酰氯的反应是教作为一个年代N2的反应。事实上,在主要醇绝对是这样。
- 二级醇的问题,反应可以作为一个教经典N2与反转,或者…作为一个反应保留! ?通过年代N我的机制。这就是这篇文章的后面部分。
表的内容
- “对不起,但谁教你机制”?
- 真正的反应发生在SOCl会2二级醇:SN我的机制
- 亲核取代和内部回报率:SN我
- 添加SOCl会2和吡啶导致反演(通过年代N2)
- 吡啶关闭N我的机制
- 摘要:SOCl会2和醇,N2与SN我
- 注:在北美学校如何处理这种二分法?
- (高级)引用和进一步阅读
1。转换的醇与SOCl会氯化物2收益与反演…对吧?好吧,也许不总是正确的
一段时间以前我发表这篇文章关于SOCl会2讨论SOCl会的机制2将二级醇转化为烷基通过一个年代氯化物与二次N2路: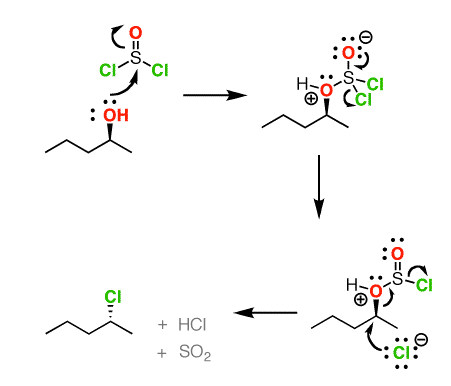
这篇文章大约六个月前抵达的评论:

Rico机制与SOCl会显示反演是正确的2不是发生了什么实验。当一个二次酒精用SOCl会处理2(什么)通常的途径是保留。
连续记录应设置,所以这篇文章将介绍:
- 真正的反应发生在SOCl会2二级醇(SN我机制)和为什么它给保留
- 为什么添加吡啶,SOCl会2结果在反演(通过年代N2),而不是保留
- 在北美大部分教科书和学校如何处理这个机械的二分法(提示:最不)
- 是一个老师做什么?
2。真正的反应发生在SOCl会2二级醇:SN我的机制
在19世纪晚期,保罗瓦尔登湖进行了一系列基本实验的各种反应的立体化学糖(糖和衍生产品)。《瓦尔登湖》时指出,(+)苹果酸治疗PCl5,产品是(-)chlorosuccinic酸——一个继续的过程反演立体化学。(+)苹果酸处理时亚硫酰氯(SOCl会2),但是产品是(+)-chlorosuccinic酸。这个收益保留立体化学。
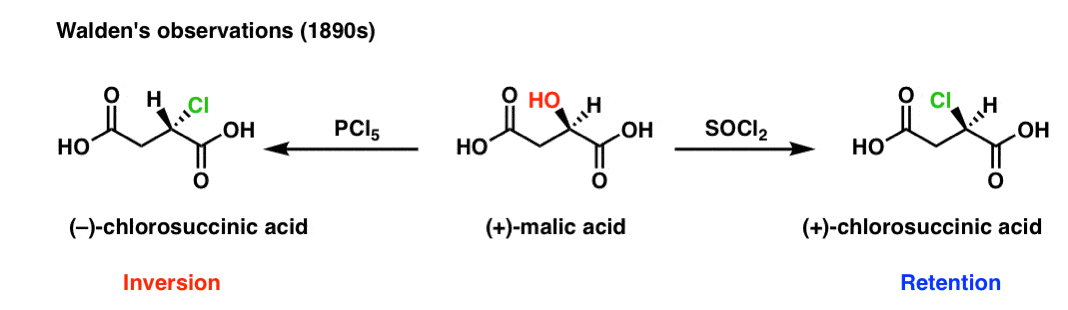
我们如何理解这个?
与PCl苹果酸的反应5导致反演的立体化学是我们现在所说的一个例子年代N2反应,《瓦尔登湖》是第一个观察到立体化学是反向的。事实上立体化学转化的过程期间观察到的N2有时被称为反应《瓦尔登湖》反演在他的荣誉。大多数学生的时候遇到SOCl会2在他们的课程中,年代N2是一个常见的反应。
更奇怪的是,苹果酸处理SOCl会吗2导致替换与保留。敏锐的读者可能还记得,“保留”的立体化学可以获得如果连续两个年代N2反应(双反转=保留)。也许这是怎么回事?也许羧酸恶意酸可以作为亲核试剂在第(分子内)N2,然后Cl -进来第二?
3所示。亲核取代和内部回报率:SN我
好主意——但这种保留的配置即使在没有团队的情况下可能发生做一个分子内的年代N2。一定有别的原因。经过大量的实验工作,这是我们最好的建议:
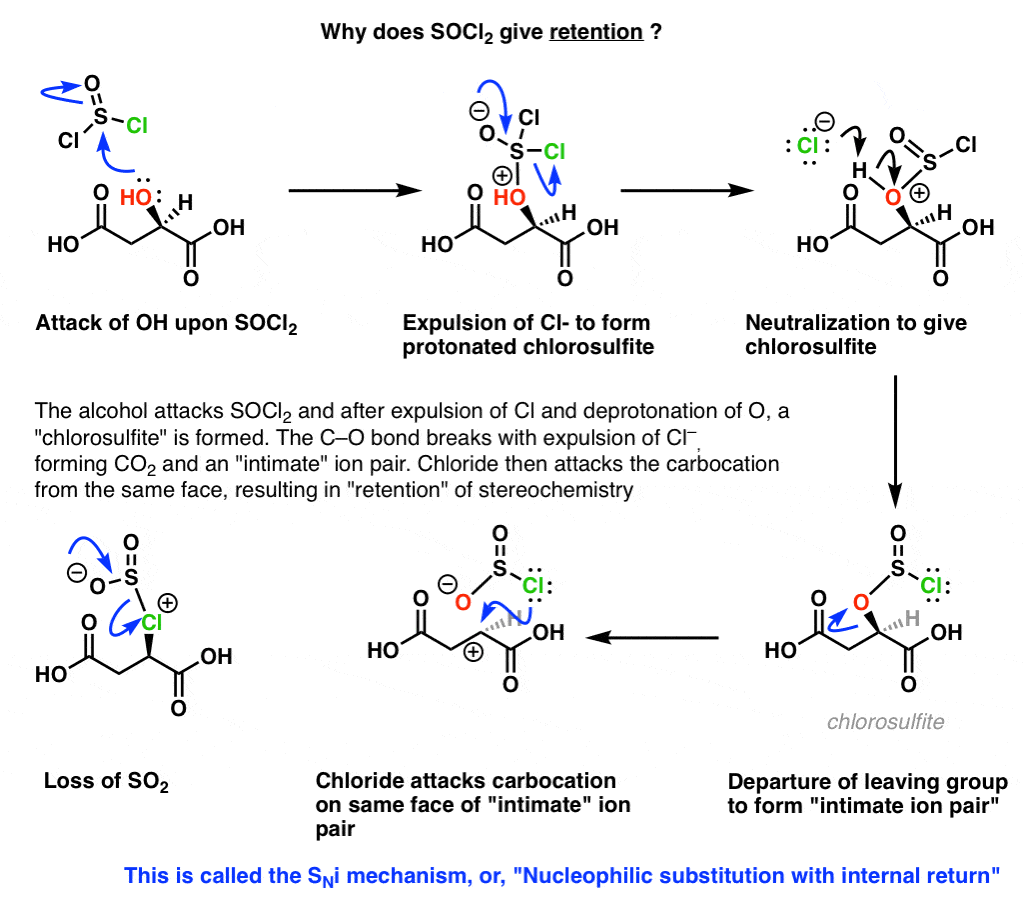
这就是所谓的,年代N我(亲核取代内部返回):是,SOCl会发生什么2corrdinates到酒精,盐酸和形成一个良好的损失离去基团(“chlorosulfite”)。的chlorosulfite离去基团可以自发地离开,形成碳正离子,当它,一个“亲密的离子对形成,碳正离子和带负电荷的吗离去基团在太空中紧紧攥在一起。从这里,氯可以作为亲核试剂——攻击相同的脸上的碳正离子被驱逐后,驱逐2,我们已经形成的烷基配置的氯与保留。
所以chlorosulfite离去基团(所以2Cl)很特殊,它可以交付亲核试剂(氯)相同的面对它离开,同时损失的2。
如果它结束了,生活可能会更简单。但不有趣!(这是一罐蠕虫被打开的声音)。
4所示。为什么添加SOCl会2并通过S吡啶导致反演N2机制
这是转折。事实证明,这个反应的立体化学可以改变反演如果我们添加一个温和的基础,如吡啶。
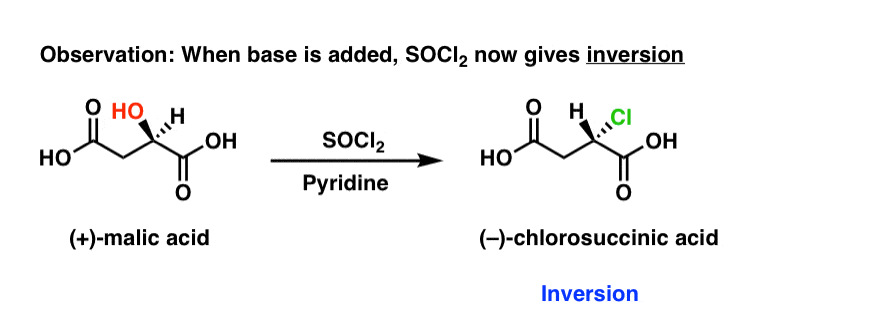
与SOCl会保留立体化学2孤独,SOCl会反转2和吡啶。这里发生了什么?如何吡啶影响反应的过程?
两种反应形成“chlorosulfite”中间。但是,当吡啶(一个像样的亲核试剂),它可以攻击chlorosulfite,取代氯离子,形成一个带电的中间体。现在,如果离去基团离开,形成碳正离子,附近没有孤对相同的脸上,可以攻击。
换句话说,通过取代氯离子,吡啶关闭的年代N我的机制。
5。添加吡啶SOCl会2关闭的年代N我的机制
即使年代N我不能在这里发生,我们仍然有一个非常好的离去基团,一个体面的亲核试剂所以——氯离子氯化碳从背后攻击,导致反演C-Cl债券的配置和形成。当然,这年代N2的反应。
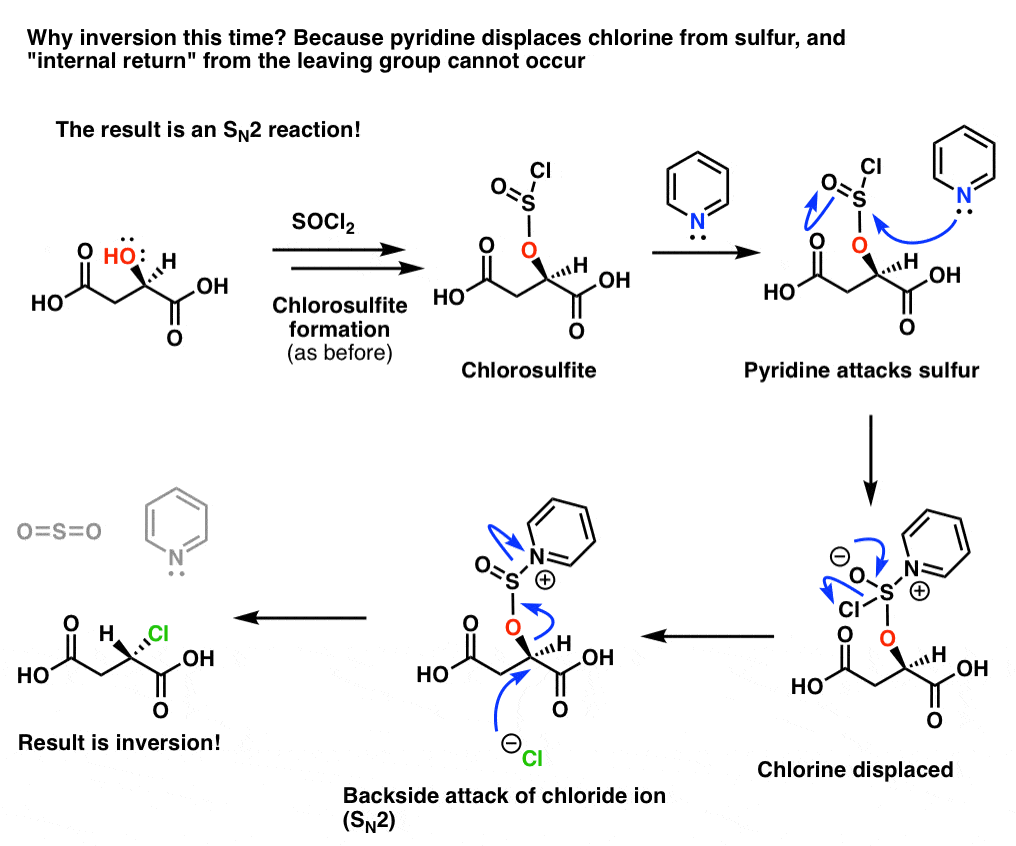
6。摘要:SOCl会2和醇,有或没有吡啶N2与SN我
底线是:
SOCl会2+酒精给了保留的配置,SOCl会2+酒精+吡啶给了反演配置的N2)
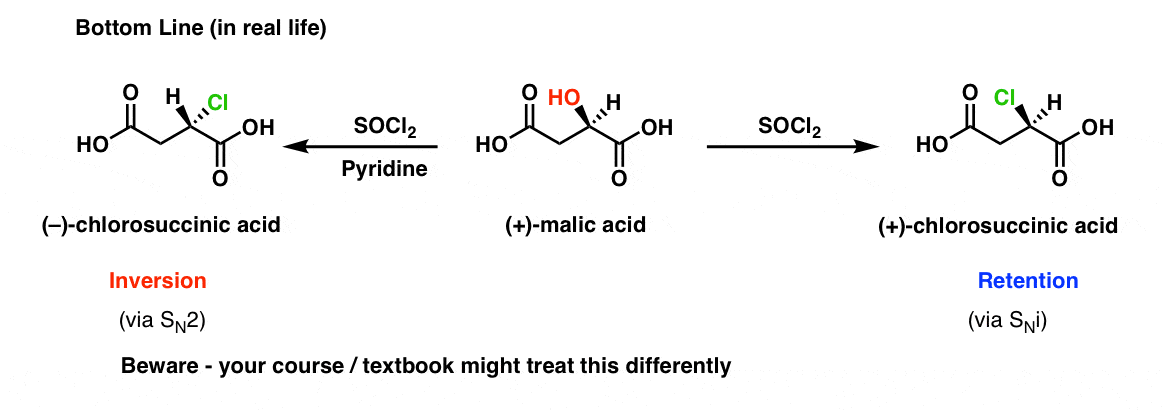
你可能会问,“这是有多普遍N我的机制吗?它是一些发生在大量的其他介绍性的有机化学反应我们一般遇到?”
坦率地说,没有。有些情况下,物种氯甲酸酯还可以进行SN我和公司的损失2但这并不是经常在典型的第一年课程。
笔记
这可能并不是利益每个人所以我把它在一份报告中指出。
在北美大部分教科书和学校如何处理这个机械的二分法?
醇类转换成烷基卤化物是一个有用的转换,因为醇离开组织本身贫穷,而烷基氯化物会容易参与替换和消除反应。在许多有机化学入门课程,SOCl会2一直被作为一个试剂醇转化成的例子吗烷基氯化物。
当我咨询我的课本收集的机制所覆盖,这是我的发现:
- 韦德(5日患儿463页)显示转换的二次酒精中学烷基氯通过年代N我(溶剂二氧六环)
- 所罗门(8 ed p . 506 - 507)显示了转换伯醇对初级烷基氯通过年代N2。没有提到的年代N我和立体化学。
- McMurry (6 p。608)显示了转换伯醇对初级烷基氯(N2)没有立体化学。
- Vollhardt(第二版288页)显示机制(SN2)伯醇;没有讨论的年代N2。
- 琼斯(第二版830页)显示N2的Cl“R”;没有提到stereochem
- Clayden,克莱恩没有提到SOCl会2作为转换的试剂醇烷基氯化物
只有一个教材(本诚然不完整样例)提到的年代N我的机制。在四个教科书SOCl会的地方2提到,反应是显示为程序通过一个年代N2机制。没有警告说:“等等!的年代N2为二级醇不会发生”。如果它不是教科书,有可能不会在。这是不足为奇的,最常见的解释转化为二级醇会发生:
这将导致出现这种情况如下。这是考试的一部分钥匙从non-obscure R1大学:
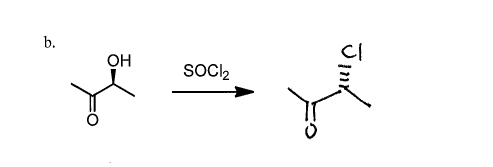
这个问题测试立体化学,和学生预计SOCl会写2在仲碳收益与反演,通过一个年代N2机制。
也有例外。另一所学校*类似的声誉)测试这个反应作为一个年代N我。
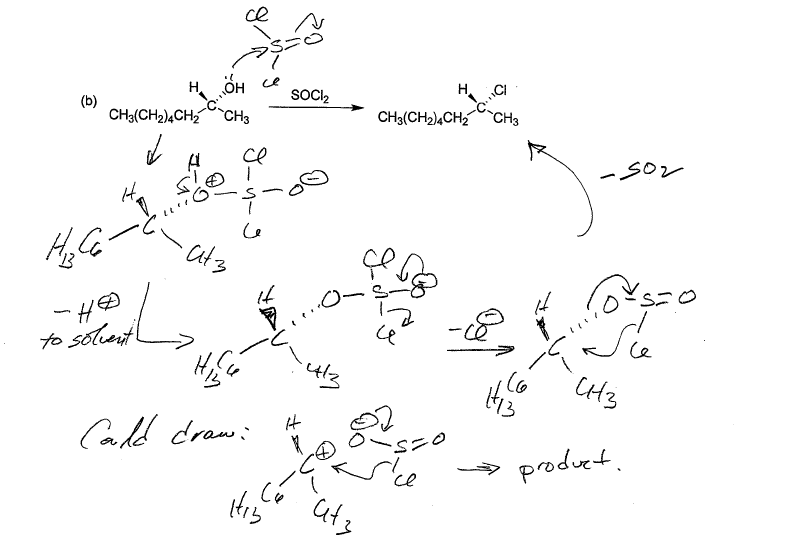
总之,至少在北美,SOCl会的立体化学的讨论2与二级醇的反应是一个巨大的混乱。我没有任何数据来证明这个观点,但在我小时的辅导我遇到了N我的反应SOCl会2接受教育…一次。
一个教练是什么?
首先,认错。我画的SOCl会2继续通过反演和SN2的过程,因为我试剂指南针对学生的广泛的小节,和这是最常教导给反演。我应该更清楚,这是更复杂的和有太多困惑的话题,所以我感谢评论者Rico和那些让我注意到这个问题。
有机化学是非常丰富和深刻。的奢侈品已经学会了这些东西,我可以回头看,觉得很迷人,只是从一个主要转向仲碳,或切换到2Cl离去基团,一个可以改变的机制N2年代N我。离去基团可以提供自己的亲核试剂!多酷!
如果我是入门班满载课程和很多其他的实验室课程不过,我的态度可能有所不同:更像,“YHGTBFKM Jeezus,这模糊的。”
我问其他老师当他们遇到这个话题。的人说:
在第二年/介绍层面,我们一直很简单。我们只谈论它作为一个年代N2,与反演,从而补充HX的反应。我们忽略的亚硫酰氯反应溶剂的影响。
这是另一个:
我教它作为反演。氯化硫氧攻击,踢出。吡啶deprotonates氧气。氯化碳攻击,切断键断裂形成2π键2,踢出氯。反演的立体化学氯攻击是SN2。
这是一个导师的特权选好战场。我完全可以理解时间和精力限制因素,和教师必然不得不做出妥协都包括什么,忽略什么,他们选择包括多少细节。立体化学的基本教训,注意手性醇在转换的时候出现烷基氯化物-最终比是否反应年代更重要N2或年代N我在某些情况下。然而,它将会很高兴看到更多的一致性这个反应从教科书的作者,这样每个人都唱赞美诗的相同。
这个老师说最好:
我的一些同事用PCl5继续他们的生活:-)
(高级)引用和进一步阅读
- Ueber死gegenseitige Umwandlung optischer Antipoden
《瓦尔登湖》
化学。的误码率。1896年,29日(1):133 - 138
DOI:10.1002 / cber.18960290127
原始出版《瓦尔登湖》反演,有趣的是跟踪这个反应机制,通过文学的发展。早期的论文在分歧有关机制协调的观察反演观察的配置(如与基地。吡啶),保留没有基本的配置。 - 反应动力学和瓦尔登湖反演。部分VI。空间方向关系在替换机制包括卤素原子和简单或取代羟基
w·a·Cowdrey e·d·休斯,c·k·英格尔德美国丈夫和公元斯科特
j .化学。Soc。1937年,1252 - 1271
DOI:10.1039 / JR9370001252
c·k·英格尔德教授和休斯发达的年代N/ E的术语用来描述反应机制,现在被称为Hughes-Ingold命名法。在本文的C部分,注意观察,SOCl会2单独与二级醇反应与保留配置,而SOCl会2+吡啶通过反演。然而,任何机制提出了,他们试图适应这些观察到他们限制范式的年代N1与SN2。 - chlorosulphinic的分解酯类
迈克尔·p·Balfe和约瑟夫·凯尼恩
j .化学。Soc。1940年,463 - 464
DOI:10.1039 / JR9400000463
早期论文还试图合理化观察立体化学特性。保留配置是由于“分子重排的立体课程由chlorosulphinate分子的尺寸控制”,而反转所致吡啶绑定到硫磺。的收益率反向使用过多的产品可以增加了吡啶。 - 醇与亚硫酰氯的反应的研究
威廉·e·Bissinger和弗雷德里克·e·龚
美国化学学会杂志》上1947年,69年(9),2158 - 2163
DOI:10.1021 / ja01201a030
一个不错的研究与SOCl2醇的反应,有用的如果一个是找个地方开始优化这个反应(关于化学计量学)。 - 分解的动力学和立体化学的次要的烷基Chlorosulfites
爱德华·s·刘易斯和查尔斯·e·布泽尔
美国化学学会杂志》上1952年,74年(2),308 - 311
DOI:10.1021 / ja01122a005 - 二次的分解烷基Chlorosulfites。二世。溶剂效应和机制
大肠布泽尔和e·s·刘易斯
美国化学学会杂志》上1953年,75年(13),3182 - 3186
DOI:10.1021 / ja01109a042
Ref。4描述了二次分解机制烷基chlorosulfites。显然不同的机制实际上是当这些分解在二氧六环或甲苯。在二氧六环,保留配置是观察,而在甲苯倒氯化物。这是归因于碳的二氧六环的协调能力,协助c债券乳沟。 - 在立体化学研究。十六。离子中间体的分解确定烷基Chlorosulfites
唐纳德j .补习
美国化学学会杂志》上1953年,75年(2),332 - 338
DOI:10.1021 / ja01098a024
早期论文教授d . j .补习(加州大学洛杉矶分校),他是同时代的扫罗Winstein(教授提出了“内部回报”的概念和亲密的离子对用于描述这个年代N我的机制)。补习后来教授在1987年获得诺贝尔化学奖为他工作分子主客体化学。这是的纸合理化的不同反应的立体化学醇SOCl会2在/(如缺乏基础。吡啶),第一篇论文在文献中描述的反应醇+ SOCl会2作为一个年代N我的过程。 - 教科书3月份的先进的有机化学(7th)提到:
”[…]醇与亚硫酰氯的反应烷基卤化物通常以这种方式所得,在这种情况下,第一步是卢武铉+ SOCl会2一个ROSOCl(这些烷基chlorosulfites可以隔离)。
这种机制的证据如下:添加吡啶的混合物酒精亚硫酰氯和结果的形成烷基卤化物与倒配置。反演结果,因为吡啶与ROSOCl反应给ROSONC5H5之前的任何进一步。的Cl- - - - - -在这一过程中释放现在从后方攻击。醇类和亚硫酰氯二阶之间的反应,这是预测的这种机制,但简单的加热分解的ROSOCl是一阶”。
不幸的是,没有provided.Prof引用。》俄文胡(在台湾)试图推广试剂反应通过内部(如SOCl会返回2)“反击试剂在他职业生涯的早期: - 反击试剂在有机反应和合成
》俄文研究会会长,科比a·吉尔伯特
四面体1989年,45(5),1233 - 1261
DOI:10.1016 / 0040 - 4020 (89)80123 - 1 - 硅试剂化学转换:“反击试剂”的概念
r .研究会会长,研究所。-蔡,刘贤国王和D.-N。Horng
纯粹的达成。化学。1999年,71年(3),445 - 451
DOI:10.1351 / pac199971030445
我学会了在Sni机构,4元环过渡态之间形成的年代,O, Cl和r .像这样:
https://drive.google.com/file/d/1sxNy_jCMSCatIadoRnARrUGabNlvmpXA/view?usp=drivesdk
我真的很喜欢你的处理方式可能对你太苛刻的评论。如果它是任何普通的人他们不会采取它。我已经从你的文章中学到了很多,这是我有机的首选网站。荣誉! ! !
多谢你详细的解释。还想说,我读过一个主题onSNi反应在参考书“有机反应:结构、机制”,莱因哈德布鲁克纳。
它给好的洞察力溶剂吡啶如何改变SNi路线SN2为什么与亚硫酰氯醚反应溶剂酒精SNi的方式。
我很想听到你的想法的机制将羧酸转化为一个使用SOCl2酸性氯化物。我见过的机制,它通过一个6元TS的第一步和第二步而其他机制更逐步并使用氯离子攻击。
如果你想看到先进的问题(这)微妙的概念类似,你应该看看iit jee考试问题。
好的。那里将会是一个好地方找到这些吗?
什么是1-heptanol与亚硫酰氯反应的机制
可能是普通SN2。
感谢你这个解释/跟进!我读了这两篇文章为一个额外的信贷分配和它帮助澄清一些事情很多!你是最棒的!
很高兴听到它LDel——你应该感谢最初的评论者鼓舞整个帖子!詹姆斯
嗨,詹姆斯。
我是一个化学老师,最近我们有一个问题在我们研究所的一篇论文中。
问题使用环氧和反应PCl5给二氯产品。现在怀疑出现在我们中间是二氯原子是否会增加通过SNi或SN2。
我无法找到任何源在线与PCl5环氧反应的一个例子。
SNi不同于SN1和SN2如何? ?
内部回报率离去基团的亲核试剂。也不属于一类。
我们可以pcl5作为SNi试剂。? ?
不,PCl5只会做SN2。
@Hi每个人. .
1。我认为只SNi顺利为初级,二级醇SOCl2,叔醇将进行消除,加上替换。任何评论在这…
2。我想一阶动力学反应,形成亲密的一对chlorosulphite RDS。任何评论…
在苹果酸的问题为什么酒精组而不是羧酸反应吗?更多的是被动的我认为。
你好,
伟大的解释!在你韧“为什么SOCl2给保留”你指出chlorosulfite可以被孤立。这怎么可能?你对这个话题有什么支持litterature吗?bdapp平台
嗨,我建议在这里,http://pubs.acs.org/doi/abs/10.1021/ja01098a024。你也可以去3月的先进的有机化学和查找“chlorosulfite”。
羧酸不会干扰SOCl2的苹果酸. . ?羧酸不受影响。如何?
请检查示例2给出链接
//m.deriinvest.com/2011/12/03/reagent-friday-thionyl-chloride-socl2/
这是只有在二级醇吗?
这是SNi只有SOCl2而不是别人的家庭(PBr3 PCl5等)
为什么? ? ? ?
只有SOCl2而不是PBr3 PCl5。的机制在很大程度上是二级醇。不可能凭主要经营醇,但你不太可能能够告诉鉴于异构中心可能是不存在的。
我o化学的一个学生给我今天这篇文章。漂亮的博览会。我其中一个有罪的教师,我教的和它如何出现在考试。
这是一个忌讳:这篇文章的路易斯结构。结构不会显示孤对经常出现,年代应该被起诉。当然,让所有的化学和结构信息只是一个额外的麻烦当教学材料(我不认为PCl5解决了这个问题)所以我们必须简化?或者你所说的那么好,我们必须选择战斗。不过,应该有一些方法来通知学生,我们告诉的故事是不完整的,不是吗?
这里有另一件事:你(和很多人一样,我也是在过去)制定最初的SN反应硫(不是碳!)通过添加/取消。这当然是一个类比羰基化合物的反应。它可能是更现实的制定作为一个协调一致的替代硫。这是因为S = O“双键”并不是一个双键,但极化单键,因此它实际上可能不喜欢添加/消除反应机制。
看到类似的情况下从SOCl2氯化酸形成的第一步,而亨利Rzepa计算:http://www.ch.imperial.ac.uk/rzepa/blog/?p=6816
关于SN2 vs SNi的主要问题(保留)SOCl2酒精氯化启动:
•我的经验告诉我,概括了教科书往往依赖于在文献中很少有实际的例子,介绍了在某种程度上,然后被其他作者模仿。许多年长的例子(pre-NMR,高效液相色谱)文学和可能不会总是生存与现代分析技术更准确的重新调查。
•你给的例子SNi(苹果酸)可能是不好的,因为他们可能会显示双SN2邻近组织的影响;更好的例子SNi是手性醇分子中没有邻近组织。
•苹果酸的例子(与其他反应条件:PCl5)经典例子walden反转,但是老化学等往往比课本可能不太理解的暗示。看到最近讨论《瓦尔登湖》的例子:http://pubs.rsc.org/en/Content/ArticleLanding/2006/CC/b517461a
•我个人已经开始检查原始文献中的大多数反应的例子我教我的讲座。同时,我几乎不再使用任何假设的问题在测试中,但实际上我搜索通过Reaxys执行示例。
可以R-OH + PCL5告诉SNi吗
尽我所知与SOCl2 SNi主要是观察。
首先,我不得不说,Rico错了说,醇类和SOCl2总是反应保留配置。
有时,你可以保留配置和有时反演的配置。要记住的关键一点是溶剂在反应中使用。
如果你想要更好的理解发生了什么必须咨询主要litterature主题。我建议大家读这些书和文章:
凯莉和桑德博格部分先进的有机化学
j . Org。化学。,20.13,78 (5), pp 2118–2127
j . Org。化学。,1993, 58, pp 2822
和引用其中
为什么它是必要的吡啶作为亲核试剂吗?更强的基础,不会只是deprotonate质子化了的氯化chlorosulfite离开自由的SN2反应。似乎有很多合理的变化。对我来说对反演,越简单越好。文献在哪里这个清理反转的机制?
我引用你3月先进的有机化学(我使用5 ed但任何患儿)进行全面的讨论。詹姆斯
我们可以用其他基础代替吡啶吗?
是的,可以使用其他基地。吡啶的优势在这种情况下是很弱(pka的共轭酸4),通常不会导致竞争E2反应产生的卤代烃。叔胺是强大的基地,pKa(共轭酸的)大约10左右,所以消除开始变成了一个问题。
@Arkya,我假设二次酒精只是防止迁移的烷基(视情况而定),形成一个更稳定的碳正离子。坦率地说,我不明白为什么这不该发生在伯醇。
有人能验证吗?
是这种机制的SNi适用一般只有二级醇类或醇吗?
我认为你不需要担心这个,主要醇由于活性部位不会异构中心(因此没有立体化学转化或保留)。
叔醇,碳正离子形成更稳定的你更有可能得到外消旋混合物。
是的,完全正确点1。
叔醇,碳正离子形成更稳定。但是有很多烷基碳正离子,阴离子不能攻击它,因为我想的立体效应。阴离子会攻击βH,产品将烯烃。
在SNi机构,形成碳正离子、碳正离子重排发生像常见SN1机制?
参照SOCl2与二级醇的反应在吡啶存在,吡啶作为基础,它消除了质子从盐酸,导致自由Cl -离子的形成,和Cl -,是一个有效的亲核试剂,攻击Chlorosulphite回到正常的SN2时尚。
如果有两个的SN2反应然后我们希望保留完整的立体化学。SNi过程中我们会通过亲密的离子对碳正离子,所以我们应该看到一些渗漏通过纯光学纯度SN1类型的途径。如果我们从一个光学纯chlorosulfite我希望光学纯度会减少与增加反应温度或溶剂极性增加这两个因素应该扰乱亲密的离子对。
我也不相信吡啶会选择性的脂肪族仲碳硫亲电,但可以或者测量反应速率对吡啶浓度。如果是直SN2,你期望一个线性增长速度随着吡啶浓缩的,而如果是拟议的SNi,你会看到一个高原反应速率增加吡啶浓缩的自慢一步可能会电离,不攻击硫磺。
我学会了,在这种情况下保留配置是由于两个净反演发生。第一个反转发生在胺(或吡啶在本例中)执行Sn2 chlorosulfite位移。这将生成二氧化硫、氯离子和激活吡啶啉。第二反转发生在氯离子取代吡啶组立体化学的总的结果保留。会有一个简单的方法来测试你提出的机制?
谢谢你,詹姆斯。我说你把书扔到了他的slapdown !这显然是一个复杂的问题。
现在,事后是20/20,但是我觉得它很好的意义,氯,弱亲核试剂,不取代chlorosulfite SN2时尚。
你可以调用形成二氧化硫气体的热力学稳定性和熵的好处是为什么氯取代的一个因素在SN2 chlorosulfite吗?
也许我不应该写“镇压”,我很高兴他提出这个问题。bdapp平台
PCl5足以导致醇通过SN2反转过程与亲核试剂氯化所以即使事后我认为很难看到。
在最新版本的所罗门他说与吡啶反应完成或其他胺基。也有一句话在括号州保留如果吡啶的反应发生是缺席。
我教它反转,因为我很少听过任何一个治疗酒精和不使用一些亚硫酰氯胺。