醇、环氧化合物和醚
的环氧化合物与酸
最后更新:2023年1月17日|
开放与水酸环氧化合物
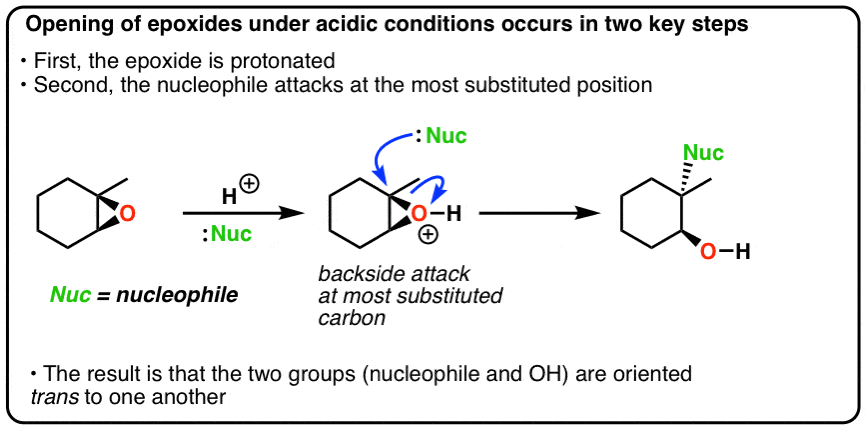
- 环氧化合物在酸性条件下可以进行开环的亲核试剂。
- 在这个反应中,环氧氧是质子化了的第一次,让它更好离去基团
- 在第二步中,亲核试剂倾向于攻击更多的取代碳,这打破了弱切断键。
- 最好的类比是很像的马氏开放bromonium或mercurinium离子。
表的内容
- 的形成反式通过开放二醇环氧化合物与酸水
- 开放的机制反式二醇与酸类似于开放Halonium离子
- 其他的亲核试剂:醇类和HX
- 酸只帮助反应如果亲核试剂与强酸兼容
- 打开环氧化合物的基础呢?
- 笔记
- (高级)引用和进一步阅读
1。的形成反式-通过开放二醇环氧化合物与酸水
过去后,我们看到一些例子环氧化合物的活性对破损远远要比普通的醚。例如,水酸(通常缩写为“H3O +”)将打开一个环氧在更温和的条件下比“普通”醚如乙醚,因为环氧化合物有相当大的环应变(约13千卡每摩尔)。
仔细看看反应,我们还指出两个有趣的模式:
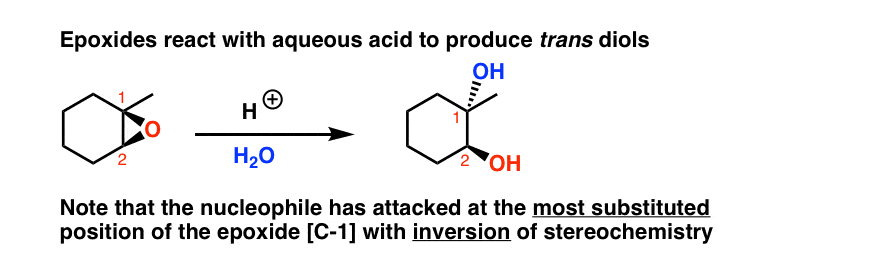
(顺便说一下,我们如何“知道”的颈- 1是从哦亲核试剂并不是环氧吗?使用同位素标签是一种方法。另一种方法是使用其他比水的亲核试剂,见下文)
应该注意的是,在没有酸,没有反应发生。所以很明显,H +中发挥着关键作用。
可能是怎么回事呢?
通过类比与酸醚的反应,第一步必须反应最基本的分子——网站环氧氧-酸,给我们一个质子化了的环氧。这将作为一个更好的离去基团比unprotonated环氧。(回忆,共轭酸总是更好的离去基团]
下一步必须是最好的反应亲核试剂出现在解决方案——H2啊,在这种情况下,我们的质子化了的环氧。这发生在最取代位置,总是立体化学的反演。所以它必须执行“背后攻击”在这个碳,我们观察N2反应。最后一个去质子化给我们中性产品。
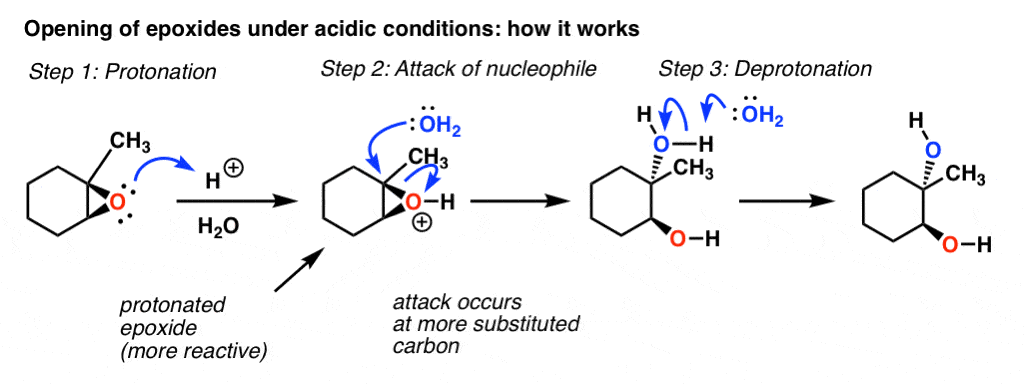
第二个。如果你还记得的关键教训N2 -这是不偏重了位阻-也许这看起来很奇怪。如果这是一个“纯”N2,反应,我们预计不会攻击发生的“替代”的立场?
显然别的东西一定是怎么回事!
2。开放的机制环氧化合物与酸就像打开Halonium和Mercurinium离子
值得庆幸的是,你可能遇到这样的反应!如果你认为这一章烯烃,你可能会看到质子化了的环氧有异曲同工之处,另外两个活性中间体在这一章你见过:“halonium”离子,和“mercurinium”离子,两三人环轴承一个正电荷:
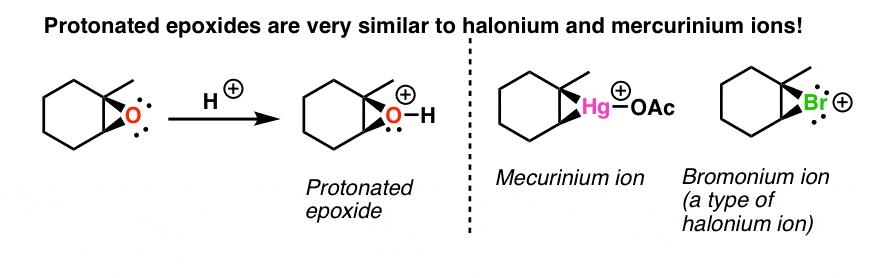
如果你回想这些物种是如何反应的亲核试剂,它总是在更多的代替位置反演立体化学。事实上,有一个全家的烯烃除了反应,这种机制进行的,我们称为“三人环通路”。Halohydrin形成是一个完美的例子:
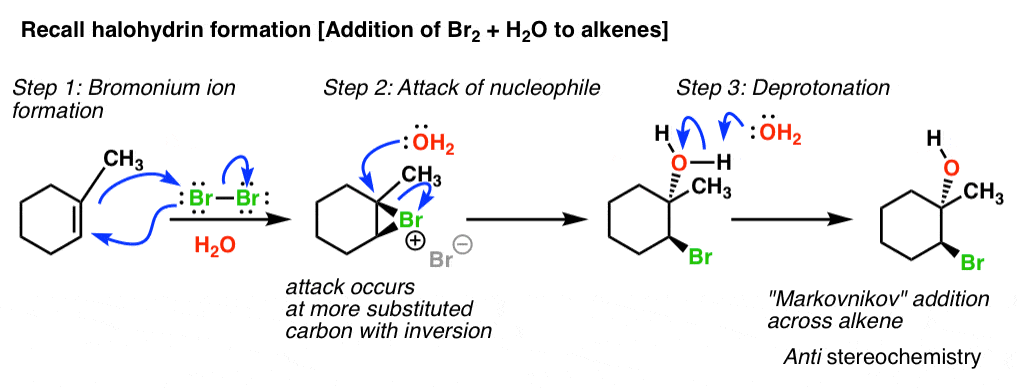
所以本质上,添加的亲核试剂使质子化环氧化合物是另一个例子的“三元环通路”烯烃!
现在,我们已经看到,这与水酸(H3O +]。我们可以扩展到其他的亲核试剂吗?当然!有一些保留,我们会在第二个。
3所示。其他的亲核试剂呢?醇类和HX也工作
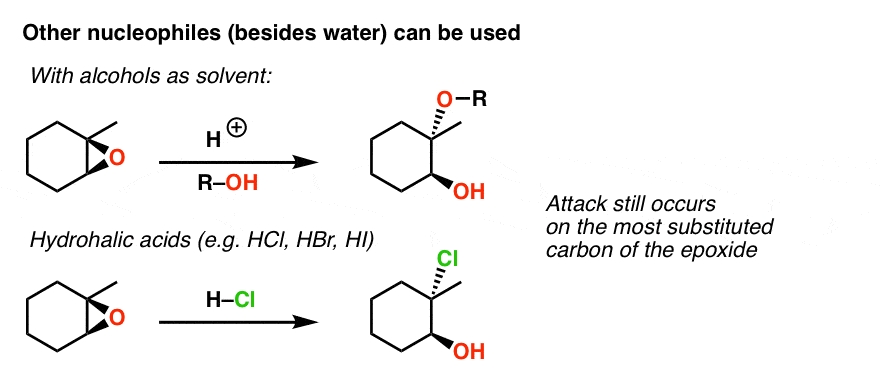
改变水的溶剂酒精将导致酒精添加。例如,如果我们使用CH3哦,作为溶剂代替水,那么我们的产品包含哟3加入最取代位置。
Hydrohalic酸(盐酸、哈佛商业评论和嗨)也能发挥作用,形成halohydrins。
4所示。当不酸帮助吗?当亲核试剂与强酸不兼容
现在,你可能会想,如果环氧化合物是由更多的活性与酸治疗,然后我们不能扩展到其他的亲核试剂吗?例如,氢氧化钠或NaNH2,甚至格氏试剂吗?
就在于此困境。酸性条件下质子化了的只有兼容的亲核试剂可逆。(换句话说,亲核试剂的共轭酸是强酸,认为pK一个< 0]。(注2]
你能看到一个小问题中加入氢氧化钠溶液水酸吗?你认为会发生什么?
大爆炸。嗯,那是夸张。但酸会使质子化氢氧化钠不可逆转,给我们H2O(回想一下,酸碱反应快]。同样,你可以想象添加NaNH会发生什么2酸或格氏试剂酸:亲核试剂质子化了的,给我们吗共轭酸。
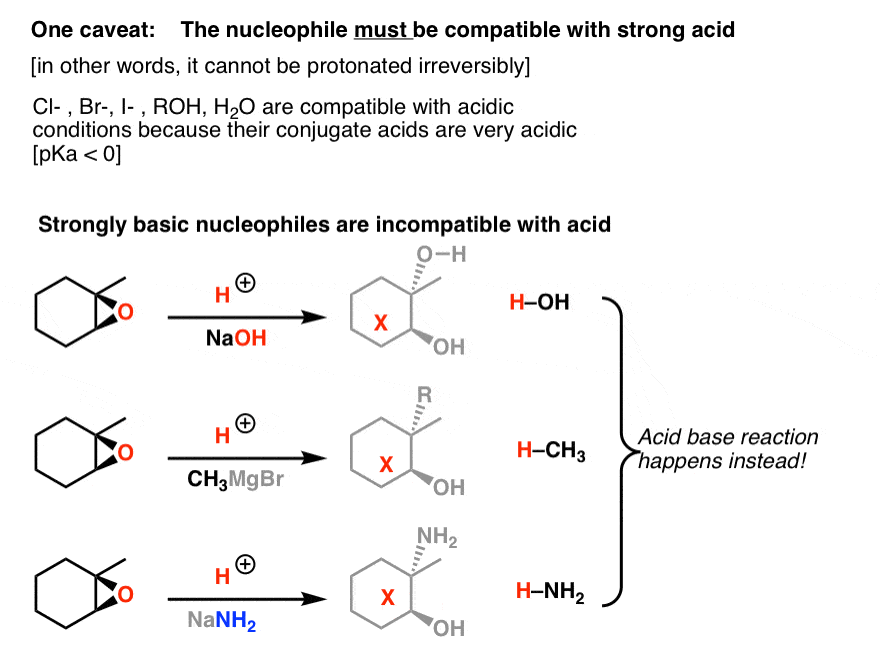
5。在基本条件下开放呢?
还有一个神秘的解决。上次后你可能会记得,如果我们只添加氢氧化钠-没有酸环氧我们见面,我们得到一个完全不同的产品。
注意立体化学的c - 2完全不同与酸。
这里会发生什么?任何想法吗?提示——这是一个反应之前我们已经讨论过,甚至在这篇文章中提到的。
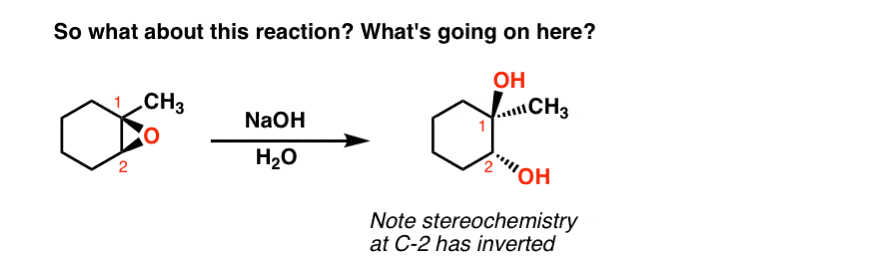
我们将在下一篇文章讨论这个。
在下一篇文章- - - - - -环氧化合物的基础
笔记
注1:为什么亲核试剂攻击代替碳越多?
- 在我们的质子化了的环氧熊一个积极的,尽管氧气形式电荷,在现实中正电荷密度主要位于碳(回想一下,氧的电负性大于碳)。
- 回想一下,正电荷的顺序最好由碳稳定三级>二级>主。因此,在我们的案例中,叔碳原子将承担更多的正电荷。叔碳将会更加electron-poor(亲电)
- 切断债券的长度不相等,切断键叔碳较长和较弱的比仲碳。
底线:叔碳更亲电子(电子差)和叔碳上的切断键较弱,长,容易打破。
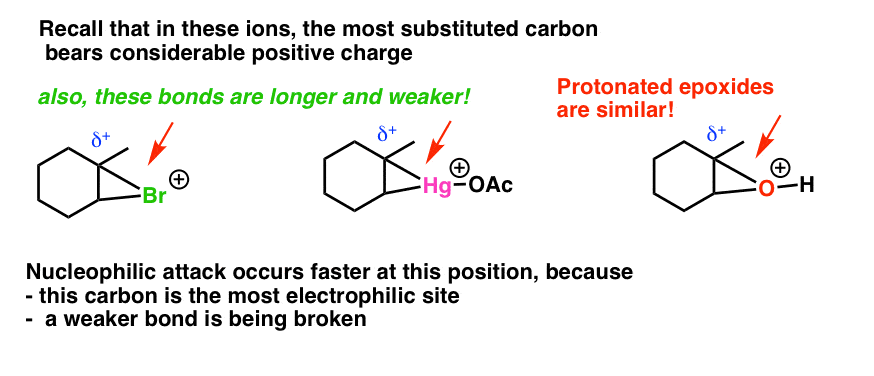
注2。这些图由马特·麦金托什在相同的背景下是非常有用的。(回到讨论]
测试你自己!
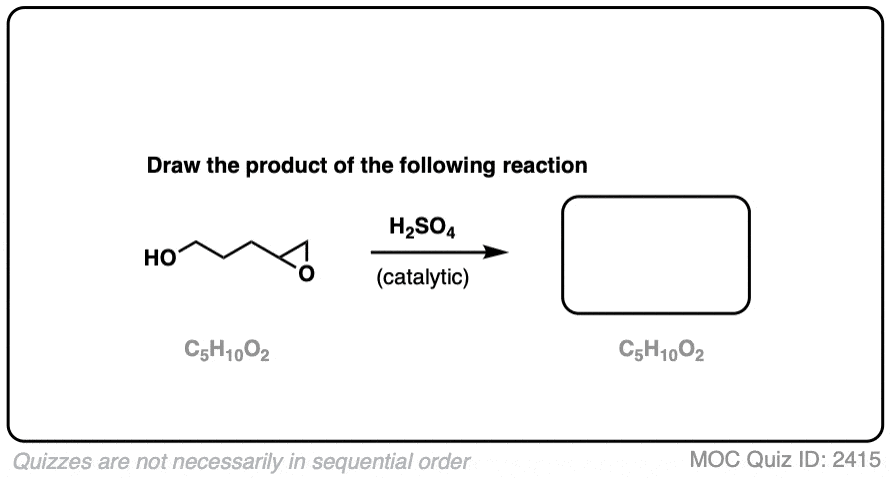 点击翻转
点击翻转
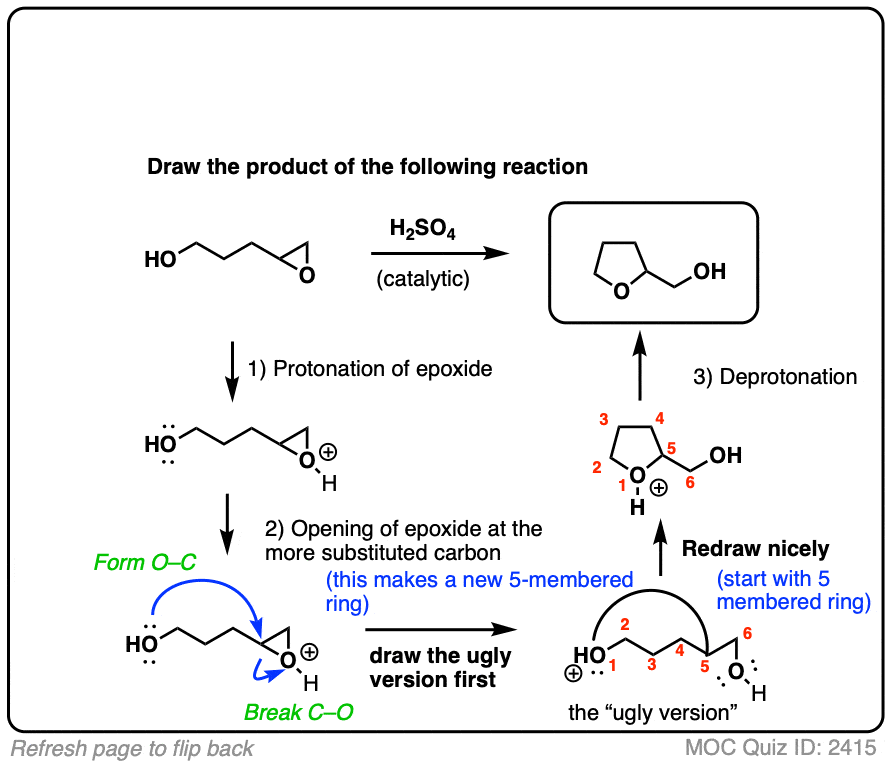
(高级)引用和进一步阅读
- 的机制环氧反应
e·帕克和n . s .艾萨克斯
化学评论1959年,59(4),737 - 799
DOI:10.1021 / cr50028a006
本文是旧的但是从基础知识开始讨论环氧化合物的反应。酸性和碱性(亲核)的反应。 - 合成方法和反应;68年1。Nafion-H-Catalyzed水化和环氧化合物的甲醇分解
乔治•a . Olah亚历山大·p·冯大卫Meidar
合成1981年;1981 (4):280 - 282
DOI:1055 / s - 1981 - 29414
在这种情况下,电解质TM- h(高分子树脂由杜邦公司,随后修改superacidic Olah教授“- h”形式)可以用作催化剂促进水解环氧化合物的开环,可。 - 傅克烷基化的芳烃和Mono - Bis (trifluoromethyl)环氧乙烷在超强酸介质:简单的合成α- (trifluoromethyl)和α,α-Bis -β-Arylethanols (trifluoromethyl)
巴勃罗·j·k·苏利耶Prakash Linares-Palomino,凯文•Glinton Sujith查柯,Golam拉苏尔,托马斯•马修和乔治·a . Olah
Synlett2007年,(7),1158 - 1162
DOI:10.1055 / s - 2007 - 977423
在Brønsted酸条件下,环氧化合物可以作为亲电试剂的傅克反应。 - 热Water-Promoted环氧化合物和氮杂环丙烷的开环水和其他Nucleopliles
之王,崔Yong-Tao Zhao-Bing徐、金衢
《有机化学》杂志上2008年,73年(6),2270 - 2274
DOI:1021 / jo702401t
标题错误,这让我有点可疑。另一方面,这是一个穆南加篇文章,应该是可靠的。结果表明,热水可以水解二醇环氧化合物,不需要催化剂!环氧s can undergo ring-opening under both acidic and basic conditions – i.e. under electrophilic and nucleophilic reaction conditions. To take this one step further, in acidic conditions, epoxides can be activated by both Brønsted and Lewis acids. Lewis acid catalysis is more common, and is described in the following publications: - 钛isopropoxide-mediated亲核的空缺,3-epoxy醇。轻微程序特定选择的开环
莫里斯·卡隆和k . b .沙普利斯
《有机化学》杂志上1985年,50(9),1557 - 1560
DOI:1021 / jo00209a047 - 不对称催化的环氧开环反应
埃里克·n·雅各布森
的化学研究2000年,33(6),421 - 431
DOI:1021 / ar960061v
雅各布森教授(哈佛)的职业发展和研究不对称反应。他的一个值得注意的贡献是Cr(伦)催化剂的发展环氧化合物的不对称开环的故事这个描述化学的发展。 - 环氧开头tert-butyldimethylsilyl cyanide-zinc碘。证据一个逐步的过程的位阻环氧
保罗·g·Gassman和伦纳德·m·哈伯曼
《有机化学》杂志上1986年,51 (25),5010 - 5013
DOI:1021 / jo00375a050
这是一个不寻常的研究但有趣的反应在已故教授的实验室开发的p·g . Gassman明尼苏达(U)。环氧化合物的反应与TMSCN(一个organic-soluble和容易处理替代传统的氰化试剂如KCN)和催化ZnI2给了1,2 -异氰醇。本文是一个机械的调查这个反应。 - 环氧化合物转换成β-HYDROXY并且:反式2-isocyanocyclohexanol
保罗·g·Gassman和托马斯·l·古根海姆
Org。Synth。1986年,64年39岁的
DOI:10.15227 / orgsyn.064.0039
一个有机合成程序的环氧化合物开环,2-isocyano醇。
我见过,如果一个格氏试剂添加到环氧化物,它不仅发生在取代碳越少,让酒精作为一个产品酸性检查。
但如果环氧是质子化了的第一次(激活),格氏试剂添加后,它仍然会在替换碳越少,或者增加更多发生在取代碳,像环氧开在酸性介质。
如果环氧质子化了的第一,酸会破坏格利雅。可以加速Grignard-type增加环氧化合物与路易斯酸(例如BF3)兼容强大的基地。
在你辉煌的图表总结所有的反应,你可能已经忘记了
70:酸性的环氧化合物开环
嗨
在酸性的环氧化合物是碳正离子重排可能吗?或者是碳正离子从来没有真正形成,只是直接攻击循环中间吗?
不,他们不会碳正离子重排,在酸性的环氧化合物,因为可能不会有一个自由碳正离子。
然而,有pinacol-related重组可能发生与环氧化合物在酸添加缺少的亲核试剂的情况下,比如epoxide-aldehyde重排。
当CH3-CH = CH-OCH3与哈佛商业评论的产品会是什么反应。
开始画共振形式。你很快就会找到一种好的碳亲核试剂。会告诉你,它会与亲电试剂反应,从那里你可以算出产品。
兄弟格氏试剂和吉尔曼试剂(organolithium试剂)给R -这是一个基本不酸。基地与环氧化合物经过sn2
假设如果格氏试剂是第一个接受epoxycyclohexane和非质子化了的。
是什么机制. .
亲爱的詹姆斯,
注1下,你国家的亲核试剂进攻取代碳越多。在你的例子中,你表现出叔碳环氧质子化了的被攻击。这怎么可能?我一直都知道一个三级衬底经受不住SN2反应由于位阻。
事实上,我的课本,如果你一个环氧与格氏反应或organolithium试剂,试剂将攻击环氧阻碍了碳原子就越少。
你好,如果你有一个环氧环己烷环与甲基groupattached碳连着的环氧乙炔和反应离子和水。会有立体化学虽然乙炔化物阴离子是线性的。
乙炔化物离子是一个基本的亲核试剂,将攻击至少取代碳SN2时尚。水被添加在反应结束后淬火醇盐离子。
一个疑问教授……NaBH4能打开一个环氧? ? ? ?
谢谢!
通常不会。LiBH4能做到。
解释的机制1,2环氧丙烷与盐酸反应
好吧,最强大的基础是什么?环氧的氧气。所以使质子化氧气,形成一个新的债券和地打破了氯键。现在你有一个质子化了的环氧Cl -漂浮。Cl -是一个很好的亲核试剂。那么接下来会发生什么呢?
如果一个胺与环氧树脂反应在酸性水溶液系统,酸能使质子化胺孤对亲核试剂实际上减缓胺和环氧树脂之间的反应。你如何解释这一现象/插图,酸的显示加速反应?
胺是至少10个数量级比环氧化合物更基本,所以任何酸添加到系统将使质子化胺、环氧化物。使质子化胺使成铵盐,non-nucleophilic。这就是为什么反应减慢。酸减慢的速度增加格氏环氧化合物。
指出,这篇文章是指注意# 2不存在。底部的链接也坏了。
就太好了如果有人能回答为什么碳得到更多来自周边组织的电子密度(因此能更好地稳定正电荷)是更积极的(尽管它得到更多的电子密度)。
这是我睡眠不足的猜测,可能错了,但是我将提出一些可能的因素围绕中间试图降低自由能。记住一个碳连着一个高电负性很高的原子是部分积极即使它有三个烷基基团。注意:当我说碳在这篇文章中我指环形原子而不是甲基取代基。
意识到这是本质上相同的困境和推理参与另一个三元环通路:打开一个环氧Br2 &水halohydrin。记住的图纸不捕获环弯曲一边到另一边,或者你可以把electroneg。一个碳原子能够倾斜,或作为共振结构。有图片的克莱因的第一学期,3日患儿p。290年,在这里http://images.slideplayer.com/16/5221039/slides/slide_74.jpg,在这里http://images.slideplayer.com/25/7654562/slides/slide_3.jpg,
这里http://courses.chem.psu.edu/chem210/mol-gallery/bromonium/bromonium.html
中间是非常不稳定的。溴或氧气在这种情况下,和碳有人称这种情况下,他们必须处理它最好的。他们不知道他们将来将由Nuc攻击松了一口气;他们只是想要尽可能的稳定。这意味着处理环应变,位阻,和理解的关键:正电荷;是要去某个地方!和O G * d * mn如果它会承担。
*记忆的,橙汁不希望一个正电荷贴在他身上,所以他尝试不管他,直到他们能找到“真正的杀手”(Nuc攻击者),包括靠在约翰尼科克伦(碳)。这些年龄,还能记得很多的可能性。(~卡托·卡林碳正离子…嗯?)
1)认为Br或O的突然困害怕恐慌的动物本能是什么都知道,那就是完全只去一个碳或其他形式carbocation-a结构更稳定的正电荷更多取代碳。这将改变更多的替换从sp3碳sp2,二级和三级,使SN2攻击可能有…想象O试图这样做有着结实的手臂抱着每一个碳的电子。O倾斜和延伸到一边,用它把电子密度(另一个原因是坏如果O相反把它对最原始的碳/前电子密度)。但如拉阿,这枚戒指…不能…很…被打破。不过,这足以使一些更取代碳sp2和次要的角色。虽然不是所需的碳正离子,这导致更多的取代碳获得足够的性格和足够的部分正电荷以允许它亲电子网站(尤其是电子越来越排斥的接近电子Nuc它越来越近)。
2)如果我们只关注这里的中间,也许孤独之间的位阻对O和甲基取代基…?
3)可能朝着一边将进一步减少O的角,从而减少之间的排斥力的孤和债券(从理想sp3角度进一步减少平衡的角度的增加减少取代碳)…?
谢谢你,波,花时间写一份解释来帮助读者。
我想知道我想介绍另一组在环氧树脂如硝基那么我先开环和介绍或添加环氧树脂是什么时候?
你会开始适当取代烯烃,然后做一个环氧化反应。对丙烯腈你需要这样的亲核epoxidizing试剂过氧化氢/氢氧化钠。
你好,詹姆斯,
我真的很喜欢你的博客。它帮了我很多。
只是有一个问题,
u表示,电荷在第三碳是最
说什么错的叔碳上的正电荷将减少由于烷基的诱导效应. . ?所以它将有至少正电荷。
邻近的归纳影响烷基组只有稳定正电荷通过分享他们的电子感应σ键。他们不改变极性的影响碳,只有稳定。我认为詹姆斯博士使用了一个很好的类比,穷人被富人的邻居可以忍受的贫穷,因为富人的邻居愿意分享他们。这并不让穷人富有但比穷人的穷邻居。
这困惑我自从我了解了它. .
如何稳定的叔碳通过归纳影响(通过电子捐赠组)电子密度低于仲碳了吗?
不应该是相反的吗?
你比较开放一个环氧在基本条件下是非常有用的。我的课本做得相当糟糕在解释产品的差异。谢谢你!
乐意帮助!
你好James-san
一个小问题:当打开环氧化合物与酸,第一步是质子化作用,那么攻击。但是如果我添加了过量的酸(如你好或哈佛商业评论)到一个未开封环氧,我会观察环氧的通常的开放吗?最终产品(一个打开环氧)能使质子化进一步的酸?
很酷的网站(由于负载)
除了哈佛商业评论或嗨醇,最终,将它们转换为卤代烃,是的,如果你打开了环氧halohydrin,哈佛商业评论或嗨过剩最终会转换R-OH r×其中X是Br或我不知道为什么你想那样做,但这是可行的。
你好,詹姆斯,
如果环氧化物治疗后,多余的水从哈佛商业评论的Br吗?多余的水把Br R-OH吗?
与水,不可能。你需要更强的亲核试剂。如果是有点基础,然后一些氢氧根离子可以添加作为亲核试剂。