消除反应
Antiperiplanar关系:E2和环己烷环的反应
最后更新:2022年12月4日|
Antiperiplanar碳氢键和之间的关系离去基团:E2反应和环己烷环
这就把我们带到一个非常可测试的的应用E2反应——如何画的产品E2在环己烷环反应!
表的内容
- E2反应,离去基团总是“Anti-Periplanar”相邻的碳上的氢被移除(“β碳”)
- 在环己烷环,E2反应只能离去基团时发生轴向
- E2环己烷环的反应,只有这样离去基团和碳氢键可以Anti-Periplanar如果对面脸上的戒指
- 一些例子:什么是主要的E2产品在每种情况下?
- 取代基环己烷可以影响E2在环己烷环消除反应的速率
- 浓度越高的构象异构体轴离去基团,消除将越快
- 笔记
- (高级)引用和进一步阅读
1。E2反应,离去基团总是“Anti-Periplanar”相邻的碳上的氢被删除(即“β碳”)
上次我们比较了E1和E2反应和提到的一个关键差异的立体化学E2的反应。记住,在E2,离去基团总是“反”相邻的碳上的氢被移除。(这意味着他们彼此直接反对,或180°;有点像分针和时针当一个时钟读取6]。
这是一个非常重要的细节能够适用于反应。
2。在环己烷环,E2反应只发生在离去基团是轴向
这经常出现的一种方法是在讨论环己烷环。如果你还记得,在环己烷的椅子上构象,组织可以是轴向(垂直向上或向下)或赤道(指向“有点”或“有点”)。
为了让一个氢被“反”离去基团,这是要求两组是轴向。仔细看看左边的环己烷,的地方离去基团是赤道——看到的是“反”是碳碳键(highlighed红色)?
那E2是不会工作!
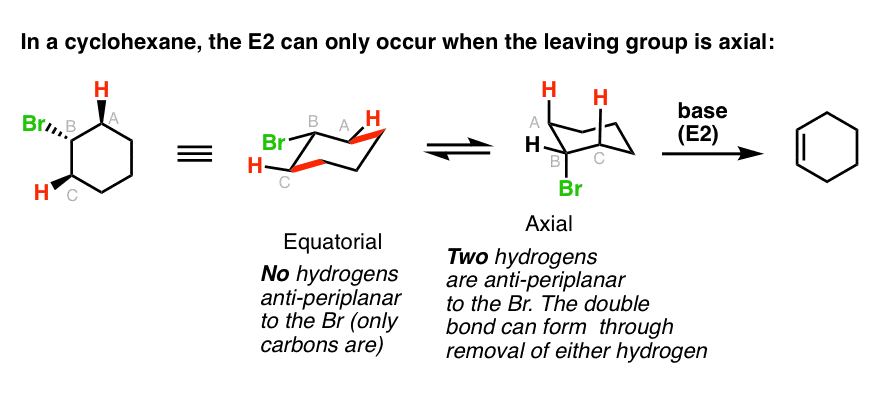
如果你画的离去基团赤道在环己烷的椅子上,你必须做一个椅子翻转,这样离去基团是轴向。右边所示的例子中,一个地方E2可以发生。
3所示。E2环己烷环的反应,只有这样离去基团和碳氢键可以Anti-Periplanar如果对面脸上的戒指
这就引出了第二点。如果离去基团假设,在环己烷的“顶级”的脸,可以吗只有形成一个烯烃相邻的碳原子氢在的地方相反的脸。
你可能还记得上次的例子,我们无法形成“扎伊采夫”烯烃因为Br楔和有一个烷基集团在隔壁的碳在相反的脸上。在这种情况下我们只能形式代替越少烯烃。然而,如果甲基转移的E2给扎伊采夫产品成为可能:
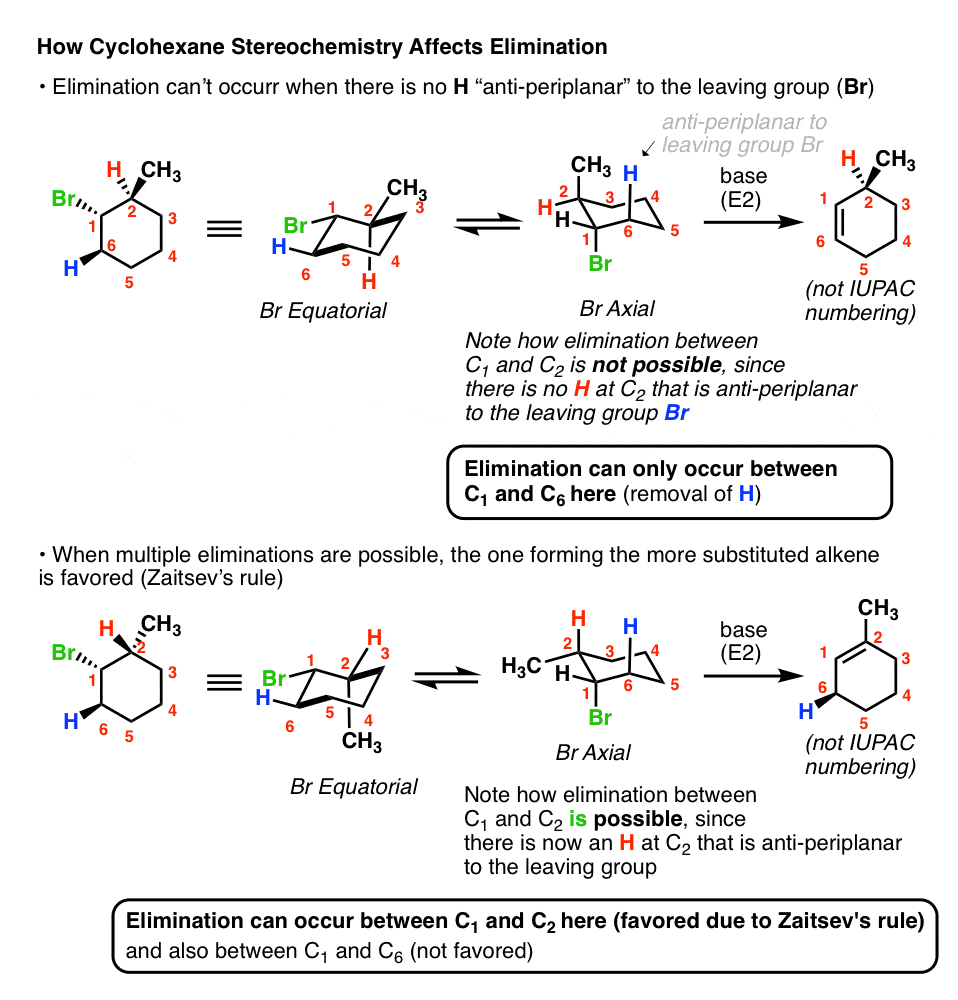
这里的底线(相信我,这是在测试,很多!)是,你总是想关注你的戒指吗离去基团是,确保E2你画确实是可能的。
4所示。一些例子:什么是主要的E2产品在每种情况下?
这里有一些更多的例子。主要是什么E2产品在每种情况下?
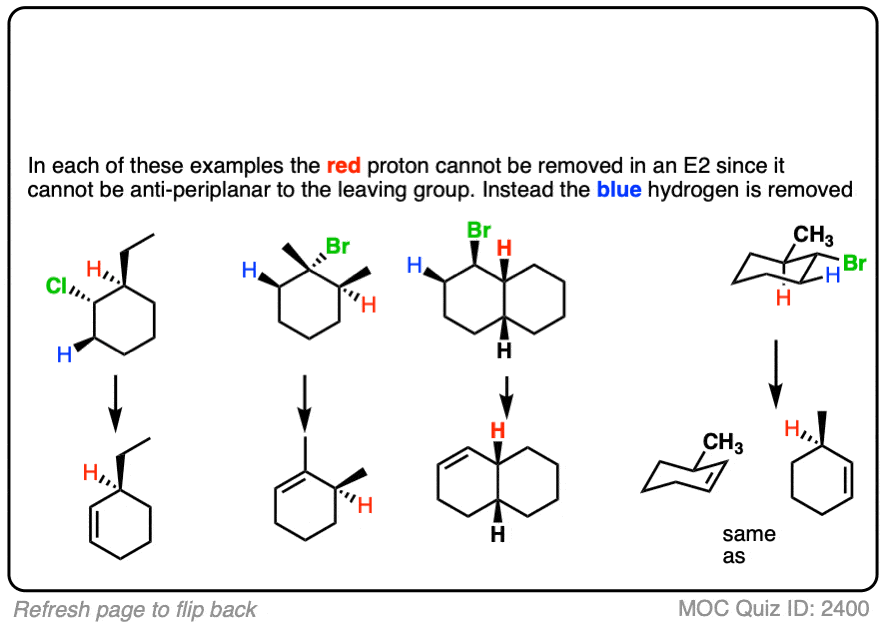
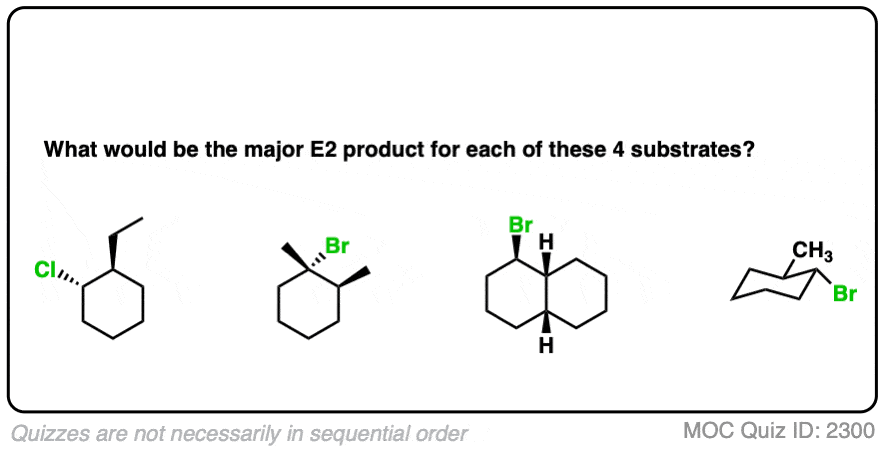 点击翻转
点击翻转
现在,让我们来谈谈我们刚才讨论的一个非常有趣的应用。这是一个小更先进,但看看你可以跟着它穿过。它联系在一起我们的讨论E2与你之前了解了环己烷椅子翻转。
5。取代基环己烷可以影响E2在环己烷环消除反应的速率
想象你有两个烷基卤化物,他们有不同的结构。我们做出如下观察:E2第二起始物料都要快得多E2第一个产品的。问:这是为什么呢?
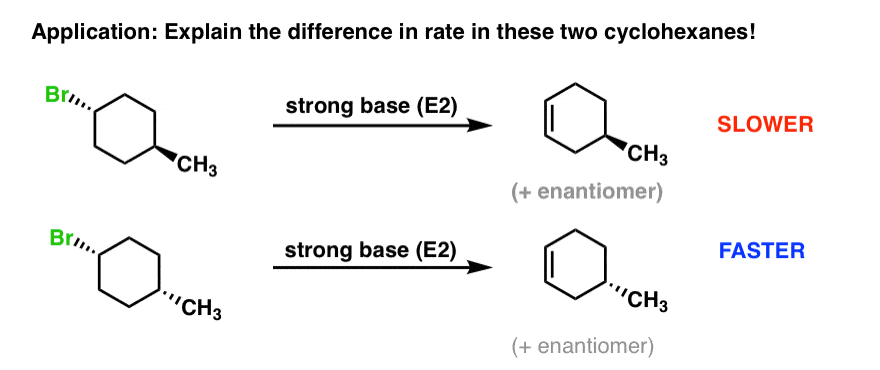
为了理解发生了什么,这将有助于吸引的环己烷椅子形式这两种分子。我们来做一下,然后仔细看。
发生什么事了?每个分子有两种椅子形式之间的平衡。
在前分子,左手构象被看好,因为笨重甲基吗(CH3实际上比Br)笨重是赤道。所以平衡将有利于左手分子。
在底部分子,最右边的构象被看好,因为笨重甲基吗赤道。所以平衡将有利于右边的分子。
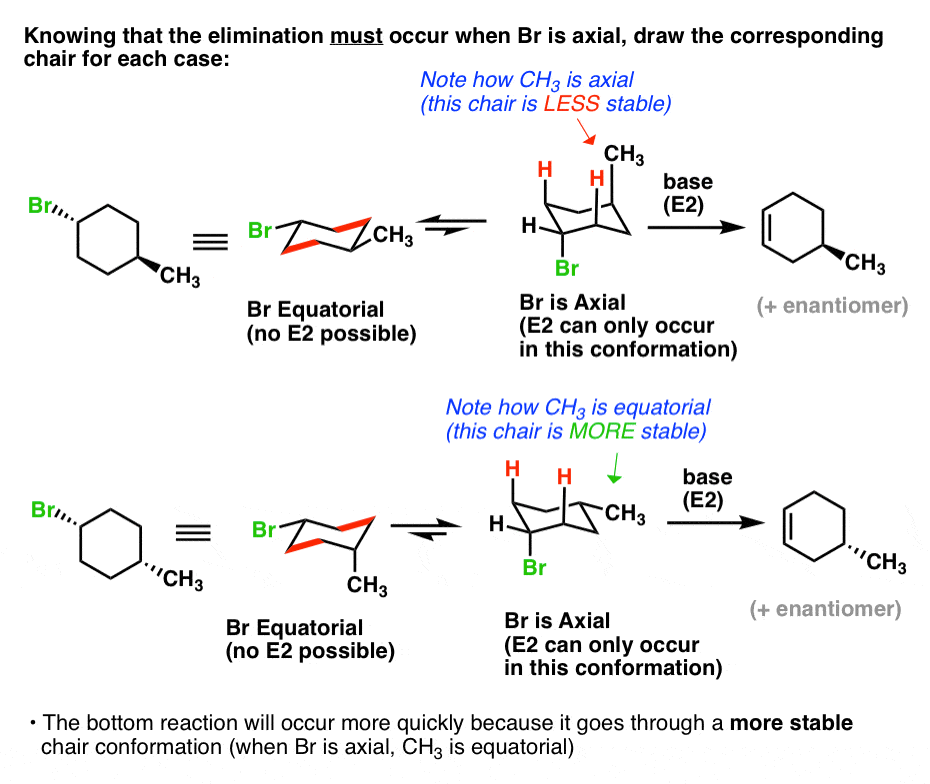
6。浓度越高的构象异构体轴离去基团,消除将越快
注意到一些有趣的事情吗?记住,为了E2发生,离去基团必须轴向。
所以只有一个构象为每一个环,这将是可能的。然而,在上面的例子中,Br轴向只有在最不稳定构象,而在底部的例子中,Br轴向在最稳定的构象。因为底部会有一个例子更高浓度Br在哪里轴向,它将更快。
是如何联系在一起吗?你学习的概念一章回来,可以应用在以后的章节!
在下一篇文章我们将讨论另一个例子扎伊采夫规则不适用。
笔记
(高级)引用和进一步阅读
- Abspaltungsreaktionen和《国际卫生条例》sterischer Verlauf
沃尔特·Huckel Werner Tappe Gunter Legutke
Lieb。安。化学。1940年,543年(1),191 - 230
DOI:10.1002 / jlac.19405430117
早期的研究E2立体化学薄荷基衍生品。 - 消除反应的机制。十八。动力学和立体异构六氯化苯的消除
e·d·休斯、c·k·英格尔德和r·帕斯捷尔纳克
j .化学。Soc。1953年,3832 - 3839
DOI:10.1039 / JR9530003832
本文的名字有点混乱,因为“六氯化苯”不指六氯苯,但是1、2、3、4、5、6所示- - - - - -六氯环己烷。六氯环己烷有几个同分异构体取决于氯原子的方向,因为在文章中解释道。根据异构体中氯原子的方向,得到不同的产品,根据是否E2途径在这些位置是可能的。 - 消除反应的机制。X。氘六氯化β-Benzene交易所Base-Promoted脱氯化氢作用
斯坦利·j·Cristol和德尔伯特·d·修复
美国化学学会杂志》上1953年,75年(11),2647 - 2648
DOI:1021 / ja01107a027
六氯化苯同分异构体——所有的经典研究氯原子相邻的碳原子上反式彼此,所以是不可能把相邻的氢和氯反不会造成环应变的关系。 - 消除反应的机制。第十九一部分。从异构动力学和立体的消除薄荷基氯化物
e·d·休斯、c·k·英格尔德和j·b·玫瑰
j .化学。Soc。1953年,3839 - 3845
DOI:10.1039 / JR9530003839
本文说明了扎伊采夫规则在环己烷系统中。氯化Neomenthyl给2-menthene 3-menthene 78%和22%在接受采访时表示- - - - - -在乙醇。 - 消除反应的机制。第二十二一部分。从trimethylneomenthylammonium异常消除离子
e·d·休斯和j . Wilby
j .化学。Soc。1960年,4094 - 4101
DOI:10.1039 / JR9600004094
本文完全说明的概念在这一节中解释。Menthylammonium离子不能接受取消3 -烯烃,因为反在占领了C4的立场异丙基组。只有2 -烯烃获得从消除menthyl-LG (LG =离去基团、氯化三甲胺等)。在neomenthyllg,异丙基集团是不反,所以3 -烯烃是可访问的。然而,3 -的收益率烯烃当埃托奥从88%降低到65%- - - - - -是用来代替哦- - - - - -,这可能会进一步减少(如tBuO当使用笨重的基地- - - - - -)。 - 相邻的碳和氢。第十九。t-Butylcyclohexyl衍生品。定量构象分析
美国Winstein和n·j·霍尔尼斯
美国化学学会杂志》上1955年,77年(21),5562 - 5578
DOI:10.1021 / ja01626a037
这是经典的论文Winstein教授介绍的概念一个值。有一个简短的提及的影响轴向/赤道取向的离去基团反应性。当离去基团是轴向,一个E2通路被看好,但当离去基团是赤道的混合E1和SN1发生。
轴向的甲基环己烷和Br集团E2较慢,和你为什么的原因是“平衡位置位于其他更多的椅式构象(在赤道与LG和CH3),不需要椅子(轴向与LG和CH3)”,通过动力学、速度慢的低浓度所需的椅子。
但在其他地方,说的原因是,因为“过渡态的椅子有甲基和Br在轴向位置更不稳定,所以活化能越大”。
的解释是正确的吗?
哇,很有帮助谢谢!
你的解释和图片都很有帮助,谢谢。但与消除产品,其他unshown产品并不是对映体,而是宪法异构体,不是吗?我害怕如果我理解完全错了。:(
把它画出来。它仍然是4-methyl环己烯,所以它不可能是宪法异构体。它看起来可以重叠其他* * 4-methyl cylohexene吗?:-)
你能解释1-bromo-2-methyl-4-tertiarybutyl环己烷脱卤化氢吗
它是安全的假设-丁基宁愿将赤道。1 -溴集团对E2 Br时只会发生轴向。所以你会有不同的反应率为顺式和反式- 1-bromo-4-t-butylcyclohexane,因为会有一个轴向Br叔丁基赤道时,和其他只会有一个轴向Br叔丁基时轴向。你可以自己决定取消将更快。情况进一步复杂1-bromo-2-methyl-4-t-butyl环己烷甲基的根据立体化学。
你好,詹姆斯,
只是想谢谢你这样一个美妙的网站!我主修生物化学,有机化学是我的激情;然而;的时候,有一些概念混淆,和你的网站帮助提醒自己,一切在化学应该是有意义的!
谢谢你!
很高兴你找到网站有用Nata !
亲爱的詹姆斯:
我想问为什么在最后一个例子,为什么两种反应给对映体?例如,环己烷甲基和溴虚线。消除后,不应该甲基在虚线吗?如何对映体?
非常感谢! !
双键可以形成两个碳原子相邻与离去基团的碳(β碳)。如果你画产品和翻转1 /你会看到他们对映体:两个同样会之间的双键碳原子但甲基将少量或楔形。
出色的詹姆斯。我以为我是像样的有机化学,但这些教训使一切变得更加简单。我发现我还有很多东西要学。
你好詹姆斯
谢谢你的澄清
两个问题(如果这些声音太天真道歉):
1。据我所知反periplanar相依仅仅意味着两组之间的双面角是180度,而这是e2所必需的。现在如果是如此,为什么不能离开组和alpha-hydrogen赤道吗?
2。为了获得这种配置以便e2,我们能从cis转化为反式,反之亦然?
1。是不可替代的模型和为自己看到这个。
2。环翻转永远cis转化为反式,反之亦然。环只翻转开关轴向赤道。再一次,制作模型,把这个给自己。
嗨,詹姆斯。4的例子你给我们尝试,我制定了第二个例子(1-bromo-1 2-dimethylcyclohexane)我得到我的主要产品是1,2-dimethylcyclohex-1-ene之间的双键(c1)。你的主要产品有c1-c6之间的双键。你能解释为什么这是主要的产品?扎伊采夫规则告诉我们没有更多的取代烯烃(我的答案)与至少替换(你的回答)?我会很感激的回应!
注:你的网站是我做好在有机的原因,我不能感谢你才好。:)
-Anum
第二个例子,E2、溴需要另一侧的环氢消除发生。这与C2是不可能的,因为氢的同侧环溴。因此,我们不能在这里形成一个烯烃- C1和C6之间形成。
第二方案,第二反应,第三结构:真的会有帮助如果你显示C2-attached氢,是直接参与反应。相同的第一反应可能不会伤害,。
否则优秀的工作,像往常一样。
再次感谢你,我非常感谢你敏锐的眼睛。
是的,这是一个有效的点。