芳香分子的反应
反应在“苄基的“碳:溴化和氧化
最后更新:2022年10月15日|
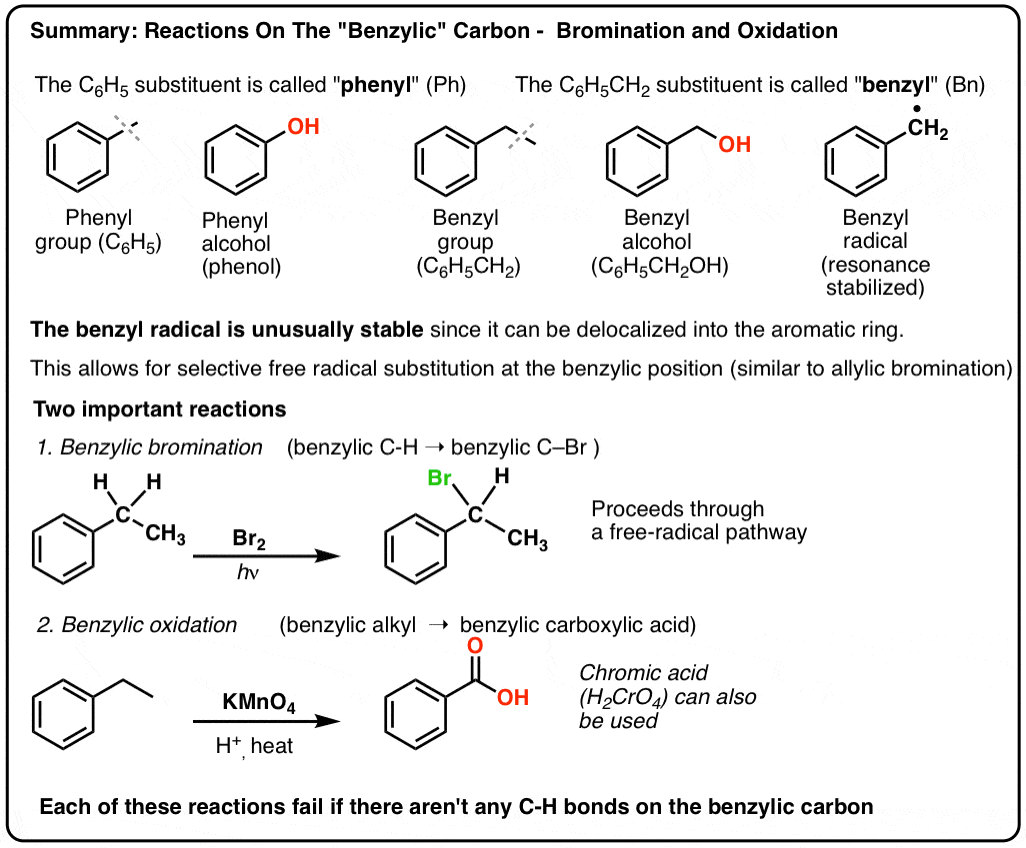
碳毗邻一个芳环-苄基的“碳可以参与一些有用的和有趣的反应。今天我们将提供的例子和机制两个关键的例子:苄基的溴化、苄基的氧化。这是快速的总结:
表的内容
- 烷基组=“粗粮”
- 有什么特别之处烷基组相邻的苯环
- “苯”与“苄”:有什么区别吗?
- 苄自由基是由共振稳定;苯自由基。
- 苄基的(和烯丙基的)碳氢键较弱,相对于其他烷基碳氢键
- 苄基的溴化
- 什么时候“苄基的溴化“不工作吗?
- 应用程序的苄基的溴化
- 苄基的氧化与KMnO4(或H2阴极射线示波器4)
- 苄基的氧化需要苄基的碳氢键
- 为什么这个很重要?(提示:在合成中的应用)
- 笔记
- 测试你自己!
- (高级)引用和进一步阅读
1。烷基组=“粗粮”
在营养、“粗粮”就是你所说的所有在场的纤维素和纤维素的食品,只是通过你的身体不被消化。
这很大程度上描述的行为烷基组在绝大多数的我们学过有机化学反应。他们的化学“无聊”。他们可能包括骨干和整体结构的分子,但他们的碳氢键是惰性反应条件。(注1]
事实上,如果你不燃烧,几乎唯一的反应烷基组织我们在介绍有机化学自由基取代。甚至这种反应往往是相当unselective,特别是如果你处理自由基氯化。(参见:选择性在自由基反应]
我们已经见过一个例外“无聊”的行为可以找到所谓的“自由基溴化的烯丙基的“碳氢键(看到:烯丙基溴化]。“烯丙基的“位置是相邻碳双键(不是一个碳氢键双键本身!这是一个“vinylic”碳氢键)。
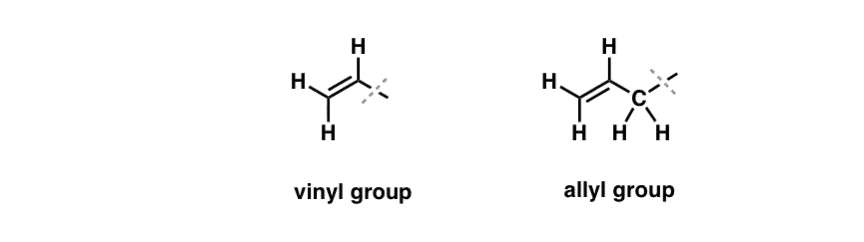
是什么让“烯丙基的“位置如此特别?烯丙基的自由基、碳正离子和负离子相当稳定共振。的轨道烯丙基的激进、碳正离子或负离子能使自己与相邻的p轨道π键,导致一个更大的“π体系“和传播在更大的区域。(参见:烯丙基自由基的分子轨道,阳离子和阴离子]
2。有什么特别之处烷基组相邻的苯环
是什么原因这个小的记忆,决定?好吧,我们最近花了一段时间了傅克烷基化反应,我不想给你留下了这样的印象:一个烷基小组苯环是合成的。
烷基组织不需要惰性!就像烯丙基的碳,烷基组邻苯戒指特别被动,这可能有各种各样的重要应用。
有两个重要的反应在这篇文章我们将讨论:
3所示。“苯”与“苄”:有什么区别吗?
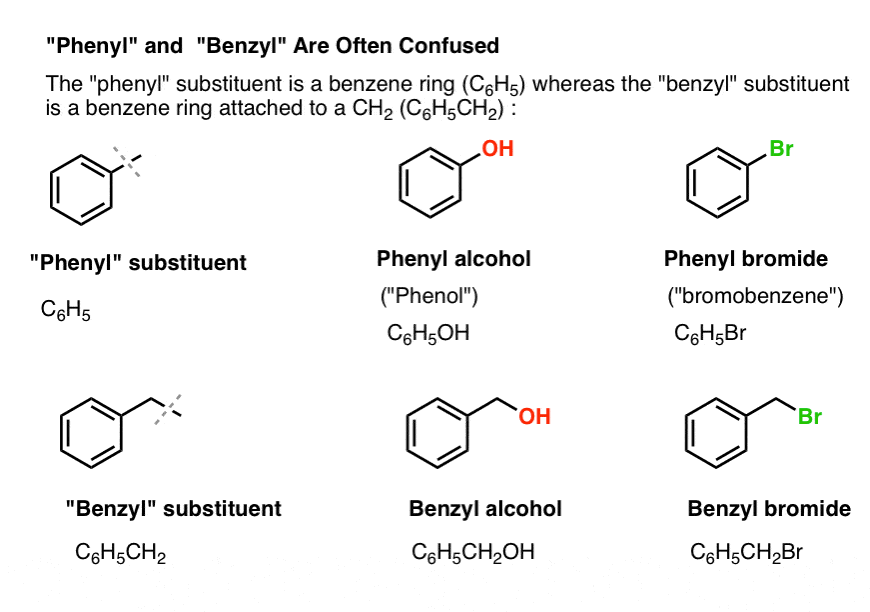
首先,一个快速的订单业务。让我们得到一些重要的术语,因为“苯基”和“苄“造成很大的困惑:
- 一个苯基集团(或苯基取代基)苯-氢:C6H5。的碳环苯基碳,氢相连苯基碳是苯基碳氢键。这是类似于乙烯基(见上图)。
- 一个苄集团甲苯-氢:C6H5CH2。碳环附近苄基的碳,和氢原子与苄基的碳被称为苄基的氢。这是类似于烯丙基(见上图)。
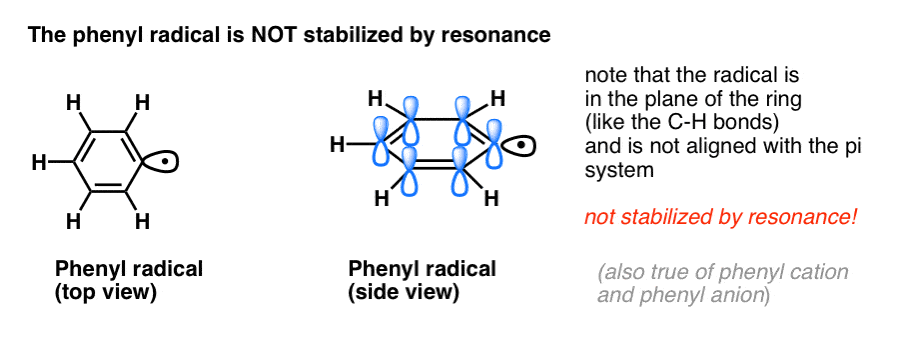
4所示。苄自由基是由共振稳定;苯自由基。
的类比苯基与乙烯基和苄烯丙基也延伸到自由基的稳定性(以及他们的碳正离子和负离子)。
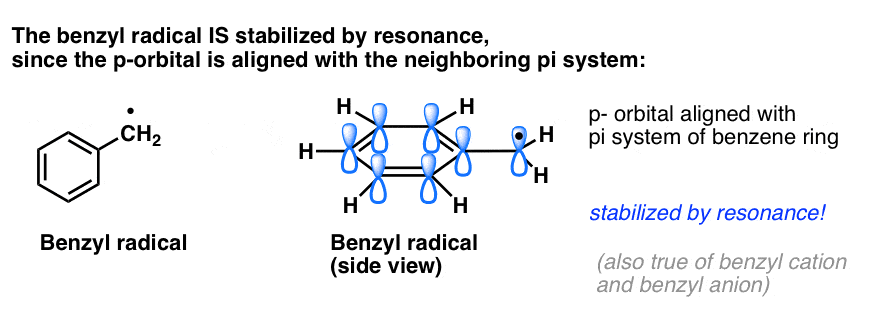
5。苄基的(和烯丙基的)碳氢键较弱,相对于其他烷基碳氢键
苄基的碳氢键键的强度(又名12,或债券离解能量)约90千卡每摩尔,这远远弱于叔碳氢键(粘结强度93千卡每摩尔)二级碳氢键(96千卡每摩尔)和初级碳氢键(100千卡每摩尔)债券。(苯基碳氢键约113千卡每摩尔,又反映出的不稳定性苯基激进分子(裁判])。
由于债券dissocation能量反映易用性均裂的碳氢键(即是多么容易分离债券为两个自由基)这是另一种说法苄基的激进分子特别容易形成相对于其他烷基激进分子。
我们之前见过的,也是如此烯丙基的碳氢键。在“烯丙基溴化”,一个碳氢键的烷基集团毗邻一个双键转化为C-Br债券,使用N-bromosuccinimide(国家统计局),光(hν):
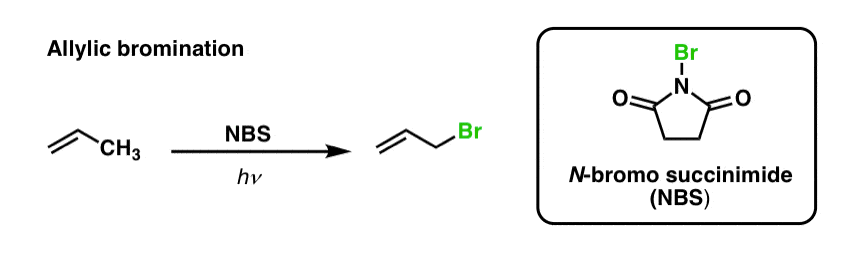
(为什么国家统计局而不是Br2吗?的目的国家统计局是提供一个常数,低级Br的浓度2这是可用的自由基取代反应。看起来简单的用Br2,但Br2迅速与双键反应给附近的二溴化!]
反应的选择性烯丙基的碳氢键的一级,二级,三级碳氢键较弱烯丙基的碳氢键强度(89千卡每摩尔)。
6。苄基的溴化
类似的过程适用于“苄基的碳原子。我们可以使用国家统计局(如上所述)或仅仅只是Br2芳香环,因为几乎不与溴反应2双键。(注2]
一旦形成(通过“热”或“光”,提升者通过均裂离解反应的Br-Br),溴激进,Br•可以打破较弱的苄基的碳氢键不碰更强烷基碳氢键。
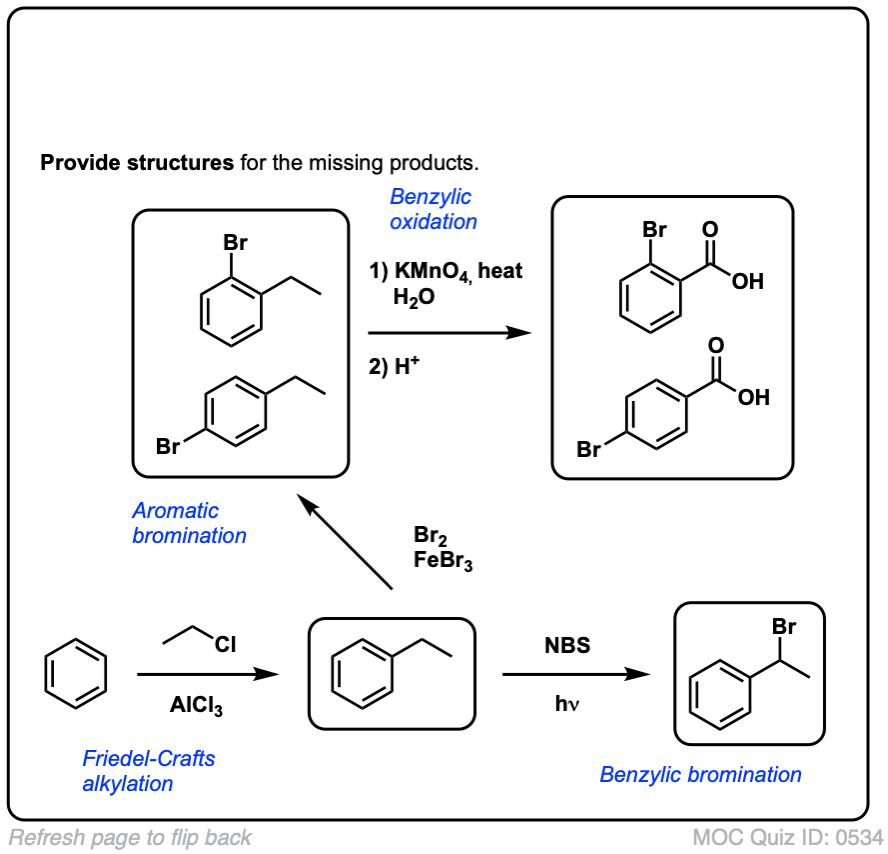
例如,下面是产品与甲苯的反应,以及茴香素。注意,只有苄基的碳是溴化。其他的都是独处!
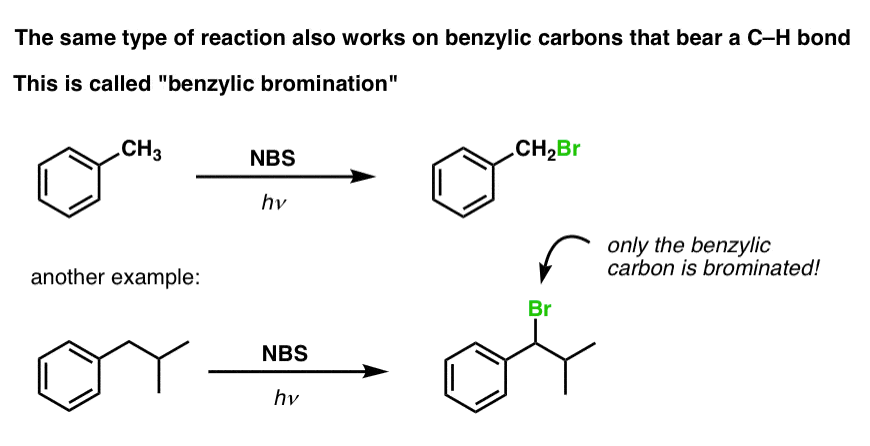
的机理苄基的溴化本质上是相同的烯丙基溴化,初始化、传播和终止的步骤。
(更多讨论,请参见这篇文章:烯丙基溴化)
7所示。什么时候“苄基的溴化“不工作吗?
因为这个反应的关键是形成(相对稳定)苄基的激进,苄基的溴化将会失败在基质生成这种激进通过打破一个碳氢键是不可能的。
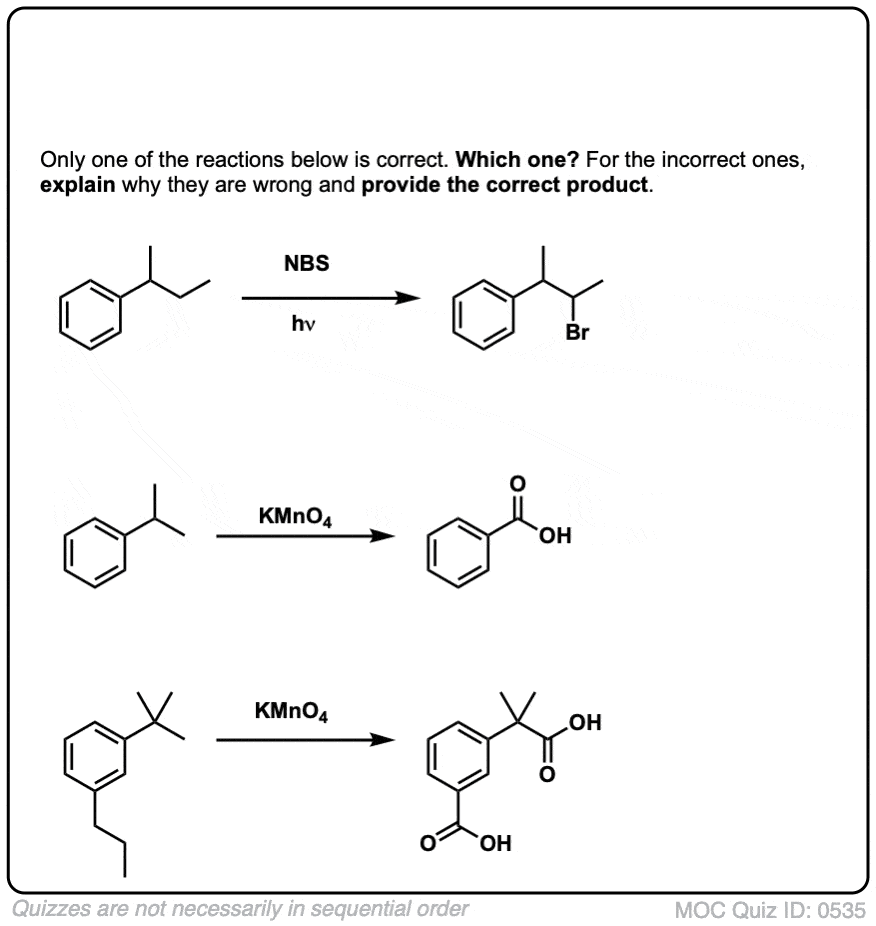
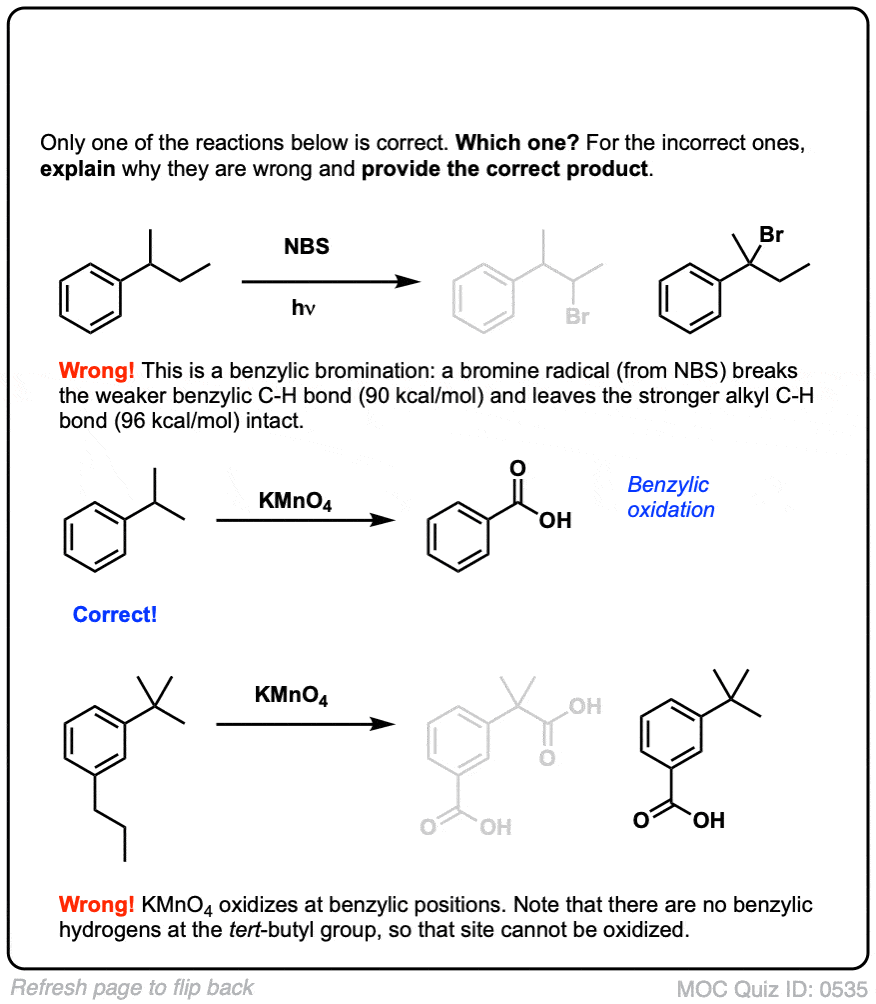
例如,看看下面的例子。苄基的激进怎么可能当苄基的生成碳有三个烷基基团吗?它不能反应失败。
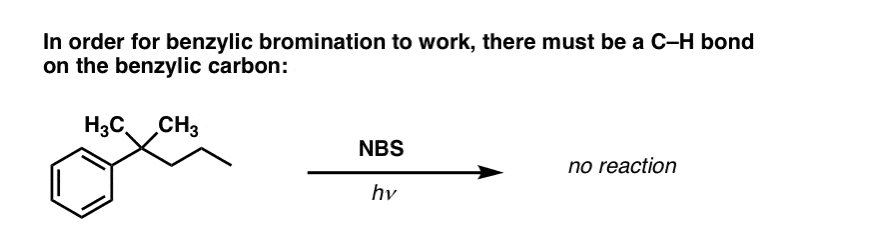
8。应用程序的苄基的溴化
为什么可能苄基的溴化是有用的吗?
嗯,它允许我们使用所有的反应烷基卤化物,覆盖在Org 1 -主要是替换和消除-提供产品,很难直接安装在一个芳环通过傅克反应。(看到的:合成:卤代烃的反应]
例如,可以使用苄基的溴化建立一个年代N傅克烷基化后2反应,如:
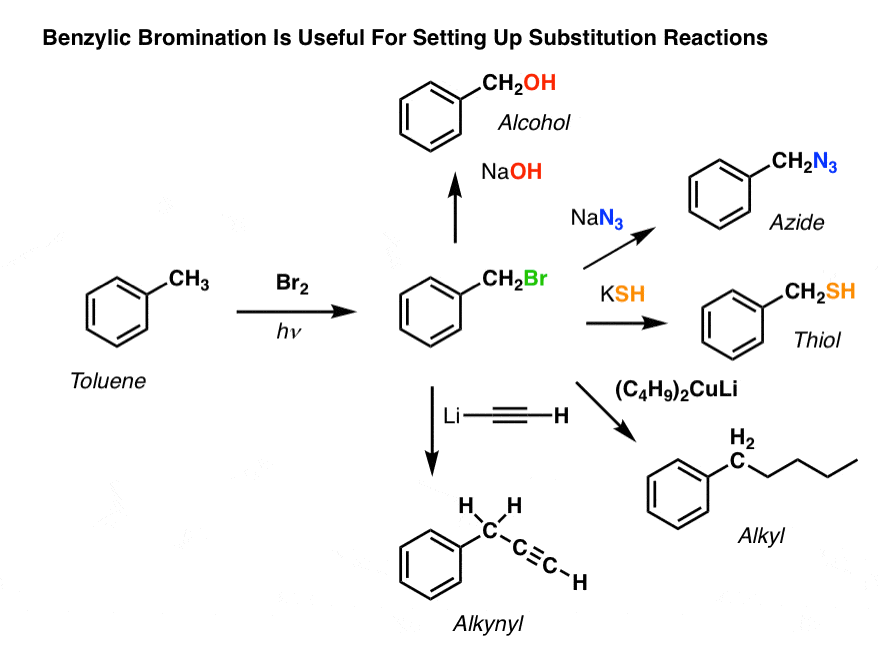
看看安装好离去基团在苄基的位置给了我们各种各样的选项,安装各种官能团?
另一个例子是苯乙烯的合成苯。乍一看,似乎最直接的方法可能的傅克反应乙烯基氯化苯。但傅克反应不工作烯基卤化物(又名乙烯基卤化物)!(乙烯基碳正离子比不太稳定烷基碳正离子)。
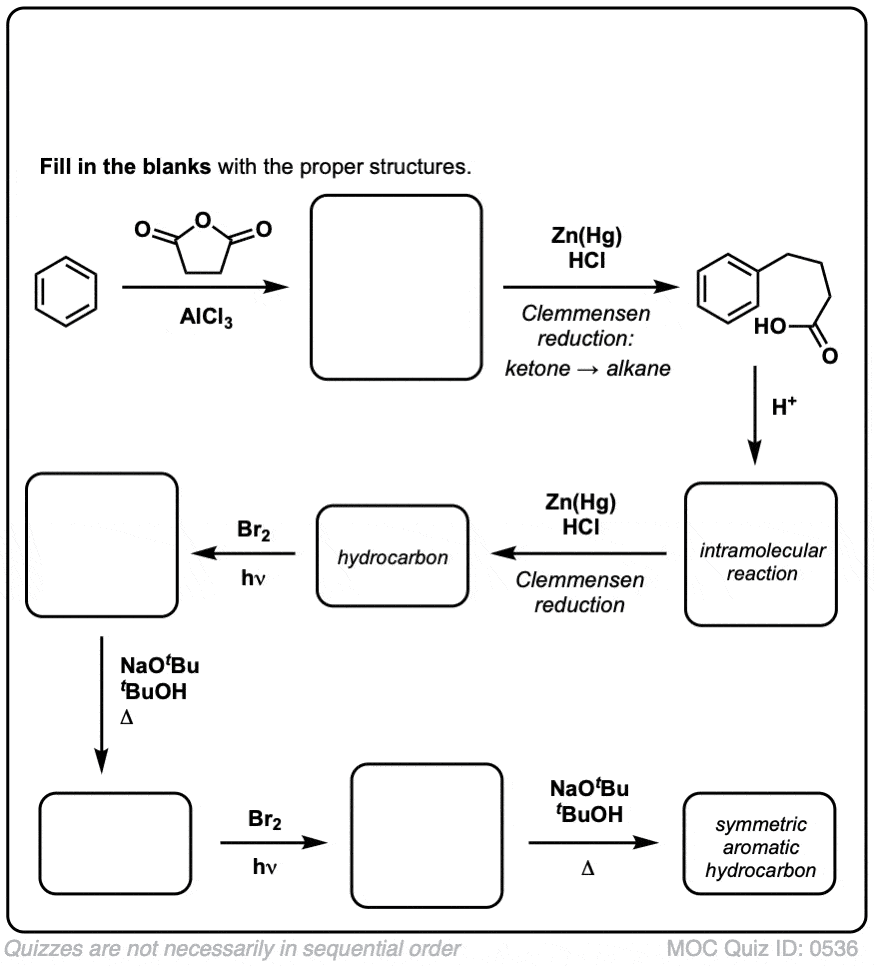
我们可以克服这个障碍通过执行氯乙烷的傅克烷基化,其次是苄基的溴化,然后消除(通过E2,与类似NaOtBu / t-BuOH)给烯烃:
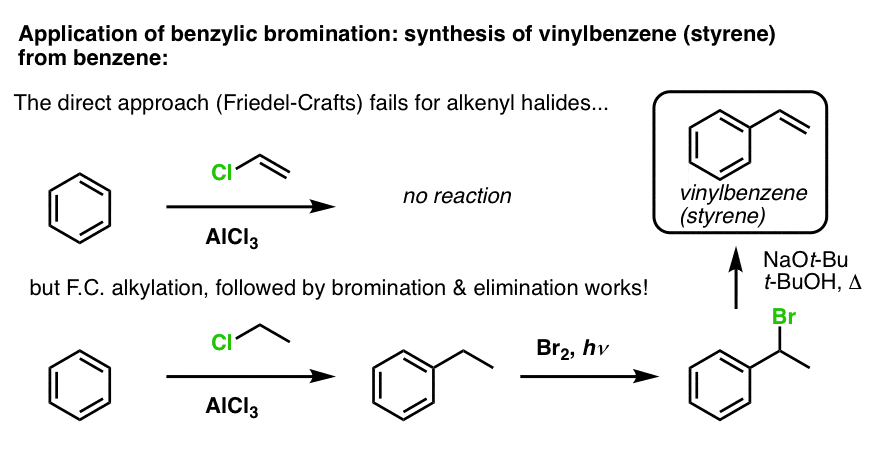
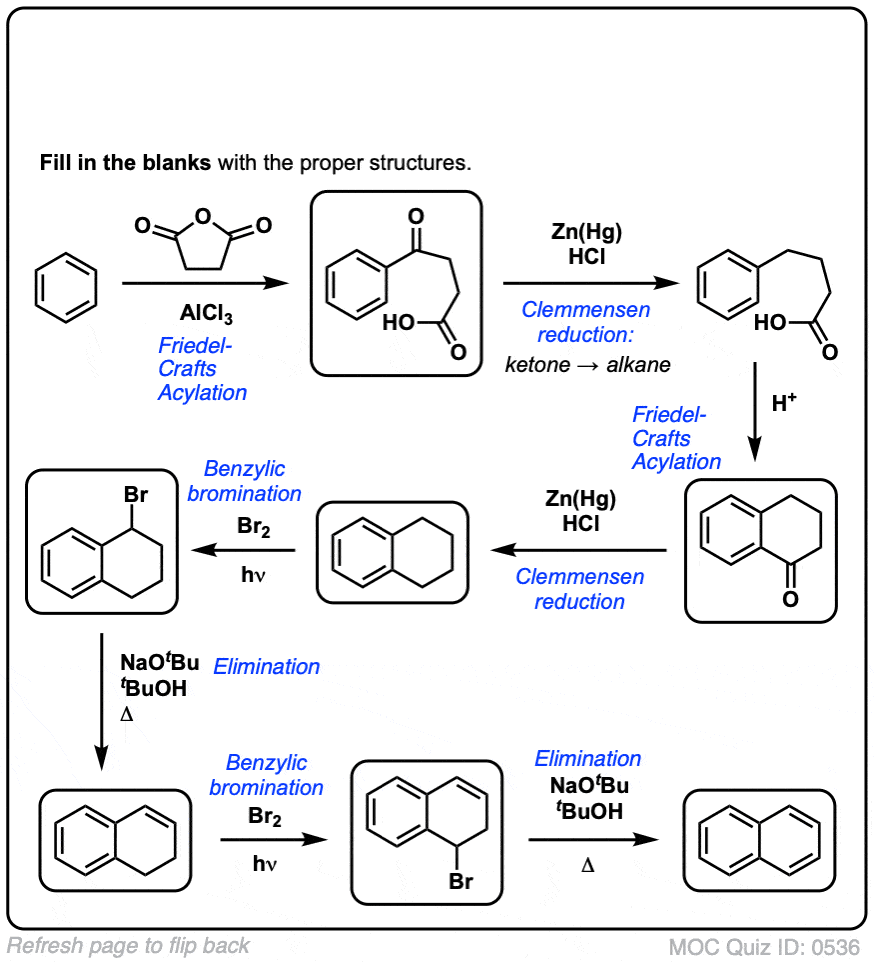
在此基础上,这里是一个快速测试。你怎么可能把萘满(下图左)萘(下图右)?答案在脚注注3]。
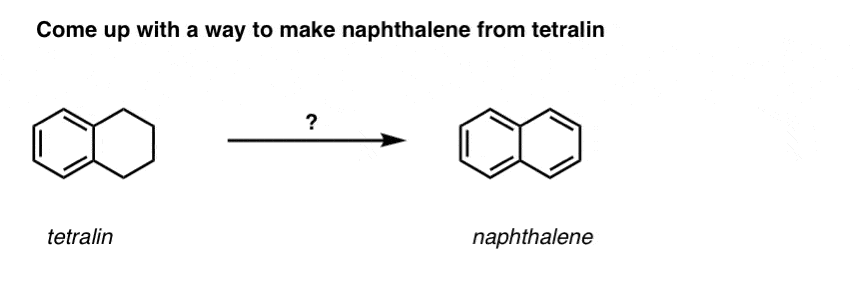
9。苄基的氧化与KMnO4(或H2阴极射线示波器4)
自从苄基的碳氢键是相对较弱的,你可能会正确地问其他类型的反应(除了溴化)可以执行在这个位置。
他们当然可以!一个典型的例子是苄基的氧化- - - - - -在苄基的碳氢键坏了和苄基的切断键形成。
现在:存在非常温柔的对苄基的试剂氧化碳氢键的化学当量挠痒痒的羽毛,导致苄基的醛或酮(酒精是一个中间,但通常氧化到什么醛/酮在这些条件下)。
这不是苄基的氧化的类型,覆盖在一个典型的介绍有机化学课程!
相反,苄基的氧化的主要试剂,覆盖在大多数介绍热高锰酸钾(KMnO教科书4)。热铬酸(H2阴极射线示波器4相结合,这是由重铬酸盐等Na2Cr2O7等强酸H2所以4)也可以用于这些目的。
KMnO4不是微妙。KMnO4不温柔。KMnO4不是那种。
溶液热KMnO4就像一个袋子愤怒的食人鱼会撕裂你肉体的分子,留下只有骨头。(想想看,它就像你的肝脏!(注意4]
热KMnO4将每个苄基的碳氢键,并将其转换成切断键。从甲苯,例如,该产品是苯甲酸(a羧酸)。
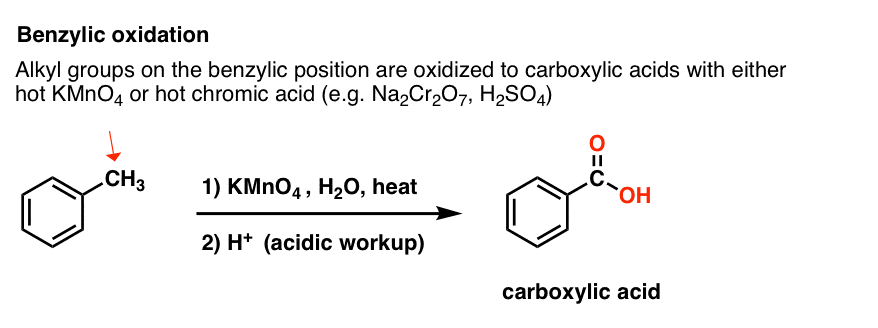
但它不只是打破苄基的碳氢键。哦,不。它追求碳碳键;至少那些不是直接连接到苯基戒指。例如,帕拉- - - - - -二乙苯转化为帕拉-benzene-dicarboxylic酸。
请注意,烷基碳碳键必须是裂解为了这个氧化发生!(它可能是氧化一直到有限公司2气体)。
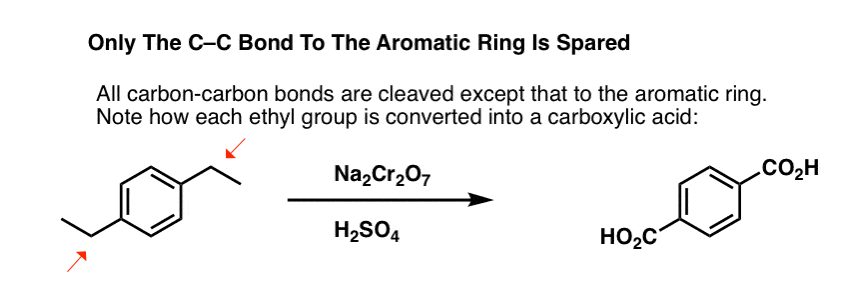
一个有趣的变化是在一个循环分子如萘满;结果是二羧酸。
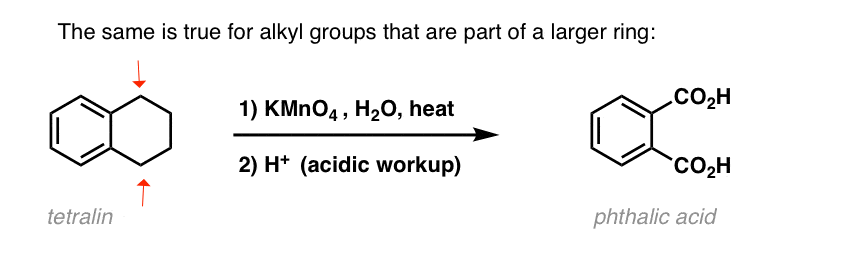
这二羧酸称为邻苯二甲酸。
10。苄基的氧化需要苄基的碳氢键
与苄基的溴化,没有反应发生如果没有苄基的碳氢键的位置。例如,反应不完全t丁苯:
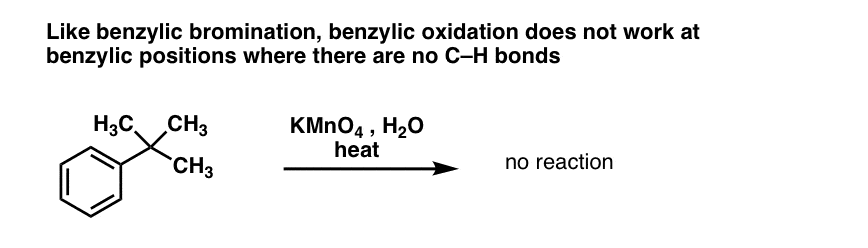
完整的苄基的氧化机制过于复杂,长,和不确定的,但几乎肯定是第一步均裂碳氢键的Mn = O形成了苄基的激进。
11。为什么这个很重要?(提示:在合成中的应用)
苄基的氧化与KMnO4是一个严厉的反应,但它可以有它的用途。最好的作品简单的分子,没有精致的官能团,可以承受一些非常粗略的治疗。
首先要注意的是,羧酸不能直接放置于一个苯环通过傅克酰化,所以烷基化之后,氧化是一个有用的解决方案。
合成是第二有用的功能苄基的氧化转化为一个o - p -主任(一个烷基集团)到一个元参演。
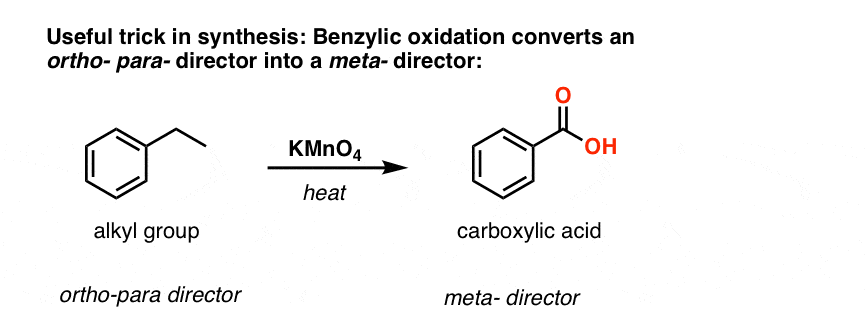
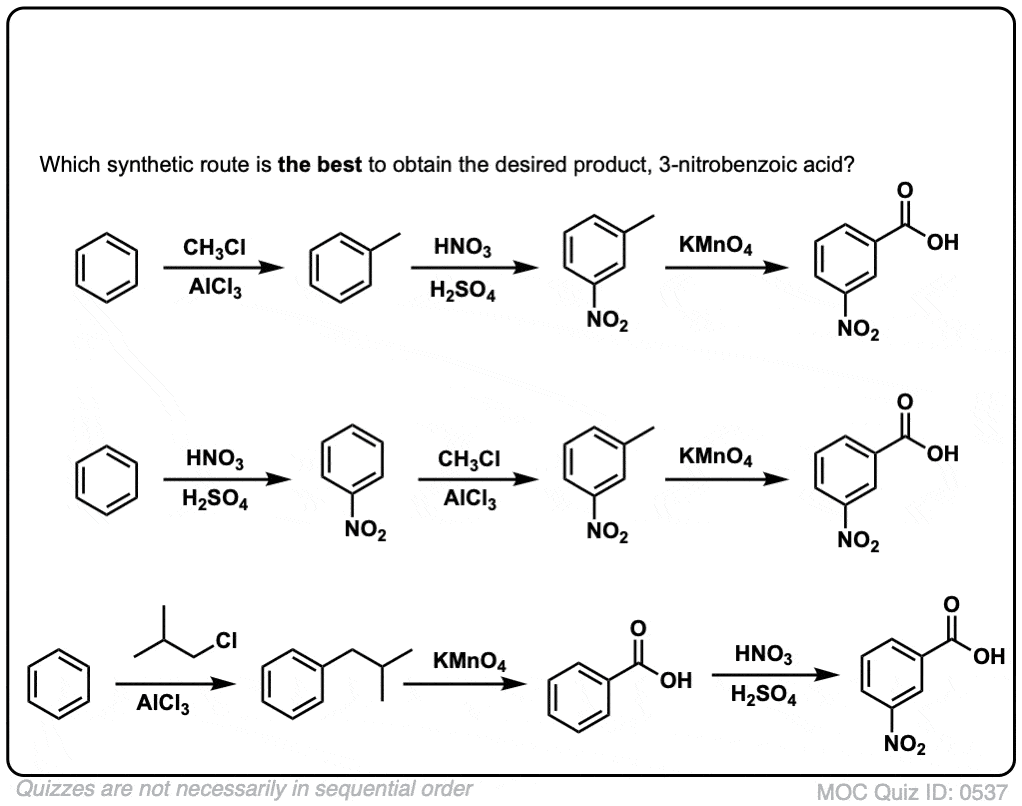
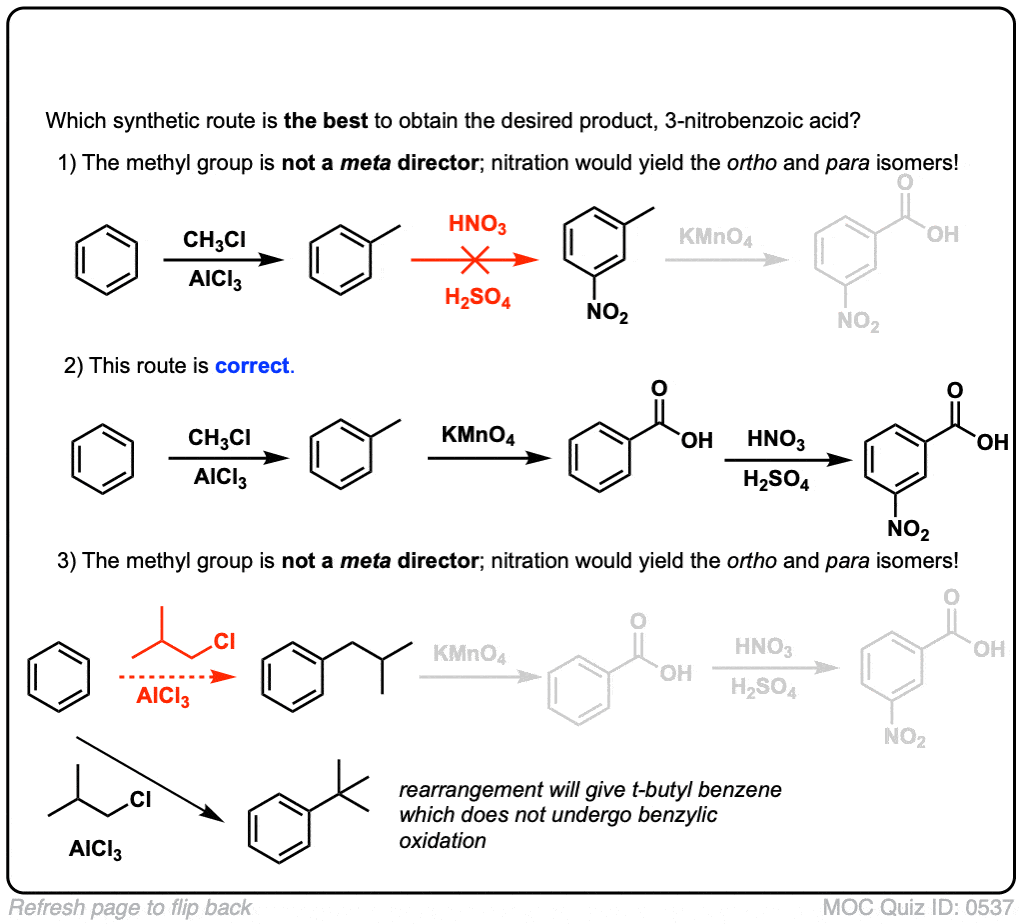
例如,面对以下的合成分子,你如何进行?(提示:它包括苄基的氧化在某种程度上)。(答案在脚注]
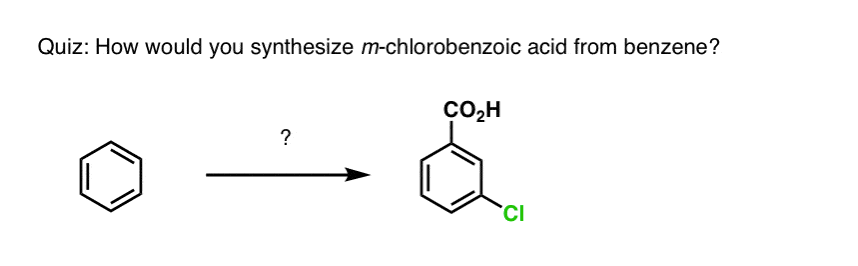
我们会有更多的关于合成芳香族化合物的一些职位。
下一个:减少苄基的羰基Clemmensen和Wolff-Kishner减少
笔记
注1。“卷心菜”也可以用于化学俚语“分子上的所有东西,您可以安全地忽略“不管出于什么原因。例如,苔藓虫素是一个野兽的分子显示承诺作为抗癌剂。问题是,它需要大量的一种罕见的苔藓虫一个像样的苔藓虫素,这是不够的对人类的临床试验。所以几组一直致力于制作简单,容易合成”bryologs”,摆脱“卷心菜”并不是必不可少的抗癌活性。
注2。Br2通常不会与芳香环没有路易斯酸催化剂的反应。但是如果存在强烈激活组(如哦,NR2等)可能发生一些环的溴化,尤其是在升高的温度下。
注3。这需要两个氧化反应和两个淘汰赛。谨慎的做法是氧化(即溴化)一次,然后消除给一个烯烃。的烯烃可以再次进行溴化(使用吗bdapp平台国家统计局,以避免双键的溴化)给另一个溴化(苄基的溴化产品所示,但是烯丙基的也是可行的)可以治疗基地给芳烃萘。
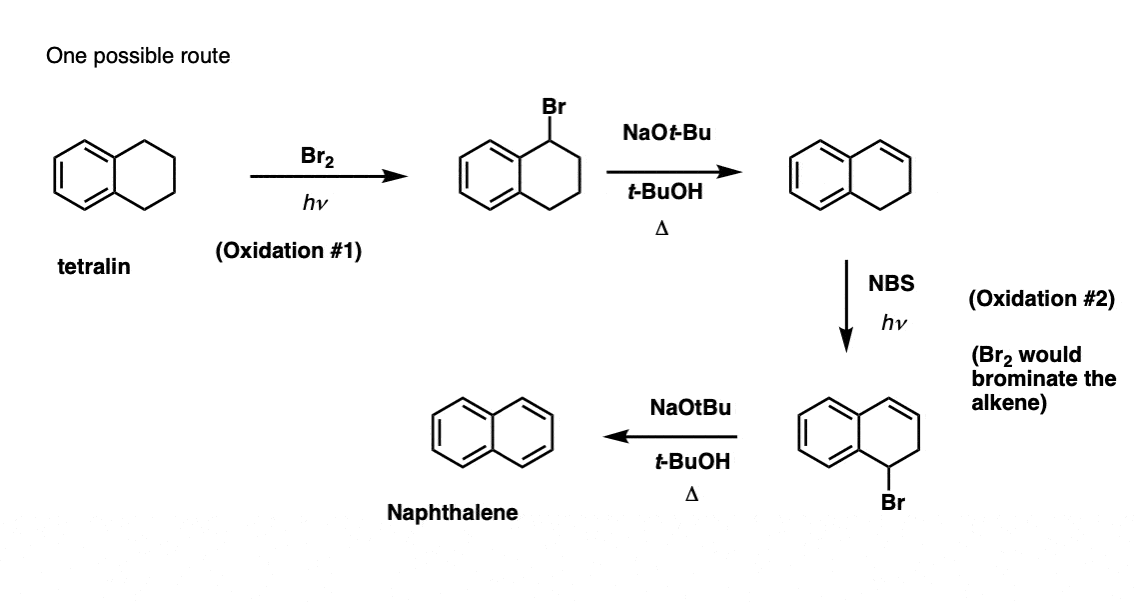
(实际上,事实证明两个溴化可以同时使用Br2高温。治疗基地可以产生萘)。
注4。有趣的事实:“苄基的氧化”的谜题的答案为什么甲苯(甲苯)不是那么强致癌物苯。这是因为你的肝脏细胞色素p450酶(包含高氧化态铁物种),可以氧化苄基的CH3组的水溶性羧酸,允许它被肾脏清除。
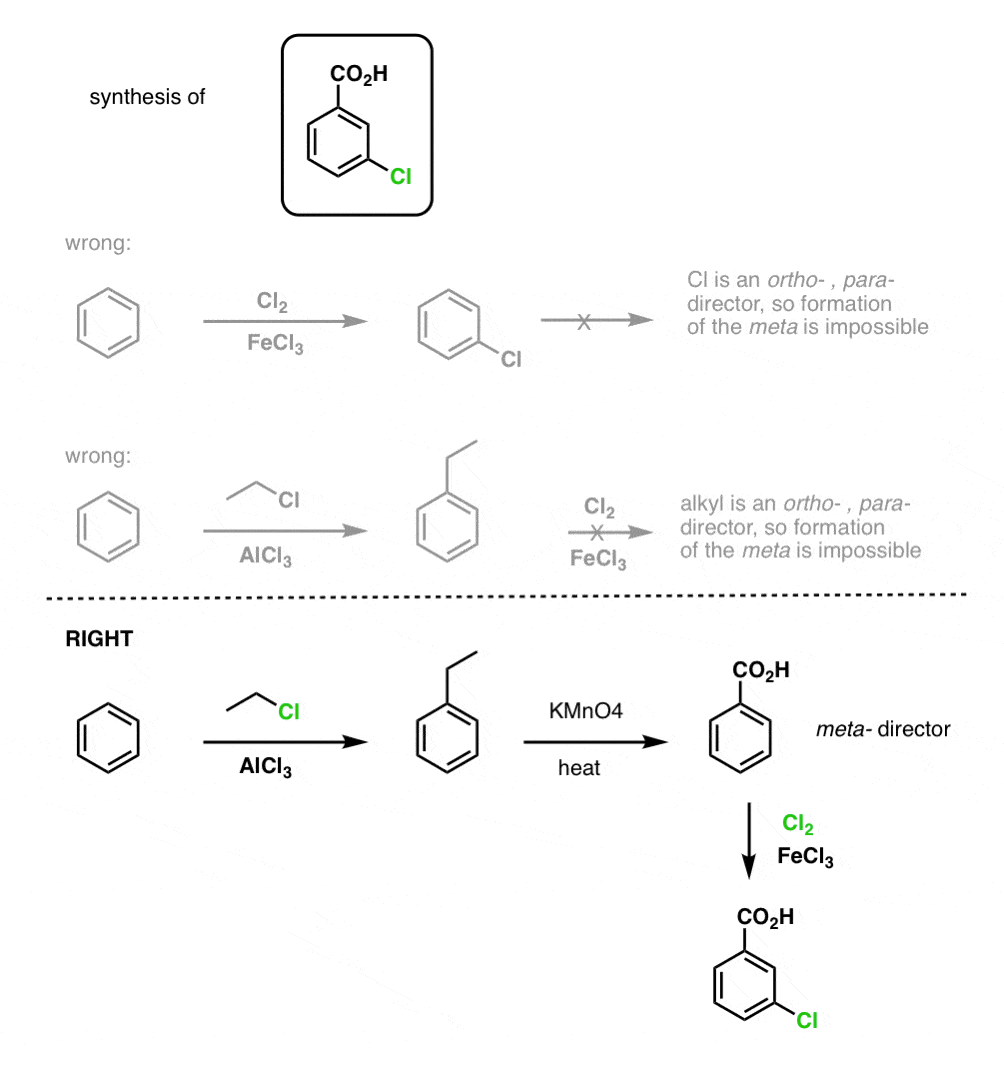
测试你自己!
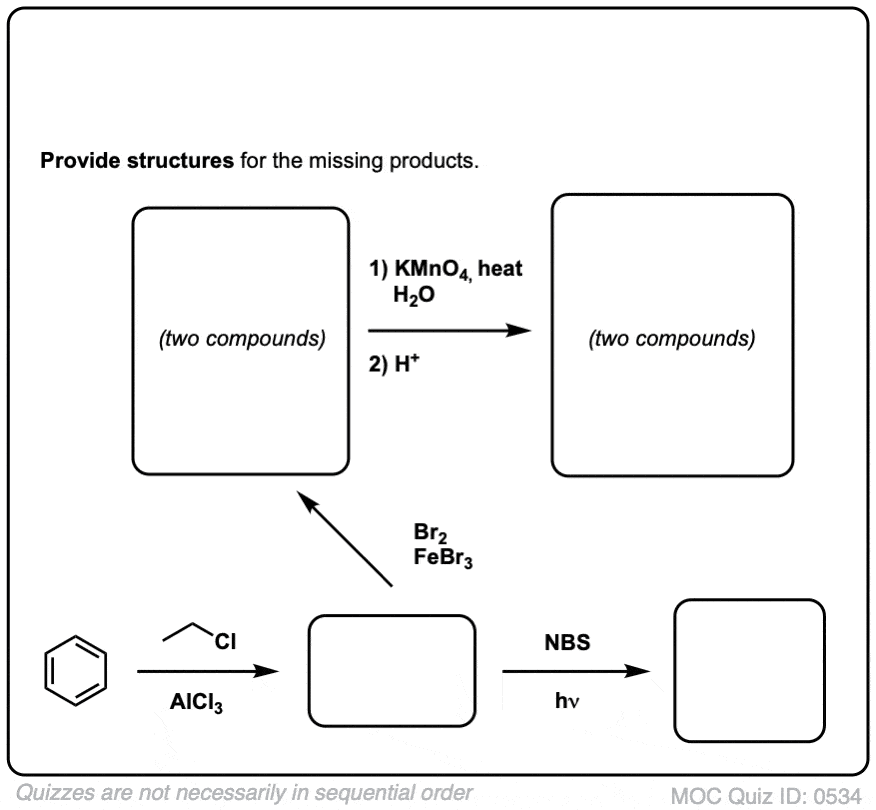 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
(高级)引用和进一步阅读
苄基的溴化:
这个反应也被称为沃尔齐格勒反应。
- Bromierung ungesattigter Verbindungen麻省理工学院N量布朗高acetamid静脉Beitrag苏珥学说vom Verlauf chemischer Vorgange
沃尔
化学。的误码率。1919年,52(1),51 - 63
DOI:10.1002 / cber.19190520109 - 死Halogenierung ungesattigter Substanzen der Allylstellung
齐格勒,a . Spath大肠Schaaf w·舒曼·e·温克尔曼
而已。Lieb。安。化学。1942年,551年(1),80 - 119
DOI:10.1002 / jlac.19425510103
前两个出版物在这个反应。沃尔N-bromoacetamide为溴化剂,使用国家统计局。齐格勒然后进行了详细的研究和报道国家统计局可以作为一个方便的溴化剂烯丙基溴化。 - 指[e]环辛烯:Multi-gram双齿配体的合成
杰拉尔丁弗兰克,马塞尔·布里尔,Gunter Helmchen
Org。Synth。2012年,89年,55 - 65
DOI:10.15227 / orgsyn.089.0055 - 与N-Bromosuccinimide苄基的溴化苯(Trifluoromethyl)
戴安娜苏亚雷斯,Gilles赖伐尔Shang-Min涂,江董,克莱尔·l·罗宾逊,理查德·斯科特·伯纳德·t·戈尔丁
合成2009年(11):1807 - 1810
DOI:1055 / s - 0029 - 1216793
使用参考# 3特征典型的苄基的溴化国家统计局在同4,由于毒性问题已基本淘汰。# 4表明PhCF参考3可以用作溶剂CCl代替吗4对苄基的溴化。 - 溴化N-Bromosuccinimide和相关化合物。沃尔齐格勒反应。
卡尔Djerassi
化学评论1948年,43(2),271 - 317
DOI:10.1021 / cr60135a004
老回顾这个反应由著名化学家卡尔Djerassi,对全球卫生的主要贡献是炔诺酮的发展——第一位女性避孕。 - N-Bromosuccinimide。三世。立体化学的苄基的溴化
h . j . Dauben jr .和莱顿l .真品
美国化学学会杂志》上1959年,81年(20),5404 - 5409
DOI:10.1021 / ja01529a038
机械研究的立体化学苄基的溴化。通过观察外消旋的形成苄基的陈词滥调的前手性的基质,独到的激进分子在这个反应是进一步加强。相同的引用烯丙基溴化可以改变用途: - 机制的苄基的溴化
格伦·a·罗素查尔斯。DeBoer,凯瑟琳·m·德斯蒙德
美国化学学会杂志》上1963年85年(3),365 - 366
DOI:1021 / ja00886a040
苄基的溴化遵循相同的机制烯丙基溴化本文解释了。国家统计局(N-Bromosuccinimide)是一种方便的自由基溴化试剂,和机械的研究包括以下文件国家统计局: - 苄基的机制与N-Bromosuccinimide溴化
r·e·皮尔森和j·c·马丁
美国化学学会杂志》上1963年85年(3),354 - 355
DOI:10.1021 / ja00886a029
这些论文教授j·c·马丁(伊利诺斯)在他职业生涯的早期,他做这工作之前最著名(研究“hypervalent”分子,包括开发的“Dess-Martin Periodinane”)。 - Chain-Carrying物种的身份与N-Bromosuccinimide:溴化的选择性取代N-Bromosuccinimides对甲苯代替
r·e·皮尔森和j·c·马丁
美国化学学会杂志》上1963年,85年(20),3142 - 3146
DOI:10.1021 / ja00903a021 - N-bromosuccinimide。的机制烯丙基溴化和相关的反应
j . h . Incremona马丁和詹姆斯·卡伦
美国化学学会杂志》上1970年,92年(3),627 - 634
DOI:10.1021 / ja00706a034 - 作为一个连锁航母Succinimidyl激进。的机制烯丙基溴化
j . c .天,m·j·林德斯特伦和p . s . Skell
美国化学学会杂志》上1974年,96年(17),5616 - 5617
DOI:10.1021 / ja00824a074 - 激进的溴化环己烯亚兰的溴:添加和替换
d . w·麦克米伦和John b . Grutzner
《有机化学》杂志上1994年,59(16),4516 - 4528
DOI:10.1021 / jo00095a029
介绍小心动力学研究表明,Br的低浓度2(如提供的不洁净的国家统计局在极地)将支持激进的替换加成反应。 - 二溴化o-XYLYLENE
艾米丽·f·m·斯蒂芬森
Org。Synth。34卷,p。100 (1954)
DOI:10.15227 / orgsyn.034.0100
一个可靠的过程与溴苄基的溴化2在有机合成。 - 溴化萘满。短而有效的合成1,4-Dibromonaphthalene
奥斯曼Cakmak,伊斯梅尔Kahveci,易卜拉欣DemirtaşTuncer Hokelek和基思·史密斯
捷克。化学。Commun。2000年,65年,1791 - 1804
DOI:10.1135 / cccc20001791
一个方便的合成1,4-dibromonaphthalene从萘满,通过苄基的溴化。苄基的氧化:
很多策略存在苄基的氧化,包括使用KMnO集中解决方案4或铬酸。 - 芳香族化合物的氧化动力学研究了高锰酸钾。n -承运和iso-Propylbenzene一部分
c . f .天沟和j·w·Ladbury
j .化学。Soc。1955年,4186 - 4190
DOI:10.1039 / JR9550004186 - 哌啶衍生物x PHENYLPIPERIDYLCARBINOLS
肯尼斯·e·克鲁克和s·m·McElvain
美国化学学会杂志》上1930年,52(10)4006 - 4011
DOI:1021 / ja01373a035
如果有另一个取代基苄基的位置,然后用给氧化酮而不是羧酸。 - 异构高锰酸盐氧化反应。7。脂肪族侧链的氧化
Nazih a . Noureldin东源赵,唐纳德·g·李
《有机化学》杂志上1997年,62年(25),8767 - 8772
DOI:1021 / jo971168e
试剂可以吸附到固体支持使反应更容易进行,减少浪费。在这种情况下,通过使KMnO4试剂异构、反应性略有变化,这可以利用一些chemoselective氧化反应。很多其他的试剂可以用于苄基的氧化,这是一个选择: - 选择性氧化与IBX碳毗邻芳香系统
k . c . Nicolaou菲尔·s . Baran和Yong-Li钟
美国化学学会杂志》上2001年,123年(13),3183 - 3185
DOI:10.1021 / ja004218x
早期的论文(现在的明星总合成的)教授Phil Baran(斯克里普斯研究所的拉霍亚,CA)当他还是一个博士生在Nicolaou教授的小组。它使用IBX (hypervalent我(V)试剂)苄基的氧化反应,通过激进的发生机制。这是一个有用的反应与广泛的底物范围,以25例子。 - 通过碳氢键直接和选择性苄基的氧化Alkylarenes抽象使用碱金属陈词滥调
Katsuhiko本森山,也陆陆续续Takemura, Hideo多哥
有机的信2012年,14(9),2414 - 2417
DOI:10.1021 / ol300853z
这对苄基的使用硫酸氢钾作为终端氧化剂氧化。 - C−H合成苄基的醇的氧化
Lalita Tanwar乔纳斯波̈rgel,托拜厄斯里特
j。化学。Soc。2019年,141年,17983 - 17988
DOI:10.1021 / jacs.9b09496
它使用mesyl过氧化氢作为氧化剂的选择性氧化醇的苄基的位置。的苄甲磺酸形成,可水解酒精。 - 电化学苄基的碳氢键的氧化
詹森•a .马克安东尼•Durgham斯泰西罗沃利亲眼见识,刘魏
化学。Commun。2019年,55,937 - 940
DOI:10.1039 / C8CC08768G
苄基的通过电化学氧化也可以影响。 - 烯丙基的和亚氯酸钠苄基的氧化反应
塞缪尔·m·西尔维斯特豪尔赫·a·r·萨尔瓦多
四面体2007年,63年(11),2439 - 2445
DOI:10.1016 / j.tet.2007.01.012
NaClO2不贵,也可以用作氧化剂。
你好,詹姆斯,
我有一个评价测验中的最后一个问题。你提到的最佳合成路线m-nitrobenzoic酸是第二个。可以提供相对FC烷基化甚至electron-poor nitrobenzen(例如benzen相比)?因为,一些教科书(如如McMurry)提到,(一般来说)不执行这种类型的反应。谢谢你的评价。
过去的路线是错误的,因为你可以´t得到丙酯/异丙benzen使用氯甲烷。
与碳发生了什么?我在想,如果我们把一个二甲基萘满的替代版本的苄基的职位都H的被甲基取代,然后氧化吗?这个位置会影响反应,但其他位置会变成一个羧酸,和我想象链会解开。但最后的链是什么?
嗨罗伯特-分子将有两个羧酸,苄基的位置和一个末端的链(2个碳/碳从dimethylated苄基的碳)。
绝对有价值的话题讨论。谢谢你,詹姆斯。虽然两个笔记。为了公平,我必须注意,当苄基的氢不可用,激进与国家统计局brominatiln仍然很可能,不会给你替换苄基的位置,但仍然反应发生,所以它可能会误导说不能完全没有反应。当它完成t-Bu-Ph,这也给了一个激进的重组,事实上确实产生苄基的激进。
同时,我相信你在你之前的帖子提到FC烷基化往往会产生多种烷基化产品,通常不是一个好的反应实际合成的目的,但你使用它是你合成的第一步。啧?
谢谢维克多。
1)我之前没有意识到neophyl激进的重组。谢谢你!
2)有罪指控re: FC烷基化。好点。
我想知道是否有可能获得一个好的收益率莫诺苯烷基化产品通过使用大量过剩?教授声称,至少在一个类中。在这种情况下,反应可能正常工作等简单的合成甲苯。
但绝大多数教授将接受monalkylation甲苯。否则你需要编写“蒸馏获得的碳氢化合物通过水力压裂”。或“从奥尔德里奇购买”。
或者别的什么尴尬的甲酰化/减少或羧化作用/减少。或有机金属转换,一些学生已经学会了。
我读过的激进的溴化主要碳并不是那么有效对应的氯化。Br2由国家统计局的浓度相当低,这导致更低浓度的Br激进,是国家统计局溴化主碳吗?例如在叔丁基苯等化合物,乙烷,& neo-pentane吗?
像往常一样,优秀的文章。不过,需要一些小的修正:
——“这是是产品”(在“苄基的溴化”);
——计划在“什么时候不工作?”a 3 is missing in the structure (CH instead of CH3);
——“为什么烯丙基溴化可能是有用的呢?”——它应该读作“苄基的溴化”;
——“苄基的氧化与KMnO4(或H2CrO4)”——它应该是“苄基的氧化”(好吧,这是一个很小的一个);
——在这个标题:“氧化酒精/酮”——它应该读“aldehide /酮”。
非常感谢。