烯烃的反应
卤化烯烃和Halohydrin形成
最后更新:2023年8月25日|
溴化、氯化、Halohydrin形成烯烃
- 烯烃进行卤化当处理Cl2、溴2我和(通常)2给附近的二卤化物
- 这些反应是立体选择并给反添加产品
- 通过循环的机制halonium离子经历背后攻击在碳亲核试剂给反添加产品。
- 当水或醇作为溶剂,halohydrins或haloethers可以形成。这些也给的产品反加法。
- 与不对称halonium离子切断债券往往会形成最取代碳(“马氏”区域选择性)。
- 二卤化物可以接受取消给炔烃;halohydrins可以用来形成环氧化合物。
- 总的来说,这些反应有类似的机制来的oxymercuration和开放的环氧化合物在酸性条件下(见文章:烯烃加成模式# 2——“三元环”途径]
表的内容
1。卤化烯烃的
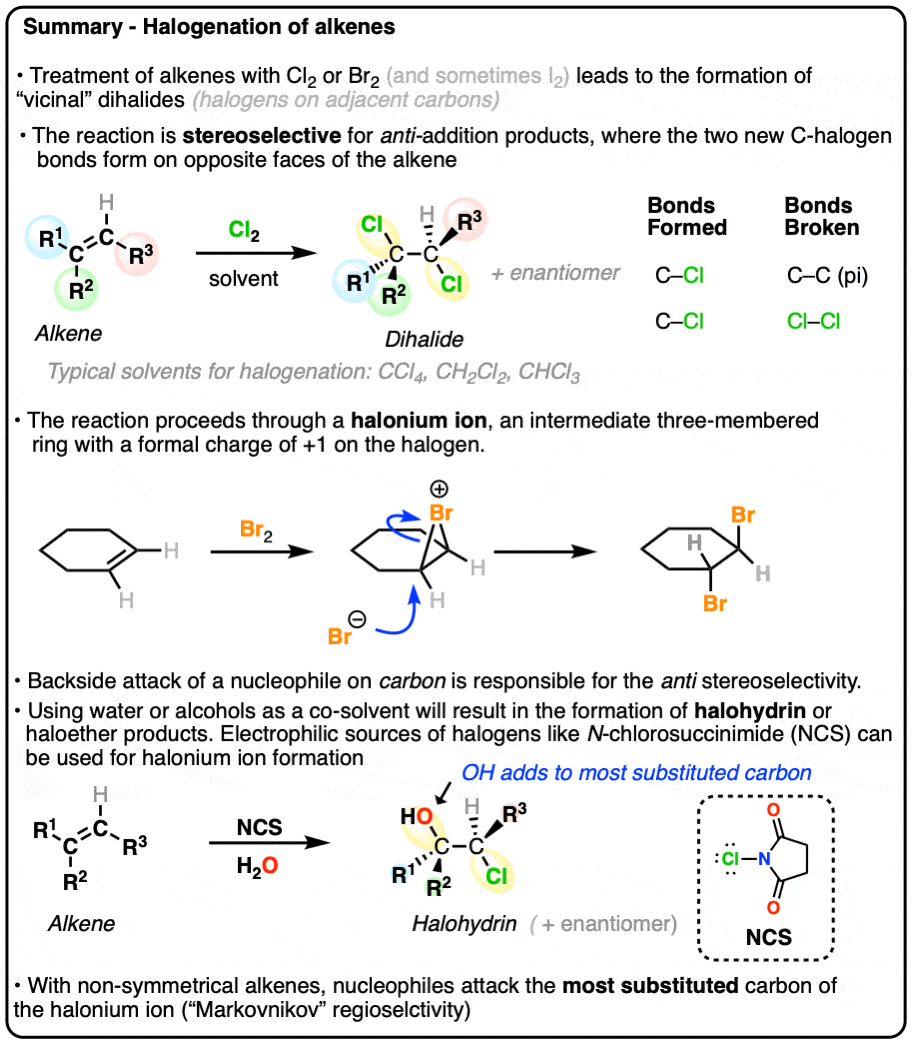
当烯烃(也称为烯烃)处理溴(Br2)或氯(Cl2)在惰性溶剂中注1CCl四氯化碳(等)4)或二氯甲烷(CH2Cl2),它们转化成二卤化物(具体来说,“本地的”二卤化物C-halogen债券以来相邻的碳原子)。
这个反应结果的形成两个新的C-halogen债券和打破了碳碳π键以及halogen-halogen债券。这两个carbon-halogen债券增加相反的烯烃。
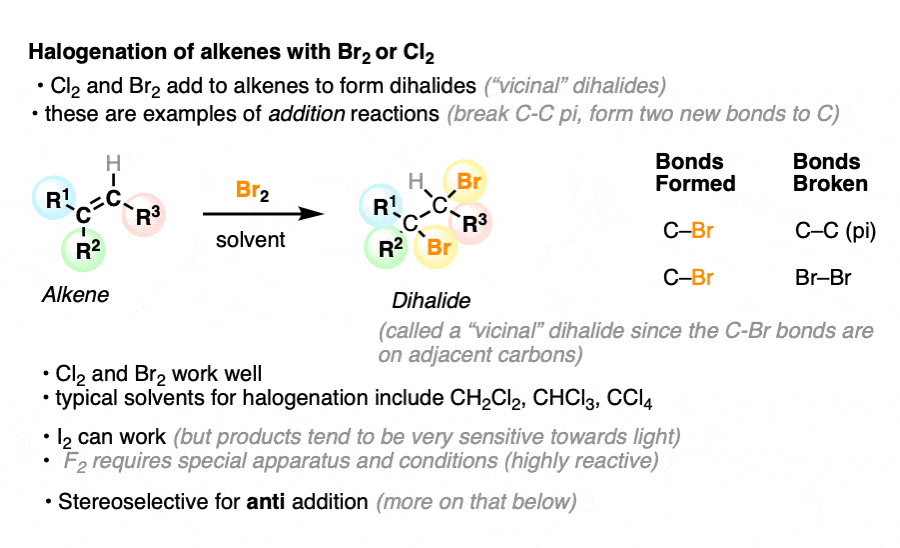
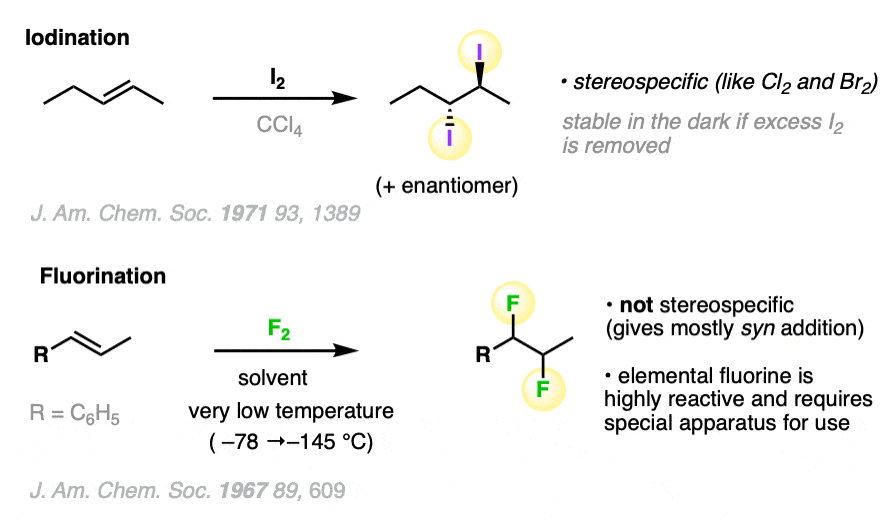
它还可以为碘(我工作2),但往往是可逆的,向光di-iodide产品往往是不稳定的。氟(F2)是一个贪婪的野兽,它需要特殊的设备,这意味着我们不会进一步讨论它。(注2]
这个反应是一个共同的基础测试中使用的教学实验室溴水测试。
溴(Br分子2)有一个橙色的特征。在烯烃的存在,橙色消失,表明发生了反应。
通过GIPHY。原始资料来源:@FranklyChemistry (Youtube)
请注意,Br2不通常与苯反应(C6H6)或含芳环分子,即使这些似乎乍一看可能类似于烯烃。更说在后面的章节。(看到基于“增大化现实”技术本文:卤化苯]
2。卤化是立体选择反添加产品
卤化烯烃的一个例子立体选择的反应。
Br的反应2,Cl2和其他卤素烯属烃导致的产品反——添加。一个典型的例子是环己烯的溴化(下图),这给了反式1,2-dibromocyclohexane作为外消旋混合物。没有顺式1,2-dibromocyclohexane就形成了。
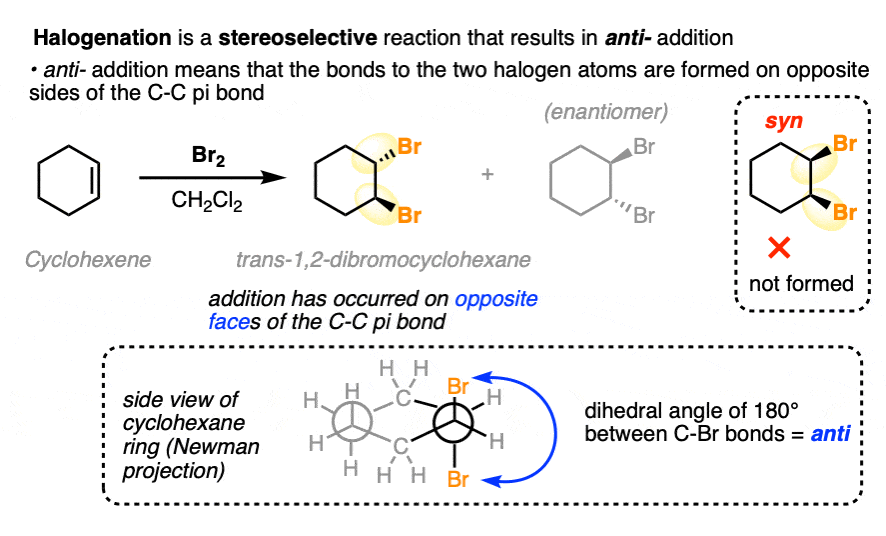
条款syn- - -反——指的是两者之间的二面角观察C-halogen债券直接当我们沿着碳碳键。我们说这是反——因为这两者之间的二面角C-halogen债券是180°。(看到,乙烷的交叉与重叠构象]
虽然可以理解时使用“反式”这个词指的是这个方向(和大多数人会知道你的意思!)我们通常储备“反式”指情况两组相反脸上的多重键或小环顺反异构(即)。“反”一词广泛得多,因为它指的是两组之间的相对取向,所定义的二面角(180°anti 0°syn)。
当画的产品反——除了一个烯烃,画出两个新的C-halogen共同债券显然在页面的平面的二面角180°。
专家提示:确保你保持相对的方向组的烯烃相同的当绘制产品:
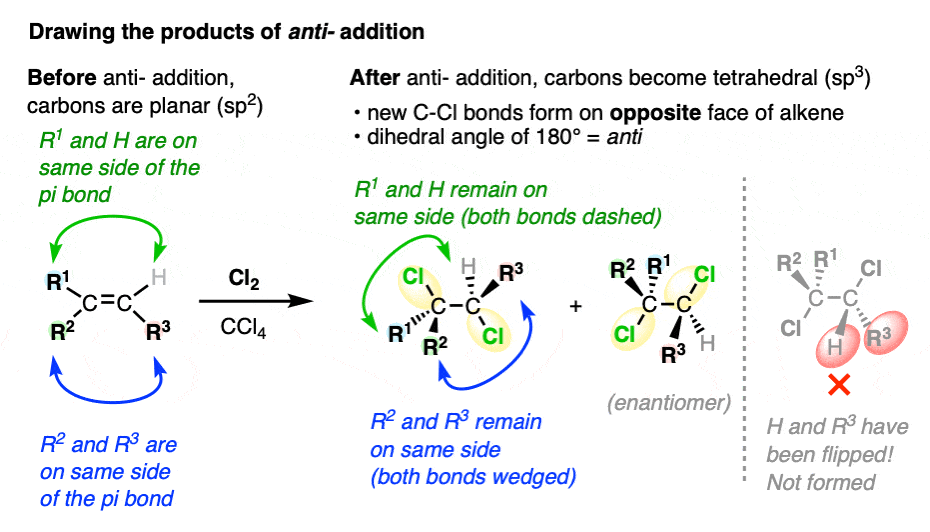
虽然这些产品往往是吸引的C-halogen债券飞机保持警惕,不会总是这样。
毕竟,一旦碳碳π键坏了,免费的关于碳碳单键的旋转可能。这意味着可以画构象异构体一个反——除了产品两C-halogen债券是在同一个碳碳单键。
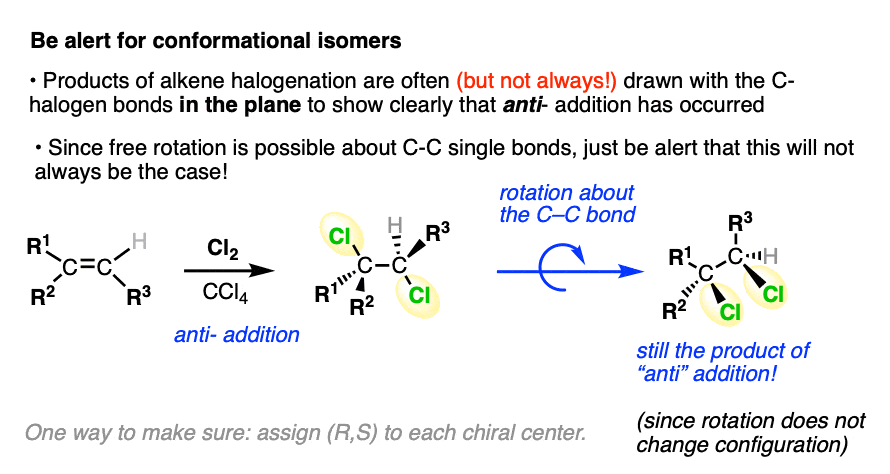
这并不突然让它syn除了产品,然而,由于旋转不改变他们的债券配置。再多的债券旋转将转换一个手性中心(年代)配置成(R)!
有时你可能需要工作向后(使用键旋转)的产品找出烯烃原料。这可能有点令人困惑。在怀疑你做了债券正确旋转,它可以帮助确定(R) / (S),以确保你没有任何立体意外翻转。
一个典型的例子显示卤化的立体选择性独联体- - -反式- 2 -丁烯。
- 当独联体- 2 -丁烯经过溴化,产品的外消旋混合物(S, S) 2, 3-dibromobutane (R, R) 2, 3-dibromobutane。
- 当反式- 2 -丁烯经过溴化,产品是(2 s, 3 r) 2, 3-dibromobutane。这个分子有两个手性中心,但由于存在一个非手性分子整体内部镜平面。这类分子被称为内消旋化合物。(见文章:内消旋的陷阱)
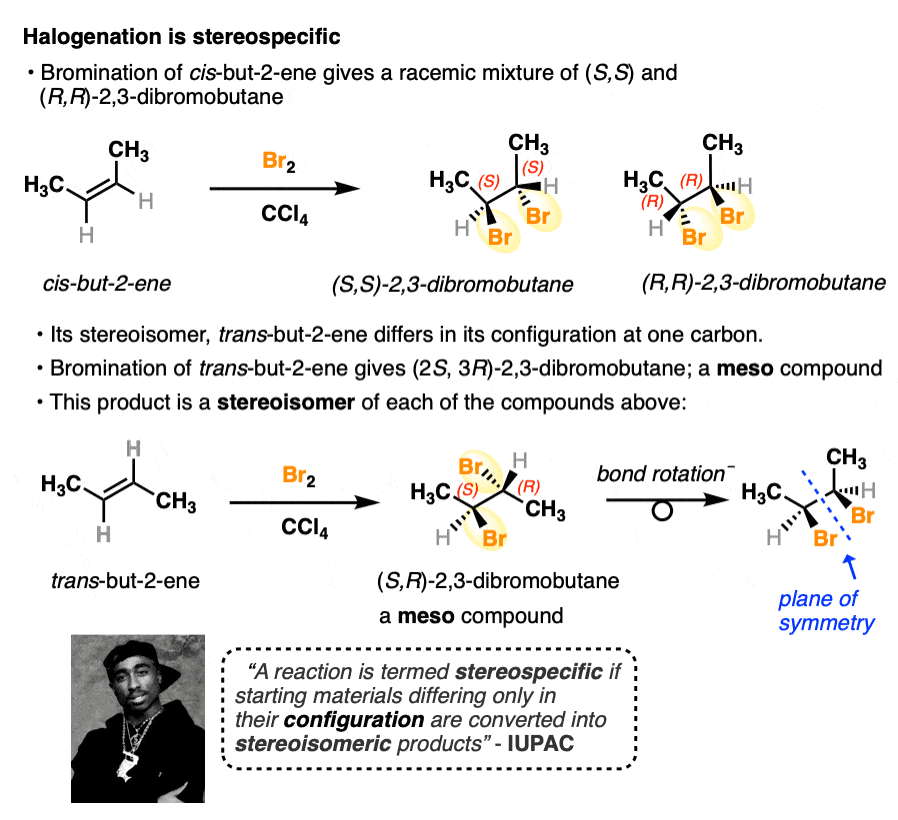
2 -丁烯的一个立体异构体产生一组立体异构体产品;2 -丁烯的其他立体异构体产生立体异构的产品。这两个反应之间没有交叉。
这符合IUPAC的定义立体定向的反应。其他几个立体定向反应烯烃的例子包括硼氢化反应、dihydroxylation,环氧化作用等等。
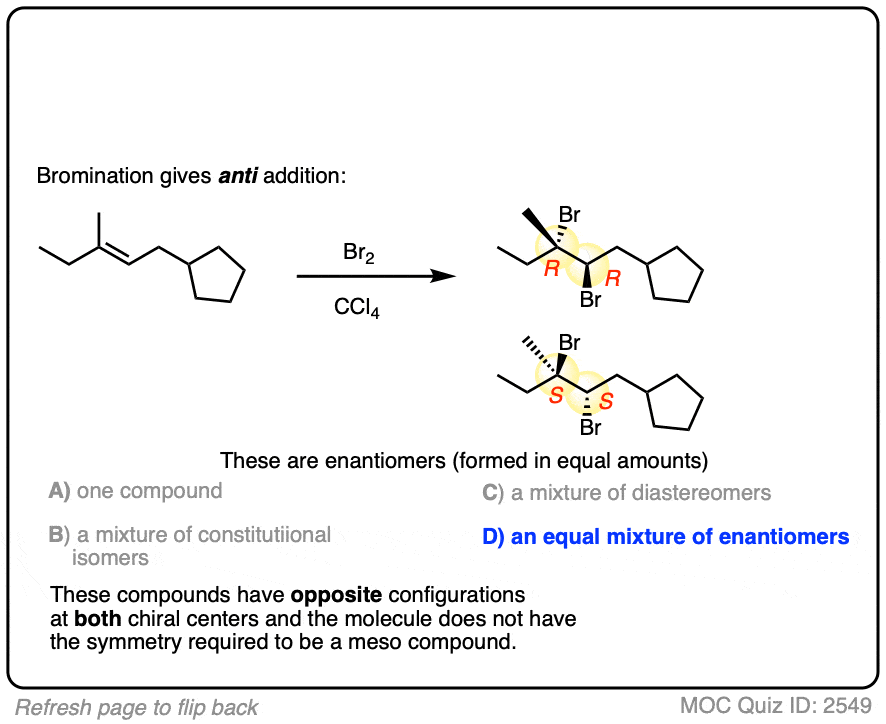
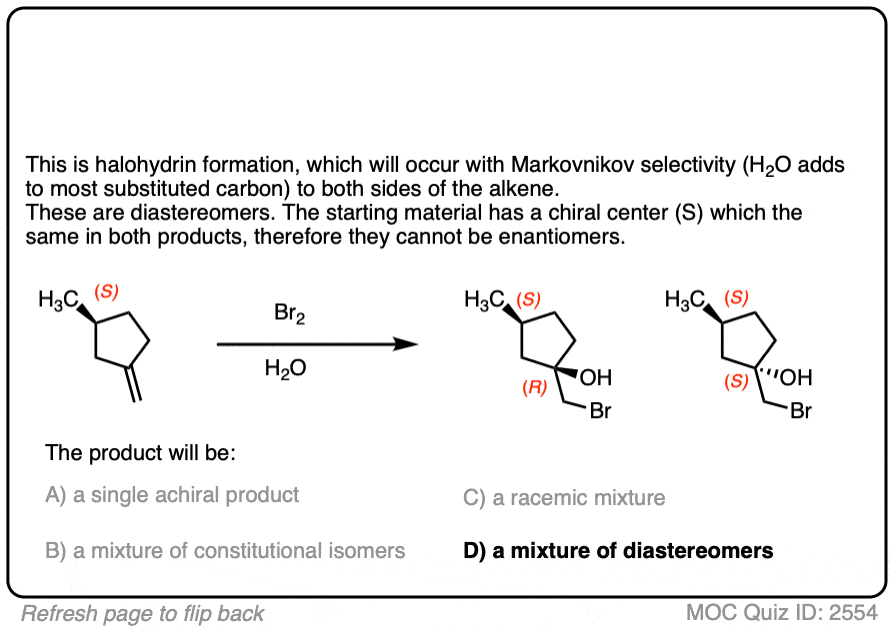
现在对于一些练习。看看你是否能画出下列反应的产品,确定产品:
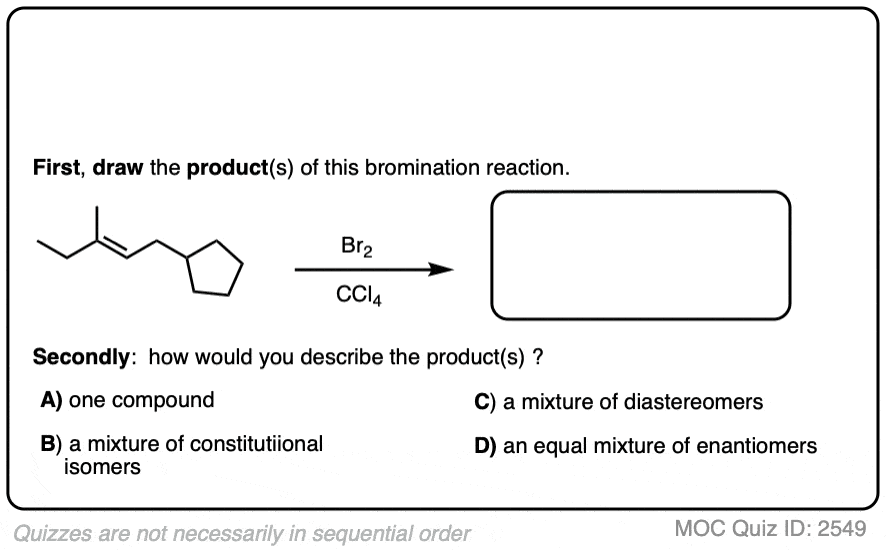 点击翻转
点击翻转
同样重要的是能够向后工作!你能确定这个卤化反应的起始物料吗?
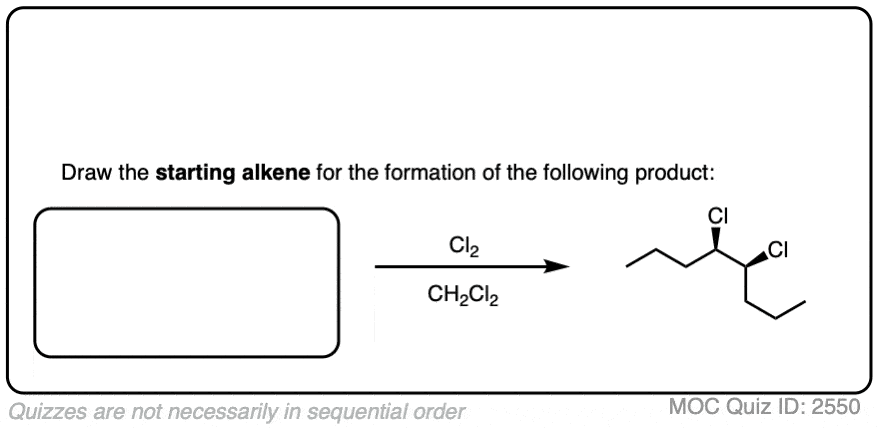 点击翻转
点击翻转
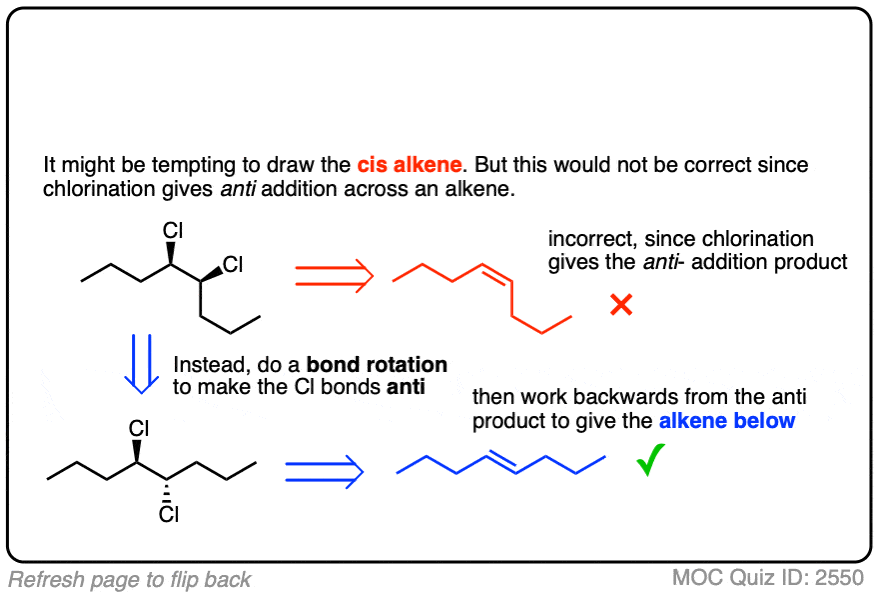
3所示。Halonium离子
好的。所以卤化烯烃实际上是如何工作的呢?
一个最初的想法是,他们可能继续通过免费碳正离子中间体,如盐酸的烯烃。(见文章-马氏的HCl烯烃]。
一个有趣的测试这个理论来自下面的烯烃卤化。独联体di -t-butylethylene有很多空间应变(9.3千卡每摩尔),由于这两个笨重t -丁组互相碰撞。(这在技术上被称为“a - 1、2株”)
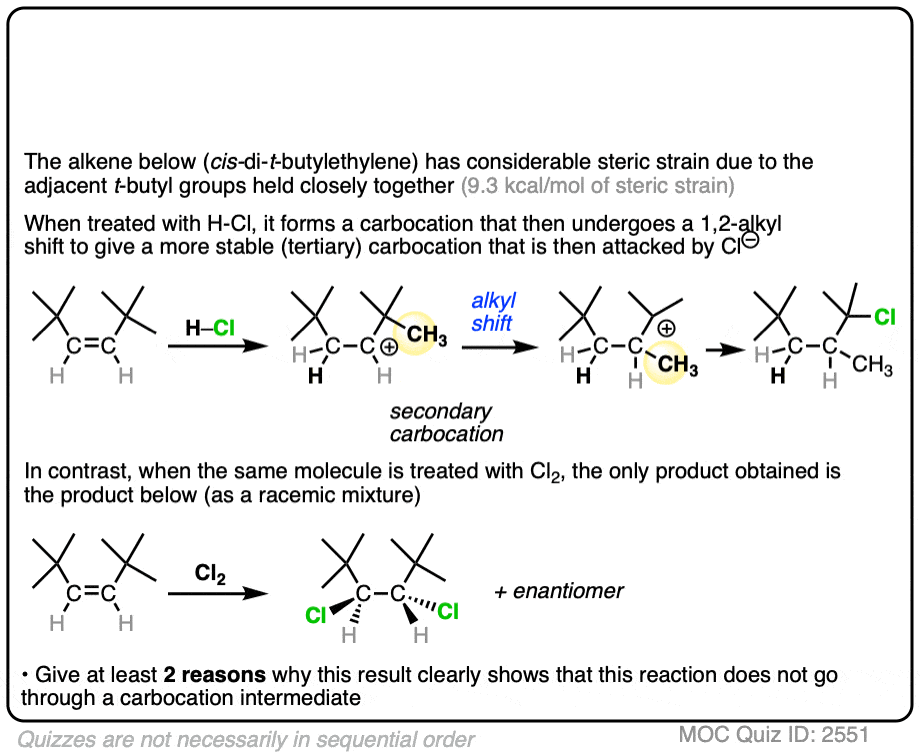 点击翻转
点击翻转
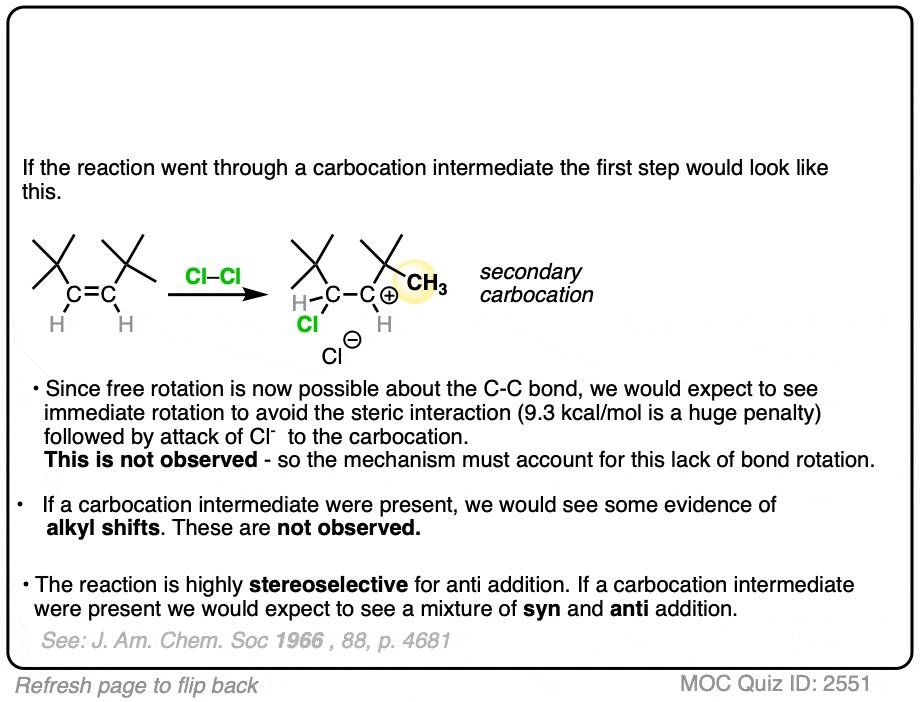
如果卤化经历了自由碳正离子,旋转就有可能在碳碳键。因此,我们期望看到的t丁组抛在来缓解压力。
发现相反的是这个反应也是吗高度立体定向,就像的反应独联体——2-butene。此外,没有烷基或氢化物转移像我们所期望的自由碳正离子。
很明显,的东西负责这个反应的立体选择性。它是什么?
最好的建议我们对正在发生的事情是形成一个循环halonium离子,这是一个三人环轴承在卤素积极的形式电荷。“Halonium离子”是当一个卤素的通用术语作为桥;我们还可以使用“chloronium”、“bromonium”或“碘鎓”指特定的卤素。
halonium arrow-pushing机制形成的一个例子,显示所有的债券形成和破碎的是这样的:
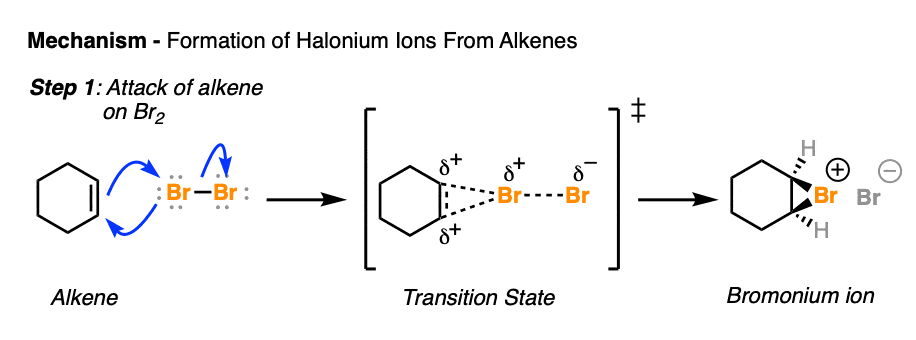
请注意,许多教科书只会显示两个箭头,像这样(徘徊)或点击这个链接。
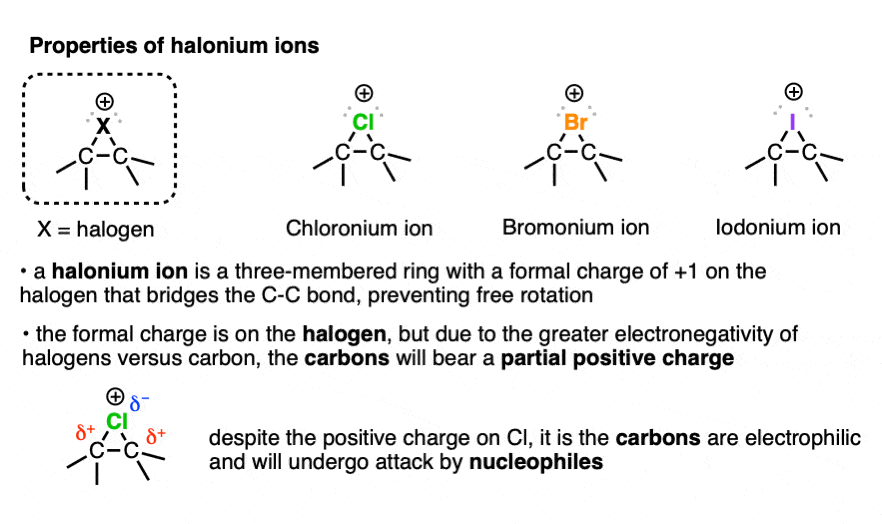
尽管halonium卤素离子具有积极的形式电荷,它实际上是碳原子这是亲电。这是更容易认识到如果你还记得,卤素电负性大于碳,所以carbon-halogen债券将会对碳部分积极的特性。这就是为什么它被称为,“正式的”。(见文章:如何计算形式电荷]
在对称halonium离子,carbon-halogen债券的长度相等,将部分正电荷在碳。
x射线晶体结构稳定的bromonium和碘鎓离子是由布朗&同事前阵子(注3]
4所示。卤化烯烃的机制
所以第一步的卤化烯烃是一个halonium离子的形成。
在卤化的第二步,卤化物离子攻击的碳背后C-halogen债券,导致形成C-halogen C-halogen破损。
这关键一步占的高立体选择性的卤化反产品。
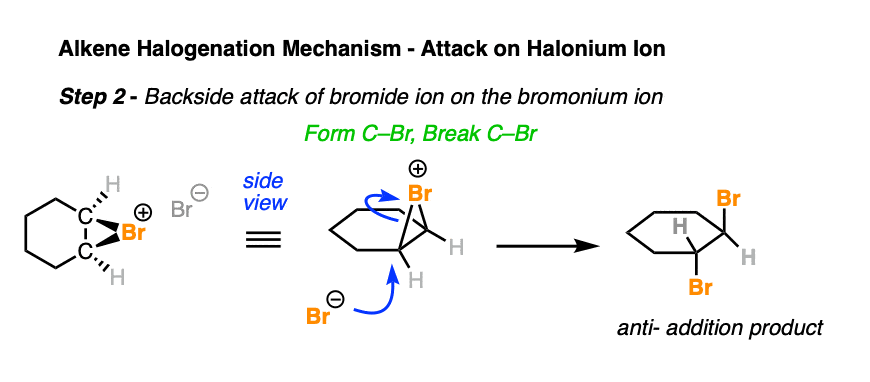
注意,形成的对映体(没有显示)也在这里。
这类似于背后袭击SN2机制(看到article -的年代N2机制]在一个孤对亲核试剂与离去基团的σ*轨道。然而,这一步并不具有相同的位阻的SN2反应敏感,正如我们即将看到的。
5。Halohydrin形成——水和醇
当溴化烯烃进行的水(通常是作为一个co-solvent),halohydrin形成的产品。
halohydrin是分子包含c哦和C-halogen债券在相邻的碳原子。
反应也通过halonium离子中间。与卤化一样,反除了产品形成。
卤化和halohydrin形成的区别之一是,这两个新σ键形成不同的原子(氧气和卤素)。这给上升到宪法同分异构体的混合物形成的可能性。当一个宪法异构体占主导地位时,我们说的反应特定选择的。
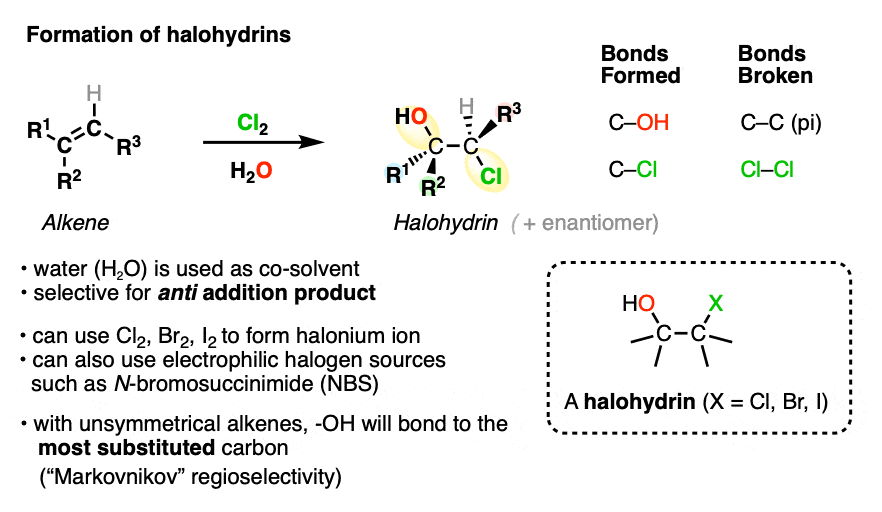
Halohydrins用于环氧化合物的形成。更多信息,见本文环氧化合物的形成
它是发现halohydrin形成区有选择性的形成的同分异构体的债券形式的哦更多的代替碳。这类似于观察到的模式除了HX的烯烃的反应,这被称为“马氏”区域选择性。(看到post -马氏规则的像)
这是为什么呢?毕竟,不应该取代碳位阻更敏感?
实验告诉我们,(相比之下N2)亲核试剂可以攻击halonium的叔碳离子很好。换句话说,位阻不是一个重要因素。
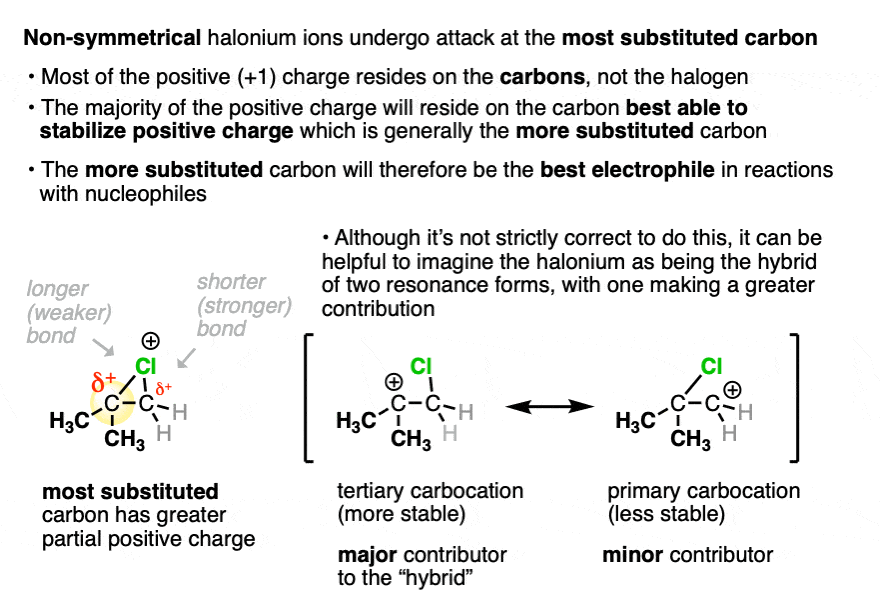
让我们仔细看看一个非对称halonium离子的结构。
正如前面谈到的,尽管有一个+ 1的形式电荷卤素,实际上碳原子熊正电荷密度由于电负性越大的卤素(> 3)与碳(2.5)。并在一定程度上,这些碳熊正电荷密度,亲电。
这两个碳的最能稳定正电荷吗?取代碳越多,一般。(以及任何碳能够delocalizing正电荷通过共振)。(见文章-碳正离子的稳定性]
不是正确的画共振形成单键打破,所以捏住你的鼻子一下:
它可以帮助想象halonium离子的“共振混合”两种不同的碳正离子。更多的共振形成碳正离子的取代碳将使更大贡献我们的“混合”。
有更多的正电荷密度,它会更亲电,因此会更容易接受与亲核试剂反应。
另一个问题是,“为什么水攻击halonium离子而不是卤离子?不是卤离子更好的亲核试剂?
是的,卤化物离子比水更好的亲核试剂。然而,回想一下,反应速率将不仅取决于亲核性也浓度。由于水通常是用作溶剂(或co-solvent)在这里,它将有一个大大更高的浓度。
所以在某种意义上我们“压倒性”halonium离子浓度更高的更糟的是亲核试剂。
6。Halohydrin形成的机制
与卤化,halohydrin形成的第一步是创建一个halonium离子。
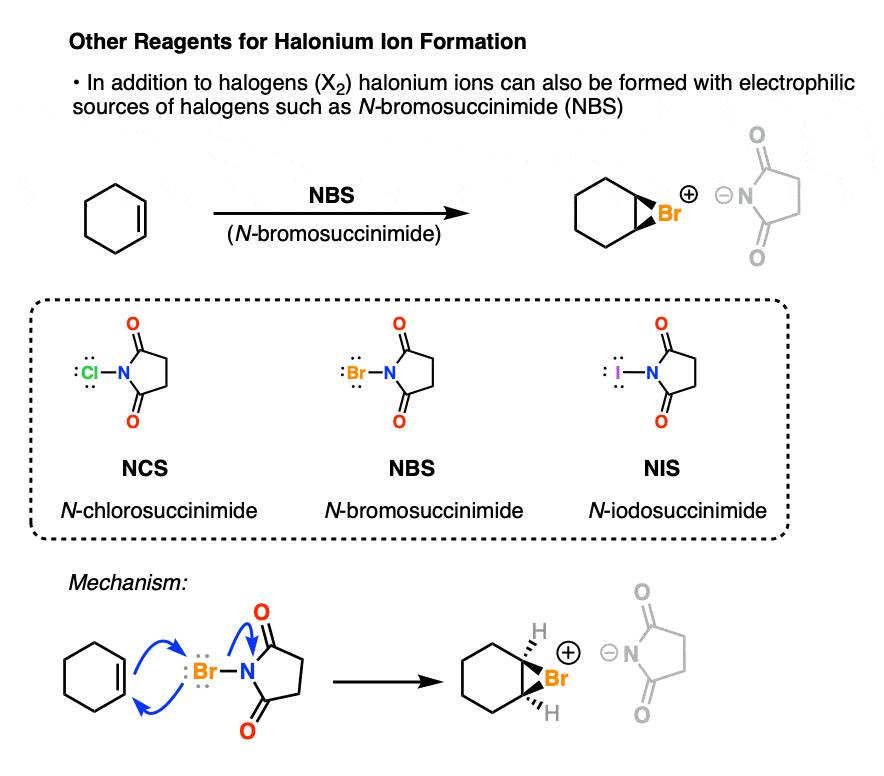
除了Cl2、溴2,我2,这也可以用阳性卤素如N-bromosuccinimide来源(国家统计局)。(见文章-N-Bromosuccinimide]
halonium离子形成后,下一步是攻击halonium离子H2啊,在取代碳越多。
为什么H2这样做,而不是抗衡离子吗?如果是作为溶剂只是数量卤离子的浓度。(注意4]
这导致反产品可以deprotonated(如溶剂)中性halohydrin。
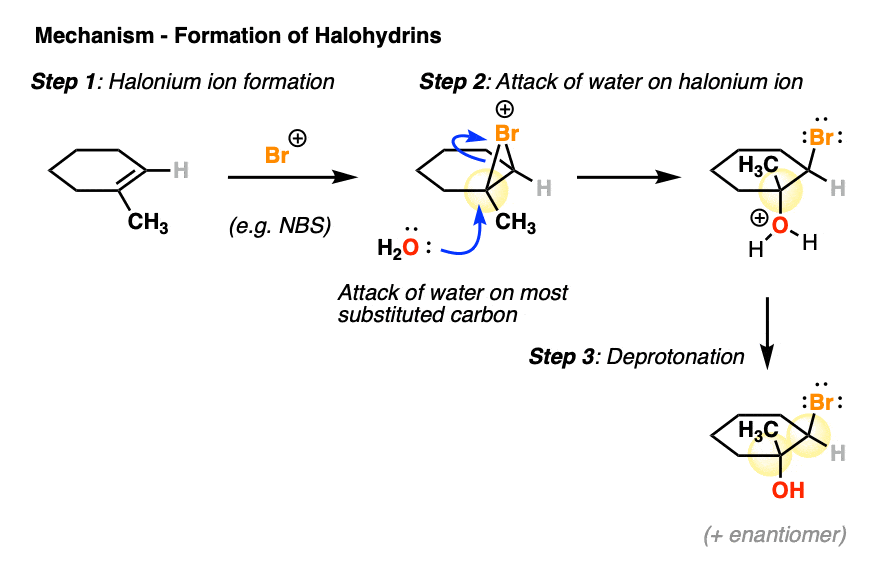
(注意,就像一个扁平的硬币,可以登陆“正面”或“反面”平等的可能性,溴可以“土地”的烯烃——这将导致对映体]。
7所示。Haloethers
类似地,如果醇作为溶剂,haloethers可能形式。形成haloethers halohydrins的通过一个相同的机制。
看看你是否能预测下列反应的产物。
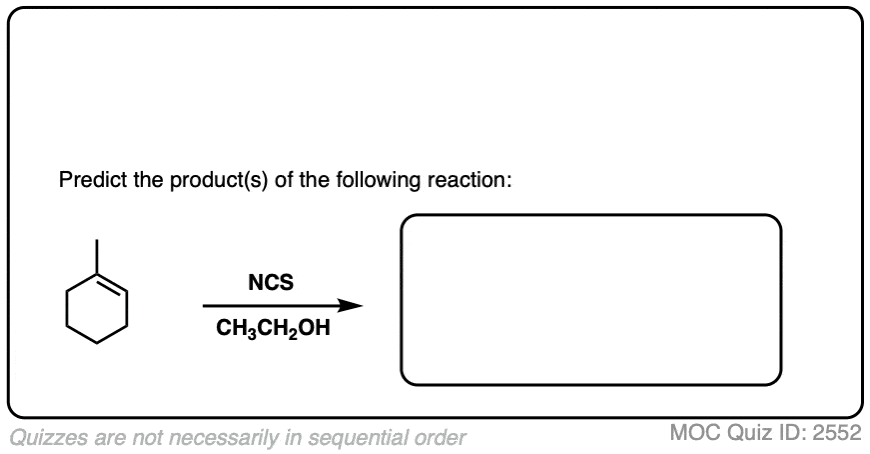 点击翻转
点击翻转
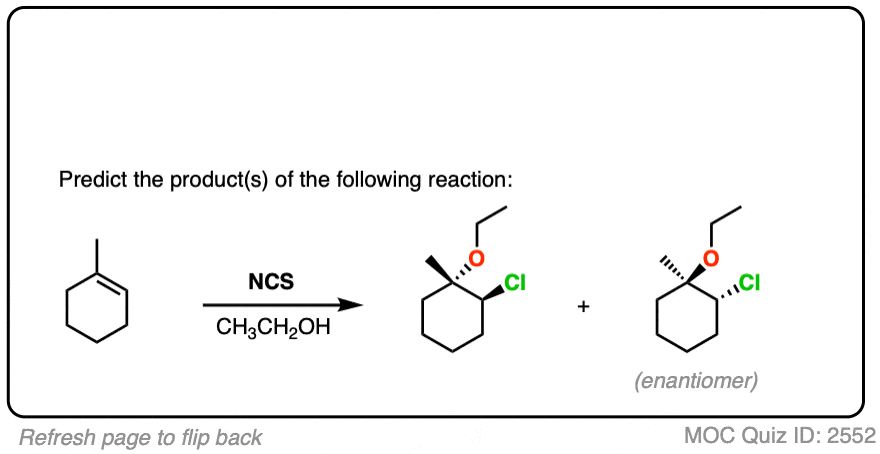
一个有趣的皱纹haloether形成的可能性分子内的反应。
例如,治疗这个烯烃与国家统计局(Br的来源+)导致新环的形成。
看看你是否能算出机制。
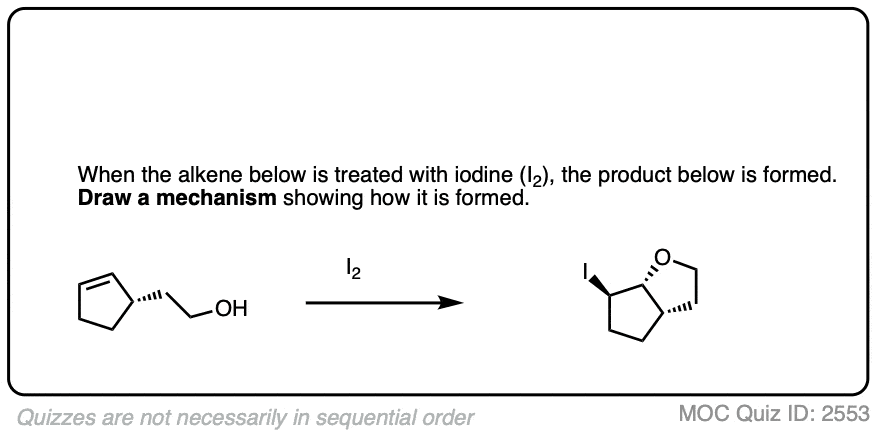 点击翻转
点击翻转
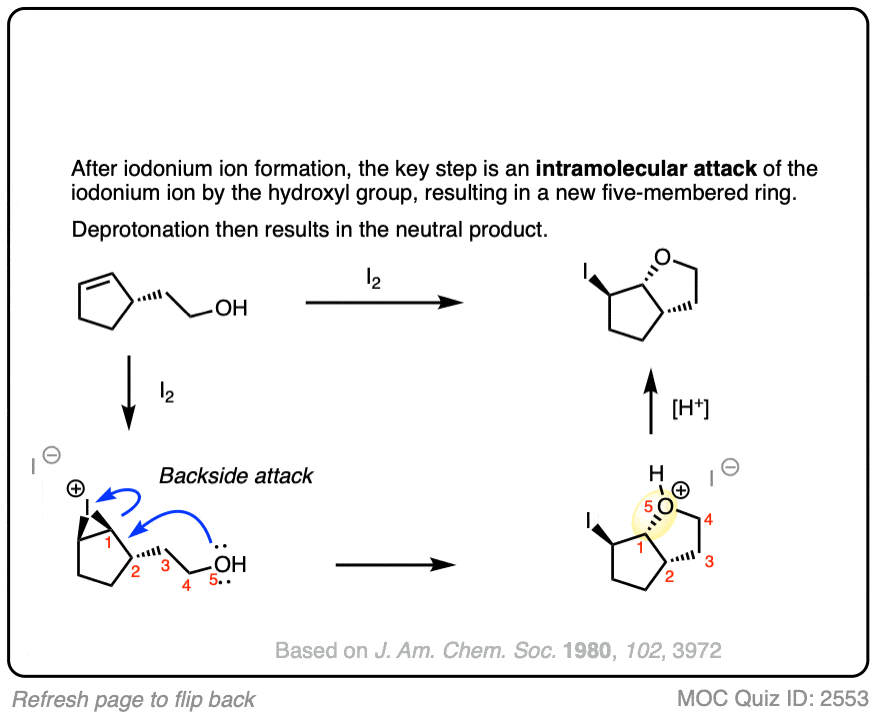
一如既往,留心观察分子内反应,因为它们让伟大的试题。
8。一些应用程序的卤化反应
值得了解的这些反应可以应用在今后的课程中。
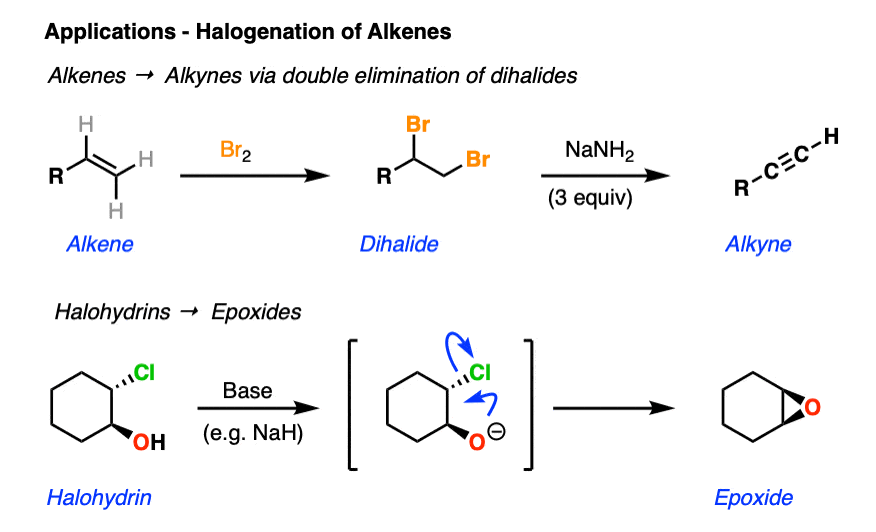
可以转化为炔烃独联体与卤素-dihaloalkenes通过治疗(见文章:卤化的炔烃)
没有直接将烯烃转化为炔,但他们可以通过组建一个间接转化为炔烃二卤化物双消除给炔紧随其后。(见文章:烯烃通过消除炔烃的反应)
(值得注意:溴化烯烃的技术上是一个氧化反应,因为每个碳从绑定到另一个碳(0)溴(1)。每一个碳的氧化态乙烯+ 2;二溴乙烷中的每个碳的氧化态+ 1。]
烯烃的环氧化合物可以形成两个步骤通过形成halohydrin跟着去质子化与强碱(如不)。中间醇盐执行一个分子内的SN2反应给一个新的三人环。(见文章:环氧化合物的形成)
9。总结
记得这个反应,记住这个机制!它与其他很多相似机制在这一章你会遇到烯烃,如:
- Oxymercuration (Markovnikov-selective,也经过一个循环,三人“mercurinium离子”中间)
- 的环氧化合物在酸性条件下(也经历最多添加取代碳)
此外,还可以应用于炔烃的反应。
的立体化学这个反应是经常测试。确保你能正确画反加法和另外的产品,可以从产品二卤化烯烃原料。
笔记
注1。”惰性溶剂“这仅仅意味着一个溶剂,不会与halonium离子反应的中间体。创新领导力4和CH2Cl2别管halonium离子;H2O、醇类和羧酸可以进行反应。
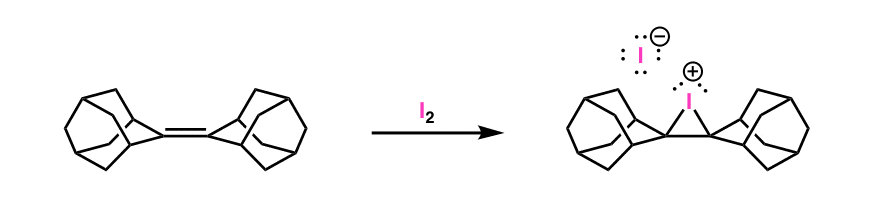
注3。Halonium离子不是虚构的化学实体。halonium离子从下面的反应特别稳定,因为它是非常困难的对碳原子的亲核试剂进攻的位阻:
R.S.布朗和同事成功地使用x射线衍射获取这个分子的晶体结构。这是碘鎓离子部分的结构:
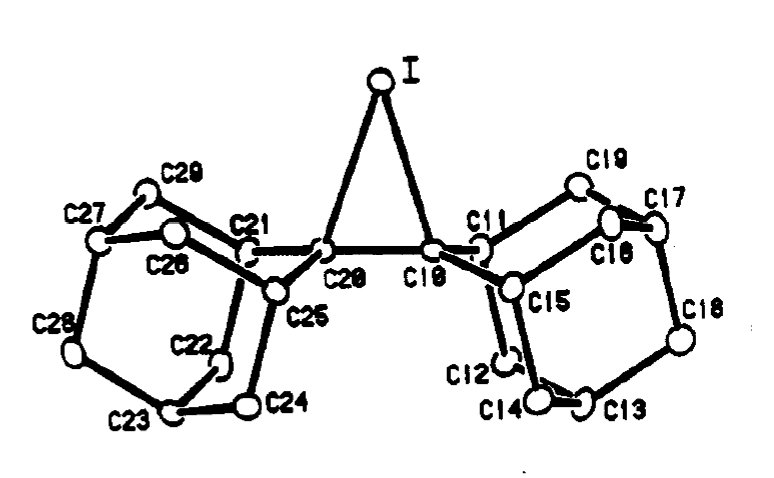
iodine-carbon债券长度是2.48埃,显著长于2.13埃一个典型的价值我键。
碳碳键的长度是1.49,这是典型的碳碳单键。
注4。有可能影响产品销售通过添加各种盐(如氯化钠,醋酸钠、溴化锂等)可能拦截halonium离子。在这里看到的(裁判)的研究。
注5。在某些情况下的高选择性反——产品可以分解。参见[裁判]。
注6。我们如何解决“的亲核试剂”和“亲电试剂的作用形成的bromonium离子?这并不容易,因为这需要对反应机理进行进一步的假设,可能不是基于确凿的证据。对冲的,这里有一个建议。:不考虑碳碳π和Br单,每个组件分解成分子轨道。碳碳π轨道可以作为亲核试剂,而碳碳π*作为亲电试剂;的Br-Brσ*轨道可以作为亲电试剂而Br孤对可以作为亲核试剂。
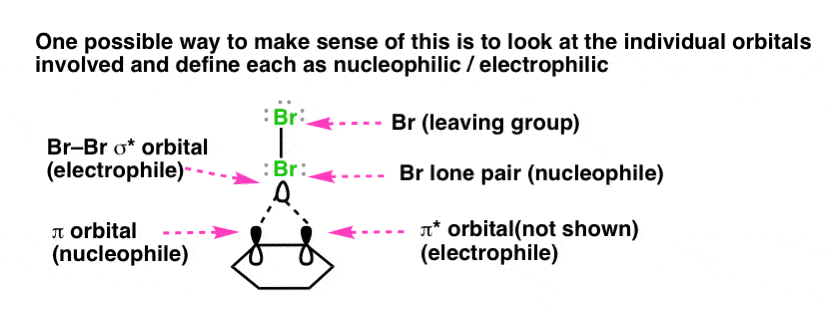
事实证明,计算表明烯烃的溴化溴2是更复杂的比我们可能最初假设。第一步是Br的协调2松散结合的烯烃结构称为“π情结”。π复杂然后分解给bromonium离子。轨道的适当治疗会因此没有严格的烯烃和Br2,但π轨道的复杂本身。
它变得更加复杂。在某些溶剂,它是积极的第二个Br分子2参与成键的Br -驱逐过程中(是的,一个“三分子的”机制)。更多细节在这里看到(j .物理化学,2007、111、13218)
测试你自己!
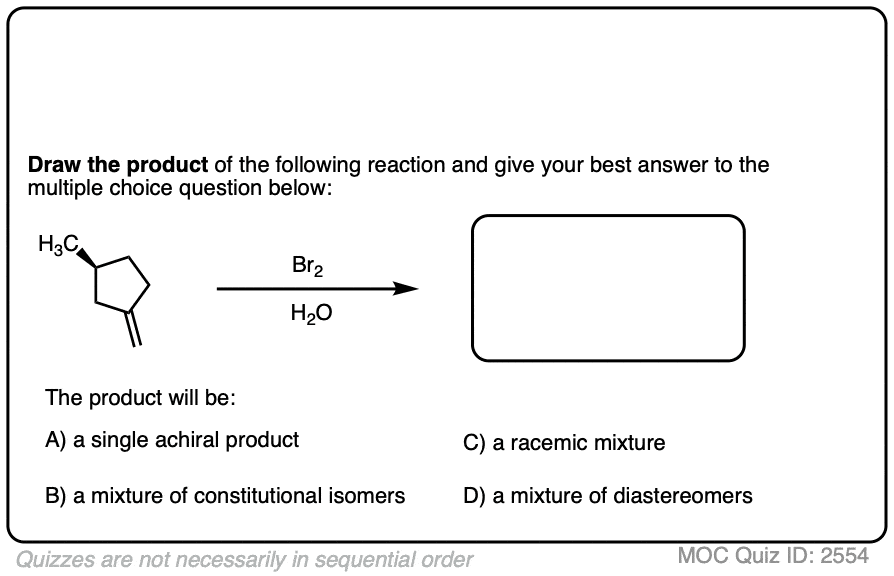 点击翻转
点击翻转
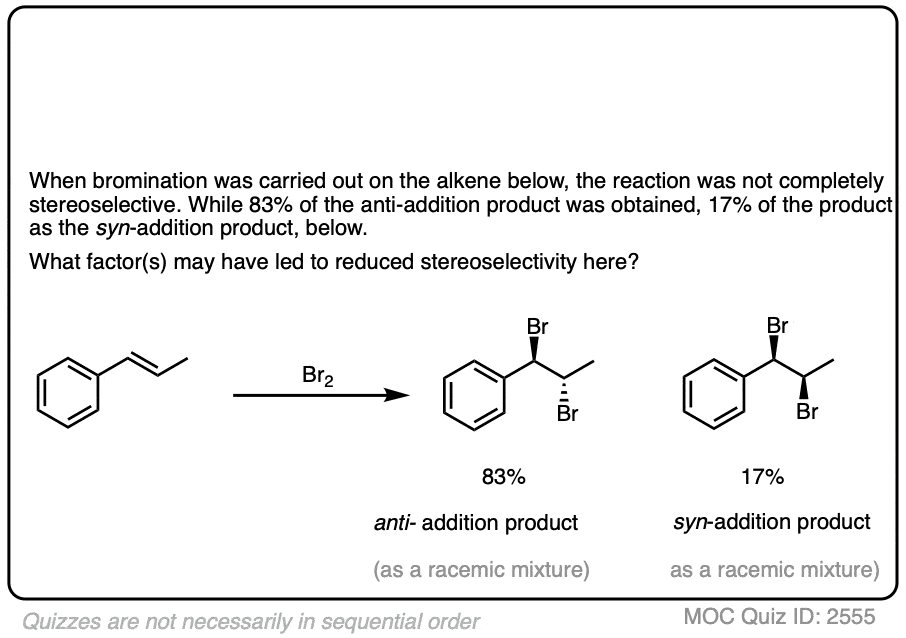 点击翻转
点击翻转
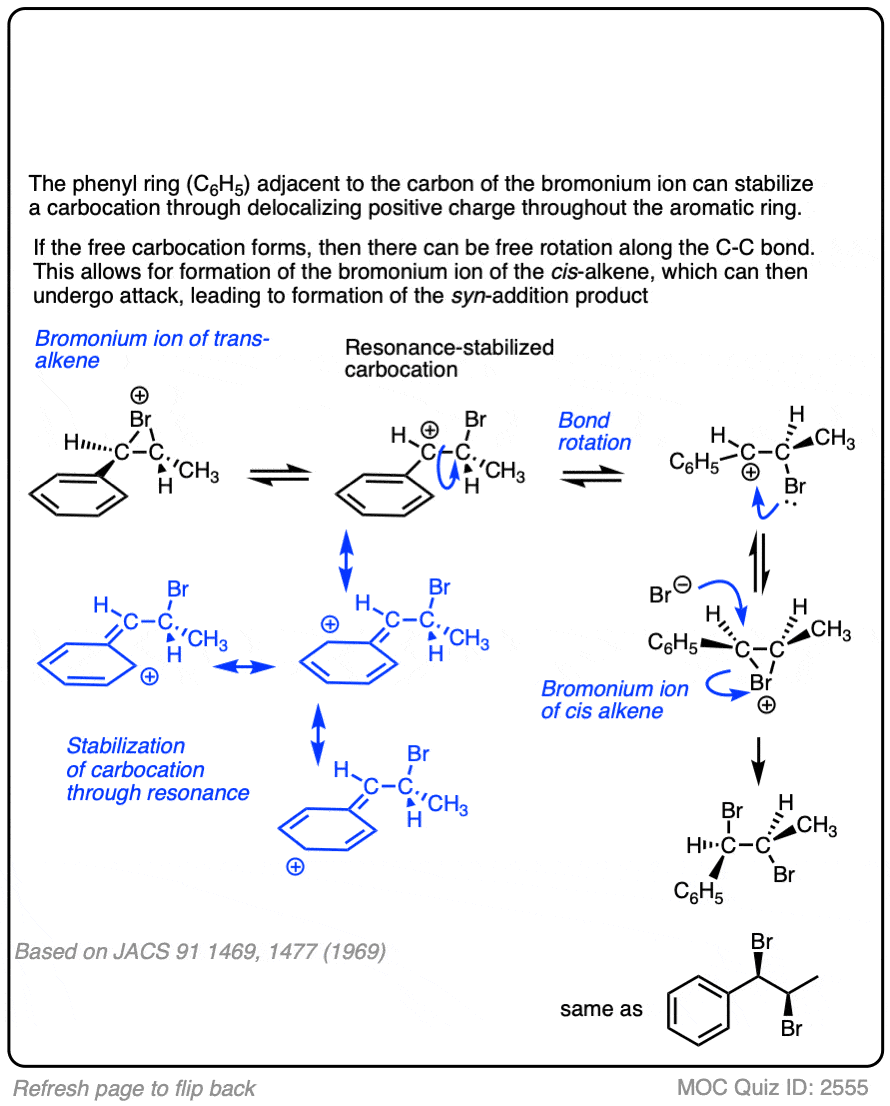
(高级)引用和进一步阅读
- 相对利率的溴化烯烃
哈罗德·s·戴维斯
美国化学学会杂志》上1928年,50(10)2769 - 2780
DOI:1021 / ja01397a031
一个早期的动力学研究在各种条件下烯烃溴化。 - 乙烯的卤化
欧文·罗伯茨和乔治·e·金博尔
美国化学学会杂志》上1937年,59(5),947 - 948
DOI:1021 / ja01284a507
最早的文献中描述的三元bromonium离子,会计的反这个反应的立体化学。 - 可逆的问题bromonium离子的形成过程中烯烃的亲电溴化。2。的晶体和分子结构bromonium adamantylideneadamantane离子
h . Slebocka-Tilk r . g .球,r·布朗斯坦
美国化学学会杂志》上1985年,107年(15),4504 - 4508
DOI:10.1021 / ja00301a021
本文描述了一个孤立的x射线晶体结构,稳定bromonium离子。这很重要,因为它证明了这些三元环的独到bromonium离子在烯烃的亲电添加溴。 - 阻碍了烯烃的稳定Bromonium和碘鎓离子Adamantylideneadamantane和Bicyclo (3.3.1) nonylidenebicyclo[3.3.1]壬烷。x射线结构,积极的卤素转移到受体烯烃,从头开始学习
r·s·布朗,r·w·Nagorski a·j·班纳特·r·e·d·麦克朗g . h . m .艾亚茨m . Klobukowski r·麦克唐纳和b . d . Santarsiero
美国化学学会杂志》上1994年,116年(6),2448 - 2456
DOI:10.1021 / ja00085a027
循环碘鎓离子,类似于bromonium离子,也可以被分离和特征。adamantylideneadamantane父烯烃在这些研究中,准备使用与2-adamantanone McMurry反应。 - 通过固液炔属烃相转移催化脱卤化氢:乙炔DICARBOXALDEHYDE四甲基乙缩醛和乙炔DICARBOXALDEHYDE二甲缩醛
Rufine Akue-Gedu和Benoit瑞格
Org。Synth。2005年,82年,179年
DOI:10.15227 / orgsyn.082.0179
通过消除双二卤化物炔烃的形成。 - 有机反应的电子理论原则。
克里斯托弗·k·英格尔德
化学评论1934年,15(2),225 - 274
DOI:1021 / cr60051a003 - ——相关指令的组织形式RO和RR′N的芳香取代反应。第四部分,观察记录部分的讨论我,II, III
詹姆斯·艾伦·阿尔伯特·爱德华牛津,罗伯特•罗宾逊和约翰·查尔斯·史密斯
j .化学。Soc。(研究)1926年,129年,401 - 411
DOI:10.1039 / JR9262900401
诺贝尔奖得主罗伯特•罗宾逊对卤化反应的机理是错误的。 - 极性增加烯烃。二世。的氯化Di-t-butylethylene
罗伯特·c·费伊
美国化学学会杂志》上1966年88 (20)4681 - 4684
DOI:10.1021 / ja00972a030
研究的卤化独联体- - -反式-di-t- - - - - -butylethylene,显示的立体定向性质卤化反应。 - 极地增加苯乙烯和2-butene系统。二世。溴化产品的媒介依赖
约翰·h·罗尔斯顿耶茨和基思
美国化学学会杂志》上1969年91 (6),1477 - 1483
DOI:10.1021 / ja01034a034
在某些情况下卤化反应的立体选择性可以通过使用高极性溶剂或明显侵蚀electron-releasing取代基烯烃,将导致更稳定的碳正离子中间体。
你好,
我正在做测试,我遇到的问题是一个烯烃加成Br-Br和氯化钠。我知道Cl应该先添加,但我似乎无法找出它的机制。
不,,你形成bromonium离子Br2然后Cl(-)是活跃的亲核试剂攻击结果最多bromonium离子取代位置。
一个奇怪的问题,因为他们可能不提及溶剂。生理盐水不溶于有机溶剂。更好的选择是Bu4N + Cl -。
我们如何调用sn2类型开环叔碳上给最代替酒精?为什么对面的开环的区域选择性观察基本条件下环氧开放吗?
离去基很好,首先。C-halogen债券长度远长于正常C-leaving组键长。(如碘鎓的我2.48 vs 2.13为正常的我)。
其次,因为三人环,碳原子上的几何形状是不一样的在你的典型的四面体碳,所以有更多的“房间”的亲核试剂的方法。
好日子先生。我知道卤化烯烃的反应涉及到离子桥中间,并没有发生重排。但我不明白如何1 4添加产品是当涉及到共轭二烯烃为原料生产。因为中间是离子的桥梁,如何形成共振?提前感谢你的回复。
看到这篇文章://m.deriinvest.com/2017/04/11/more-on-12-and-14-additions-to-dienes/
我怎么能只合成cis dibromo从烯烃烷烃吗?
东西我不明白(我的教授不能解释):逻辑上我认为第二次攻击会少取代碳将会有更少的位阻。同时,更代替(更邻近碳原子)意味着这些碳将捐赠更多的电子密度相同的碳,这将使它更负面的(因此减少亲电和活性)。
我注意到你没有比“[…]详细碳的反应将最能稳定正电荷。“这有一个更深的解释?
嗨,艾丹•。原因第二攻击发生在取代碳越多,而不是取代越少,由下面的解释。过渡态导致的产品,C-Br债券之一bromonium离子已经部分坏掉了。因此,一个两个C原子将承担部分将cation-like积极充电,换句话说。现在,考虑相对稳定的碳正离子。因为更多的取代碳正离子更加稳定,取代碳将进行部分C-Br债券乳沟,因此在叔碳亲核攻击将优先发生在上面的例子中。
而你是对的,更多的取代碳更多的位阻,这种效果不如电子效应的重要碳正离子的稳定性。
这是复杂的事实,主要产品不是1,核。水也会参与反应,大部分的产品是2-bromoethanol。
有什么原因的水,水反应之前Br -呢?水比Br -应该是一个较弱的亲核试剂。
水溶剂,所以它是出现在非常高浓度(纯水的浓度55米)。这就解释了为什么优先/ Br -水攻击,否则更亲核试剂。
嘿,教授,我把一切都和你在一种更简单的方法解释一切,但我不明白的部分关于“碳的反应将最能稳定正电荷吗?“也许你能告诉我它是C和更大的部分电荷在相应的例子使用部分电荷符号?
谢谢,
Soji
这将是最取代碳-碳正离子的稳定性,它遵循这一趋势三级(最稳定)>初中>主(不稳定)
我也想知道关于这个。谢谢你花时间来解释它。