普通化学复习
化学动力学
最后更新:2023年1月12日|
化学动力学反应速率的研究。它可以是非常重要的在确定化学反应的机制。这是你需要记住什么化学动力学的本质从创化学有机化学。
1。反应速率与浓度和温度成正比。
首先,化学反应发生在原子或分子间发生的碰撞,产生的化学键的变化安排。因此,反应速率正比于碰撞分子的数量。并不是每一个碰撞会导致化学反应;总数的碰撞,只有一定比例将发生在适当的能量使化学键断裂和形成的过程。认为电话销售忍者刀——只有一小部分的电话他会导致销售,但总销售额将调用的数量成正比。
在化学反应中,任何增加了碰撞率会增加反应速率。一种方法是增加浓度。另一个是增加的温度-你可能还记得,我们称之为“温度”可以看作为衡量原子和分子运动。

2。第一和第二阶反应
根据反应类型,一个或两个化学物种可以参与转换。涉及两个以上的化学物种的反应几乎从未见过的不同时三个物种都碰撞的能量。
的订单反应的物种的数量参与反应。
的率的反应是有多少分子化合物正在单位体积每秒,在M / L•s表示。我们可以写一个方程如果我们把比例关系,(鱼)浓缩的速度,改变成一个方程,通过引入一个常数k称为速率常数。每一个反应都有独特的速率常数在恒定的温度是有效的吗,这是有道理的,因为增加的温度将增加碰撞,导致不同程度的数量。

对于一个单分子的反应涉及一个物种,就等于k [A],[一]mol / L的浓度。双分子反应a + B,速率等于k[一][B][一]和[B] a和B的浓度。
例如SN1反应中,您将了解在Org 1中,第一步是弱键的断裂提供卤溴化(在这个例子中)和碳正离子。这是一个一阶,单分子的反应。我们可以把这个反应的速率常数速率= k(一个)
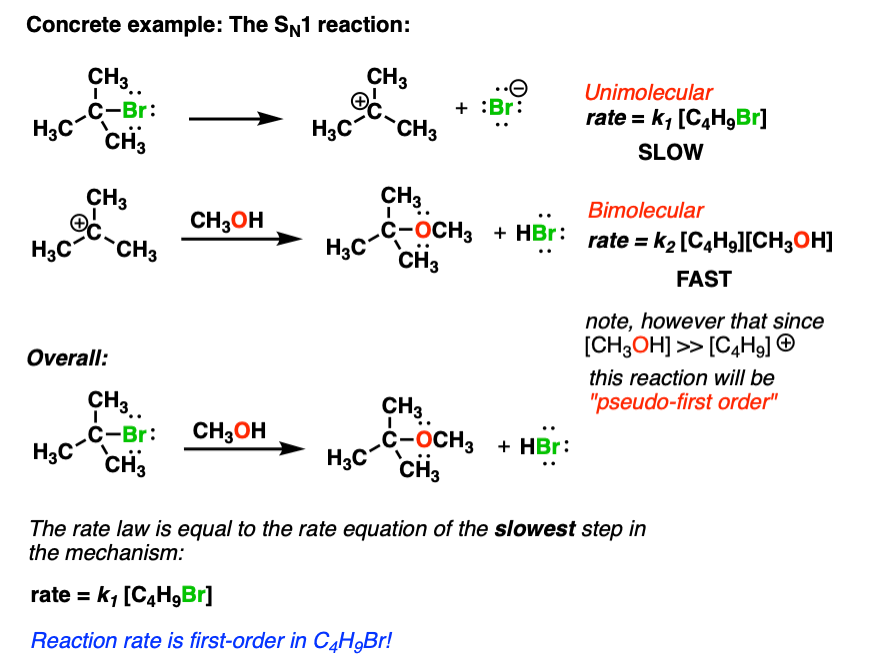
第二步涉及到一个分子的碳正离子反应溶剂(例如甲醇)提供一个醚。这是一个二级反应。注意,然而,由于甲醇的浓度非常高(溶剂)它的浓度将少量的甲醇的影响在这个反应。因此,反应速率只取决于碳正离子的浓度,C4H9。这是一个例子准一阶反应。
虽然有很多反应的例子包括一个整体转换(如盐酸+氢氧化钠水,例如),你会很快发现在有机化学反应的SN1进行多个步骤更常见。反应,导致一个特定的序列被称为产品反应机理。
3所示。反应的速率取决于最慢的一步。
这里的反应速率:他们取决于最慢的一步。SN1上面的例子,因为第一反应是缓慢的一步,我们可以近似的反应速率定律的这一步。SN1反应的速率定律,上面会写率k [C4H9OCH3] = [C4H9Br]。换句话说,C4H9OCH3的生成率在一个给定的温度将是直接与C4H9Br的浓度成正比,不会依赖CH3OH的浓度。
4所示。速率定律可以洞察机制:
这是一个有用的提示:我们可以使用速率定律给我们信息机制。例如,上面的SN1反应是反应称为置换反应的一般类的一部分。还有第二种类型的替代所谓的SN2反应机制。SN1是单分子的速率决定步骤的速率决定步骤SN2双分子的。
让我们改变我们的例子从甲醇的亲核试剂(-)(作为溶解碘化盐如碘化钾)。
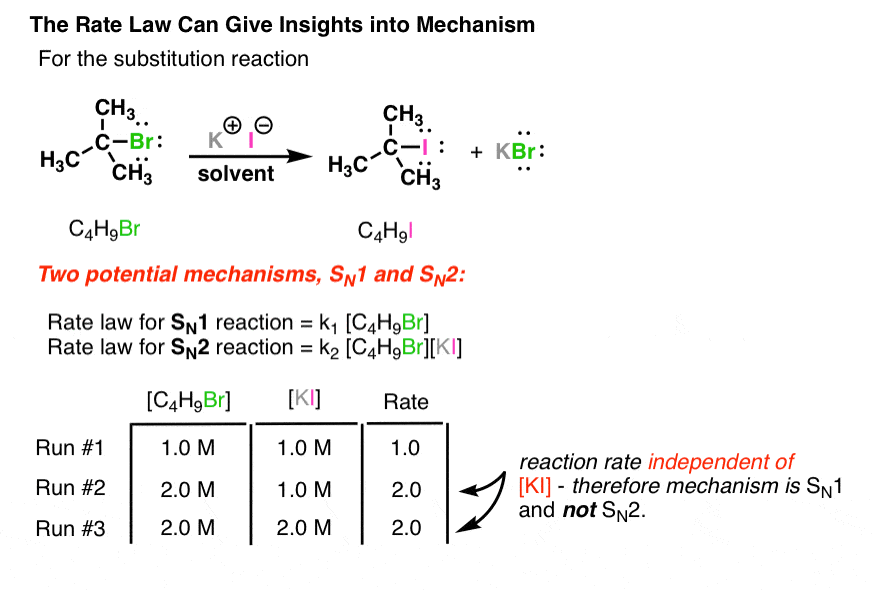
两种反应C4H9I将相同的产品。我们告诉机制如何运作?简单!如果利率的变化,当我们改变碘的浓度(我(-)),我们将知道SN2,如果它不会改变,它将SN1。
在这个例子中,缺乏改变的速度当我们双我(-)的浓度可能意味着SN1机制(或更准确地说,它会反驳SN2,但那是另一个讨论)。
5。障碍的反应被称为活化能。
我的二年级物理化学老师明确活化能的概念令人震惊我们曾经告诉我们,在热力学方面,人肉的燃烧二氧化碳和水热力学非常有利,但是我们继续在他的教室是一个证明活化障碍的存在。他试图让点的热力学过程一点儿也不告诉你的。
的率的反应取决于一个值称为活化能,这本质上是需要达到一个过渡态的能量,将导致产品的形成。
活化能之间的关系,温度,和反应速率在阿仑尼乌斯方程的形式:

方程中速率常数k, T是温度,气体常数R是,Ea是活化能,和神秘的信是所谓的pre-exponential常数。
它可以归结为速率常数k是碰撞,导致反应的数量/秒,一个是碰撞发生的总#每秒,和e ^ (Ea / rt)的概率是任何给定的碰撞会导致反应。
这是一个棒球类比。假设您希望想出一个方程,将给你一个估计的数量支全垒打在一个给定的球场。你能想出一个方程,看上去是这样的:
#支全垒打=(总#球击中)[概率球有足够的能量一个本垒打)
“活化能”在这种情况下将距离本垒外场栅栏,这将是“百分比”术语的一部分(连同栅栏的高度,大概)。随着栏栅击退,垒将不可避免地下降。如果你想要,你可以找到一种方式重新安排这个方程可以算出距离围墙的#如果你知道球击中,明确所需要的能量的围墙。
阿仑尼乌斯方程是非常强大的,允许你计算活化能的值以及速率常数的值在不同的温度下。在你的课程是怀疑你也会被要求去深入阿仑尼乌斯方程,但它仍然是重要的去欣赏它的微妙之处。
最后需要注意的一点是,阿仑尼乌斯方程的一个有用的经验法则是,反应速率的双打每10度之温度。
在下一篇文章- - - - - -从创化学有机化学,13 -平衡
这是一个神奇的网站,一个伟大的复习工具对于我们这些没有有机化学在十年或二十年。有类似的资源在物理化学的建议吗?
你好约翰,谢谢你。我不知道任何我的头顶,虽然有时我做得到这个问题!
我认为有一个错字ini第二节的Sn2反应。碳正离子的分子,碳被列为CH2之一,但应该甲基。
谢谢你!固定
你好詹姆斯,
首先,我非常感谢你的辛勤工作。我是一个很好的准备即将到来的组织。化学。类。
在图像SN1反应C4H9Br - > Br - + C4H8
一个氢原子去了哪里?这是一个错误吗?
这将是伟大的如果你能澄清这尽快!
在图上的错误。固定!
我困惑于三阶及以上反应很少发生。事实上,我不同意这一点。这里是一个很好的例子,事情等等从2最简单的组件,甲烷和氯:
甲烷和氯溶解在彼此所以没有溶剂与溶质,反应物2。光(阳光可以触发)和氯分子自发分裂。
1)+氯甲烷- >盐酸+ CH3Cl
2)接头1)CH3Cl +氯- >以+盐酸
子2)2 Cl2 CH3Cl - > + C2H6
3)子1)以+ - > CHCl3氯+盐酸
子2)C2H6 +氯- > C2H5Cl +盐酸
等。
这当然是自由基氯化导致每个烷烃和氯碳化合物(碳氯键)可能是理论上∞。
这三阶以上的另一个例子是如果你把炔,氢化烯烃,然后氢化烷烃,比添加卤素来得到一个烷基卤化物。
我爱这个教程中,我喜欢数学,我很擅长化学反应器,但我从未相关实例。bdapp平台谢谢你这么做…
谢谢你这个非常有用的网站。我遇到了我在准备组织。化学课程,在几周内开始。这是一个很好的复习。
问题:我只是想澄清你最后注意…你说的是速率常数,或利率本身?
谢谢。
嗨,詹姆斯!你为什么使用上面的“无穷符号的一半”。顺便说一下,这是有史以来最好的网站。我之前学习有机化学在秋天。谢谢你!
这意味着“与”
嗨,詹姆斯!再次感谢发布这些快速、普通化学的简要总结。我正在评估一些自由基卤化,我意识到我忘记了如何编写一个速率定律。再次感谢进修!