二烯烃和MO理论
Electrocyclic反应
最后更新:2022年10月27日|
Electrocyclic反应和4-Membered戒指:顺旋和对旋开环和关闭
在本文中,我们调查electrocyclic开环和ring-closing与4π电子系统(“4π”系统)。
Electrocyclic反应在“热“条件(即加热,没有紫外线)导致比下得到不同的产品“光”条件(即与紫外线照射)。
仔细看看下面的立体化学!
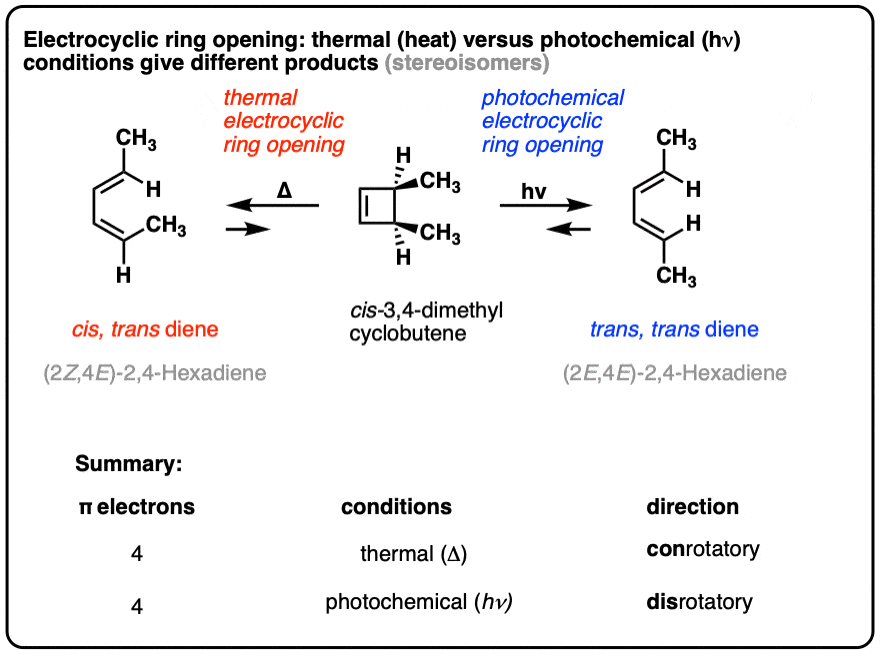
这些不同的结果的原因是,最高占据分子轨道(HOMO)在热的情况下有不同的轨道对称性比最高占据分子轨道(HOMO)光化学。
轨道对称性的变化导致的改变如何结束碳必须旋转形成新的σ键,也可以是“顺旋”(两端旋转方向相同)或“对旋”(两端旋转方向相反),下面我们将会看到。
下面的更多细节。在以后的帖子中我们将讨论的规则系统有六个π电子(“6π”)和更高。
表的内容
- Electrocyclic开环的环丁烯给丁二烯
- Electrocyclic环关闭1,三丁基给环丁烯
- Electrocyclic反应是立体定向
- 轨道对称性和“热”Electrocyclic反应
- 在“热”轨道对称性Electrocyclic开环
- 运用“顺旋”旋转预测从Electrocyclic开环取代基的立体化学
- 预测产品顺旋Ring-Closing
- Electrocyclic“光化学”条件下的反应
- 如何“光化学条件”(紫外线)影响Electrocyclic反应?
- 的轨道对称性Electrocyclic“光化学”条件下的开环
- “对旋”规则应用到Electrocyclic光化学条件下开环
- 简介:热与光化环打开和关闭
- 笔记
- 测试你自己!
- 引用和进一步阅读
1。Electrocyclic开环的环丁烯给丁二烯
今年是1905年。化学家理查德Willstatter和他的合作者沃尔夫冈·冯·Schmaedel加热反应混合物在慕尼黑大学的实验室。他们表演很常规消去反应现在被称为霍夫曼消除。
预期的产品是环丁烯。
分析了反应混合物时,环丁烯确实形成了。神秘,然而,大量的三也被孤立。
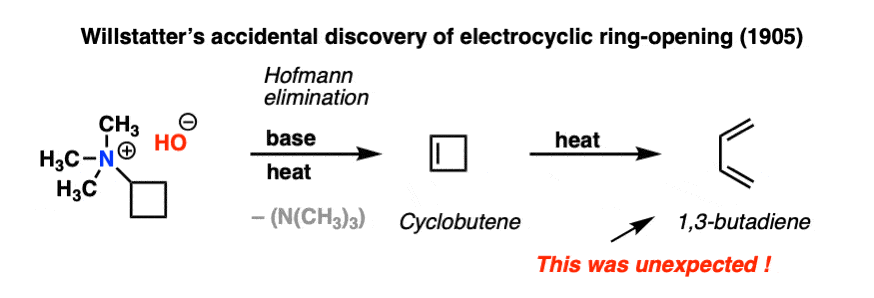
这是一个奇怪的和意想不到的结果!Willstatter没有明确的了解1,当时三丁基成立了,它仍将如此。他将去他的坟墓(1942年)不知道,他意外地发现了后来被称为一个electrocyclic反应;具体来说,electrocyclic开环的环丁烯。这并不是像Willstatter是笨蛋;几年后,他是第一个合成环辛四烯,几年之后他会赢诺贝尔化学奖确定叶绿素和其他植物色素的结构。(注1]
在接下来的几十年里,反应(和它的许多变体)详细研究了。是验证加热环丁烯确实形成1,三丁基。
然而,有趣的是,加热环丁烷没有导致任何开环反应。
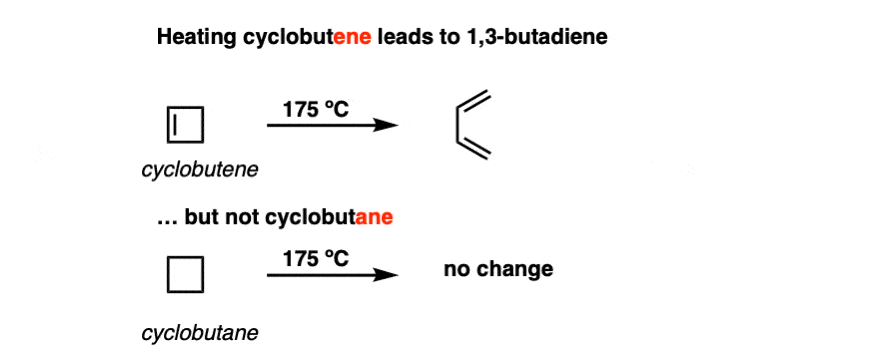
开环的环丁烯(和其他循环分子,我们将看到)一直被称为electrocyclic反应。electrocyclic反应是一个反应,形成一个单键界标之间的π体系。逆过程(即开环,打破一个单键组建一个新的pi系统)也是一个electrocyclic反应。
注2。官方的定义electrocyclic反应。
2。Electrocyclic环关闭1,三丁基给环丁烯
随着时间的推移,它也发现1,三也能够接受相反的反应:一枚戒指给环丁烯关闭。
由于环应变(看到帖子:计算在环烷环应变]关闭1,三丁基丁二烯通常是不利的,但某些取代二烯烃可以哄骗关闭环(看到下面]。
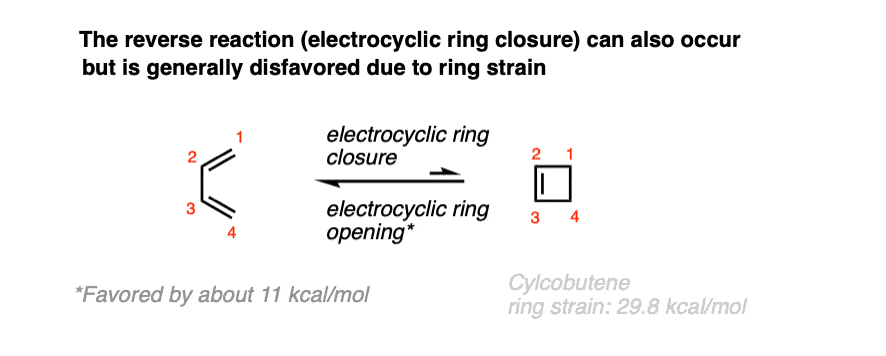
(请注意:环丁烯的环应变约为29.6千卡/摩尔比为26.3千卡/摩尔环丁烷)
因为环丁烯和1,三可以互换,这意味着electrocyclic开环和electrocyclic ring-closing穿过一个共同的过渡态,和有一个平衡在这两个分子在高温下。
它有助于检查债券形式和休息。
- 前进的方向,一个碳碳π键和碳碳σ键断裂,和两个碳碳π键的形式。
- 在相反的方向,两个碳碳π键断裂,和一个碳碳π键和碳碳σ键形成的。
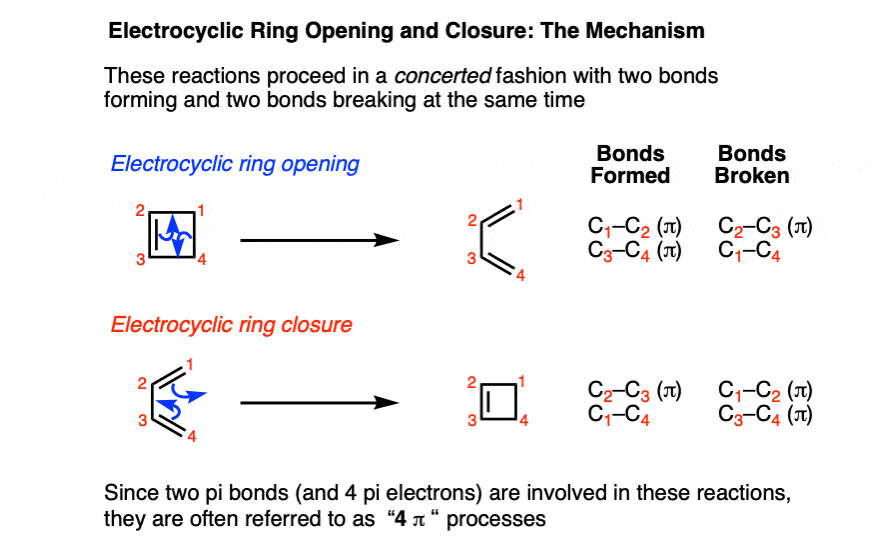
Electrocyclic开环和ring-closing也共享相同的过渡态。
3所示。Electrocyclic反应是立体定向
超越环丁烯取代环丁烯,非常有趣的模式是观察:立体化学在这些反应遵循一个明确的模式。
Electrocyclic开环是一个立体定向的过程。反应称为立体定向如果起始原料的不同只有在它们的配置转换成立体异构的产品。注3]
一个典型的例子是独联体- - -反式- 3,4-dimethylcyclobutene是不同的立体异构体只有在他们的配置。【审查,请参阅:类型的同分异构体]
换句话说,如果如果你知道你的起始物料的配置,你知道反应遵循的“规则”,你可以预测产品有100%的准确度。
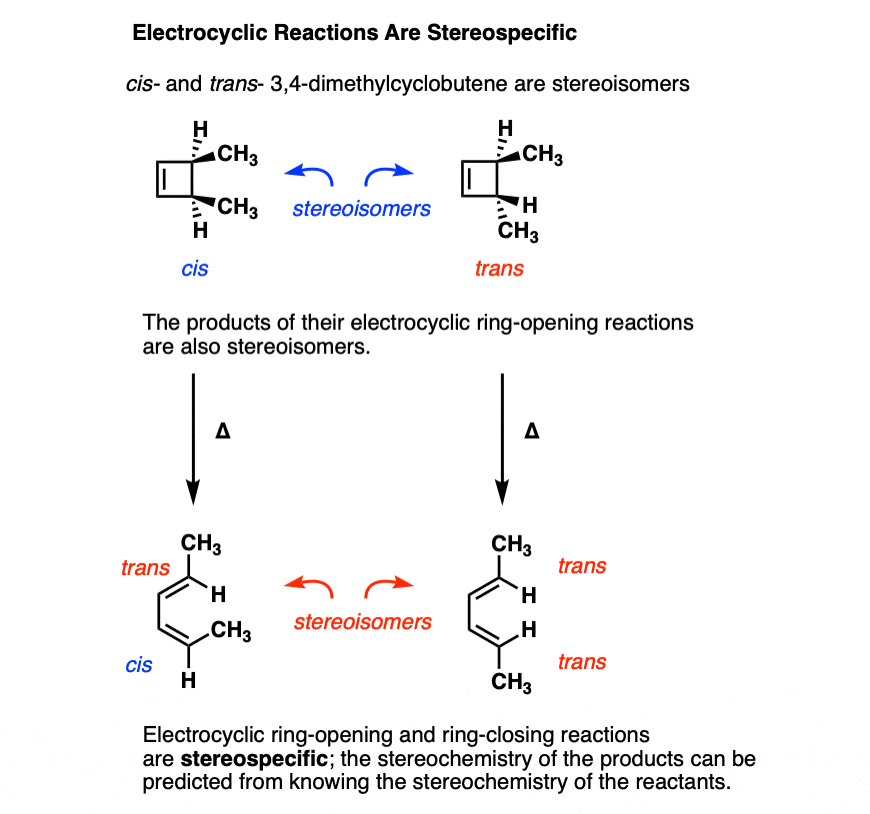
为什么这些反应可预测的呢?因为这些反应遵守规则轨道对称性守恒(“伍德沃—霍夫曼定律”)。
把它的另一种方法是,我们可以理解这些反应的过程中通过检查前沿轨道(“最高占据分子轨道”(HOMO)和“最低占据分子轨道”[LUMO]π体系),下面我们将会看到。
[Electrocyclic环是立体定向——关闭盘旋的图像或点击这个链接。
我们之前见过的(Woodward-Hofmann规则作用于Diels-Alder反应(见:HOMO和LUMO Diels-Alder反应],建设性的轨道重叠的最高占据分子轨道(HOMO)二烯和最低未占据分子轨道(LUMO)负责Diels-Alder“亲二烯体”作为一个“简单”的反应。他们也在工作应对和克莱森重组等疾病。]
4所示。轨道对称性和“热”Electrocyclic反应
像Diels-Alder反应,管理模式electrocyclic反应也理解分析分子轨道。在这种情况下反应发生在只有一个π系统以来,我们只需要担心人类。
的最高占据分子轨道(HOMO) 1,三是什么样的?我们已经看到了如何建立π分子轨道。(参见:丁二烯的π分子轨道以及如何吸引他们)我们会跳过妙语。
丁二烯下面画的最高占据分子轨道。注意,它只有一个节点(即有标志的改变),c - 2和颈- 3之间。(没关系,你画出轨道的两种方法,只要它只有一个节点!)
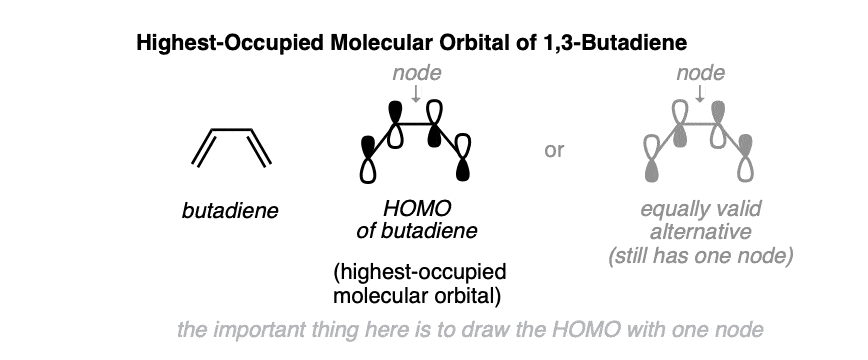
在1的反应,三丁基- >环丁烯,颈- 1之间形成一个新的σ键和c - 4末端。
哪里的轨道形成这个σ键从何而来?p轨道的颈- 1和c - 4打破他们的π键分别为C2和C3 !
为了使债券形式,必须有建设性的这两个轨道重叠。通过“结合互动”我的意思是,他们都必须有相同的阶段两个阴影或白色。
如果这个键相互作用可以发生这两个轨道在一个顺时针方向运动,或者如果他们这两个将在一个逆时针方向的运动。
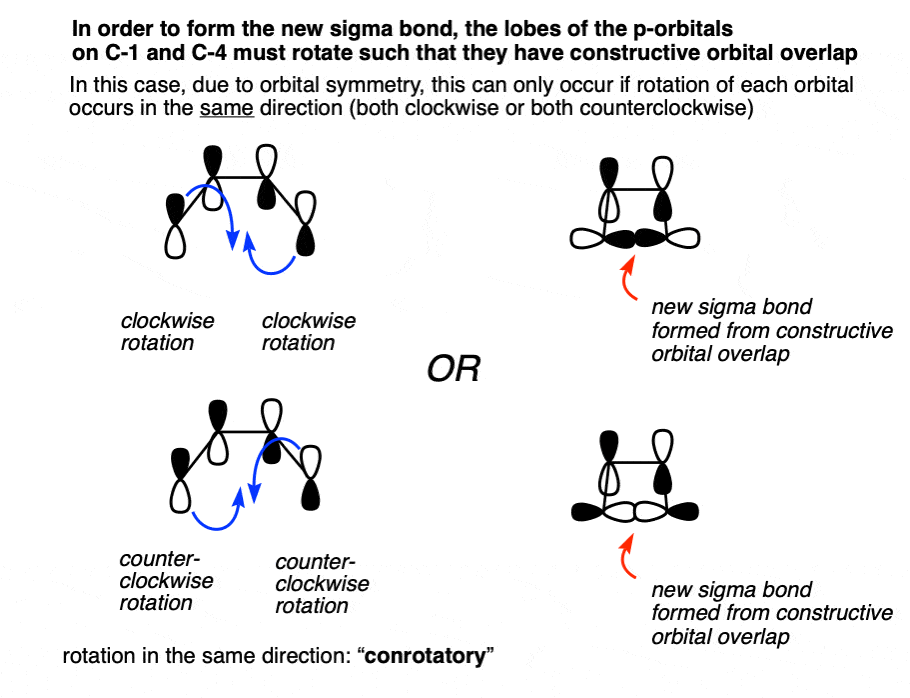
如果他们不把顺时针或逆时针方向吗?没有债券形式,因为轨道产生相反的阶段,因此破坏性轨道重叠!盘旋的图像或点击这个链接
5。在“热”轨道对称性Electrocyclic开环
我们也可以分析的反应相反的方向,其中σ键被改造成一个π键。在这种情况下,叶转动方向相同为了被转化为丁二烯的人类。
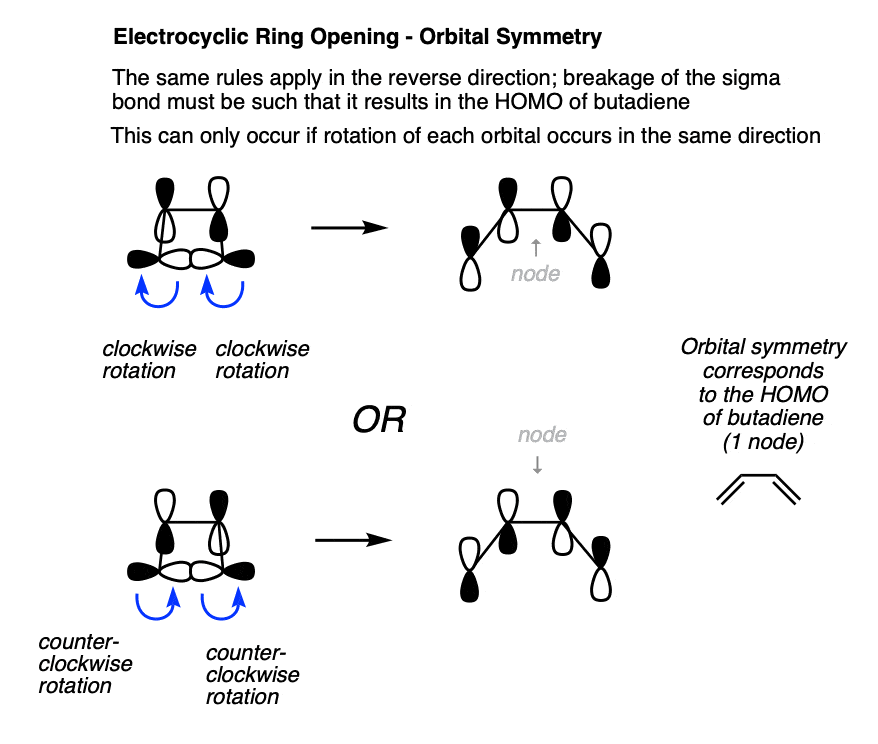
请再次注意,这两个叶旋转方向相同;顺时针或逆时针方向。
自“旋转方向相同”一词出现,它被授予一个特别的名字。我们称之为“顺旋“旋转,以在这些“双出口”医院的大门。(注5]
6。运用“顺旋”旋转预测从Electrocyclic开环取代基的立体化学
不仅仅是p轨道旋转顺旋的方式——它的原子本身,这意味着另外两个取代基出现。
理解终端碳必须“顺旋”的方式旋转4πelectrocyclic反应是整个能够预测立体化学的关键。
这些反应,它帮助如果你想象看分子从前面。
这里有一个例子3 4-dimethylcyclobutene展示两个甲基旋转的“一样”(顺旋),导致的独联体- - - - - -,反式- - - - - -产品。
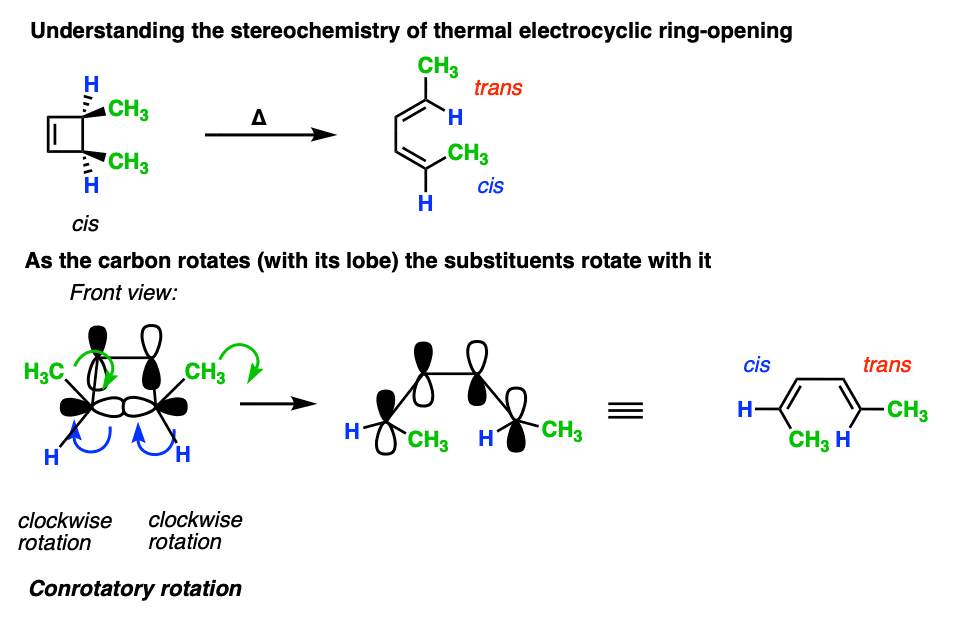
应用同样的规则反式3,4-dimethylcyclobutene导致反式,反式二烯。(注意4]
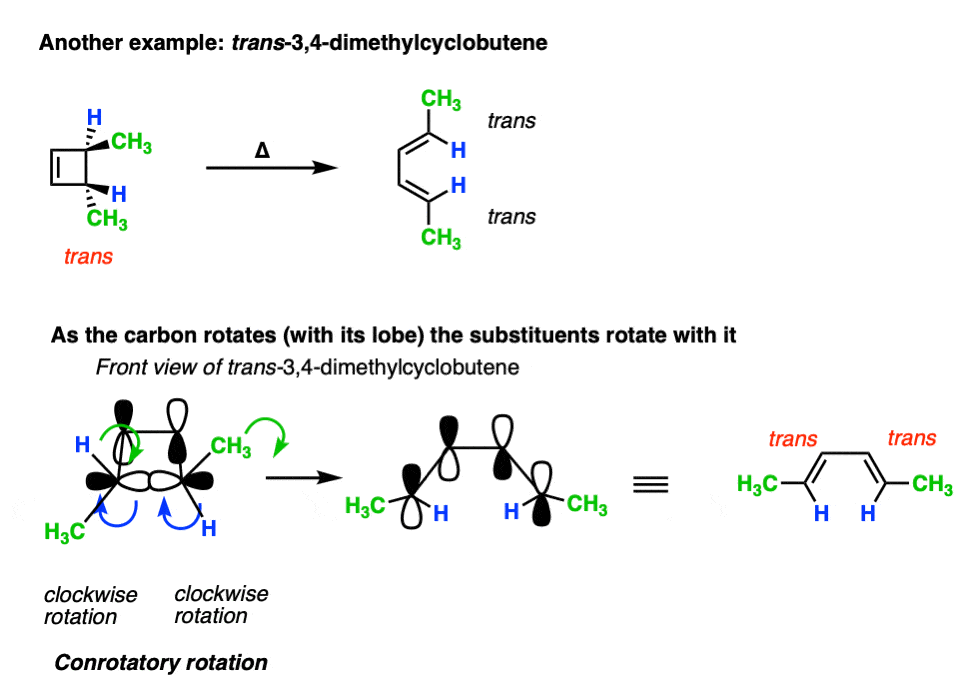
准备试一试自己吗?试试这个小测验。
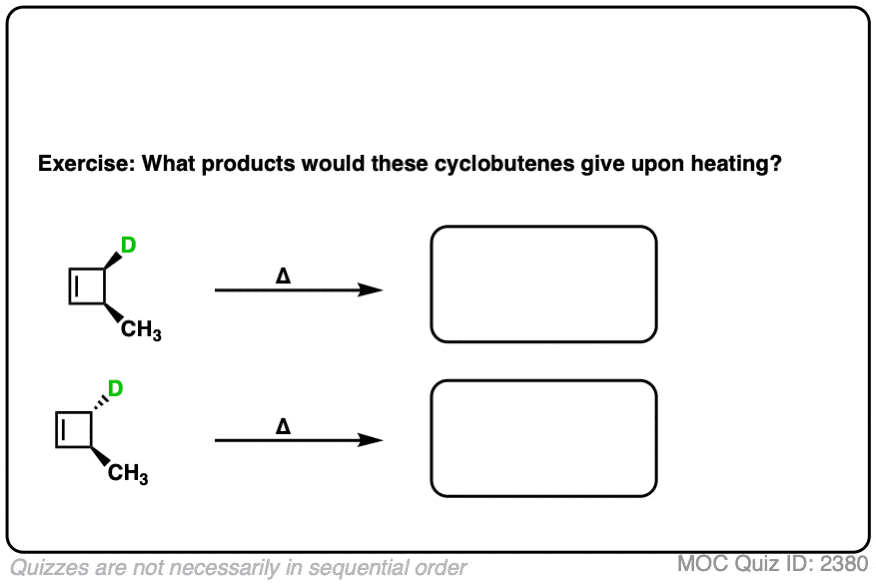 点击翻转
点击翻转
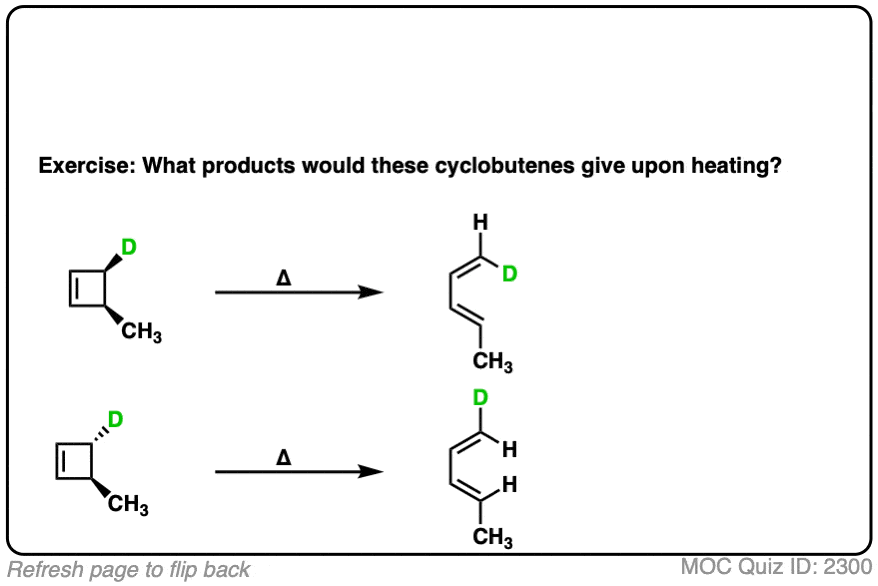
7所示。预测产品顺旋Ring-Closing
的相反的方向,从二烯环丁烯吗?在这种情况下我们如何预测产品?
运用相同的方法。终端碳旋转顺旋的方式。
再一次,这是有助于从前面看分子。这里有一个例子独联体- - - - - -,反式- - - - - -二烯经历顺旋环闭合,顺时针或者both-counter-clockwise。
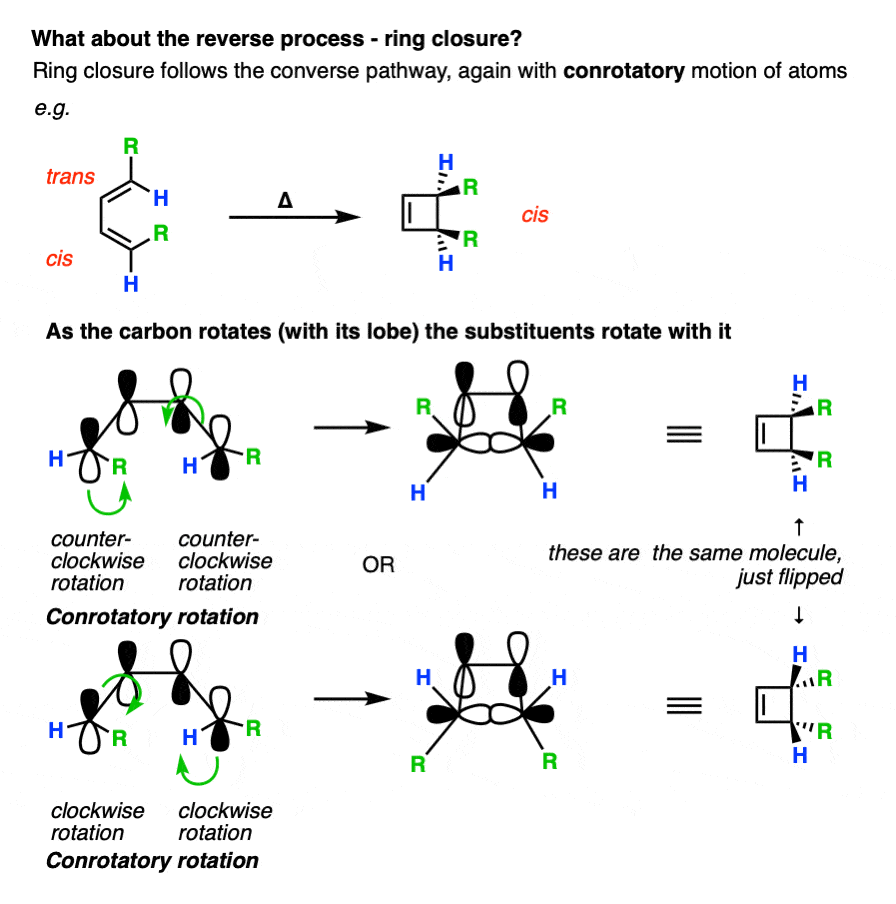
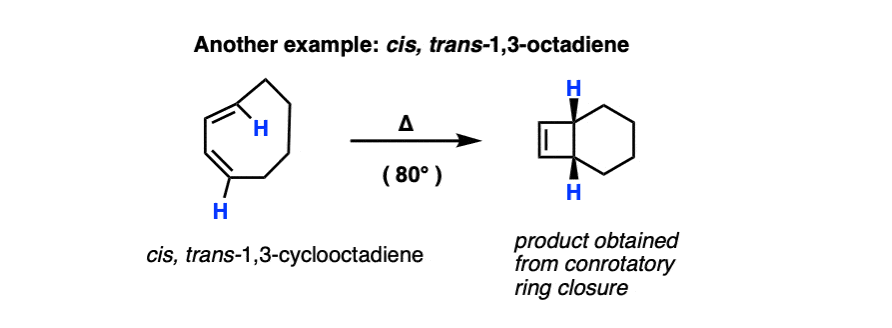
记住electrocyclic环关闭给双烯通常不宜由于环应变?这是一个有利的例子electrocyclic环关闭,因为它可以缓解压力在一个包含一个环二烯反式- - - - - -双键。
8。Electrocyclic“光化学”条件下的反应
原来还有另一种哄electrocyclic反应发生,除了加热垃圾。
光(我们表示hν)也可以达到目的。(双烯的情况下,我们通常讨论的是紫外线,因为他们吸光度最大值深入紫外线)。
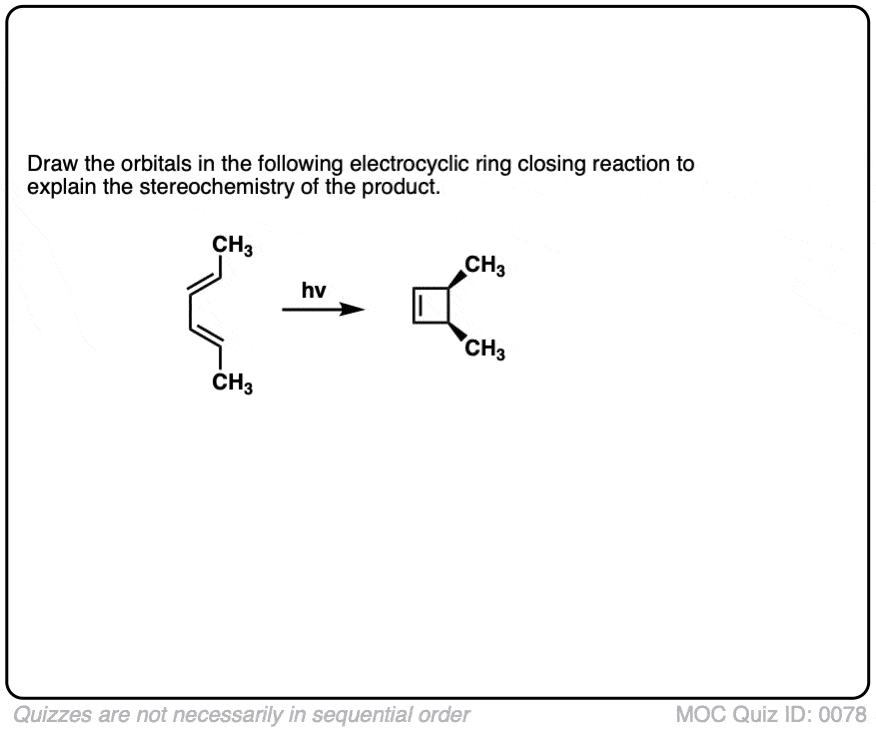
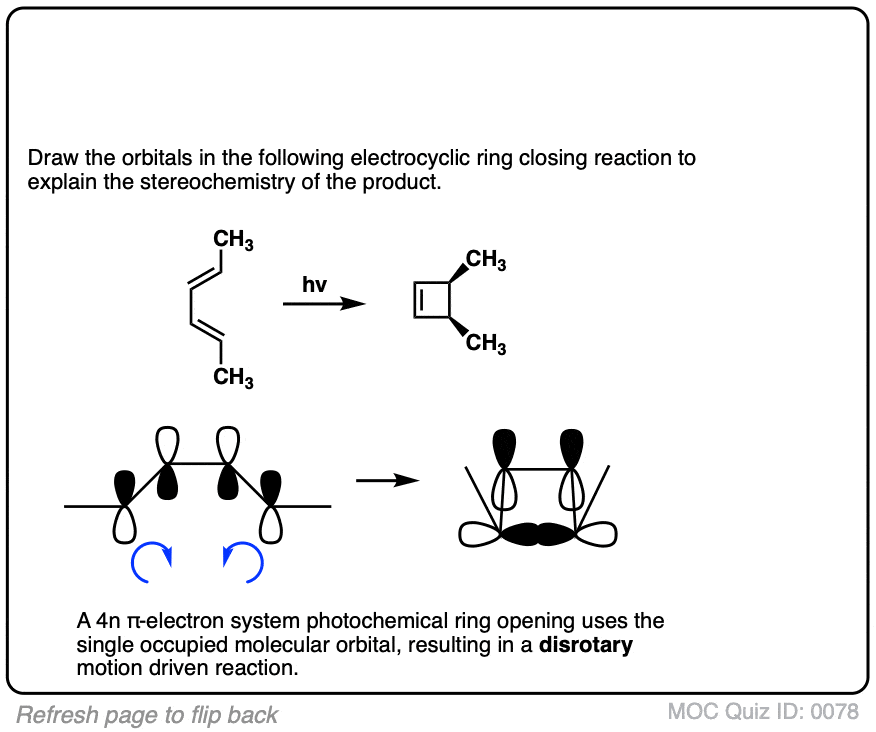
然而,当一个人使用紫外线,立体化学的产品不同于我们看到“热”的条件下。在electrocyclic开环的独联体- - - - - -3,4-dimethylcyclobutene反式,反式- - - - - -二烯形成相反的独联体- - - - - -,反式- - - - - -产品我们观察在“热”的条件下。
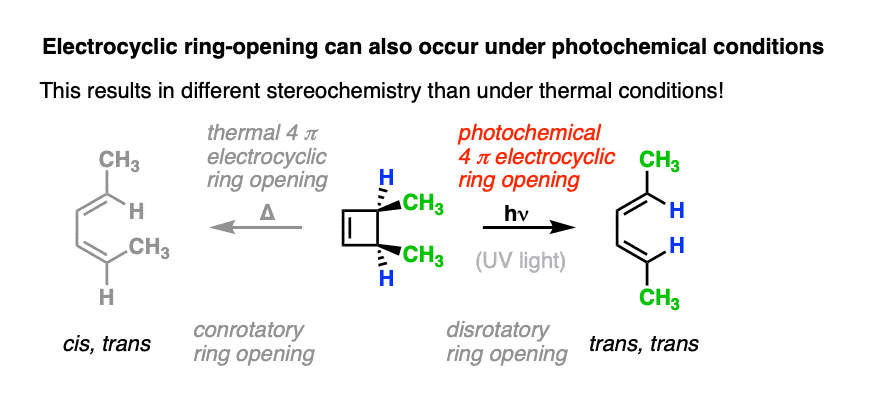
还要注意,反式- - - - - -3,4-dimethylcyclobutene给出了独联体- - - - - -,反式- - - - - -产品在光化学条件下!
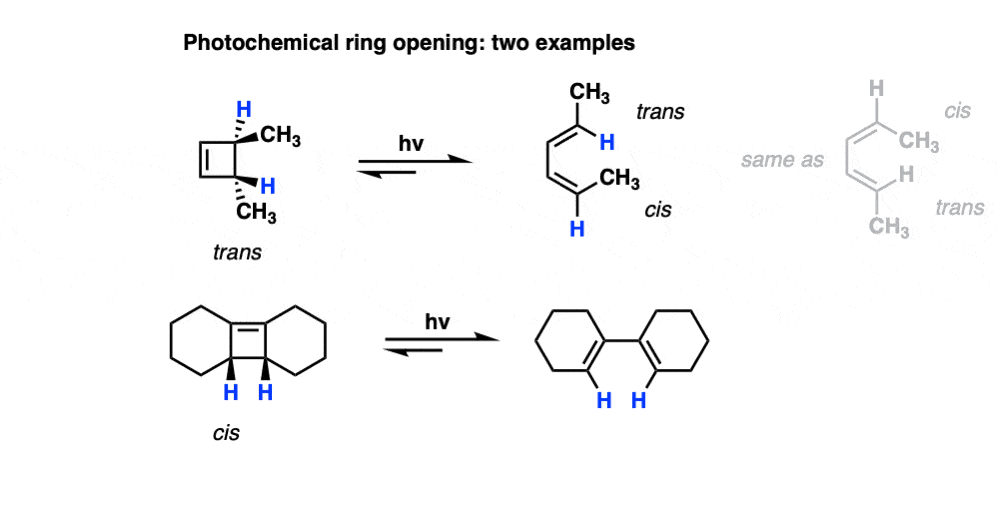
9。如何“光化学条件”(紫外线)影响Electrocyclic反应?
那么发生了什么?首先要注意的是,紫外线将促进电子的最高占据分子轨道(HOMO)二烯π体系的最低未占据分子轨道(LUMO)。看到的:介绍了紫外可见光谱
如果我们检查外观的HOMO丁二烯的出现比率与轨道(π3),你会注意到两个在π体系,而不是一个节点,但更重要的是,叶的结束pi-system有不同的关系。
人类的丁二烯(π2)叶颈- 1 c - 4在相反的方向是一致的,而在LUMO的叶颈- 1和c - 4是一致的,在同一个方向。
所以当紫外线能促进人类的一个电子的LUMO丁二烯(π2)丁二烯(π3),轨道成为“新”人类。
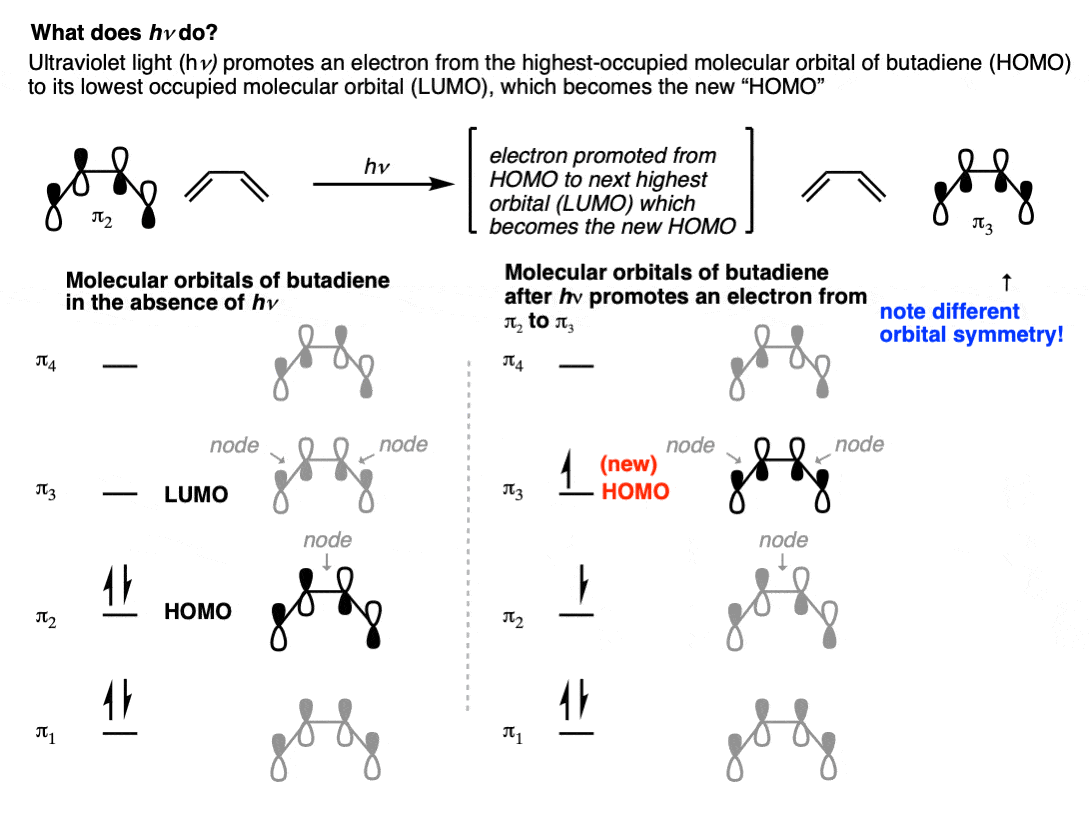
自对称叶之间的颈- 1和c - 4不同π2π3,终端碳需要旋转相反的方向为了形成一个键,与“热”的情况下,他们需要旋转方向相同。
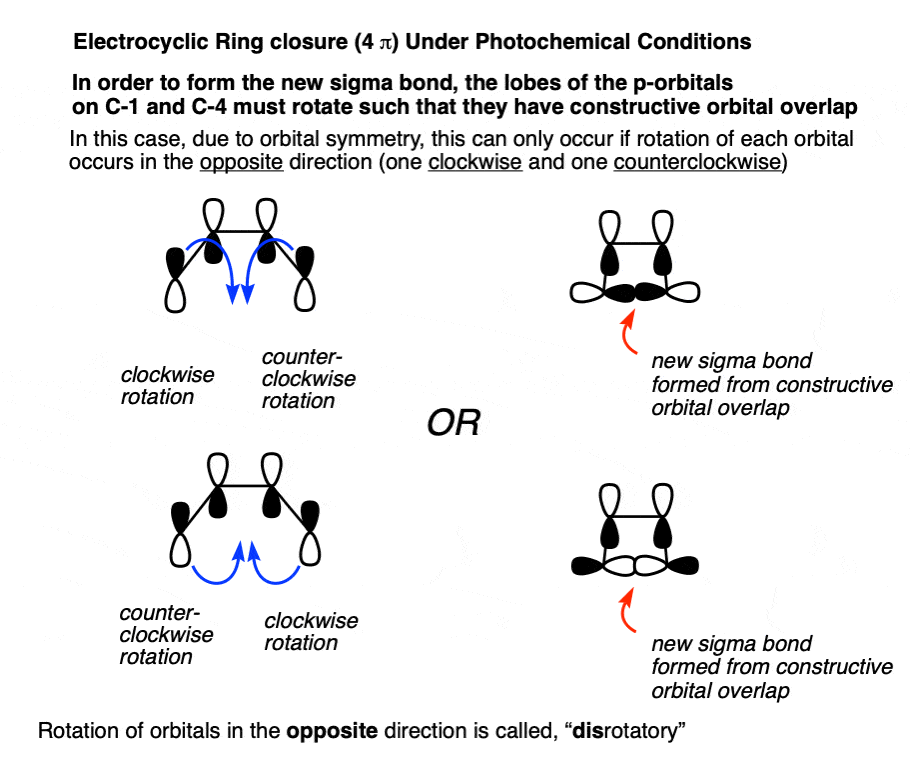
这一项,“旋转相反的方向”的名字,“对旋”,证明了这些双扇门的开启和关闭。
10。的轨道对称性Electrocyclic“光化学”条件下的开环
从ring-closing自electrocyclic开环是相反的途径,我们可以应用同样的规则相反的方向。
打破了碳碳σ键时,叶必须打破他们对齐再形成π键,通过采用的轨道对称性发生π3轨道(即两个节点)。这只会发生,如果碳旋转相反的方向。(注6]
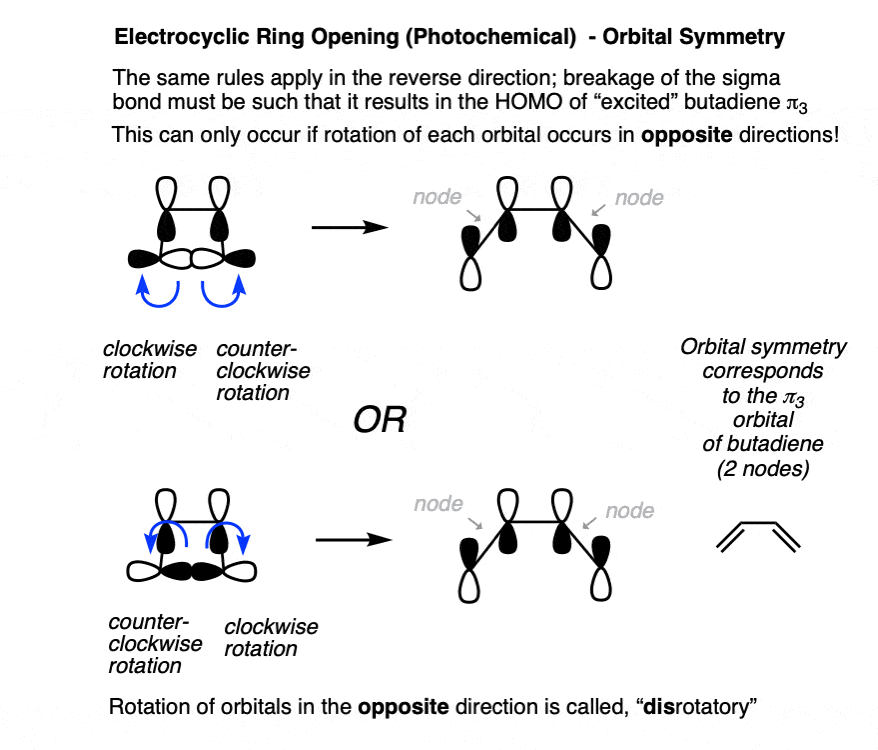
11。“对旋”规则应用到Electrocyclic光化学条件下开环
现在让我们应用这些规则,看看会发生什么在光化学条件下取代基的立体化学。
当独联体- - - - - -3,4-dimethylcyclobutene辐照,反式,反式- - - - - -二烯。
再一次,这通常有助于看环丁烯端点的形象化叶作为一组推或拉的双扇门打开。
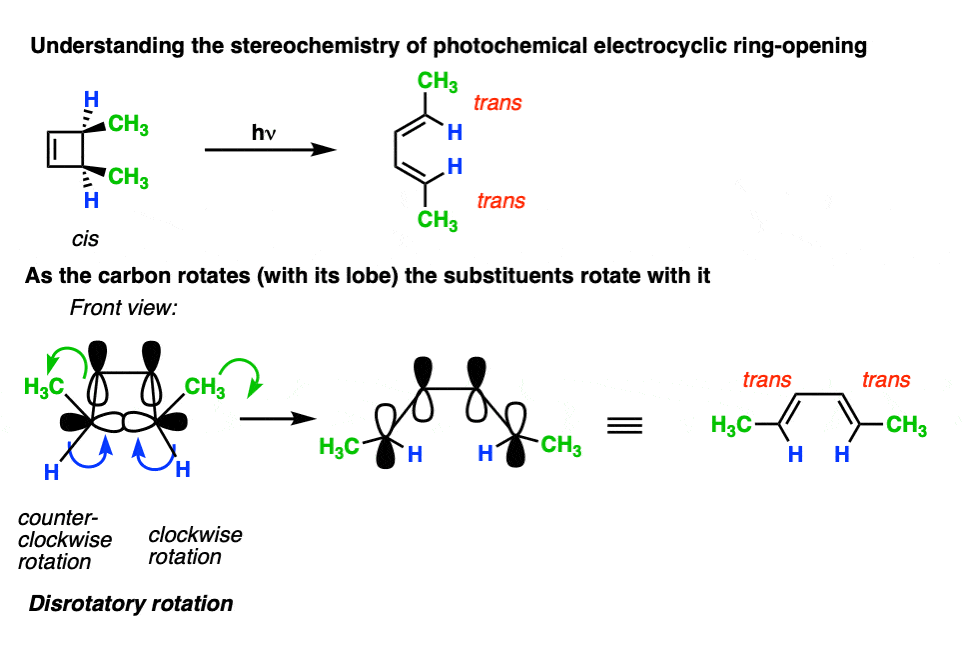
这是另一个例子。
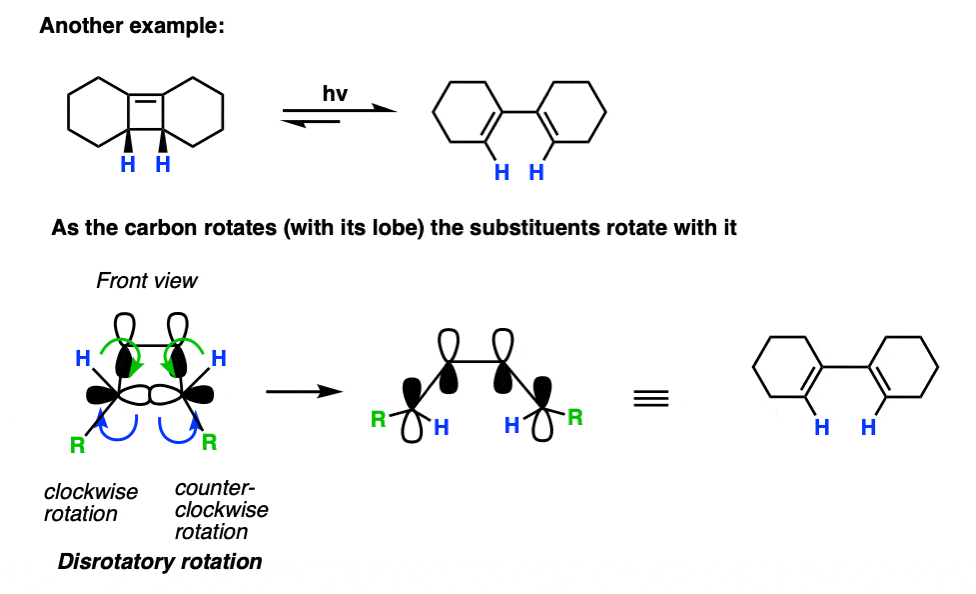
注意,在这个例子中,只有一个对旋选择是可能的,因为另一种会导致一个高度紧张反式——内双键环己烯戒指。
12。简介:热与光化环打开和关闭
这是很多。这是我们所看到的。
- 环丁烯可以接受electrocyclic开环给1,三丁基。相反,1,三可以接受electrocyclic ring-closing给环丁烯。这些物种都处于平衡状态,反应是一致的,通过一个共同的过渡态。
- 因为涉及到两个π键这些作为“4π”classifed electrocyclic反应。
- 这些反应是立体定向。
- 可以预测产品通过检查的HOMO轨道终点碳的π体系。
- 下热条件下(即热)终端碳取代基(和他们)旋转顺旋时尚(都顺时针或都逆时针)electrocyclic反应。
- 下光化条件(例如紫外线,hν)终端碳取代基(和他们)旋转说旋转时尚electrocyclic期间(一个顺时针和一个逆时针)反应。
这都可以在这个简短的总结表:

那么大的π体系呢?在下一篇文章我们将讨论6π电子系统(如果我们有时间和8)。相同的概念将!
笔记
注1。这种事情在中国经常发生在有机化学、实验观察之前的理论理解这些观察。这个过程的细节并没有完全解决,直到1960年的与伍德沃德和霍夫曼的工作轨道对称性守恒(裁判]。(尽管“显而易见”教科书如何做出这些反应似乎我们现在,有机化学不是一系列的逻辑推理,喜欢数学。)
注2。伍德沃德和霍夫曼electrocyclic反应的定义:

注3。立体定向反应的定义,从IUPAC:“反应称为立体定向如果起始原料的不同只有在它们的配置转换成立体异构的产品。”
注意4。对我们来说我们对待,“顺时针”和“逆时针”等价,但有两种模式之一是支持的情况。这就是所谓的“torqueselectivity”,(见ref)。
注6。你可能会想:如果光化开环发生在一个顺旋时尚吗?这真的是这样一个大问题吗?轨道对称性不同于π3以来,电子不会π体系的一部分(至少在最初),而将“di-radical”字符。这些“不允许”的途径可以有时会发生,但通常有过渡状态的能量高于“允许”的途径。
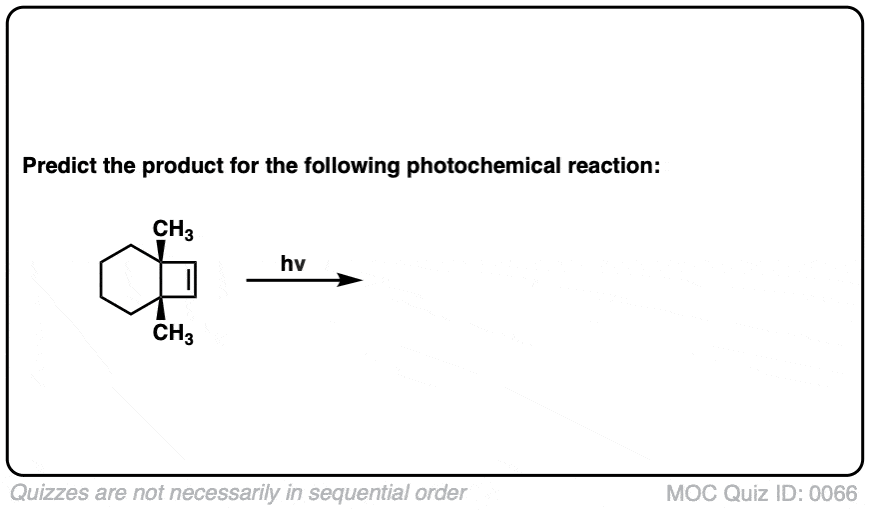
测试你自己!
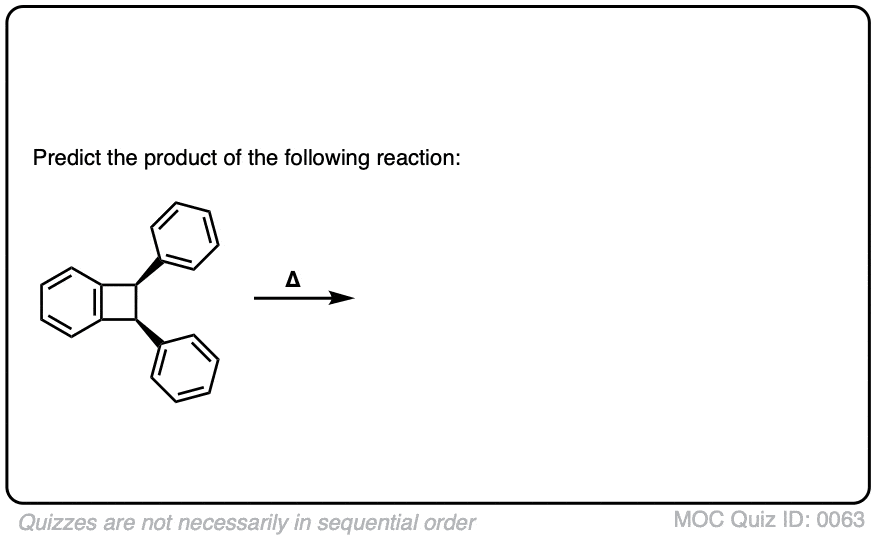 点击翻转
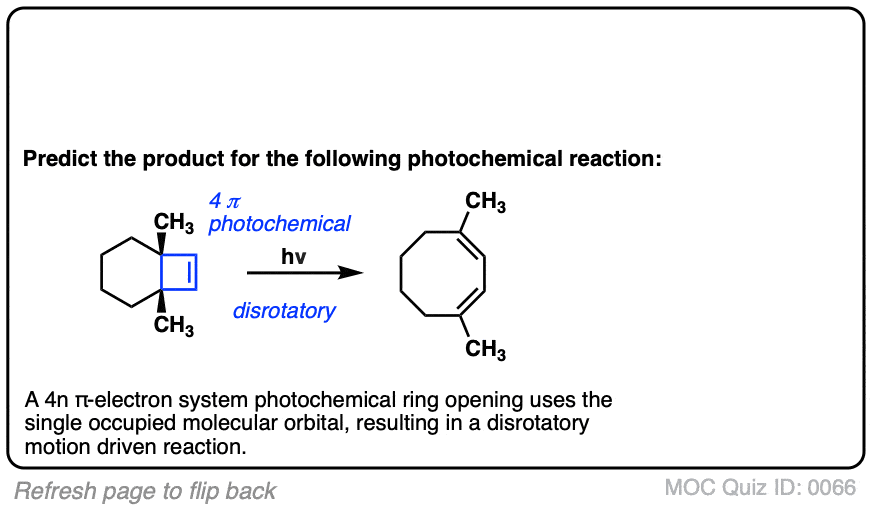
点击翻转
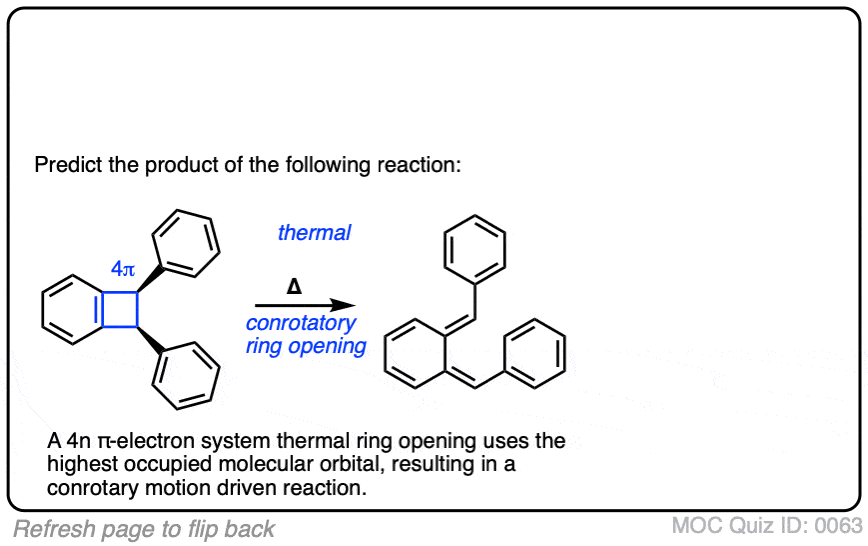
 点击翻转
点击翻转
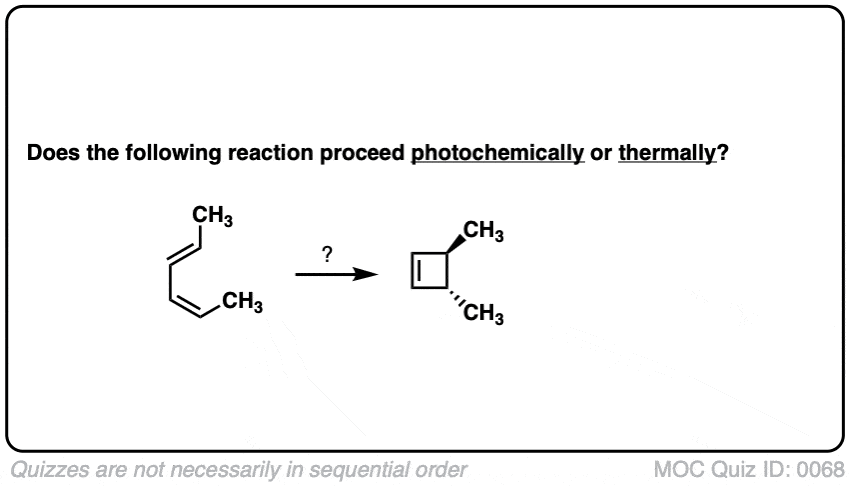 点击翻转
点击翻转
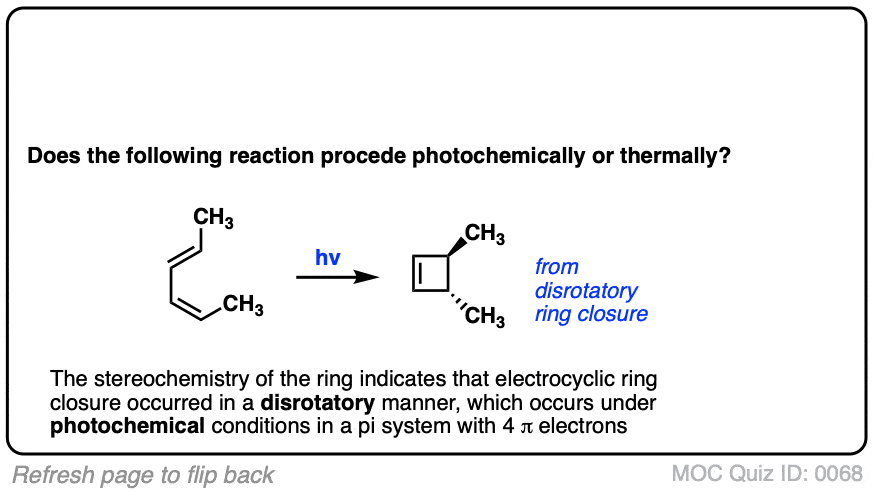
 点击翻转
点击翻转
引用和进一步阅读
- des Cyclobutans Ueber einige衍生物。
Willstatter, r·冯·Schmaedel, W。
的误码率。Dtsch。化学。全球经济。1905年38:1992 - 1999。
DOI:10.1002 / cber.190503802130
从1905年Willstatter和他的同事在温度升高,形成环丁烯异构化的(通过electrocyclic开环)丁二烯。 - 的准备和异构化独联体- - -反式- 3,4-dimethylcyclobutene
鲁道夫·e·k .冬天
四面体的信问题17,体积6日,1965年,1207 - 1212
DOI:10.1016 / s0040 - 4039 (01) 83997 - 6
经典的研究热4πelectrocyclic开环,示范反应立体定向的。 - 共轭Cycloheptadienes光化学转换
o·l·查普曼·d·j·帕斯托·g·w·博登,a . a . GriswoldO.L。查普曼,d·j·帕斯托·g·w·博登,格里斯沃尔德
美国化学学会杂志》上1962年84年(7),1220 - 1224
DOI:10.1021 / ja00866a030
第一批的例子光化学4πelectrocyclic环关闭循环双烯环丁烯。 - 1的热环合,3-Dienes环丁烯
肯尼斯·m .家住彼得·n·纽曼和g . j . Fonken
美国化学学会杂志》上1965年87年(17),3996 - 3996
DOI:10.1021 / ja01095a047
热环关闭双烯给环丁烯由于环应变通常是不好的。在这种情况下,循环双烯是相当紧张的存在反式双键,使环闭合更加有利。 - 能量的交替electrocyclic通路。热解的独联体3,4-dimethylcyclobutene
约翰。布鲁曼和小威廉·c·阿奇。
美国化学学会杂志》上1972年94年(12),4262 - 4265
DOI:10.1021 / ja00767a038
经典研究的立体化学electrocyclic开环。 - 直接调查的光化学开环动态环丁烯与共振拉曼强度
玛丽k .无法无天的史蒂文•d•韦翰和Richard a .数学
美国化学学会杂志》上1994年116年(4),1593 - 1594
DOI:10.1021 / ja00083a064
观察cyclcobutene的光化学开环,三是困难的因为的高能量光子导致多个重排的产品。本研究使用拉曼光谱数据来支持对旋开环。 - 取代基影响利率和立体选择性的顺旋Electrocyclic环丁烯的反应。一个理论研究
Satomi Niwayama E。亚当Kallel大卫·c·Spellmeyer Chimin功能,k . n .胡克*
《有机化学》杂志上1996年61年(8),2813 - 2825
DOI:10.1021 / jo950884i
在上面的文章中,我们把两个顺旋起“顺时针”或“逆时针”是相等的。本文探讨“torqueselectivity”,其中一个可能的旋转模式是青睐。 - Electrocyclic反应的立体化学
r·b·伍德沃德,罗尔德·霍夫曼
美国化学学会杂志》上1965年87年(2),395 - 397
DOI:10.1021 / ja01080a054
在这个经典论文伍德沃德和霍夫曼定义术语“electrocyclic反应”,“顺旋”,“对旋”。 - 应变能的小环碳氢化合物。C−H键离解能量的影响
罗伯特·d·巴赫*和和奥尔加Dmitrenko美国化学学会杂志》上 2004年 126年(13),4444 - 4452
DOI:10.1021 / ja036309a
环丁烯的应变能是29.8千卡/摩尔比为环丁烷26.3千卡每摩尔。 - 轨道对称性的光化学Cyclcobutene
威廉·j·利
加拿大化学学报,1993年,71年,147 - 155。
DOI:10.1139 / v93 - 021 # .Xm5OsJNKh24
本文的例子光化学几个环丁烯的开环。有时会发生,现实比理论的混乱。
非常感谢你这样漂亮的解释
很好. .我很容易理解谢谢。
非常可以理解的和明确的。没有留下任何东西也彻底解决所有方面怀疑