醇、环氧化合物和醚
劈理的醚酸
最后更新:2022年11月7日|
酸醚能够通过一个年代的乳沟N2或年代N1机制,根据不同的结构
- 醚不经历很多反应。
- 醚键的反应之一是,他们可以接受乳沟醇在强酸的存在,如你好,或强烈的路易斯酸,如三溴化硼(BBr3)。
- 这些反应涉及的质子化作用醚氧气,紧随其后的是一个年代N1或年代N2反应途径,根据结构(醚醇的主要倾向于接受通过年代乳沟N2,叔醇的醚往往通过年代经历乳沟N1)。
- 如果使用过量嗨的乳沟烷基醚类,产品往往是烷基碘化。
- 因为醚所有但最不起化学反应的酸性条件下,他们可以找到使用作为醇保护组。
表的内容
- 醚的反应在一次地方(har)
- 醚劈理的第一步是质子化作用
- 甲基和初级醚,乙醚乳沟的第二步是SN2
- 三级醚,乙醚乳沟的第二步是SN1
- 二次醚,第二步可能发生的途径
- 劈理的机制不对称醚很难概括(有一个例外!)
- 摘要:酸性醚的乳沟
- (高级)引用和进一步阅读
1。醚的反应在一个地方(har !)
我一直都盼望着今天的帖子很长一段时间!我们经历了很多不同的方法合成醚,最后我们去讨论我们得到的所有令人激动的事情做。
在这里,你一直在等待的时刻。醚的反应在一个地方:
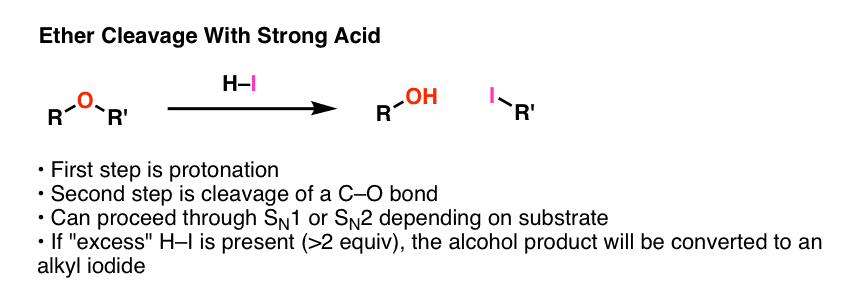
我们已经介绍了醚的反应。
谢谢你的关注。
是它吗?是的,真的:唯一重要的醚反应你需要知道…。如何打破他们。
(我只是把你的腿“令人激动的事情我们得到与醚”。)
这使醚最无聊的官能团有吗?是的! ! !(只要你不计算烷烃作为“官能团”)。
所以,你可能会问,有什么意义?
现在所有我要说的是,有些“无聊的很好”的时候。醚,稍后我们将学习,可能是有用的作为屏蔽“保护组织”(活性)醇。但那是以后的讨论。(看到的:保护组醇]
现在,让我们在如何挖掘醚裂解反应的作品,因为它确实有它的微妙之处。这个讨论应该很简单如果你一直沿着后,然而,因为它是要涉及到熟悉的质子化作用机制,SN1和年代N2。
2。酸性的乳沟醚的第一步是氧气的质子化作用
耐中性醚通常在替换的亲核试剂的反应——这是因为离去基团必须RO -,这是一个非常强大的基地。
出于这个原因,在任何的第一步醚乳沟被强酸质子化作用。为什么质子化作用帮助我们吗?记住,“共轭酸总是更好的离去基团”。质子化作用的醚允许卢武铉的损失离去基团,这是一个比RO -大大较弱的基础。这是我们下一步要设置——乳沟切断的债券。
通常的选择通常是氢碘酸强酸(你好)。它不仅是强大的(pK一个-10),我们会看到碘抗衡离子起着作用。
3所示。甲基和初级醚,乙醚乳沟的第二步是SN2
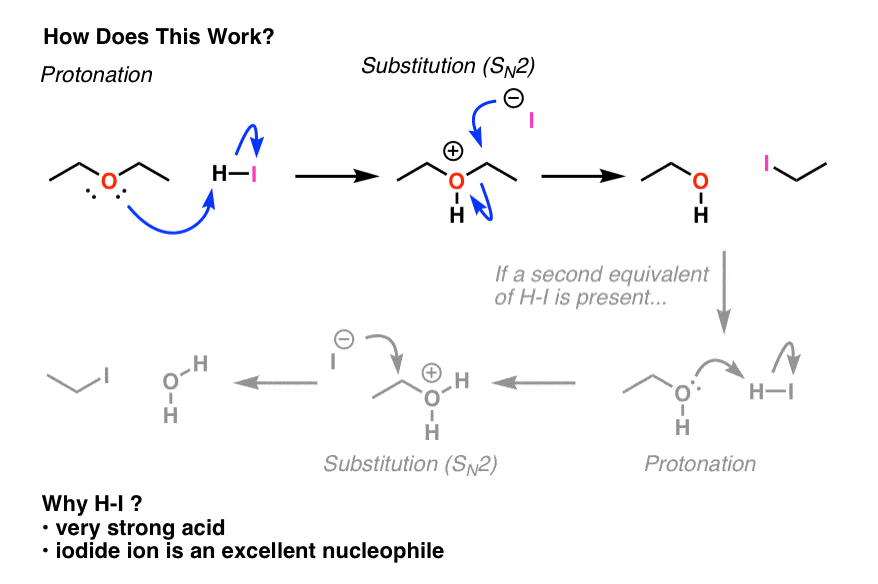
质子化作用后,接下来会发生什么?如果我们从小学开始醚就像乙醚,我们将会有一个好离去基团(卢)主要碳的存在一个像样的亲核试剂(碘离子)。听起来是不是很熟悉?它应该- - - - - -这些理想条件的年代N2的反应。这是发生了什么。
该产品将卢武铉和我。
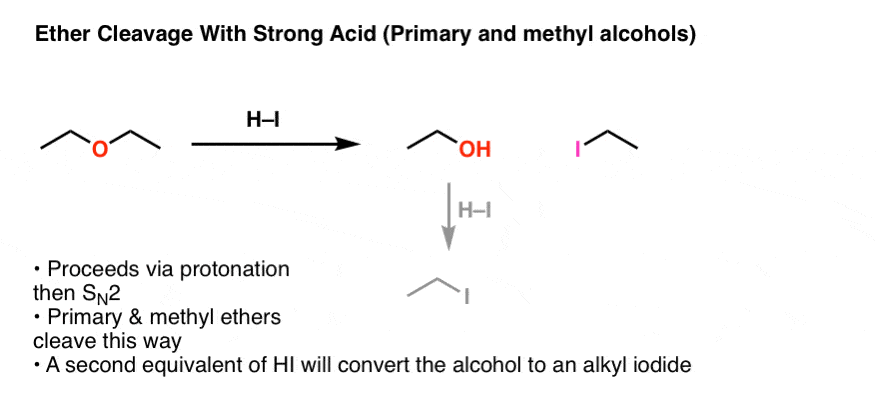
如果过量(2枚或更多)嗨,酒精能被转换成一个烷基通过两个后续步骤(碘化质子化作用/ SN2)。
这种“年代N2”途径将主导小学和甲基醚。
4所示。三级醚,乙醚乳沟的第二步是SN1
显然,年代N2不在这里,叔碳原子太妨碍背后攻击。然而,三级碳正离子是相对稳定的,和“电离”(即丧失离去基团留下一个酒精(R-OH)和叔碳正离子,然后可以被碘离子给我
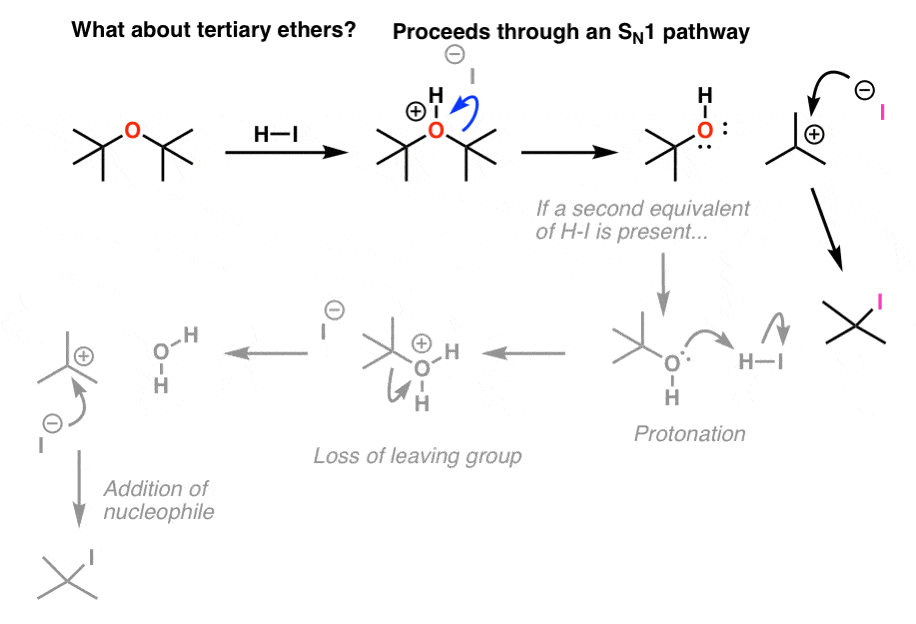
同样,如果存在过剩嗨那酒精将被转换成一个烷基卤化物。我们将会有更多的说在几个帖子。
5。二次醚,第二步可以进行的途径
二次醚呢?我没有一个好的答案。年代N1和年代N2是一个连续体。你可能会有一个混合物的年代N2和年代N1通道操作。如果有人告诉你他们能看一个醚像di -异丙基醚和年代N2或年代N1通路将100%占主导地位,这是不正确的。
6。劈理的机制不对称醚很难概括(有一个例外!)
一样棘手的情况下二次醚的混合醚。如果你有两个不同的基团的氧气(“不对称醚”)。哪条路是要休息吗?
例如,叔丁基甲基醚吗?当你把它酸,首先会发生什么呢?你做一个年代吗N2甲基碘化,或电离给一个叔碳正离子吗?
这是问题的类型不容易回答不知道实验的结果。
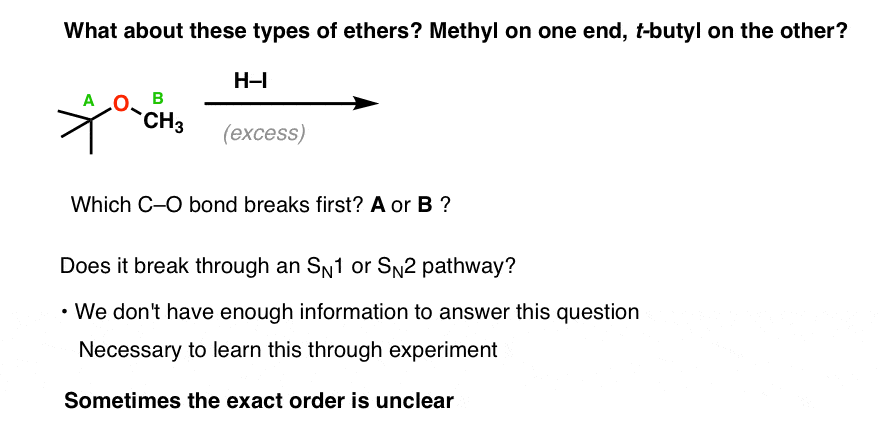
然而,少数情况下的混合醚哪里有一个直截了当的回答。
以这个问题为例。会发生什么呢?答案是非常清晰和100%的一种方法。看看你是否能做到。
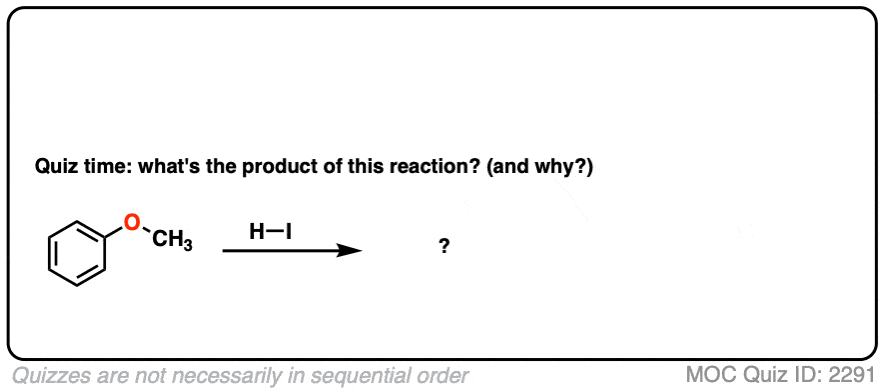 点击翻转
点击翻转
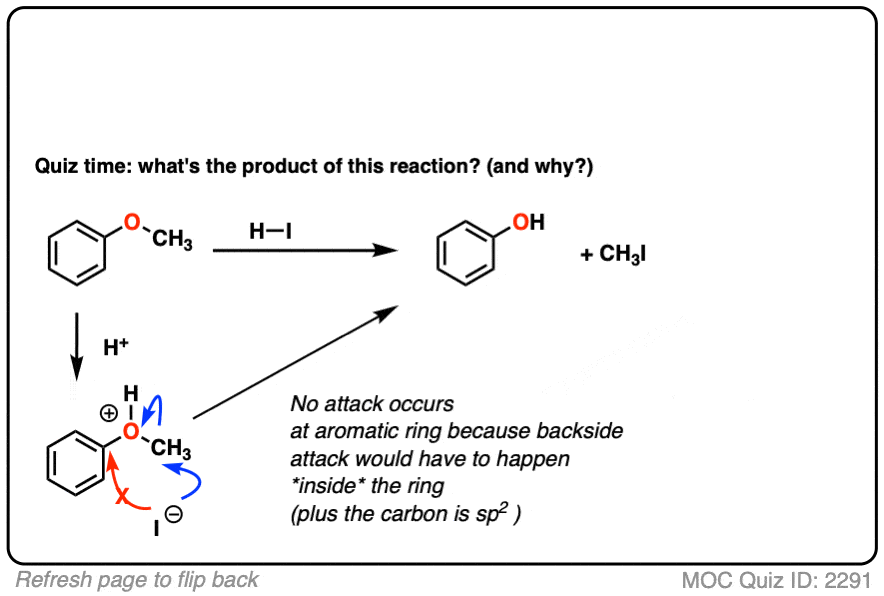
如果你好奇答案,你必须留下你的评论。
7所示。摘要:酸性醚的乳沟
好的。所以醚,迄今为止我们已经讲过,很无聊。但(和总有但是)——有一个特殊的醚类,事实上,非常有趣,非常被动。如果你覆盖烯烃,你见过他们,但在一个不同的名称。你能猜猜官能团我谈论吗?在下一篇文章!
在下一篇文章- - - - - -环氧化合物醚家族的离群值
笔记
(高级)引用和进一步阅读
醚广泛惰性很多条件,从而找到常用的溶剂(如。乙醚,四氢呋喃(四氢呋喃),二氧六环,glyme等等)。醚乳沟通常需要强酸和热量,这迫使条件。或者,可以使用硅烷试剂,在室温下反应。
- 一种新方法制备的有机碘化
赫尔曼·斯通和哈罗德SHECHTER
《有机化学》杂志上1950年,15(3),491 - 495
DOI:1021 / jo01149a008
而不是使用你好,这是昂贵的,可以使用磷酸+ KI的结合醚乳沟,你好原位。 - 1,4-DIIODOBUTANE
赫尔曼·斯通和哈罗德Shechter
Org。Synth。1950年,30.,33岁
DOI:10.15227 / orgsyn.030.0033
这个过程从有机合成可靠来源的独立测试实验室有机合成过程,演示了的乳沟四氢呋喃与回流强酸。 - 醚的乳沟溴化氢
主任罗伯特·l·波和米尔顿·e·富勒
美国化学学会杂志》上1957年,79年(9),2332 - 2336
DOI:10.1021 / ja01566a085
经典论文的乳沟醚与哈佛商业评论。下面是各种各样的论文使用silane-based试剂醚乳沟。诺贝尔奖得主已故教授乔治Olah在这个领域做了大量的工作在他的职业生涯。 - 劈理的酯类和醚Iodotrimethylsilane
谢霆锋洛克Ho博士教授乔治·a·Olah
Angew。化学。Int。。1976年,15(12),774 - 775
DOI:10.1002 / anie.197607741 - 合成方法和反应。62年。转换与三甲基/碘化钠,方便现场iodotrimethylsilane试剂
乔治•a . Olah Subhash c·纳b·g·巴拉罗姆古普塔和Ripudaman Malhotra
《有机化学》杂志上1979年,44(8),1247 - 1251
DOI:10.1021 / jo01322a012 - Trichloro(甲基)硅烷/碘化钠,一个新的特定选择的试剂醚的乳沟
乔治•a . Olah阿尔塔夫侯赛因,Subhash c·b·g·巴拉罗姆Gupta纳
Angew化学。Int。。1981年,20.(8),690 - 691
DOI:10.1002 / anie.198106901 - 硅烷/ iodine-based乳沟酯类在中性条件下和醚
Ho T-L。,Olah, G. A.
Proc。国家的。学会科学。美国。1978年1月;75年(1):4 - 6。
DOI:10.1073 / pnas.75.1.4 - 合成方法和反应;32:温和而有效的乳沟酯类和醚Phenyltrimethylsilane /碘试剂
g。,Ho T-L。
合成1977年,417年
DOI:10.1055 / s - 1977 - 24423 - 轻微的乳沟methoxymethyl (MOM)与溴化三甲基硅烷基醚
丹尼尔Delorme斯蒂芬•Hanessian伊夫
四面体。1984年,25(24),2515 - 2518
DOI:10.1016 / s0040 - 4039 (01) 81219 - 3
妈妈醚通常用作保护团体在有机合成-哦,所以妈妈醚的选择性去保护策略下温和的乳沟是无价的。 - 合成方法和反应;951年。铈铵Nitrate-Catalyzed氧化的乳沟烷基并与溴酸钠甲硅烷基醚
乔治•a . Olah b·g·巴拉罗姆Gupta亚历山大·p·冯
合成1980年;1980年(11):897 - 898
DOI:10.1055 / s - 1980 - 29258
这个不使用硅烷试剂,但仍然是一个有趣的试剂醚乳沟。
如果有共轭体系即(CH3) 2 c = CH-O-CH = CH2我们如何决定应该是碳正离子,双键会如何影响?
先生我们可以考虑溶剂在不对称醚键断裂的情况下? ? ?
确定sn1或sn2
与不对称di-alkyl醚很难预测。经常发生的是,过多的使用设定h,烷基碎片都转化为烷基碘化。
更容易与芳基烷基醚,这不会导致aryl-O债券的乳沟
如果我们带着异丙基甲基醚嗨,那么主要的产品是什么?请告诉
很难预测从第一原理不做实验。
然而,确定的一个方法是使用大量过剩你好,这将给你两个异丙基碘和碘甲烷。
苯酚+ Ch3I
我们将获得苯酚和methyliodide如果我没有错。
正确的。
什么反应,1,4 -二恶烷和1,在稀酸3-dioxane吗?
1,3-dioxane是一个缩醛,应该坚持在温和的酸性甲醛和1,探索。1,4 -二恶烷不是一个缩醛(这是一个醚)和要求苛刻的酸裂开(例如嗨)
什么反应,1、4二氧六环过剩嗨给吗?
每个切断债券换成我债券,你懂的。
在第4部分中,“如果存在过剩嗨,酒精会转化为酒精。”
这是卤代烷
固定的。谢谢你!
为什么妈妈保护团体通常与HCl删除吗?
妈妈不是一个醚,它是一种缩醛。更容易裂开。https://www.organic-chemistry.org/protectivegroups/hydroxyl/mom-ethers.htm
醚与盐酸反应吗?
一般来说,HCl将贫穷裂开醚比你好。
如果我们继续水解甲基乙烯基醚在酸性介质。我想知道的是我们应该首先使质子化醚或水解烯烃? ?
谢谢你的很棒的工作
乙烯基醚是一个特殊的例子。
第一步是烯烃的质子化作用,这是由于pi-donating氧气的存在异常反应。第二步是添加水,形成半缩醛,然后很容易水解。
先生如果使用浓缩的嗨如果任何变化是什么?
目前醇可能转换为卤代烃。
苯酚和methyliodide
有区别,当水嗨和无水嗨+醚使用吗?
在水嗨最强的酸可能是H3O +, (pka约3)而在无水嗨最强的酸可能是嗨本身(pka -10)。所以无水嗨更强大。
回答测试问题是苯酚+ CH3I
是的。
仍然不太确定这是如何工作的
不会甲基/乙基碳正离子反应与新形成的复合回馈回来原来的化合物,因为他们都是优秀的基地?
不是比水碘弱基地将使它成为一个更好的离去基团吗?
碘化,如何既一个好的亲核试剂(可极化的)和一个好的离去基团(可极化)加起来?哪个优先?
在段落“案例# 2 -叔醚”下,我相信“如果存在过剩嗨这酒精将被转换成一个酒精”应该读“酒精将被转换成一个烷基碘化”。
不要说这是唯一可能的反应一个有机金属化学!
好文章,谢谢。
哈哈。这是一个关键反应大学生学习入门课程。
是的,当然。稍微提前,你可以讨论的机制去甲氧基组BBr3,不是远离你所写。
真的!
这篇文章是伟大的。谢谢你的分享。希望听到你更多的消息。
第一步是氧气的质子化作用,在后者留下一个正电荷。
第二步当然有两种可能的方法:
——Sn1反应与苯酚或甲醇作为离去基团,形成一个相当不稳定的甲基阳离子或一个很不稳定的阳离子苯,respectivley。两种方法似乎不像第二种方法合理…
——的Sn2反应。质子化作用后的氧气,有一个亲核攻击的methylcarbon碘化,生成苯酚作为离去基团和碘甲烷。
另一个可能的考虑将碘离子的亲核攻击,而富电子芳香碳与氧。那就´t是一个合理的机制。
正确!
为什么苄基的阳离子不稳定?我认为这是由于共振稳定。
我认为phenylmethylether反应通过SN1机制,以便得到我和甲基苯哦
啊,你叫什么”苄基的“碳实际上是苯阳离子(C6H5 +)。碳正离子的p轨道在同一平面上的氢苯环——垂直于π键,能够稳定通过共振。
我们称之为“苄基的“碳其实是C6H5CH2 +。这有碳正离子邻苯基环,可以稳定的共振。
我应该写一篇常见的混乱。
实际上,你必须,因为它是一个主要的混淆人们对苄苯组
是的,这只是其中的一个事情你必须习惯,继续前进。
是的他决定“苯”还C6H6 C6H5是“苯”组和“苄”集团与甲基苯附加到戒指吗?我认为这是一个来源的混乱,许多新的O-chem。
是的,绝对!
我仍然不知道为什么它是假定的Sn2反应methylcarbon(而不是环)将受到碘?这是做简单的Sn2反应的特点,我错过什么?我认为可以形成碳正离子在“方向”,因此碘可以攻击任何一方。
回忆很重要的碳正离子稳定性影响因素可能SN1 / SN2期间学到的。和替换的碳碳正离子稳定性增加,所以比甲基叔碳正离子更稳定的碳正离子。以来的SN2位阻敏感的亲核试剂必须做背后攻击,所以甲基比三级(初级)要快得多。
底线是,甲基碳正离子不会形成,SN2将主导和最快的SN2甲基碳会发生。sn2芳环上是不可能的,因为空sigma星轨道(亲核试剂需要攻击)被埋在中间的芳环,因此无法访问)。
另一个有用的文章。关于这个问题最后,你好会增加苯甲醚给碘苯?
思考的SN2反应。它必须经历背后攻击。是一个SN2比另一个更青睐吗?
的产品肯定是苯酚…引起酚一旦生成,它不会被转换成碘化合物:)
苯酚确实是一个产品。
我想说苯酚形成由于苯基碳正离子或苯基碳正离子字符会比甲基碳水化合物更不稳定的阳离子。因此苯酚和甲基碘化形成。
它不会通过甲基阳离子,它会通过SN2。