烯烃的反应
m-CPBA (meta-chloroperoxybenzoic酸)
最后更新:2023年5月22日|
m-Chloroperoxybenzoic酸(米- - - - - -CPBA)的环氧化作用烯烃
- 米- - - - - -CPBA(元-chloroperoxybenzoic酸)是一个有用的试剂对环氧化合物的形成烯烃(注意——通常称为,m-chloro每苯甲酸,没有“氧”)
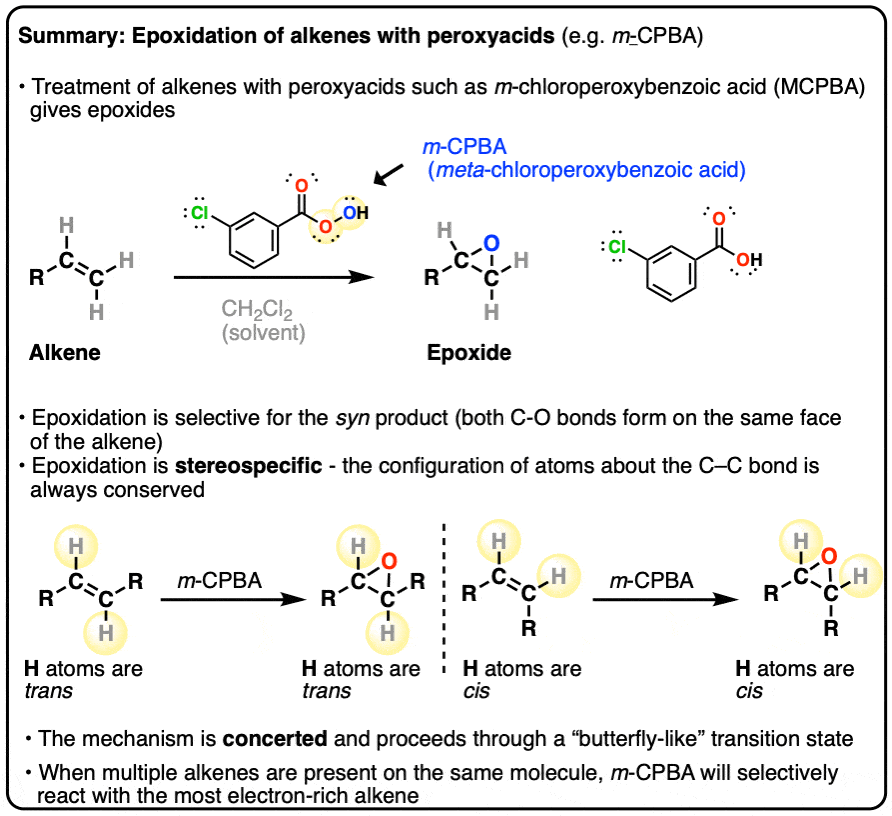
- 在这个反应中,碳碳π键坏了,和两个新的碳氧单键形成相同的脸烯烃π键。因为债券形成相同的脸,这是一个例子syn加法。
- o - o键的弱者米- - - - - -CPBA也坏了。peroxyacid的-哦是新的氧的来源环氧
- 环氧化作用的烯烃与m -CPBA的一个例子吗立体定向的反应。原子的碳碳键的配置一直是守恒的。通过协同过渡态反应所得。
- 等peroxyacids过乙酸、过苯酸、和trifluoroperacetic酸试剂的环氧化作用也是有效的烯烃。
- 炔烃不进行反应,米- - - - - -CPBA给环氧化合物
- m -CPBA也有用Baeyer-Villiger氧化,反应转化为酮酯类(更多信息,见后Baeyer-Villiger反应]
表的内容
1。与Peroxyacids烯烃的环氧化反应
当烯烃peroxyacids如对待吗元-chloroperoxybenzoic酸(米- - - - - -CPBA),形成两个新的切断债券和碳碳π键坏了,导致的形成环氧。(o - o键从一个m-CPBA也坏了,中氧的来源是什么环氧。副产品是m-chlorobenzoic酸)。
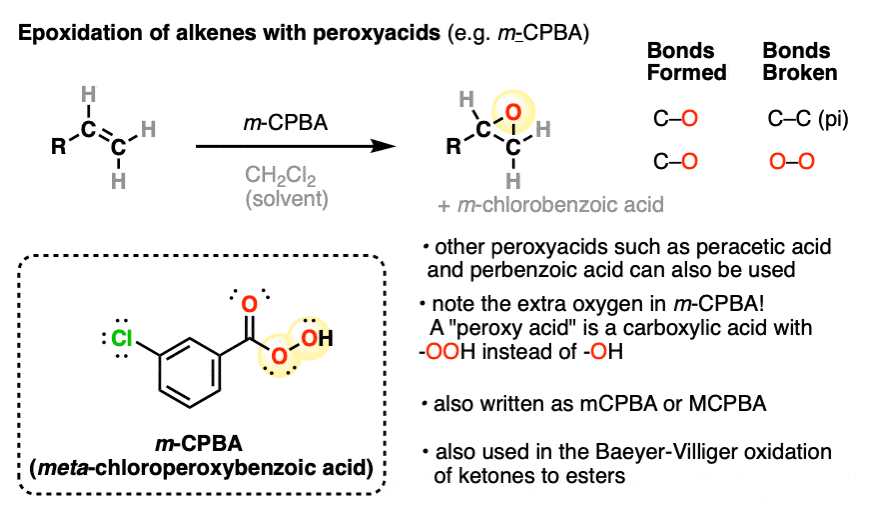
也称为环氧乙烷,环氧化合物三人环醚。自内心的环氧化合物的键角(约60°)显著偏离首选四面体几何在碳(109.5°),他们拥有可观环应变(约13千卡每摩尔),并进行大量的有用的开环反应与亲核试剂。(更多关于环氧化合物的反应,看到环氧化合物醚家族的离群值]
环氧化作用的烯烃与peroxyacids如米- - - - - -CPBA总是发生在这样一种方式,切断债券形成的相同面对烯烃,结果被称为“syn添加”。
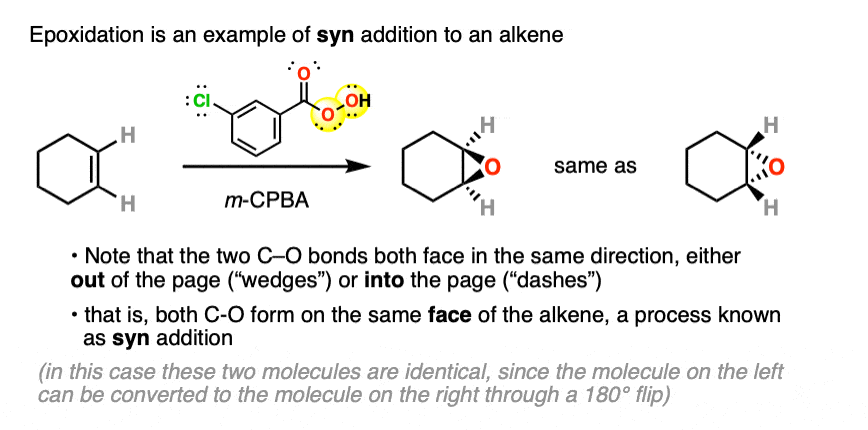
你可以告诉这之外syn因为新的切断债券这两个画的是“楔形”(指出页面的)或“破折号”(指成页面)。
在这种情况下,这两个产品是相同的,因为分子旋转180°导致相同的产品(见下文)
通过GIPHY(看看如何不开心这些塑料碎片——模型工具包真正帮助您可视化环应变:-))
在其他许多情况下,这将导致一对的形成对映体或者diasteromers,取决于结构的开始烯烃。
环氧化作用的烯烃与peroxyacids从来没有结果反加法。
它是不正确的画这个环氧化反应的产物是一个切断“楔形”和一个“缓冲”切断,因为这代表反加法。
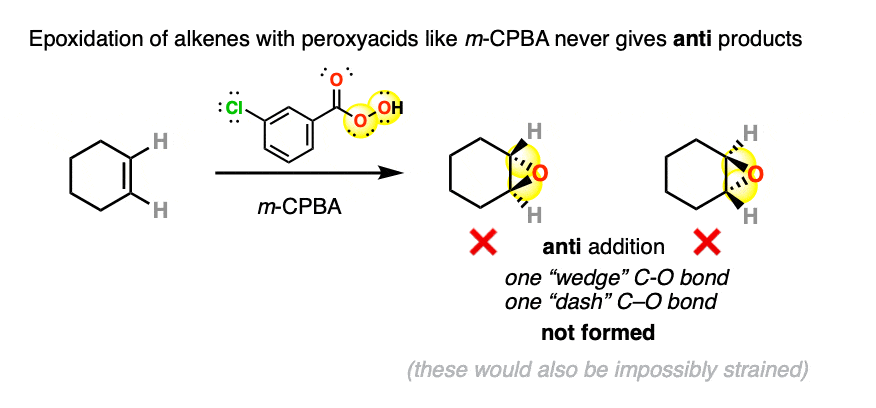
(顺便说一句,如果你试图让一个模型,您将看到,这一结果也会无比紧张)
2。烯烃的环氧化反应是立体定向
在环氧化反应中,配置的原子烯烃总是守恒的。
例如,反式烯烃下面给只有的反式产品(作为一个平等的混合物对映体)。注意,在产品一个,反式安排碳氢键的碳碳键是守恒的。
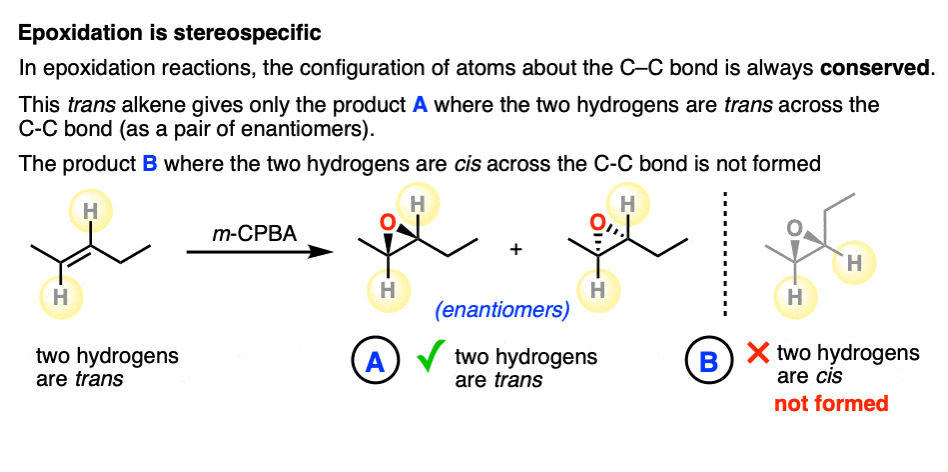
该产品B这两个碳氢键在哪里吗独联体对不形成碳碳键。(注意,这个产品B将产品的非对映异构体一个)。
同样,独联体烯烃只给了产品B。(产品一个,非对映体的产品B,都是不形成。)
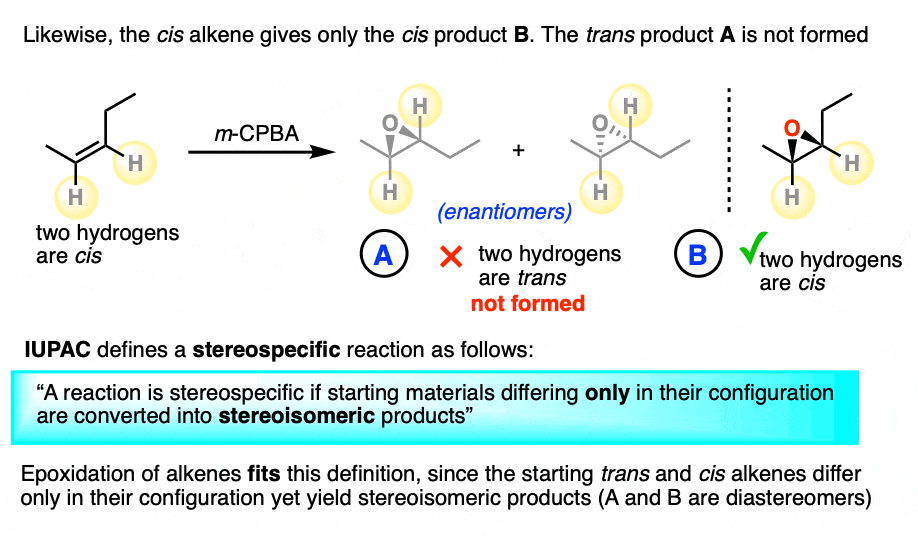
自从开始反式和独联体烯烃只有在它们的配置不同但收益率产品立体异构体,环氧化作用烯烃因此,的一个例子吗立体定向的反应。(看到IUPAC定义]
 点击翻转
点击翻转
3所示。烯烃的环氧化反应的机理m -CPBA
既然我们已经确定了债券形式和决裂,和预期的立体化学反应,我们可以开始问自己这个反应如何作品。
同位素标记研究可以验证的氧气环氧来自于哦peroxyacid,不内部连接到C = O。
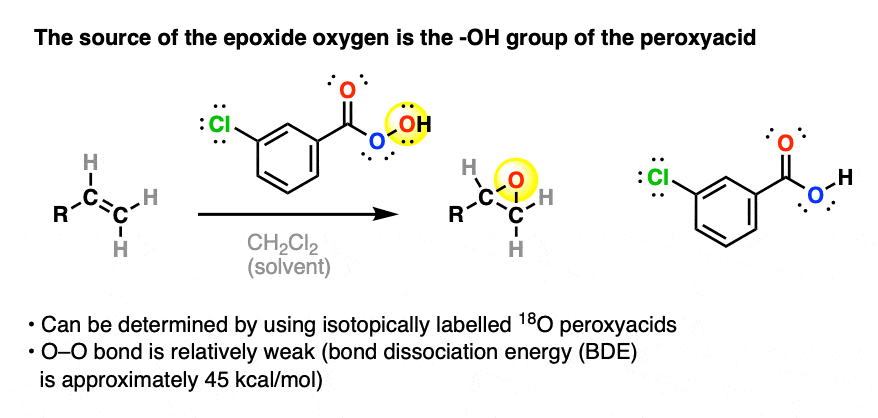
反应的驱动力之一是相对较弱的oo的破损和碳碳π键(债券dissocation能量约45千卡每摩尔和60千卡每摩尔,分别),以换取两个相对强劲切断σ键(约90千卡每摩尔)。
的过渡状态的反应米- - - - - -CPBA(和其他peroxyacids)烯烃被称为“蝴蝶机制”,由于四(!)部分债券在中央氧给large-winged昆虫的出现。
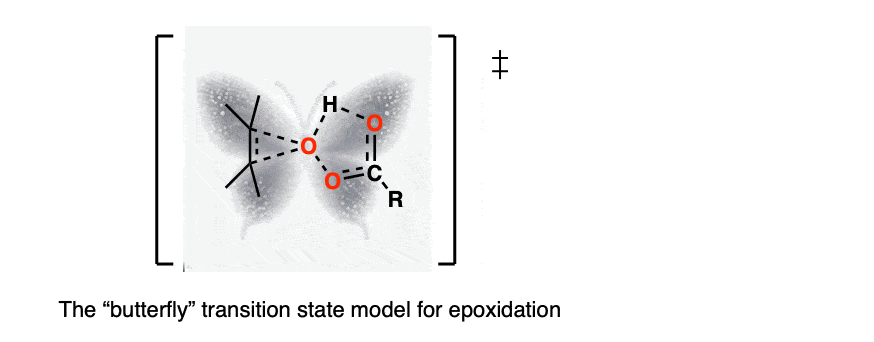
这个反应让我投票给最繁忙的一步arrow-pushing机制的介绍有机化学:
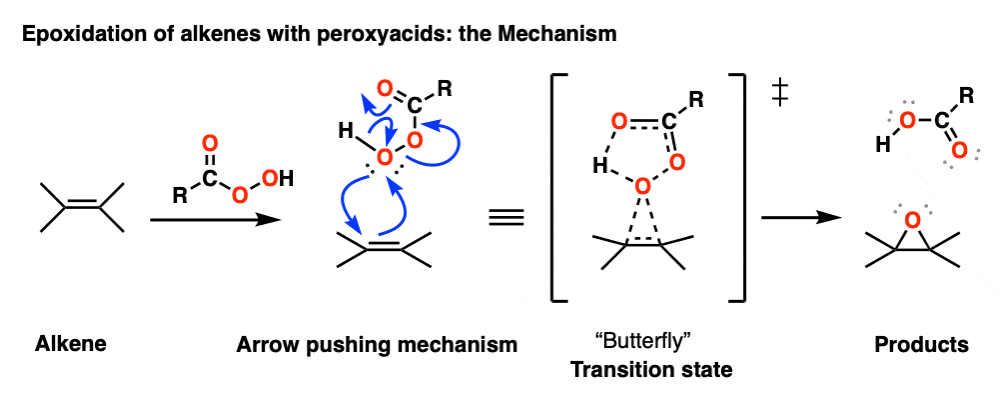
让我们打破在这个发生的每一件事一个(!)步骤:
- 碳碳π键的断裂
- 两个新的碳氧单键形式
- (弱),债券了
- 与此同时,由此产生的羧酸转置:新的切断π键形式,而现有的切断π键作为基地移除一个质子从终端氧气。
这个“蝴蝶”机制占实验观察结果如下:
它还占反应的定向性。我们会不期望通过碳正离子反应所得中间立体定向,例如。(盐酸的反应烯烃例如,不是立体定向)
两个额外的事实值得注意。
4所示。烯烃的反应?
假设我们有一个分子包含多个碳碳处理的π键米- - - - - -CPBA。
有可能得到环氧化作用发生在只有一个吗烯烃π键,或者我们只是最终的产品?
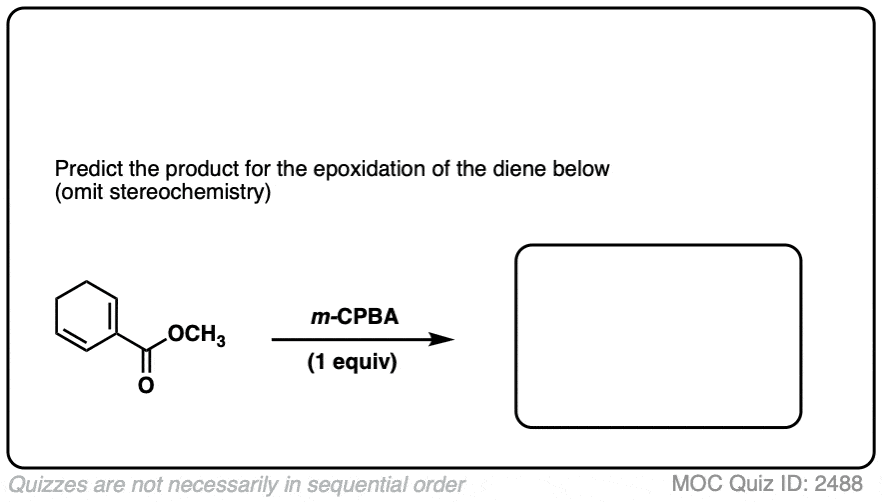
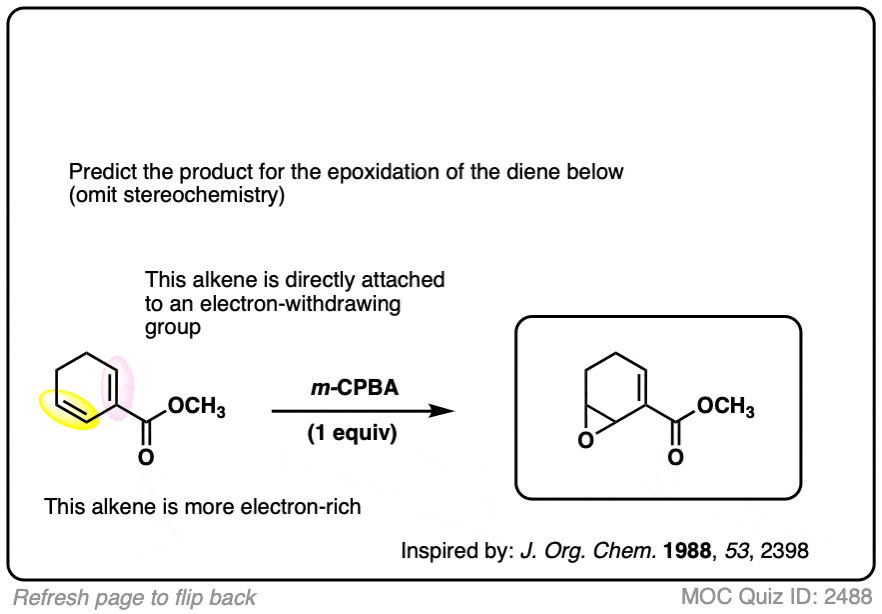
观察到的是,最是什么电子的烯烃进行环氧化作用第一个非常好的选择性。
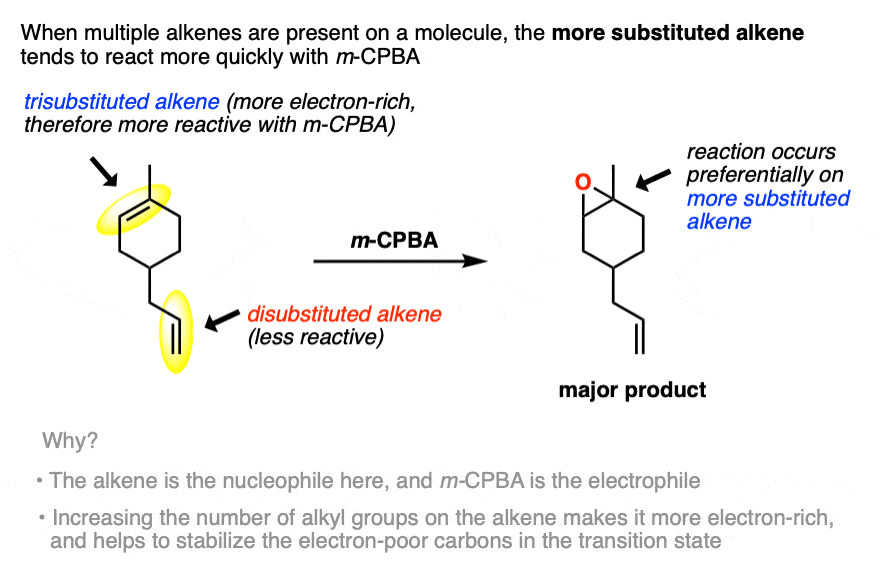
“最富”通常意味着烯烃这最碳原子直接相连烯烃(即“大多数”代替),只要他们不吸电子集团。
例如,在烯烃以上,三代的烯烃优先进行环氧化作用而mono-substituted烯烃是不变的。
这似乎是反直觉的,因为我们可能期望更多的替代烯烃更多的位阻,但在实践中反应的速率更敏感比立体电子效应(即电子与electron-poor)的影响。(注2][裁判]
看看你是否可以应用这个概念在以下问题:
 点击翻转
点击翻转
5。立体选择性
当环氧化作用在执行烯烃包含预先存在的手性中心,还有潜在的立体异构体的形成。这是因为的两副面孔烯烃不会等价空间环境,从的角度亲电试剂(如米- - - - - -CPBA)。
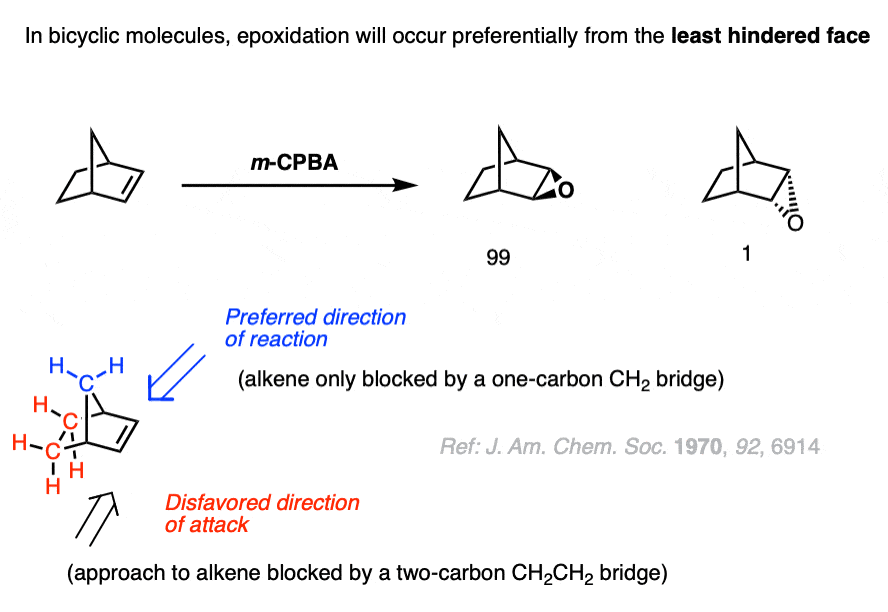
一个特别引人注目的例子是二环烯烃在下面。时处理米- - - - - -CPBA99:1混合物的产品(非对映体)组成。的高选择性的原因亲电试剂(米- - - - - -CPBA只遇到一个CH2集团在其方法顶面(喜欢),而它遇到二碳桥底部脸上方法(不好)。
在这种情况下,结果是一个99:1比率的产品支持攻击最阻碍的烯烃。
有一个更系统的方法命名的面孔烯烃,(被称为再保险和Si),目前我们不会进入。
6。其他试剂环氧化反应
其他peroxyacids用于环氧化反应,如过氧乙酸、peroxybenzoic酸,trifluoroperoxyacetic酸。
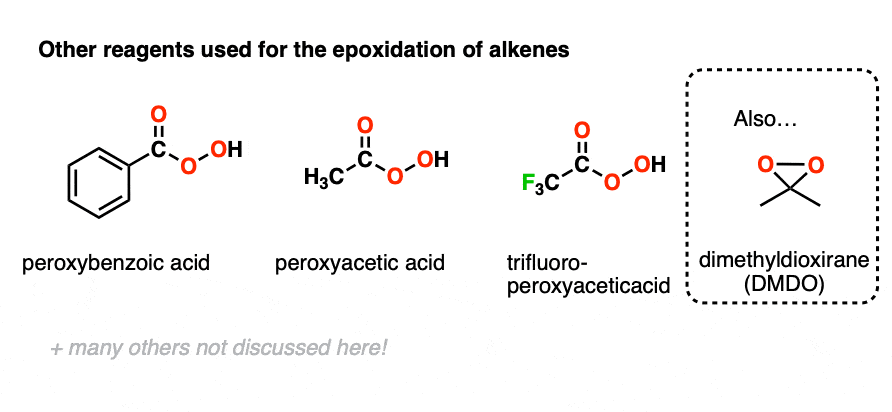
就像使烯烃多电子反应的速率增加,它也被观察到,吸电子试剂添加到亲电试剂(peroxyacid)增加了反应速率。
环氧化作用的烯烃peroxyacids自1909年以来已众所周知,但只有在1960年代米- - - - - -CPBA开始获得广泛使用,大大改善了环氧化反应的范围。(注3]
此外,尽管他们不是经常覆盖着入门课程,还有其他epoxidizing的方法烯烃不涉及peroxyacids。例子包括金属,如钒、钛、锰和其他过氧化物的存在(或氢过氧化物),或者使用试剂如dimethyldioxirane (DMDO)。
7所示。沙普利斯不对称环氧化作用
拆分的环氧化作用烯烃也是一个已知的过程。
拆分反应,开始于一个非手性分子并添加一个手性试剂,选择性攻击的起始物料,导致产品丰富的对映体的混合物。(一个不能使用任何手性试剂——有很多参与得到正确的配方试验和错误)[注]
一个著名的拆分环氧化的方法烯烃是由k·巴里•沙普利斯(斯克里普斯),被称为沙普利斯环氧化作用。
沙普利斯环氧化作用涉及到治疗的烯丙基的酒精钛异丙醇盐与一组神奇配方(Ti (O我- - - - - -Pr)4)]t-butylhydroperoxide(氧化剂),这取决于对映体,(,年代)或(R, R)酒石酸二乙酯(或di -异丙基酒石酸,在某些情况下)
这是一个简单的例子。
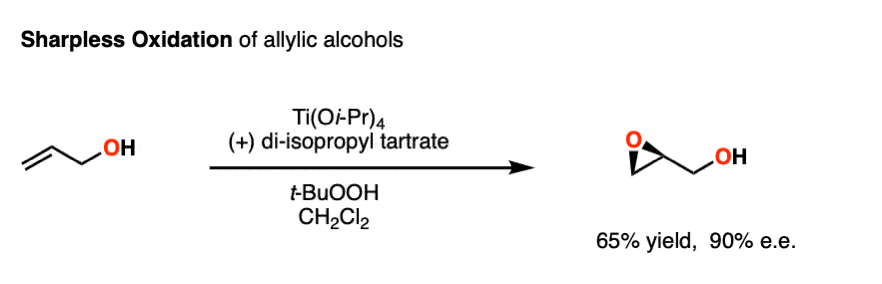
反应不是拆分不哦组碳毗邻烯烃。(这类分子被称为“烯丙基的醇”)。需要协调的羟基钛和直接环氧化作用。
沙普利斯更多的环氧化作用,我强烈推荐这些笔记(化学115年,哈佛大学教授安德鲁·g . Myers)。
笔记
对于本文,百科全书的有机合成试剂是非常有用的在archive.org上看到),3月的安德鲁·迈尔斯教授先进的有机化学和化学115(哈佛大学)。
注1。一个典型的溶剂对环氧化作用米- - - - - -CPBA是相对非极性溶剂二氯甲烷。有趣的是,环氧化作用的速率是氢键溶剂要慢得多,因为这些往往会破坏的内部氢键“蝴蝶”过渡态。(裁判]
注2。这让我想起了一个老笑话在有机化学研究生:如果你问一组会议上解释为什么一个特定的反应发生(或不发生),股票的回答是,“电子和立体的结合”。涵盖所有基地!
注3。的反应性米- - - - - -CPBA高度优于peroxybenzoic酸,但仅在1963年之后才开始广泛使用。对于一个比较peroxybenzoic酸和的范围米- - - - - -CPBA,比较裁判]和[裁判]-m -CPBA提供清洁和更快的反应,以更大的范围。这也是一个很好地白色结晶固体。商用m -CPBA由大约80%米- - - - - -CPBA其余的是米酸氯苯。它可以进一步纯化处理缓冲区,但与高纯度应格外注意米- - - - - -CPBA由于其潜在的爆炸特性。
注4。给一个想法的试验和错误的发展这个反应,看到沙普利斯诺贝尔演讲。(第一个,在2001年,不是第二个从2022年开始)。两个完整的论文(在这里]和[在这里在决定反应的机制是细致的经典例子,系统的实验工作。
测试你自己!
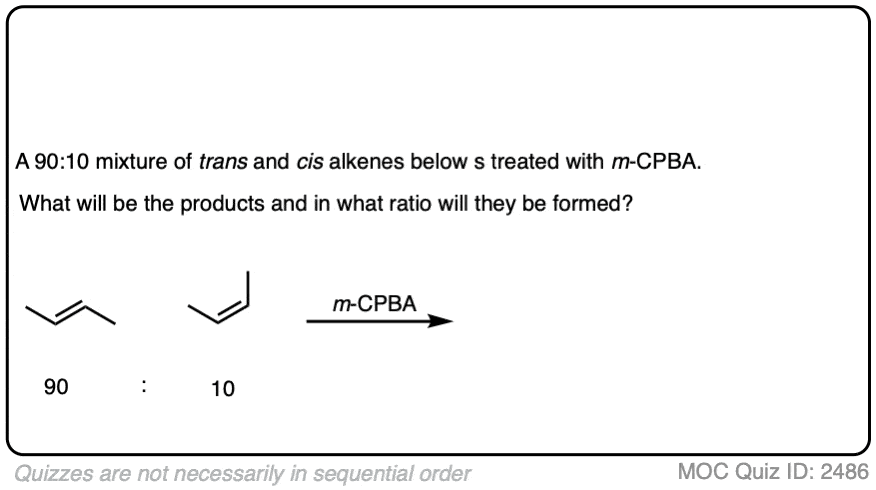
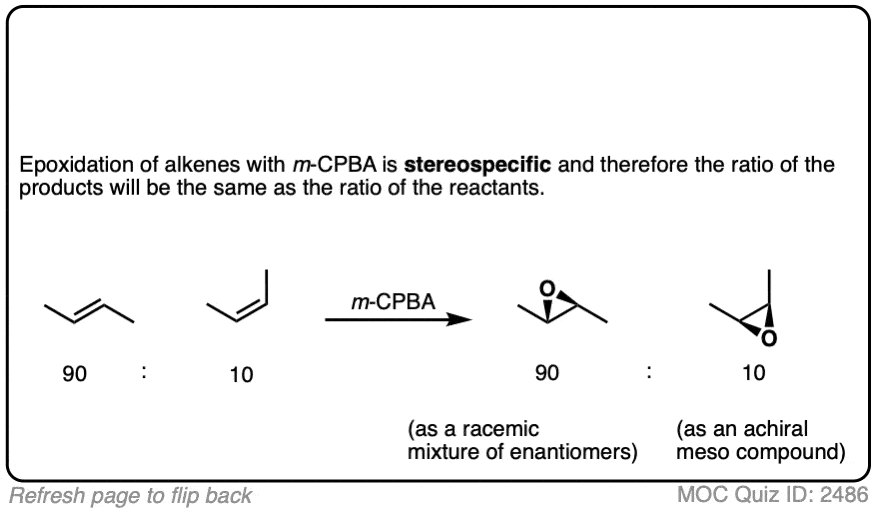
这里有一个测试在识别产品的环氧化反应之间的关系。(注意:这些类型的测试的例子,看到这篇文章”什么是外消旋混合物”。)
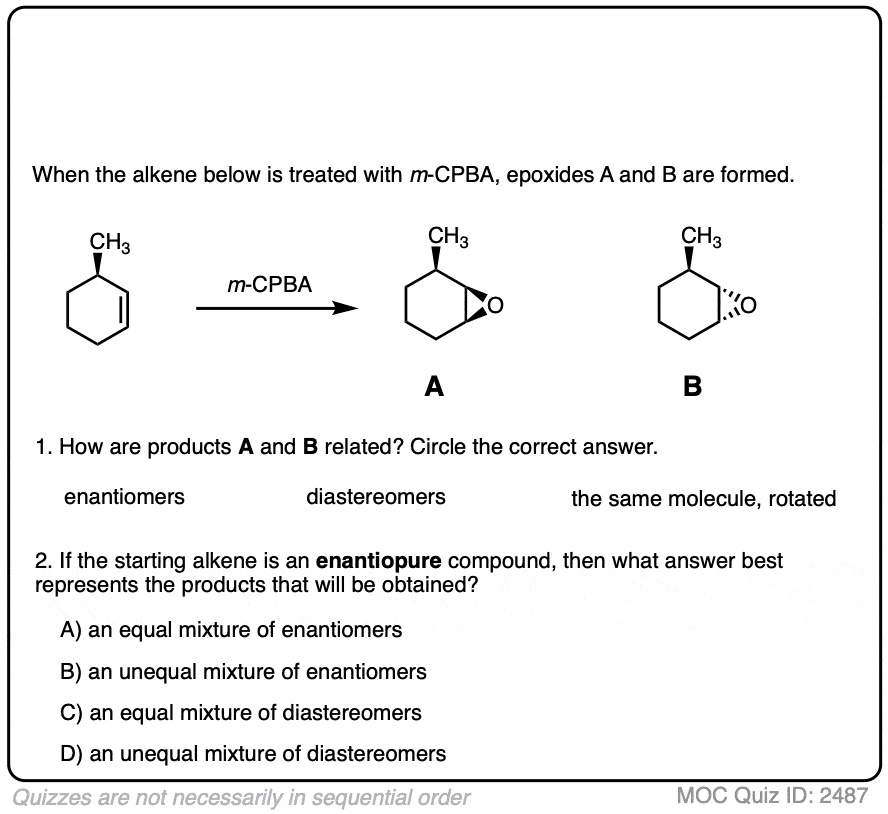 点击翻转
点击翻转
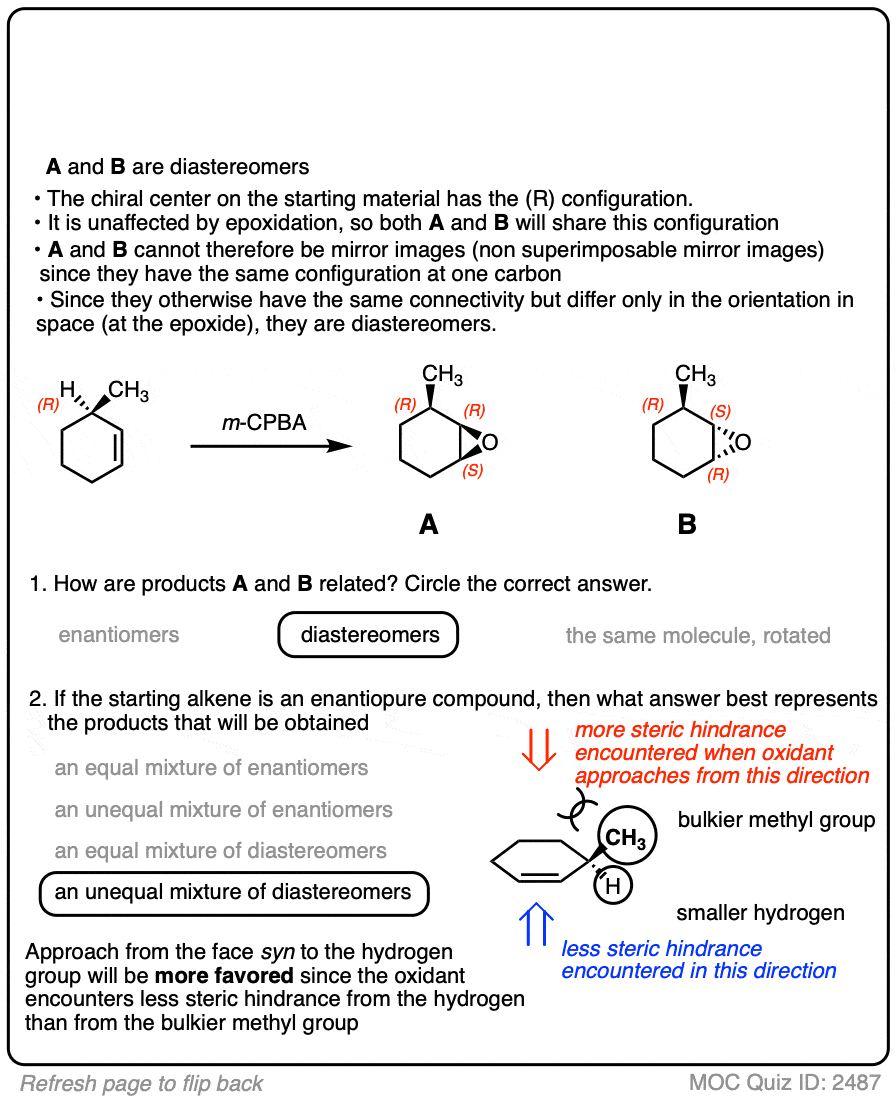
(高级)引用和进一步阅读
(高级)引用和进一步阅读
- 氧化ungesattigter Verbindungen mittels organischer Superoxyde
尼古拉斯Prileschaev
化学。的误码率。1909年,42,4811年。
DOI:10.1002 / cber.190904204100
这个反应(环氧化作用烯烃高酸)也被称为Prizelhaev反应后的作者。 - 的氧化烯烃与过苯酸。动力学的研究
m·林奇和k h . Pausacker。
j .化学。Soc。1955年,1525 - 1531。
DOI:10.1039 / JR9550001525
最早的报纸在环氧化作用米- - - - - -CPBA,比较其与其他替代高酸反应。正如所料,peroxyacids的反应是增加了吸电子集团。 - m-CHLOROPERBENZOIC酸
理查德·n . Steppel理查德·n·麦克唐纳和詹姆斯·e·多尔西。
Org。Synth。1970年,50岁,15岁。
DOI:10.15227 / orgsyn.050.0015
一个可靠的准备米- - - - - -CPBA(商用)有机合成。这个过程显示,米- - - - - -CPBA并不像一个纯化合物的准备(这是一个混合的过酸和酸,和商业样品可能含有残留水稳定性)。 - 环氧化作用与m-Chloroperbenzoic酸
尼尔森·n·施瓦茨和约翰·h·布隆伯格。
j . Org。化学。1964年29日,(7),1976 - 1979。
DOI:1021 / jo01030a078
本文描述了机械的研究米- - - - - -CPBA氧化,证明离子中间体不参与反应,溶剂极性不敏感率。 - 化学进展的记录
巴特利特,p D。
化学。掠夺。1950年,11,47岁
(链接]
这是出版p·d·巴特利特教授描述了“蝴蝶机制”m -CPBA环氧化作用。 - MCPBA环氧化作用的烯烃:重新调查率和电离势之间的相关性
泰迪·g . Traylor母婴感染Kim和查尔斯·l·佩兰。
j。化学。Soc。1998年,120年,(37),9513 - 9516。
DOI:1021 / ja981531e
一个有趣的论文描述了动态测量方法的发展不同的环氧化反应的速率烯烃与米- - - - - -CPBA。 - 环氧化作用的实验几何过渡状态
丹尼尔·a·Singleton,史蒂文·r·Merrigan博士曾剑Liu和k·n·胡克。
j。化学。Soc。1997年,119年,(14),3385 - 3386。
DOI:1021 / ja963656u
结合实验和理论研究环氧化作用的过渡状态,表明两个切断键形成事件几乎是同步的。 - 环氧化作用的机理烯烃通过高酸
v . g . Dryuk。
四面体。体积32问题23日,1976年,2855 - 2866。
DOI:10.1016 / 0040 - 4020 (76)80137 - 8
讲述了作者对环氧化作用的动力学研究的工作烯烃与高酸为了确定确切的机制。 - 过氧化物的键离解能再现
https://pubs.acs.org/action/showCitFormats?doi=10.1021/acs.jpca.0c02859&ref=pdf - 不对称环氧化作用的第一个实用的方法
Tsutomu Katsuki和k·夏普
美国化学学会杂志》上1980年102年(18),5974 - 5976
DOI:10.1021 / ja00538a077
Katsuki和沙普利斯的第一份报告从1980年的不对称环氧化反应烯丙基的醇。
那么如果有酮等乙烯基群1-phenylbut-3-en-1-one,有环氧化作用或亲电加成吗?
除了与富电子烯烃环氧化作用不会发生。最可能的结果是一个Baeyer-Villiger。
如何满足mcbpa如果sm材料酸和产品还酸吗
刚和亚硫酸氢淬火的氧化剂,酸化和提取。您可以运行列羧酸如果你洗脱液酸化。
为什么m-CPBA作为亲电试剂在环氧化反应?
o - o键很弱的(约35千卡每摩尔)和羧酸盐是一个很好的离去基团。所以在终端氧亲核攻击非常容易。
嗨! ! !mCPBA能够与炔烃反应吗?我感觉没有但我不是100%确定(我想确保我以后不要误会这考试)。
有趣的你应该问,我是非常接近的东西了!为你的目的,我想说,“不”,因为与炔烃反应mCBA不是很有用。
然而…与炔烃反应mCPBA *并*发生非常之旅。我可以99.9%确定它不会出现在考试中。https://imgur.com/a/Ibvqy8y
发生了什么当一种化合物在反应与mcpba已快键和酮moeity
视情况而定!我曾经使用mCPBA已二烯和两个酮的反应。二烯是电子(连接到一个酯)和酮的只有一个是真的。所以做了一个Baeyer-Villiger !
你好,
我有一个问题关于环氧树脂。
我想形成一个环氧树脂在我左边一个右边酒精和dubble绑定。所以对于一个例子[(2 r, 3 s) 3-allyl-2-oxrianyl]甲醇。有人能帮助我吗?因为我知道如何形成但不是左边右边。
听起来像缩水甘油。你可以买。
https://www.google.com/search?q=glycidol&rlz=1C5CHFA_enUS503US504&oq=glycidol&aqs=chrome. . 69 i57j0l7.1372j0j4&sourceid = chrome&ie = utf - 8
o在mcpba电子不足和y电子defficient plzz答吗
回答我:什么是更好的离去基团:R-CO2(-)或(-)?这才是你的答案。
我知道过酸和苯的反应会给我epoxystyrene。然而,在
是一个由产品苯甲酸在大约25%的收益率。什么是这个反应的机制。
你确定这不是一个从peroxyacid副产品吗?
苯乙烯+过苯酸为氧化苯乙烯的收益率。看到的:
http://www.orgsyn.org/demo.aspx?prep=CV1P0494
如果酮是循环,就像4-methyl环己酮吗?环打破吗?
好问题!你形成内酯-环酯——在这种情况下7-membered戒指。
的反应不同当mCPBA在酸性或碱性溶剂还是严格依赖于反应物被顺/反式
环氧化反应是立体定向。在相同的条件下,顺式烯烃和反式烯烃的环氧化反应将给两个立体异构的产品。这是真的mCPBA是否以酸性的形式使用,或者如果一个温和的基础(例如NaHCO3)是用于mCPBA促进反应。
为什么氧与氢作为亲核试剂而不是其他氧气吗?
因为在最初的亲核攻击,可以迅速中和氧与氢质子,而“氧气”不能回到作为一个中立的物种没有打破切断和移植性。试着画出箭头与氧气反应。
做迁移能力在拜耳村民氧化苯大于H . .吗?
如果是的那么ph-CHO /酸不会给ph-COOH吗? . .请回复
不,H的迁徙能力最好。BV的氧化醛将羧酸。
环氧化合物可能呈现出几何异构? ? /
两个切断债券环氧总是在相同的脸。
为什么每酸氧氧键太弱? ?
oxygen-oxygen债券疲软是由于孤独之间的斥力对驻留在相邻的氧。
嗨,我有一个问题,
为我的硕士项目mCPBA没有工作我烯烃环氧化合物,我该如何解释?(这是一个一个烯丙基醚)的环氧化反应
和有没有引用我可以用来解释这一机制?
谢谢你:)
很难回答这样的一个一般性的问题,没有更多的细节。有很多原因可能不会起作用,如试剂的质量,电子密度的烯烃,烯烃立体效果,等等。
为什么只有元Cpba使用。为什么不使用对位Cpba氧化吗?
使用元异构体,因为它是便宜。很容易准备的氯化(廉价)苯甲酸,由于羧酸meta-directing组。电子撤回组添加到芳环会使它更活泼。
如果有两个双键的呢?会有更多的aklye卤化物得到优先?
双键连接到多个烷基组(或更少的氢,如果你喜欢)优先级,因为它会更富。
这对我来说似乎有点奇怪,因为如果你看看产品的稳定性,有注意超共轭会更稳定,而在12月提到意味着少双键连接烷基组会喜欢?
这是一个亲电加成反应吗
是的,这是一个加成反应,试剂(mCPBA)是一个亲电试剂。这将有资格。