自由基反应
奖金主题:烯丙基的重组
最后更新:2022年12月7日|
- 在烯丙基溴化反应,碳氢键的烯丙基的碳分解,形成一个新的C-Br债券。
- 这个反应有时发生烯丙基的重排。即新C-Br债券形式的结束碳π键,和π键移动,这样原来的sp3杂化碳成为碳氢键烯基碳。
- 这可以支持的情况下代替双键的结果(即。扎伊采夫规则)
表的内容
1。烯丙基溴化,给出了两种产品
今天的话题流从最后一篇文章的主题,bdapp平台烯丙基溴化。它在烯丙基溴化反应发生重组。
在过去的文章烯丙基溴化使用的例子实际上是非常简单的。
例如,如果你带环戊烯和治疗国家统计局光和CCl四氯化碳溶剂((高压)4),你得到这个产品:
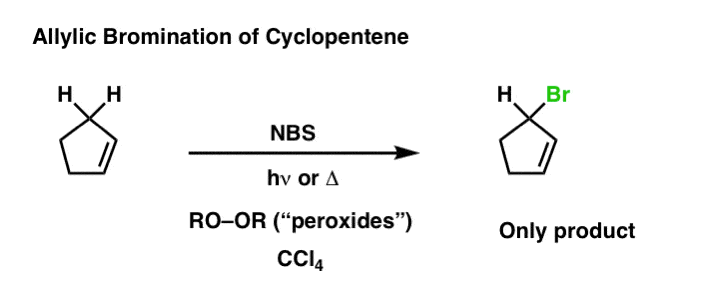
没有其他的可能性。
现在让我们扩展基质的复杂性。只是替换C-CH碳氢键之一3债券,做相同的反应。
在这里,我们不是一个产品,但是两个。注意,我们的主要产品是不同的!
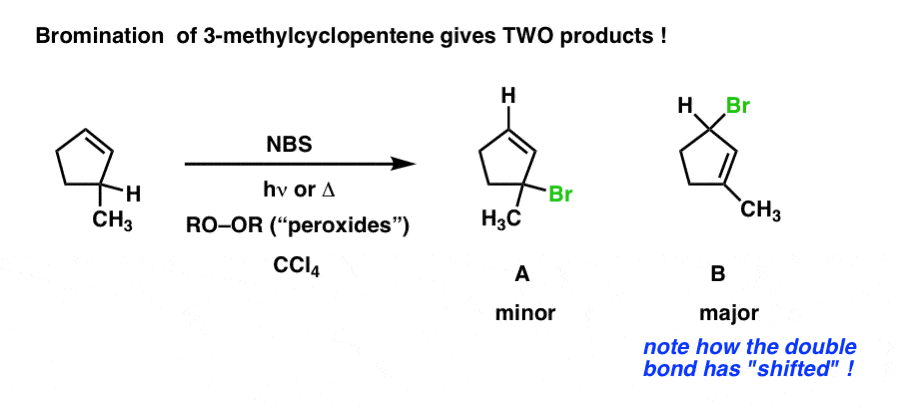
这是怎么回事?
2。“产品B”就是一个例子,烯丙基溴化伴随着烯丙基的重排
让我们想想这个反应的机制。首先要发生什么(当然,启动后)?
删除最弱的碳氢键的溴激进!这留给我们一个烯丙基的激进的,然后与溴反应2给我们的产品。
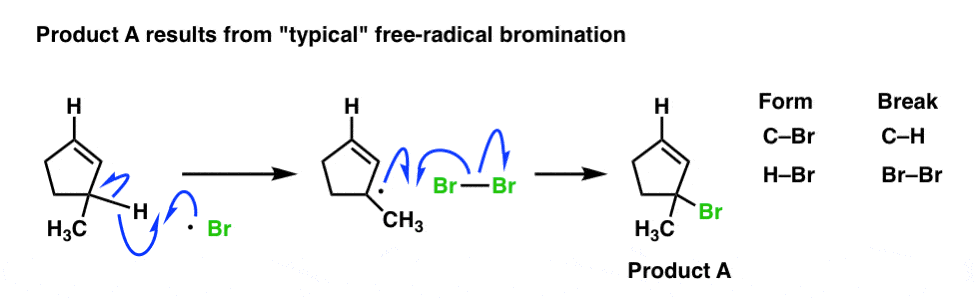
很简单。但是我们如何解释产品的形成B吗?
再看看产生的自由基。注意到什么特别的呢?
我们可以画一个共振的形式!
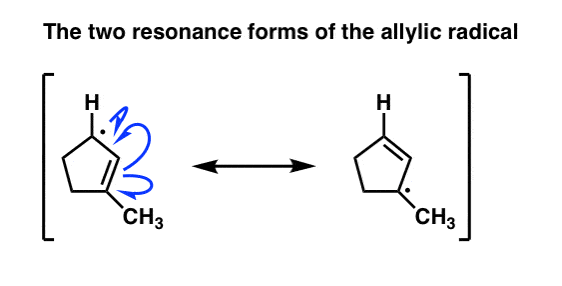
这意味着两个在这个分子可能参与碳自由基反应。因此,我们也可以画显示了Br的反应机理2反应在这个底部(三级)碳: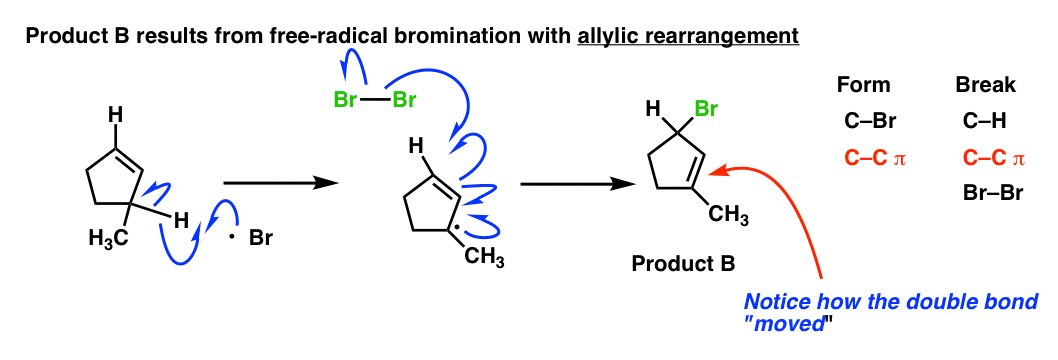
看到第三激进形式新π键,而另一个π键断裂?这使得一个电子的“顶级”烯烃形成一个与溴新债券,给我们一个新的C-Br债券。
如果你分析债券形式,打破这个反应(总是有用的练习),注意,这个反应有一个额外的一双事件——一个碳碳π键断裂,和一个碳碳π键形式。
净效应是,它看起来像π键了。这种现象被称为“烯丙基的重排”。
注意:正如评论者基斯”指出,记住共振形式是“混合动力”。绘图机制时,最好给这一切发生在一个步骤(在中间画,上图)而不是画出共振,然后画出溴化形式。
3所示。为什么“B产品”可能青睐呢?记得扎伊采夫法则!
最后一个问题。你能想到一个原因产品B可能更青睐,尤其是在高温的情况下?
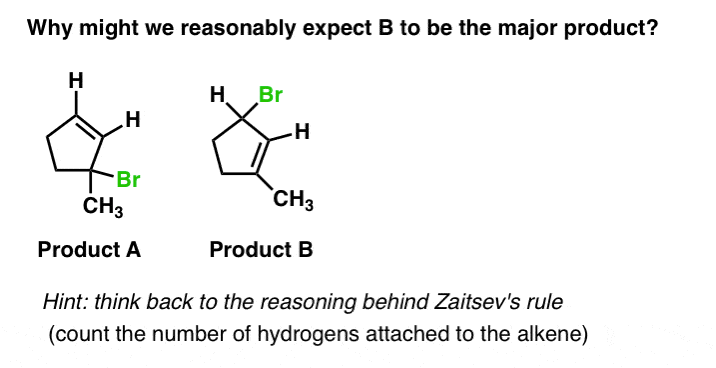
(为什么?原因是复杂的,通常不是在介绍性教科书——这与一个现象叫做“超共轭现象”)。
的烯烃在产品就是我们所说的“di-substituted”——它直接连接到两个碳原子和两个氢原子。的烯烃在产品B是“三代的”——这是直接连着三个碳原子和一个氢原子。因此有理由期望产品B是一个重要的产品在这种情况下。
[我套期保值的比率,因为我没有一个文献引用。你不应该完全相信我没有坚定的文献参考数据;我会尽量挖一个)。
在下一篇文章:烯烃自由基的哈佛商业评论
笔记
(高级)引用和进一步阅读
- 溴化N-Bromosuccinimide和相关化合物。沃尔齐格勒反应。
卡尔Djerassi
化学评论1948年,43(2),271 - 317
DOI:1021 / cr60135a004
老审查由著名化学家卡尔Djerassi,对全球卫生的主要贡献是炔诺酮的发展——第一位女性避孕。本文包含的几个例子烯丙基的在自由基的条件下重新排列(溴化的系统国家统计局)。 - 取代反应和重排反应的烯丙基的化合物
r·h·德·沃尔夫和w·g .年轻
化学评论1956年,56(4),753 - 901
DOI:10.1021 / cr50010a002
早期评论提到自由基烯丙基的重组短暂- pg。761。w . g .年轻教授建立了加州大学洛杉矶分校化学系今天,还有一个在加州大学洛杉矶分校大楼以他的名字命名。 - 循环聚烯烃。二世。从氯丁二烯环辛四烯的合成
阿瑟和威廉·j·贝利
美国化学学会杂志》上1948年,70年(7),2305 - 2309
DOI:1021 / ja01187a002
早期论文教授阿瑟处理(应对重排的名声,现在同名ACS处理学者奖)在环辛四烯的合成。的一个步骤包括溴化1,5-cyclooctadiene国家统计局,给一溴化合物。应对提到他们不确定的确切位置Br在产品和2可能的化合物可以形成(iii a和希望),由于重排。 - 在添加试剂过氧化效应不饱和化合物。十三。丁二烯的溴化氢
m . s . KHARASCH艾莉·t·马戈利斯,弗兰克·r·梅奥
《有机化学》杂志上1936年,01(4),393 - 404
DOI:10.1021 / jo01233a008
另一个早期的论文m . s . Kharasch他研究的哈佛商业评论丁二烯,他试图严格分开的两种模式——亲电与激进。有一个例子的一个“烯丙基的教授,重排Kharasch表明,与哈佛商业评论3-bromo-1-butene自由基的反应条件(过氧化物)可以给1,3-dibromobutane。这将是获得通过中间烯丙基自由基,可以添加一个在1 -或3 -溴激进的立场。 - 环丁烷衍生品。四。齐格勒Methylenecyclobutane溴化
埃德温·r·布赫曼和大卫·r·Howton
美国化学学会杂志》上1948年,70年(7),2517 - 2520
DOI:1021 / ja01187a063
齐格勒methylenecyclobutane反应给了“正常”和重新安排烯丙基溴化产品(正常占主导地位)。 - 环己烯3、3、6,6-d4一个有用的复合机制研究和结构
扫罗沃尔夫和p·g·c·坎贝尔
可以。j .化学。1965年,43(5),1184 - 1198
DOI:10.1139 / v65 - 156
烯丙基的陈词滥调可以很容易地进行重排,而最初的“正常”的产品可能反应混合物中形成,检查会导致混乱。本研究发现,烯丙基溴化发生“正常”,但经检查,给异构烯丙基溴发生重排。
你好詹姆斯!我仔细阅读你的文章
但是我有一个问题. .
比较激进的结构。
激进的结构是三级烯丙基自由基,激进的B是次要的烯丙基自由基的结构。
前者是更稳定的激进的结构。
但主要产品是B。
只是扎伊采夫规则(超共轭)比激进afffection稳定?
优秀的解释
我认为你的解释更多的取代烯烃B比一个更稳定的,但是如果我们看一下过渡状态导致B,我们发现有一个三级比二级自由基更稳定自由基(B),所以为什么不应该是这条线的主要产品想,即使我同意最终产品B比但难道我们也更稳定比较过渡状态导致这两种产品…我很困惑,为什麽我们不考虑这个自由基稳定…请详细说明这部分吗?
嘿,詹姆斯。可能也与甲基溴的悬挂双键在产品B ?
嗨——如果一个人过度的国家统计局(> 1当量),那么第二个烯丙基溴化发生,和CH3悬挂双键的B是一个位置可能发生。
这个反应的速度将与国家统计局的浓度成正比,B的浓度,所以随着反应的进行和B的浓度上升,我们应该期待看到一点点的发生。
这就跟你问声好!我来这里问类似的问题——具体来说,如果一个人开始1-methylcyclohexene (unbrominated版本的产品B),将国家统计局对甲基溴化?非常感谢!
爱这个网站!只是想鼓励完成这个对话。a和b都看起来像他们的主要产品可以相互排斥的原因。寻找一种调和的观点,得到明确的答案。
产品B是主要因为双键是更多的替换,最终更稳定(类似于为什么取消往往发生在一种给最取代烯烃-扎伊采夫规则)。
我们应该检查的稳定自由基中间或最后的烯烃?
在B的自由基相比是不稳定…
所以不应该是主要产品?
很好的解释
但是我只有一个疑问关于上述机制。
我们为什么不考虑自由基的稳定性?
在我看来应该是一个重要因素是整个事情遵循自由基的机制。
期待你的解释。
这取决于温度!
我想要点为什么我们覆盖热动力产品是因为它的概念上的重排。最稳定的烃基的主要产品在低温下,因为这是活动青睐由于更快的速率决定步骤。然而在HT,特朗普热力学动力学给你多取代烯烃/ (pdct标志)。
好点!
多取代烯烃更加稳定,因为诱导效应和hyperconjugative效果满足饥饿的(相对)电子饿sp2碳原子。
但这里,不是多溴electrong比sp2碳‘饿’吗?
不会产品溴在一个叔碳原子更稳定吗?
由于詹姆斯和安德里亚Jurado。
你写了一篇文章关于激进的替换。这将是完美的如果你给一些解释关于为什么化合物代替SN1并不遵循E1。谢谢你的辛勤工作:)
优秀的文章,但我真的不喜欢“更稳定的共振形式”一词。共振结构不是离散实体,所有共振必须完全相同的能量形式由于只有一个真正的结构。更好的方式来表达这个概念是,正如你所说,这一种形式使得共振混合动力更大贡献。
我也惊讶,复合B(1)以来的主要产品它包含更少的高度代替双键(通过哈蒙德postule冷宫热动力)和(2)卤化发生更阻碍了网站(大概不好的活动)。此外,我希望复合B重新排列在反应条件下通过SN1机制形成化合物a有特定的文献参考这个反应或你能提供实际产品比吗?谢谢,保持良好的工作和博客!