芳香分子的反应
亲核性芳香取代(NAS)
最后更新:2022年10月15日|
亲核性芳香取代(NAS)
在许多方面,亲核芳香替换是亲电芳香取代的对面的镜子。
- 在亲核芳香取代,一个electron-poor芳环是攻击亲核试剂,导致取代反应
- 通过一个反应所得带负电荷的(负碳离子)中间
- 加速反应的存在吸电子集团芳环上的
- 电子的位置撤回组昊图公司- - - - - -或帕拉- - - - - -到离去基团导致更快的反应比电子的位置退出组元- - - - - -到离去基团
- 氟可以作为离去基团在亲核芳香取代反应(!),因为它是相当吸电子和氟键断裂不是病原反应步骤。
表的内容
- 可能不是你所期望的芳香取代反应
- 引入…。Nucleophilic Aromatic Substitution
- 环上的取代基的影响
- 离去基团的影响
- 替换模式的影响
- “Meisenheimer”中间的机理提供了一个线索亲核芳香取代反应
- 亲核性芳香取代的机制
- 为什么帕拉-同分异构体超过了元-同分异构体?这都是为了稳定负电荷
- SNAr的反应能量图
- 几个例子
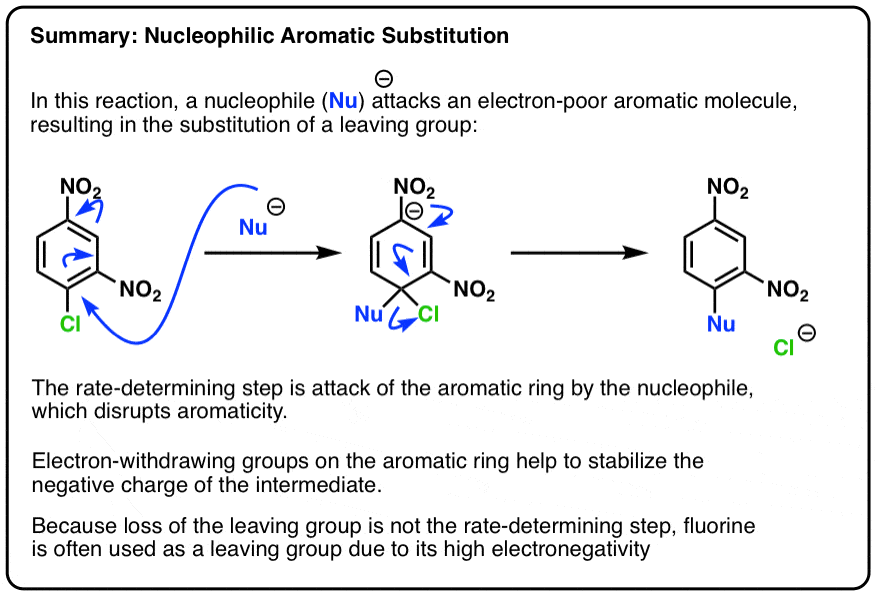
- 摘要:亲核芳香取代反应
- 笔记
- 测试你自己!
- (高级)引用和进一步阅读
1。可能不是你所期望的芳香取代反应
让我们来回顾一下亲电芳香取代(EAS)。我们学到了什么?
- 的芳环作为亲核试剂,一个额外的攻击亲电试剂E
- 一个形成碳正离子中间体缺电子(速率决定步骤),然后deprotonated恢复芳香性
- 芳环上的电子基组(如哦,哟3,烷基)提高反应速度,因为它们有助于稳定electron-poor碳正离子中间体
- 路易斯酸可以亲电试剂更electron-poor(反应),提高反应速率。例如FeBr3/ Br2允许溴化苯发生在一个有用的速率,而Br2本身是缓慢)。
到目前为止我们学过的所有关于替换的芳香环教我们与硝基苯与茴香醚比收入更快,并与一个快得多亲电试剂像Cl2比,比如说,一个负电子亲核试剂像NaOCH3。
我们下面的反应。芳环electron-poor,我们添加一个负电子亲核试剂。
会发生什么呢?没有什么,对吧?
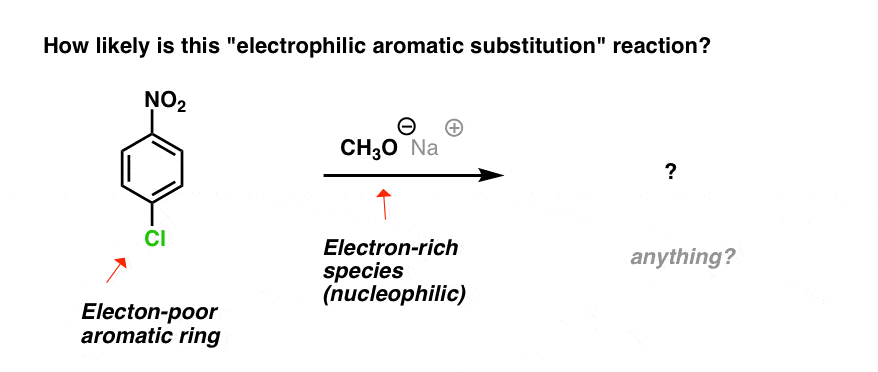
“无”是一个很好的猜测!当然,作为一个思考亲电芳香取代,你认为答案是正确的”这里发生了什么?“是”杰克蹲”。
2。引入…。Nucleophilic Aromatic Substitution
事实上,一个取代反应做发生!(但是,你可能会怀疑,这不是一个亲电芳香取代反应。)
在这个取代反应C-Cl键断裂,切断债券形式在相同的碳。
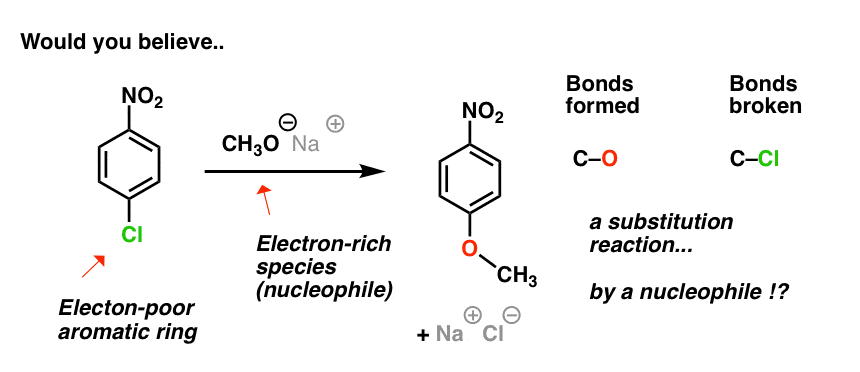
因此,尽管它是一个取代反应它有一些重要的区别:
- 攻击环是一个物种亲核试剂,而不是一个亲电试剂
- 芳环electron-poor(亲电子),而不是电子丰富(亲核)
- “离去基团“是氯,而不是H +
- 的位置亲核试剂是由其中的攻击离去基团是,不由电子和立体因素(即。没有混合昊图公司- - -帕拉- - - - - -产品与亲电芳香取代)。
简而言之,芳环和攻击物种的角色是相反的!
攻击物种(CH3O- - - - - -)是亲核试剂,环亲电试剂。
自亲核试剂是攻击的物种,这种类型的反应被称为亲核性芳香取代反应。
3所示。环上的取代基的影响
在亲核芳香替换(NAS),所有你在亲电芳香取代的趋势操作,但是在逆转。
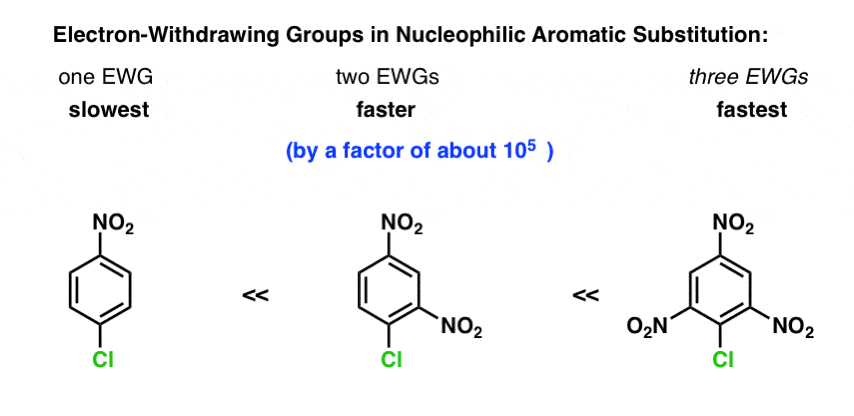
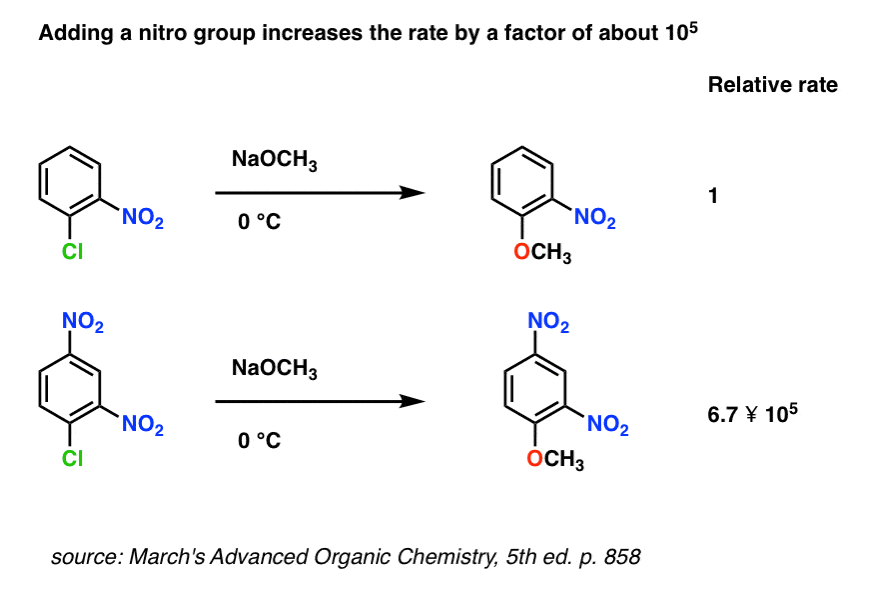
第一个趋势是理解电子撤回组(EWG)增加反应的速率,而不是减少它。
由此,它遵循EWG的越多,反应越快。
例如,NAS 2,氯化4-dinitrophenyl大约是105倍的p -nitrophenyl氯。(注1]
(我没有一个速率常数为2,4,6-trinitrophenyl氯容易获得,但它仍然数量级的速度)。
4所示。离去基团的影响
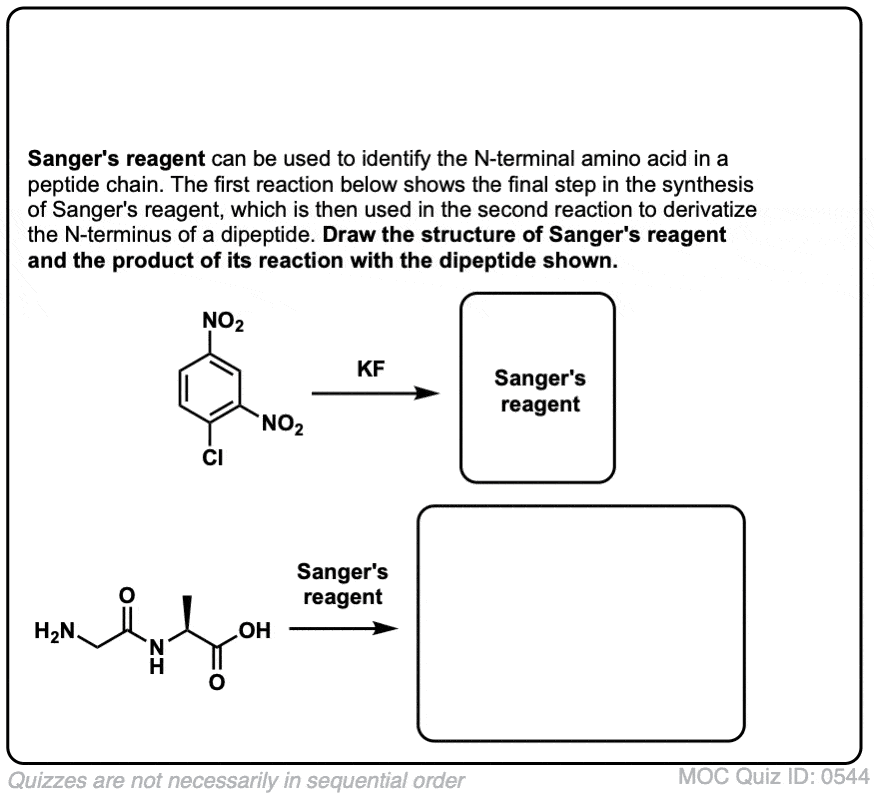
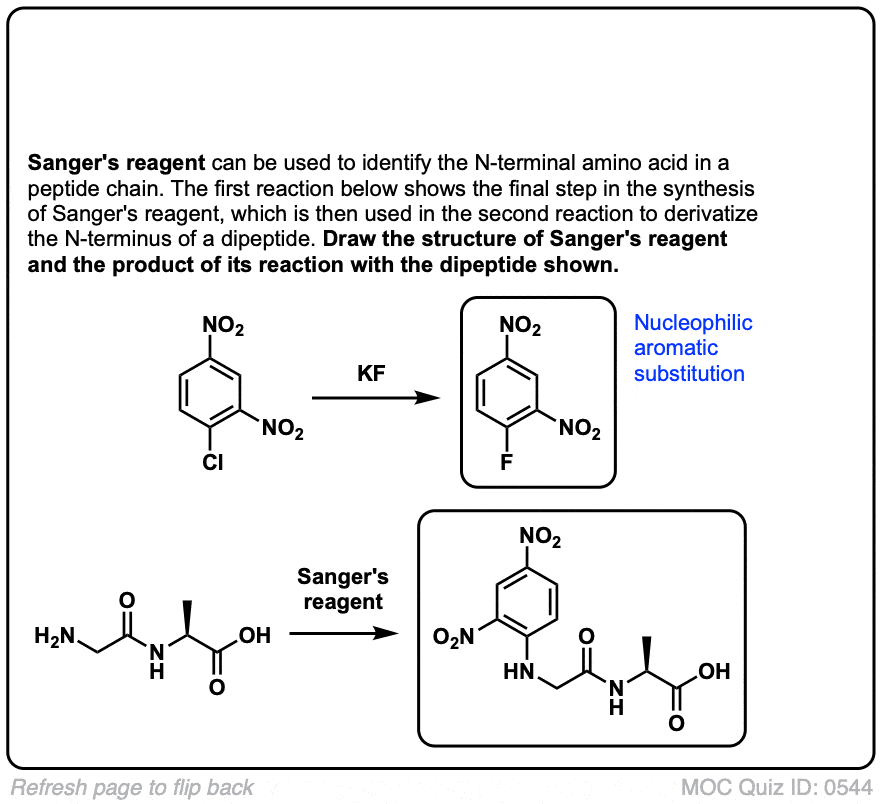
亲核芳香取代最令人瞠目结舌的一个方面是指出氟是常用的作为离去基团。这是出现在桑格的reagent测序肽,举个例子(可以更低)。
毕竟,鉴于我们教官的严厉的音调中使用Org 1在这个问题上,“氟从来都不是bdapp平台离去基团在年代N2和年代N1反应”也可以被雕刻在石碑的传给摩西在西奈山上。
这里有一个想法:如果连一个“坏”离去基团如氟在亲核芳香替换工作,那么一个“更好的”离去基团如溴或碘会工作得更好。对吧?
这是一个很好的预感。这——这也是错误的不让它一个愚蠢的想法,只有有机化学是深。
、氯、溴、碘、区别只有大约3倍。
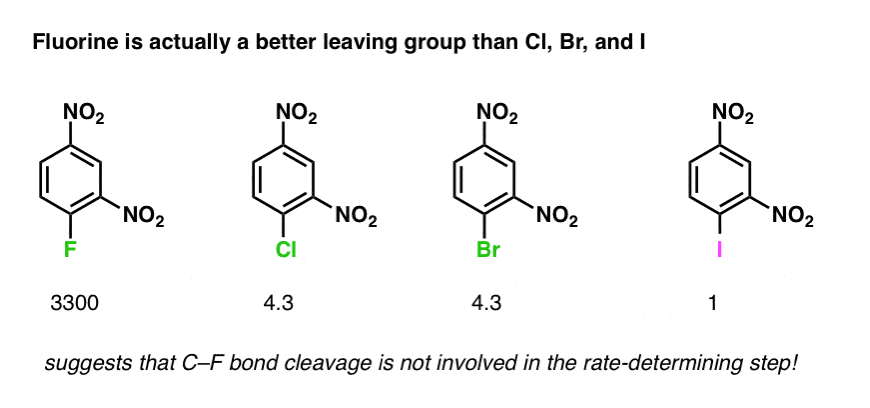
那么可以不同亲核芳香取代,使反应的速率不太敏感的身份离去基团比年代N1和年代N2反应?
嗯,首先,这将表明,不同年代N1和年代N2反应,氟键乳沟不发生在速率决定步骤。这些信息有助于提出的反应机制。
5。替换模式的影响
与亲电芳香取代,没有“昊图公司- - - - - -,帕拉- - - - - -”或“元- - - - - -”导演。替换的位置由的位置控制离去基团。
然而这并不是说,反应的速率不受的相对位置的影响离去基团和吸电子集团。
例如,亲核芳香替换p-nitrophenyl氟化物是数量级的速度比米-nitrophenyl氟化物,即使没有2更接近的离去基团和应该发挥更多的诱导效应。
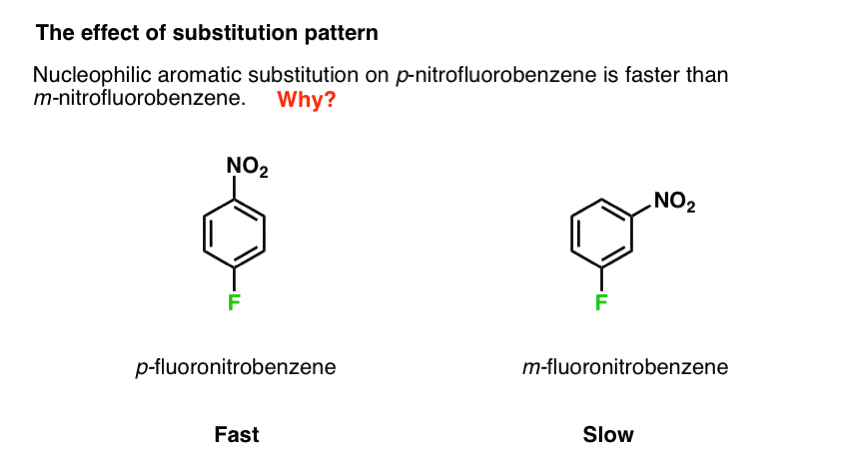
发生什么事了?
6。“Meisenheimer”中间的机理提供了一个线索亲核芳香取代反应
过程中添加各种electron-poor芳香分子的亲核试剂离去基团,中间体已经被隔离。第一个被雅各布Meisenheimer孤立的1902年,和普通的名字“Meisenheimer情结”这些中间体。
中间是(non-aromatic)除了产品和芳环之间的亲核试剂。在下面的案例中,负电荷的离域是一个氧的硝基组:
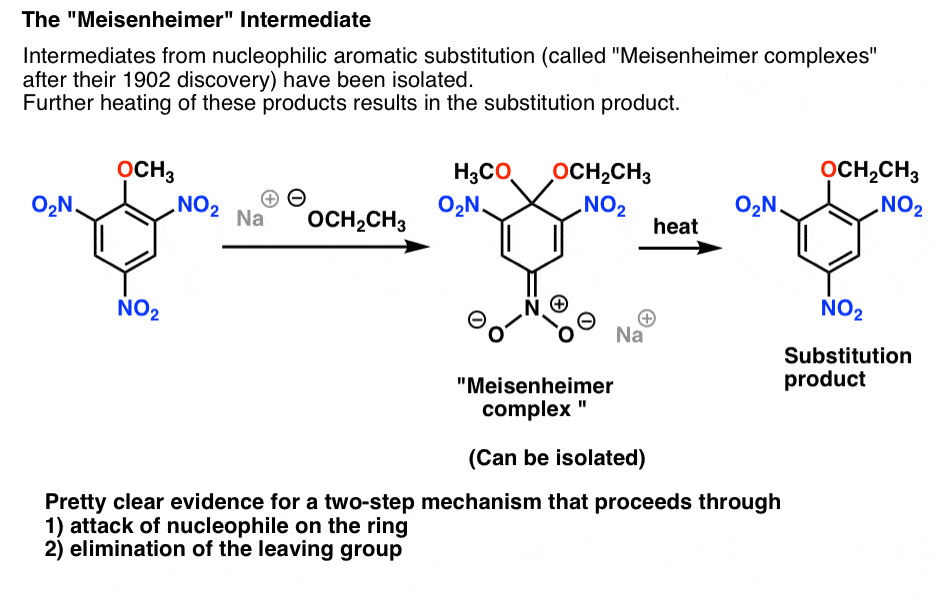
Meisenheimer中间体可以孤立和特征。然而,如果加热,复合生成最终的亲核芳香替换产品。
这是非常暗示,至少可以这么说。
7所示。的亲核芳香替换机制
考虑到所有这些观察我们现在可以提出这个反应机制。
第一步是攻击的亲核试剂electron-poor环上生成一个带负电荷的中间(如。上面的“Meisenheimer”中间,)
因为这扰乱了环的芳香性,这也是病原反应步骤:
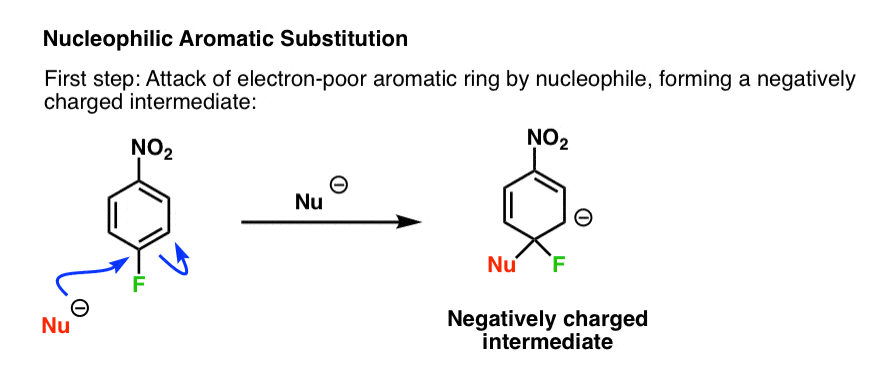
在亲电芳香取代(EAS)我们发现电子的取代基稳定electron-poor中间。
但在亲核芳香替换(NAS)表了!相反,中间是富,是稳定的吸电子取代基,如没有2。
第二步在亲核芳香替换的驱逐离去基团:
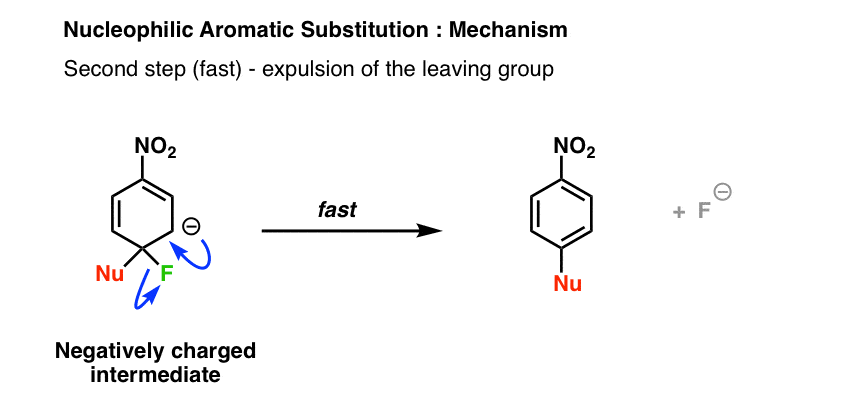
8。为什么帕拉-同分异构体超过了元-同分异构体?这都是为了稳定负电荷
这两步机制增加速率决定步骤有助于解释我们困惑为什么早些时候的反应帕拉- - - - - -硝基速度比元- - - - - -同分异构体。
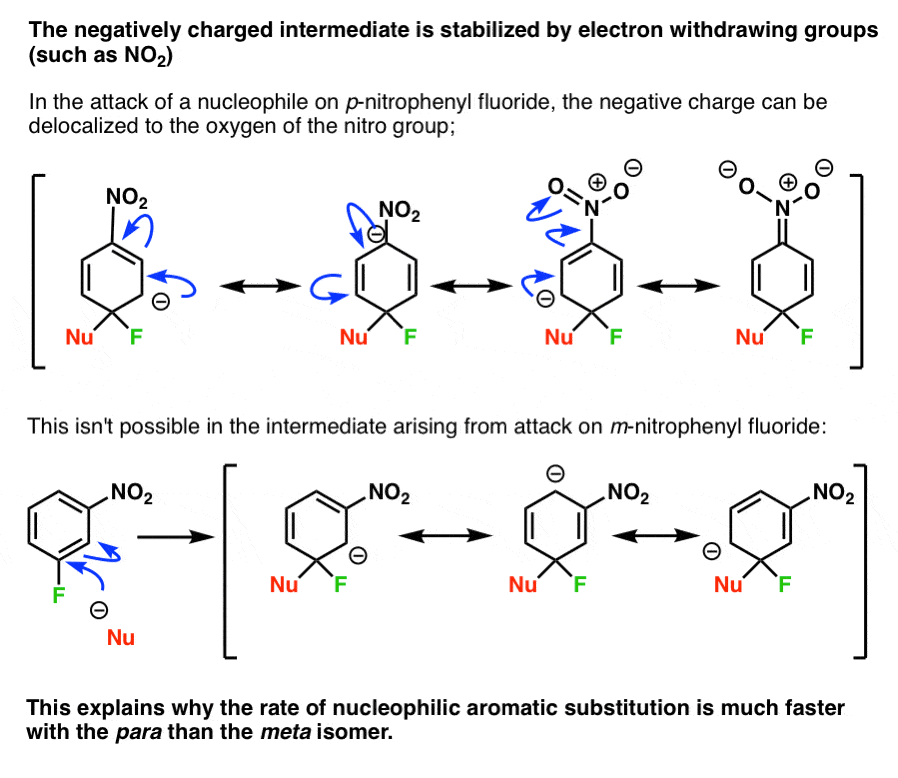
(这也解释了为什么还快昊图公司-异构体)。
这也有助于解释为什么氟取代基增加亲核芳香替代率:速率决定步骤是芳环的攻击,没有违反很强的氟键。高电负性氟拉电子密度的戒指,激活对攻击它。
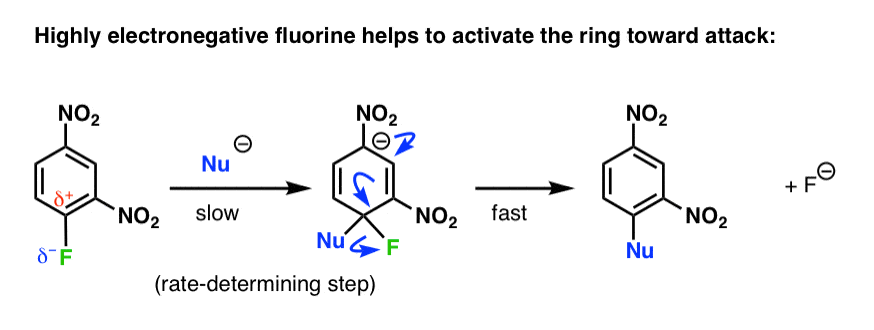
所以即使打破了氟键通常是不积极的,这是补偿,恢复芳香性。
(更新马特:在评论中,引出了一个非常有趣的最近的研究表明,一些亲核芳香取代反应,没有F离去基团可以通过协同机制进行。我同意在考虑这种更高级的材料不太可能覆盖在大多数入门课程,(也许除了尤金的),但很值得。)
9。SNAr的反应能量图
把它们放在一起,我们可以勾勒出一个反应能图机制,会看起来像这样:
(记住:transitition州“山峰”,和中间体“山谷”。中间体(至少在理论上)可以分离;转型国家部分债券,仅在飞秒,不能是孤立的)。
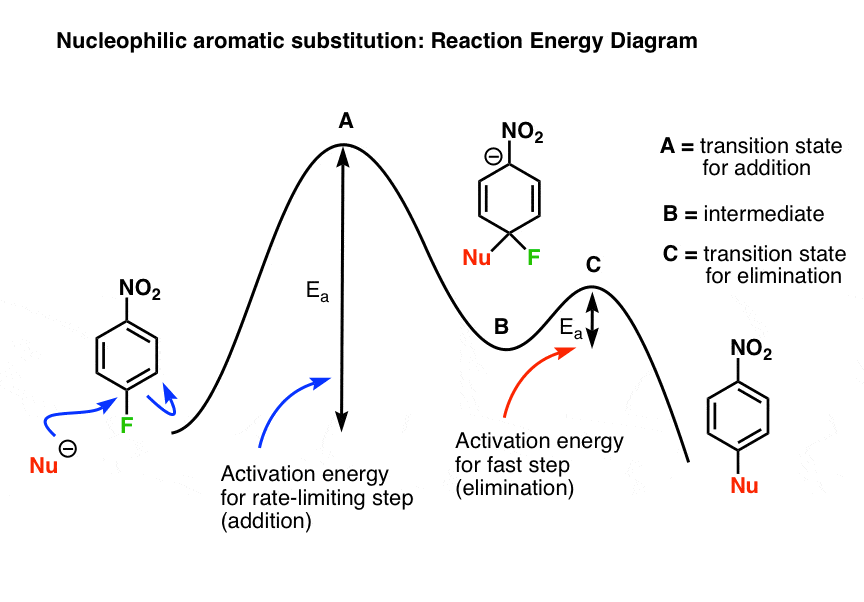
的亲核试剂增加了芳环通过过渡态速率限定(步骤)给B带负电荷的中间,与进一步的能量输入(Ea)提升过渡态C(损失离去基团快速步骤)和从那里,最终的产品。
10。几个例子
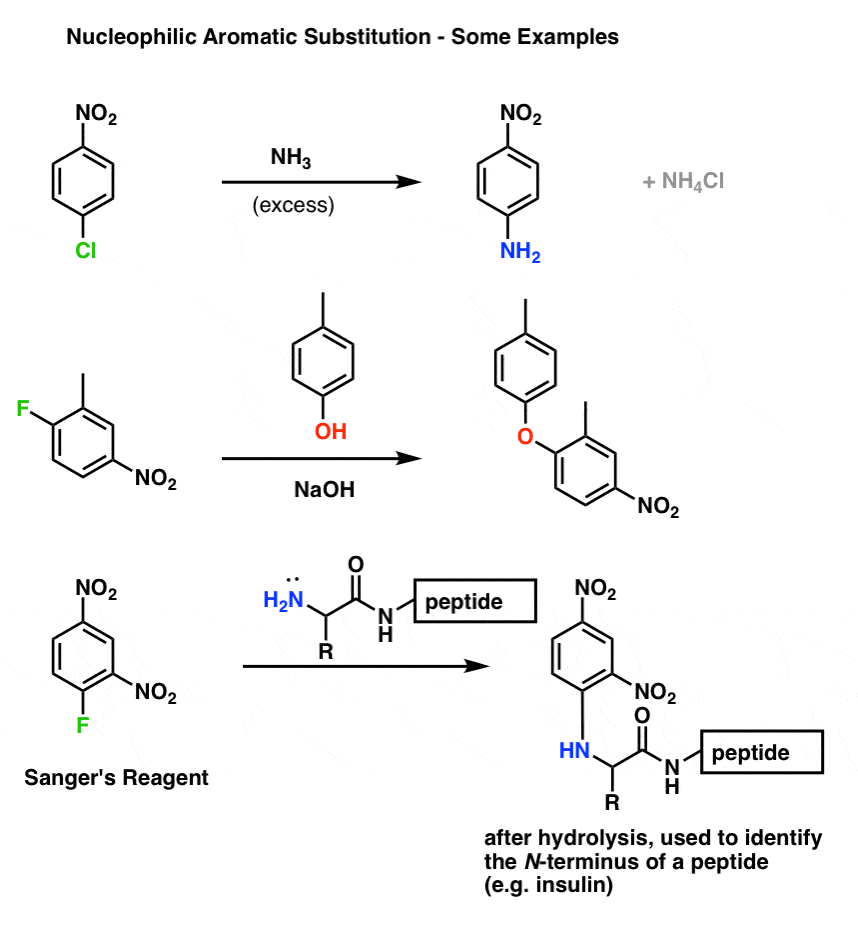
这里有三个代表性的例子:
- 第一个是一个简单的使用一个亲核芳香取代胺作为一个亲核试剂。
- 第二次使用更强的基础(氢氧化钠)(一个较弱的基地共轭碱electron-poor环酚)的攻击。(这个反应的一种变体是用于合成抗生素万古霉素)
- 第三个例子显示了N终点站的肽反应2,4-dinitrophenyl亲核芳香氟化物取代反应。弗雷德·桑格使用该试剂标签终端残留的胰岛素,导致(后很多侦探的工作注2),第一个报道的蛋白质序列(1958年诺贝尔化学奖)。
11。摘要:亲核芳香取代反应
好吧,现在你已经看到我们曾经说过是不可能的:氟作为离去基团。在我们这里,什么其他的诫命从Org 1我们可能打破吗?
如何把一个芳环的三键吗?

这就是下一个!
在下一篇文章中,我们将介绍一个反应,也有资格作为“亲核芳香替代”虽然经历一个完全不同的机制,涉及“三键”,以上。
在下一篇文章:亲核性芳香取代(2):芳炔
笔记
注2。桑格的侦探工作详细在这里。
注3。这项研究是链接在这里。
测试你自己!
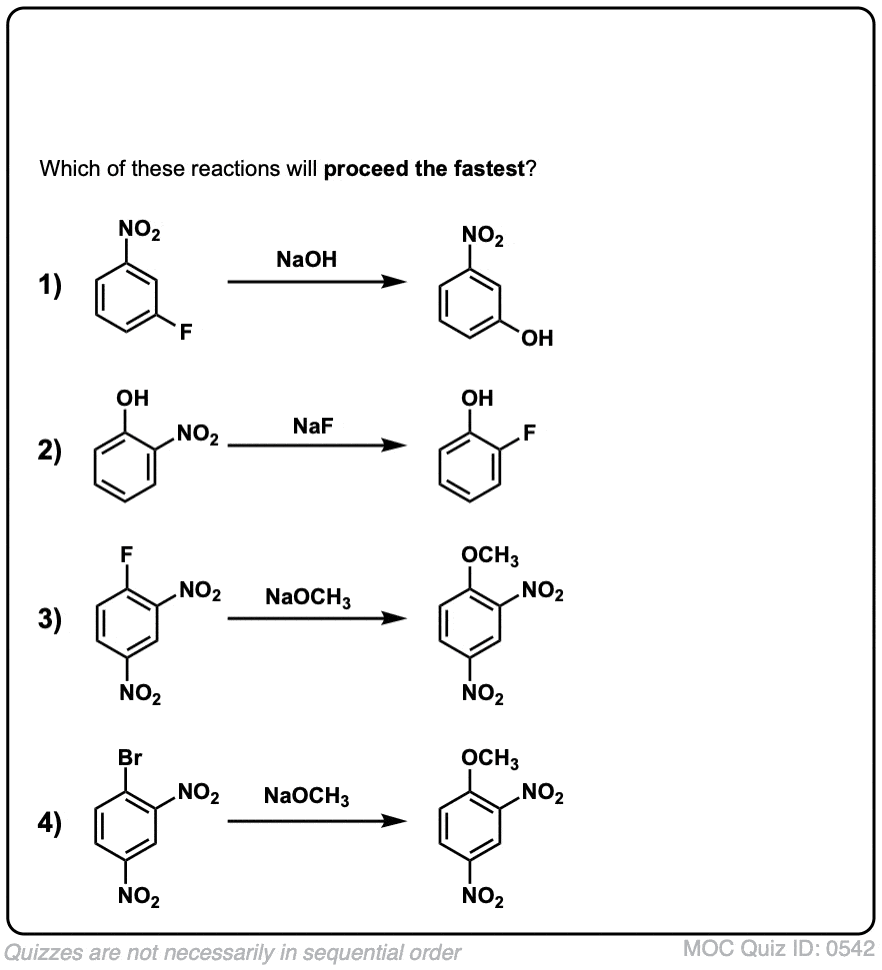 点击翻转
点击翻转
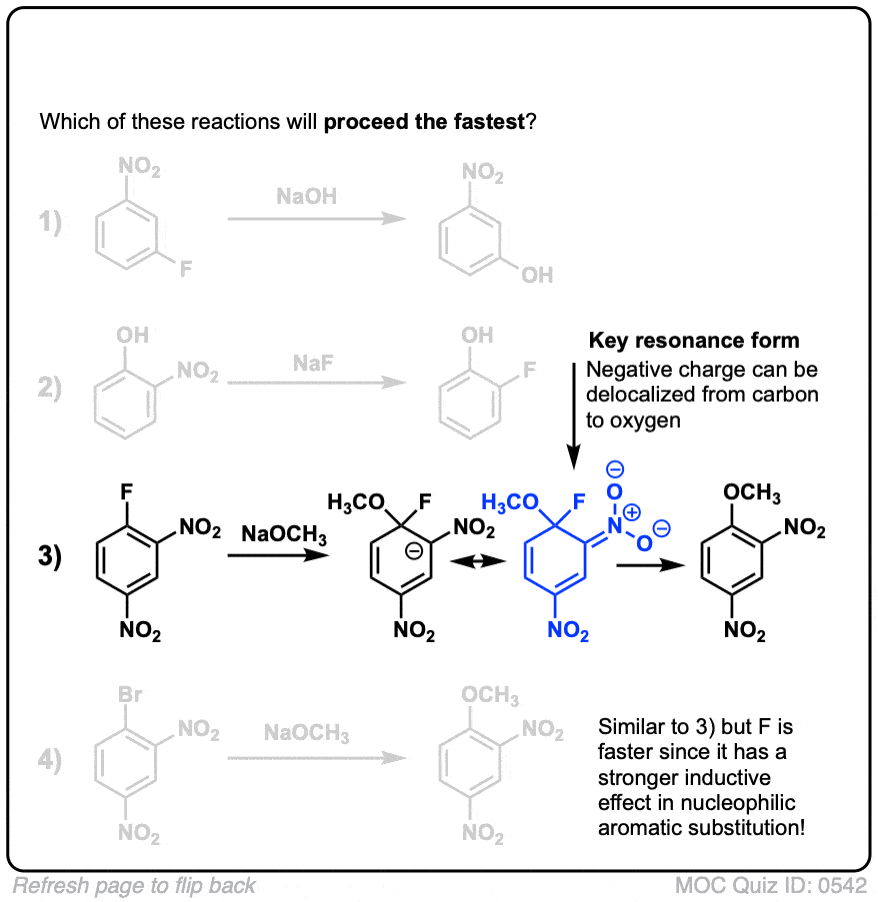
 点击翻转
点击翻转
 点击翻转
点击翻转
(高级)引用和进一步阅读
这是在亲核芳香替代,特别是添加-消去反应。
- Ueber Reactionen aromatischer Nitrokorper
Jakob Meisenheimer
李比希。安。化学。1902年,323年(2),205 - 246
DOI:10.1002 / jlac.19023230205
添加从SNAr反应中间体可以经常被发现或孤立,和被称为Meisenheimer复合物,Jakob Meisenheimer之后,第一次证明了它们的形成。 - 的年代N芳香族化合物的机理。第七部分
彼得•布林m .伟诚,约瑟夫·米勒(小姐)P。g·鲁茨
j .化学。Soc。1954年,1265 - 1266
DOI:10.1039 / JR9540001265 - “元素效应”的标准机制激活芳香亲核取代反应
f . Bunnett埃德加·w·Garbisch Jr .)和肯尼斯·m·普瑞特
美国化学学会杂志》上1957年,79年(2),385 - 391
DOI:10.1021 / ja01559a040 - 亲核取代。线性自由能反应和物理性质之间的关系离开组和基质
朱塞佩莎娃和保罗·埃德加多·Todesco
的化学研究1977年,10(4),125 - 132
DOI:10.1021 / ar50112a004
这些机械的反应进行了研究,证明反应的顺序是F > Cl > Br >我在亲核芳香取代,除了中间的形成通常是cx债券的速率决定步骤因此减轻破坏不会影响率。 - 亲核性芳香取代芳基氟化物的次要的腈:2 - (2-METHOXYPHENYL) 2-methylpropionitrile的准备
Stephane Caron吉尔·m·Wojcik,恩里克·巴斯克斯
Org。Synth。2002年,79年,209年
DOI:10.15227 / orgsyn.079.0209
的一种程序有机合成一个年代N基于“增大化现实”技术的反应,亲核取代的芳基氟化。 - 的终端肽胰岛素
弗雷德里克·桑格
生物化学杂志(1949年1月1日)45 (5):563 - 574
DOI:10.1042 / bj0450563
这个历史上最重要的一个例子的芳香亲核取代反应胺2,4-dinitrofluorobenzene。这个反应是由弗雷德里克·桑格(谁赢了2不共同参与的诺贝尔化学奖)开发方法识别的n端氨基酸的蛋白质。 - 共同亲核芳香替换
尤金·e·关颖珊宇文曾庆红,哈里森·a·贝瑟和埃里克·n·雅各布森
化学性质10卷,917 - 923(页2018年)
DOI:10.1038 / s41557 - 018 - 0079 - 7
这是化学的前沿——作者用有趣的核磁共振实验断言N基于“增大化现实”技术的反应通过协调而不是逐步推进机制。
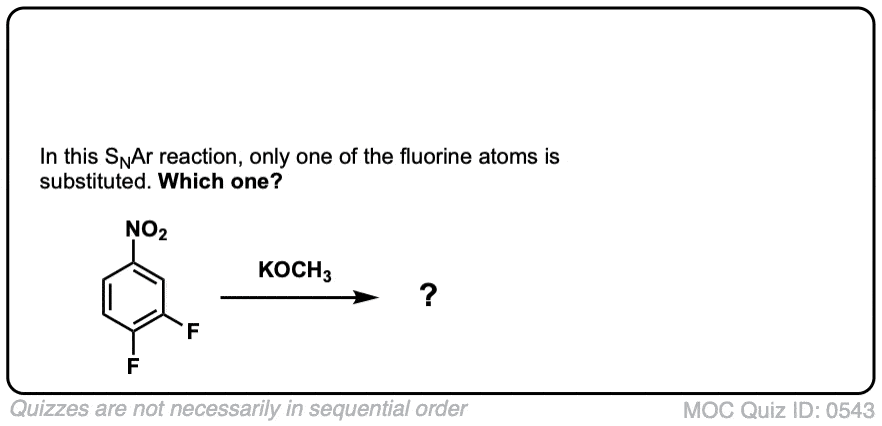
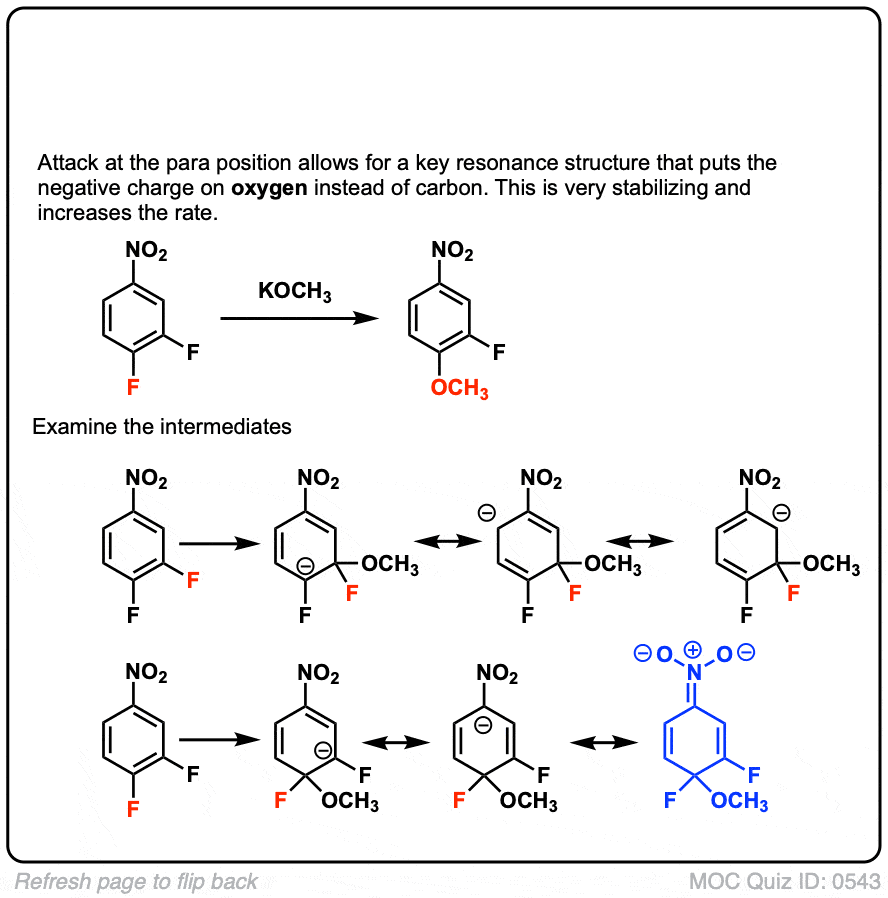
测试的问题我们如何决定哪些氟原子会被亲核试剂代替了? ?
先画除了芳环的产品在每个位置有一个氟原子。阴离子将更稳定?
在以下情况下产品是什么?
甲醇2-bromo-4 6-dinitrophenol +离子- > ?
你将CH3O Br
你能解释测验id 0543对我来说,好吗?
只有卤素作为离去基团或任何其他组织也可以作为LG吗?
最好的离去基团是F,但其他团体也可以离开团体像Cl, Br, OTs。
欧洲药物化学杂志》,2020,第192卷
一般程序:芳香胺的解决方案(0.7更易)和相应的氯化1,6-naphthyridine(0.7更易)异丙醇(10毫升)、盐酸(20更易%)添加drop-wise,然后加热到90°C下氮2 h。混合物过滤,固体溶解在乙酸乙酯。的解决方案是拨了K2CO3(1更易)在保留时间1 h和过滤。滤液集中在真空和纯化的闪光色谱法(以/甲醇= 20:1)产生相应的目标。
我想问:对于一些Heteroaromatic氯,为什么一些酸(如盐酸、几滴)能促进SNAr反应在高温下。谢谢
特定的反应是什么?执行替换什么?
我可以要求3,4-dibromonitrobenzene反应过度的吡咯烷,只有Br para NO2将取代对吧?
思考的负电荷通过增加吡咯烷环形成,以及由此产生的共振形式。攻击在一个位置将大大青睐。你可能认为这,从你的回答,所以我不需要进一步置评。
所以,你的意思是负电荷攻击时将更稳定在NO2在F比吗?吗?
为什么NO2的攻击碳亲核试剂不连接?
良好的亲核试剂是没有必要的,将会有更多的部分正电荷NO2的s碳比F吸引了亲核试剂更好?
如果它攻击,碳负电荷哪里去了?:- ?
谢谢很有帮助
很好,谢谢Pracheta。
你可能已经读过这个,我认为这是不合适的在二年级教过有机食品,因为它包含太多的例外的例外,但是…。
最近的研究表明许多底物反应通过协同机制。计算证据暗示,最近和实验研究了。更好的离去基团,如溴和弱电子退出组织,倾向于一种协调机制。“原始”与氟化物离去基团反应,和多个硝基组,仍在步进式。
我想阅读原始论文,但这里有一个漂亮的简介:
https://chemistrycommunity.nature.com/users/108263-eugene-kwan/posts/36587-one-step-at-time-most-nucleophilic-aromatic-substitutions-are-concerted
同样的争论我们可以炔hydrohalogenation-is机制逐步或共同三分子的吗?我认为重要的是要注意对学生有一些变化的机制,超越了课程的范围,这里我们只看一个“经典”机制。否则学生可以得到很困惑和失望当他们遇到不同的版本或更深更多的参与讨论的机制和感觉他们被教导“错误”或开始质疑他们教什么和多少是“不正确的”。