炔的反应
硼氢化反应和炔烃Oxymercuration
最后更新:2022年11月14日|
硼氢化反应的炔烃和Oxymercuration炔烃通过酮烯醇互变异构现象
碱性yne化学碱有很多相似之处烯化学,但是在前几篇文章,其目的是说明一个看似微小的变化会导致——一个π键bdapp平台重要的不同的化学行为。
之前,我们看到的sp杂化的炔烃导致酸度增加,第二个π键炔烃导致部分减少的可能性独联体或反式烯烃。在本帖里,我们将看到如何添加额外的π键有一个非常重要和令人惊讶的结果。
表的内容
- 水化的烯烃水酸醇
- 炔烃的水合作用与水酸…酮? ?…什么? !
- 的第一步炔烃的水合作用形成的烯醇”
- “烯醇”转化为酮通过这一过程被称为“互变异构化”
- 通过Oxymercuration炔烃也可以“水分”(HgSO4 / H2O)
- 硼氢化反应的炔烃与Anti-Markovnikov选择性(R2BH)发生,给从终端炔烃醛
- 注意:根据炔,混合物的产品可以获得
- 笔记
- (高级)引用和进一步阅读
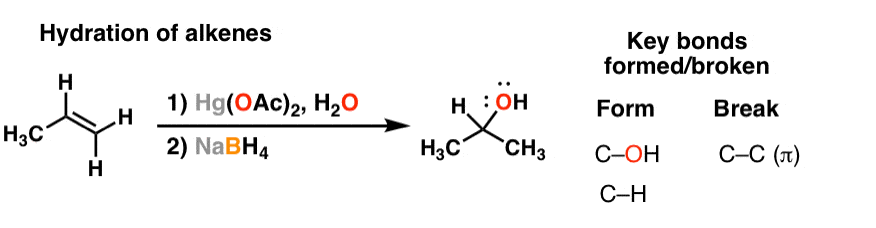
1。的烯烃水合醇
以前我们谈过几个帖子水化的烯烃。可以与水酸,或用汞和水(“oxymercuration”——稍后将进行更详细的讨论)。观察反应烯烃模式相当简单:打破一个碳碳π键,形成一个碳氢键和c哦债券。还记得,氧气最终最取代碳["马氏“选择性)。
2。炔烃的水合作用与水酸…酮? ?…什么? !
所以当我们尝试这个反应炔烃吗?我们可能会希望观察相同的模式,对吧?毕竟,这只是一个简单的加成反应。
嗯…这是我们实际观察。我们得到…酮! ?
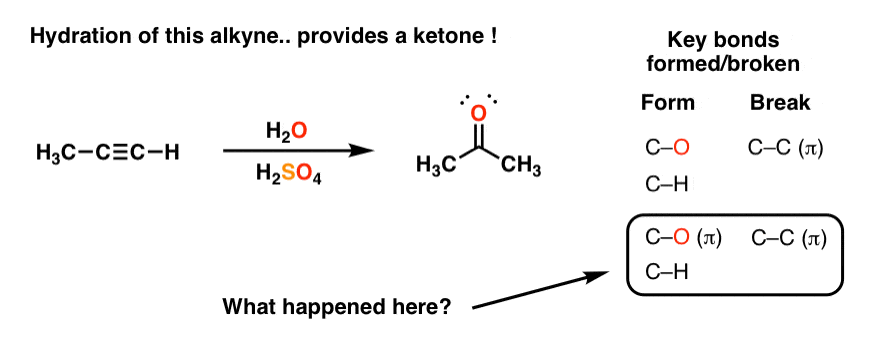
现在是怎么回事?这似乎类型的驱动器新的有机化学学生疯狂的。就在你认为你了解你的环境,你捡起最无害的岩石,和下面找到一条毒蛇!
别慌!这是一个新概念有机化学中我们将探索叫互变现象——一个让更多的讨论在组织2中,但它不是像你一样奇怪的最初的想象。(看到帖子:Keto-Enol互变现象)
看和破碎形成的债券。第一组,我们应该理解。切断和碳氢键形式,打破碳碳π。那就是下一个组债券/破碎形成一个大惊喜。
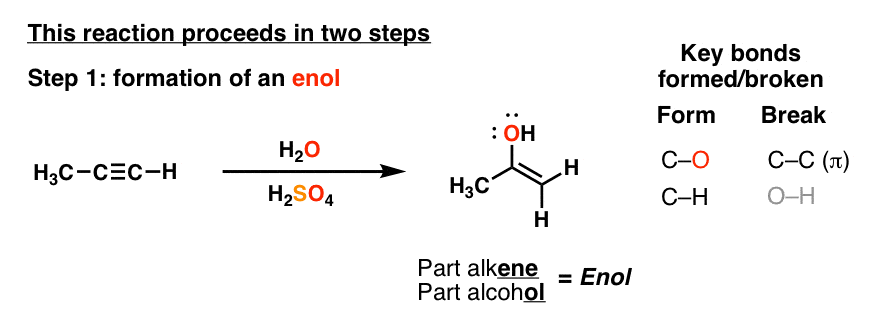
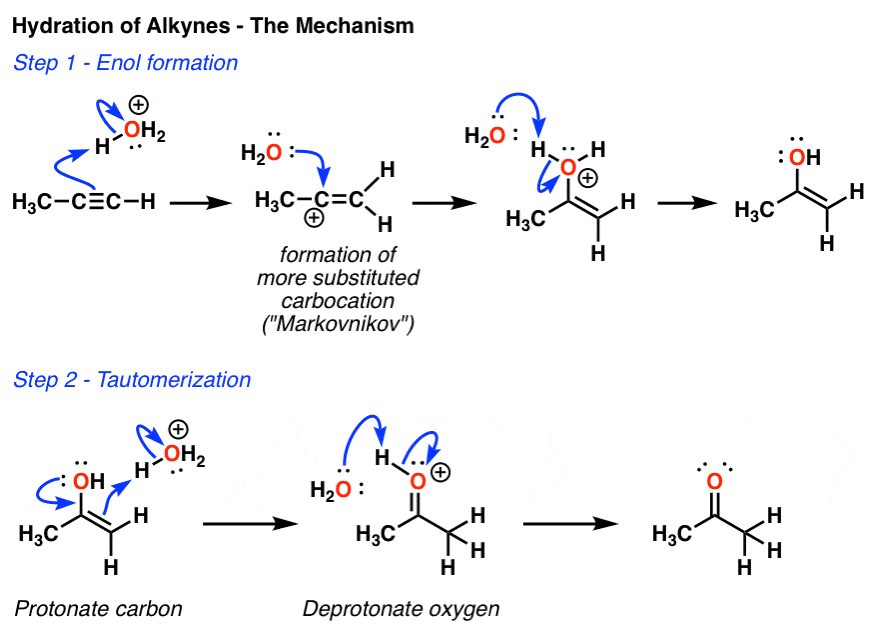
3所示。的第一步炔烃的水合作用形成的烯醇”
如果你密切监视这个反应——这样做的一个方法是在一个核磁共振管——它实际上可以观察这个反应的第一个产品,就是如下所示的一个。我们称之为一个“烯醇”,顺便说一下,有点像叉勺(半勺半叉)部分烯烃,部分酒精。(看到帖子:烯醇的反应)
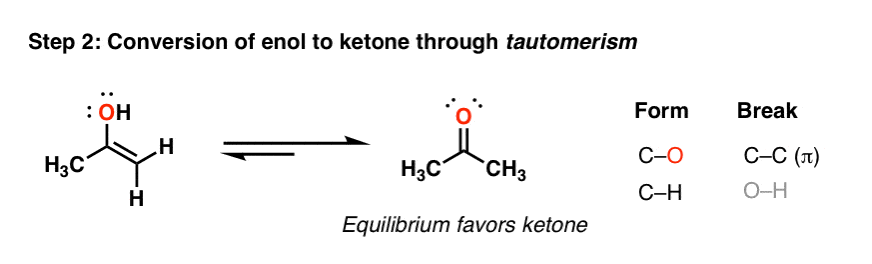
4所示。“烯醇”转化为酮通过这一过程被称为“互变异构化”
随着时间的推移,这个烯醇自发地转化成的酮。注意,两个具有相同的分子式,宪法的同分异构体。他们在互相平衡。
我们称这些宪法互变异构体,”互变异构体”。这个平衡通常更喜欢的形成酮由于强烈的切断π键(碳碳π相比)。
这是整个过程是如何工作的——箭头的箭头。
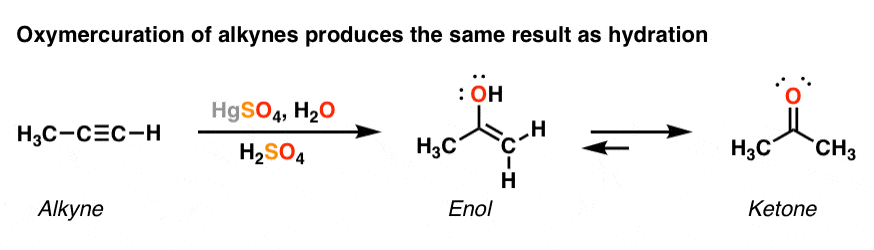
5。通过Oxymercuration炔烃也可以“水分”
等待——我们还没有做完!有另一种“水合物”炔烃,就像有烯烃。我们也可以执行相同的反应与汞、水和强酸(硫酸、H2所以4通常是酸的选择)。有趣的原因我们不会进入,NaBH4不是一般的去除汞炔烃;仅仅是足够的水和酸。
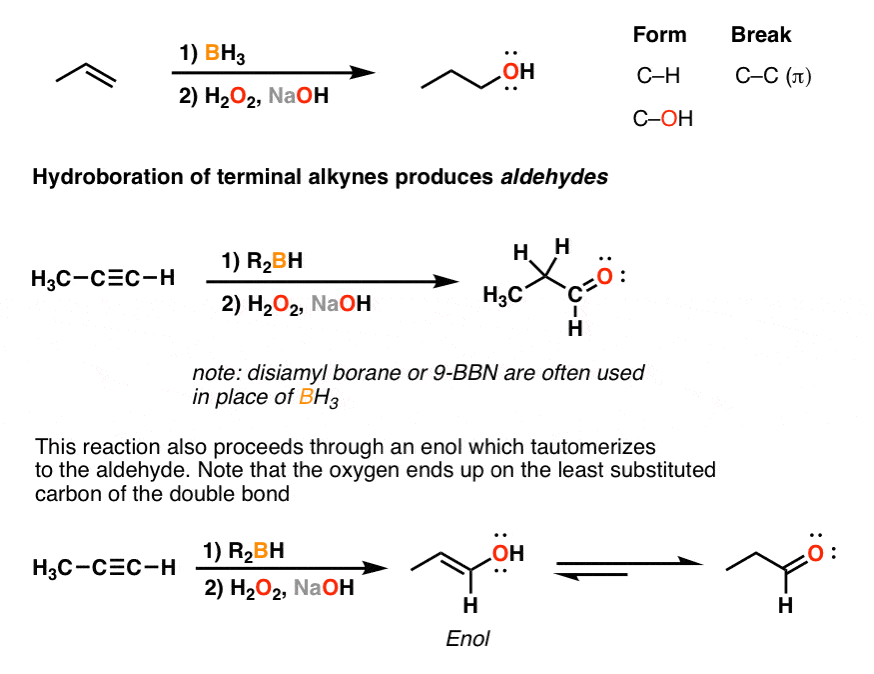
6。硼氢化反应的炔烃发生“Anti-Markovnikov选择性”,给从终端炔烃醛
还有硼氢化反应。还记得hydroboration-oxidation的烯烃与黑洞3和H2O2给了我们“anti-Markovnikov“水化烯烃吗?(看到帖子:硼氢化反应的烯烃)
同样地,我们可以使用相同的反应执行”anti-Markovnikov“硼氢化反应炔烃。
正如在上面的案例中,我们最初获得一个烯醇。然而,在反应条件下,酮烯醇互变现象形成的结果醛。
底线:如果我们从一个“终端”炔烃,这是一个炔烃一个碳原子连接直接到H -然后我们将获得酮与H3O + /小时2所以4或通过oxymercuration,醛通过硼氢化反应。
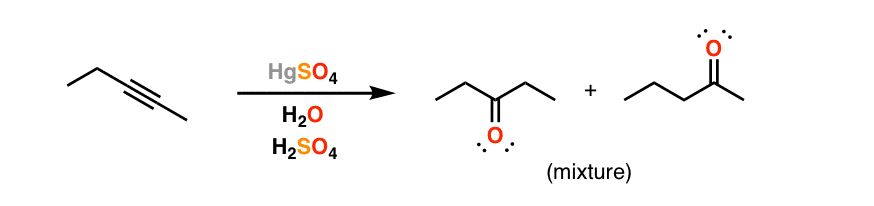
7所示。根据炔,混合物的产品可以获得
最后注意:如果我们使用一个炔烃在两端直接连接到碳,我们将获得产品的混合物。这就是“马氏规则的像”——记住,如果每个碳多重键连接到相同数量的氢,然后我们不能确定哪个是“替代”为我们的目的。在这个例子中。
在下一篇文章:炔反应模式——碳正离子通路
笔记
注1。注意:尽管黑洞3有时写的,不是吗严格正确的。为什么?双之外(见裁判)
不是经常使用位阻硼烷,比如disiamyl硼烷9-BBN之外,增加的比例越少也取代碳和防止二次硼氢化反应的反应。
(高级)引用和进一步阅读
- 乙炔的硼氢化反应——内部乙炔的方便的转换独联体烯烃高纯度和终端的乙炔醛
布朗,H.C.;Zweifel G。
j .我。化学。Soc。1959年81年(6),1512年
DOI:10.1021 / ja01515a058
原始的硼氢化反应描述炔烃教授,诺贝尔奖得主h·c·布朗(普渡)。 - 钯催化反应的1-ALKENYLBORONATES VINYLIC卤化物:1 - (1 z, 3 e)苯基1,3-OCTADIENE
Miayura:;铃木。
Org。Synth。1990年、68、130
DOI:15227 / orgsyn.068.0130
过程由诺贝尔奖得主Akira Suzuki的硼氢化反应炔烃catecholborane。由此产生的产品可以随后用于Pd-catalyzed铃木耦合反应。
各种其他试剂是由h·c·布朗对硼氢化反应,包括catecholborane,9-BBN,disiamylborane。这些试剂的优势在于,他们会接受monoaddition来炔烃,而硼烷将增加两倍。代表参考这些试剂的反应炔烃是下面的: - Catecholborane (1、3、2-Benzodioxaborole)作为一个新的通用Monohydroboration试剂炔烃。一个方便的合成Alkeneboronic酯类和酸炔烃通过硼氢化反应
布朗,h . c;古普塔,美国K。
j。化学。Soc。1972年94年(12),4370年
DOI:10.1021 / ja00767a072 - 50。硼氢化反应的代表炔烃与9-Borabicyclo (3.3.1) nonane-a多才多艺的简单合成乙烯基拉博拉和gem-Dibora中间体
布朗,h . c;Scouten, c . g .;李欧塔,R。
j。化学。Soc。1979年101年(1),96
DOI:10.1021 / ja00495a016 - 习Acetylenes-A方便转换的硼氢化反应的内部乙炔独联体- - - - - -烯烃和终端乙炔成醛
布朗,h . c;Zweifel G。
j。化学。Soc。1961年,83年(18),3834
DOI:10.1021 / ja01479a024
本文描述了使用的选择性monohydroboration disiamylborane炔烃。 - 乙炔的酸和未饱和现象酯类。三世。一些水银的宪法衍生品
威廉·惠利Myddleton阿瑟·w·巴雷特和约翰·h·西格尔
美国化学学会杂志》上1930年,52(11),4405 - 4411
DOI:10.1021 / ja01374a032
最早的报道在oxymercuration文学。 - 1-ACETYLCYCLOHEXANOL
加德纳w .史黛西和Richard a . Mikulec
Org。Synth。1955年35岁1
DOI:10.15227 / orgsyn.035.0001
非常标准的oxymercuration-hydration反应的终端炔烃在有机合成,一个著名的独立消息来源的证实和可再生的有机化学实验室程序。 - 烯醇醋酸纤维素,烯醇醚,胺乙炔的汞化
保罗·f·Hudrlik和安妮·m·Hudrlik
《有机化学》杂志上1973年,38(25),4254 - 4258
DOI:10.1021 / jo00964a009
作者在这个出版物显示,中间mercurinum离子可以与亲核试剂反应除了水,扩大了这个反应的范围。 - 一个高效的合成.gamma.-methylene可以利用。丁内酯(.alpha -angelicalactone)。应用程序的合成deoxyobtusilactone deoxyisoobtusilactone
理查德·a·阿莫斯和John a . Katzenellenbogen
《有机化学》杂志上1978年,43(4),560 - 564
DOI:10.1021 / jo00398a007
Mercurinium离子也可以接受内部分子环化——在这种情况下,终端炔烃可以使环化羧酸在另一端的汞盐产量lactones.Prof。Bassetti(意大利)发表了一系列漂亮的论文的机理mercurinium离子形成从炔烃: - 金属化作用的炔烃。1。的影响炔烃结构acetoxymercuration的速率
毛罗·Bassetti和芭芭拉Floris
《有机化学》杂志上1986年,51(22),4140 - 4143
DOI:10.1021 / jo00372a007 - 金属化作用的炔烃。第2部分。的行为炔烃与甲醇醋酸汞(二):一个系统的重新调查
毛罗·Bassetti和芭芭拉Floris
j .化学。Soc。,Perkin反式。2,1988年,227 - 233
DOI:10.1039 / P29880000227 - 偕的有机金属化合物。我的合成和结构1,1-Diborohexane
g . Zweifel和h . Arzoumanian
美国化学学会杂志》上1967年89年(2),291 - 295
DOI:10.1021 / ja00978a022
当接受BH3 1-Hexyne经历双硼氢化反应的反应。这就是为什么笨重的硼氢化反应试剂如disiamyl硼烷9-BBN使用。
通过定义一个手性中心必须有四个不同的基团。两个氢原子的α碳酮交付。因此对映体的形成是不可能在这个反应。
在第4部分中(水)的机制,在步骤2(互变异构化)
我想问关于氢,h3O捐赠。H可以添加到任何方面我们将对映体或立体定向吗?
什么一个了不起的页面!关于这个话题都清理了我的怀疑。我的化学老师无法教好:请保持良好的工作。
如果通过oxymercurium路径添加水,不要第二个阶段,利用hydroboran减少oxymercurium inermidiate,需要吗?
我知道在烯烃的情况下,这些反应(Hg和BH3)重组没有观察到。
重排是可能的吗?(如形成更多代从而更稳定的C +)
提前谢谢。
不,没有自由碳正离子。
在最后一个示例(“最后一点”),我们为什么不使用碳正离子的稳定性,马氏规则的原因吗?
我们可以说,右边的碳将会形成一个更稳定的碳正离子,由于超共轭。(因为它有3个alpha-hydrogens而左碳只有2)
这将意味着,第二产品将占据主导地位。
还是我遗漏了什么东西?
如果炔的分子和反应,如何将它与硫酸反应和HgSO4。是醛或酮吗?
硫酸反应的总酮Bh3反应可以酮或醛
终端炔烃的水合后首先会形成一个烯醇马氏规则的像。烯醇会接受Keto-Enol甲基酮互变异构化和重新排列。
这将是一个酮
步骤1 -烯醇形成的机制”“a +电荷是失踪的第三结构。
固定的。谢谢你!
我真正想知道的是为什么ANTIMARKONIKOV产品是硼氢化反应中形成的反应。基本上我想要简化机制,我找不到我的书。
恭喜你成为爸爸,詹姆士。
这与硼氢的电负性比的事实。
的区域选择性BH3好吗?似乎通过9-BBN硼氢化反应或其他笨重R2BH试剂大大增强了anti-Markovnikov通过立体产品。电负性差异是真实的,你希望碰撞导致的π键攻击硼syn H的转移到更多的取代的烯烃或炔烃是有一些小东西,比如BH3可以可靠地选择anti-M产品?
谢谢你的这句话。这个问题不是区域选择性,但1,1-dibora产品形式,这就是为什么必须使用笨重的硼烷。看到江淮1967卷,89 p。291。https://pubs.acs.org/doi/10.1021/ja00978a022
你这样容易理解。谢谢!:)