醇、环氧化合物和醚
保护组醇
最后更新:2022年11月10日|
酒精保护组织
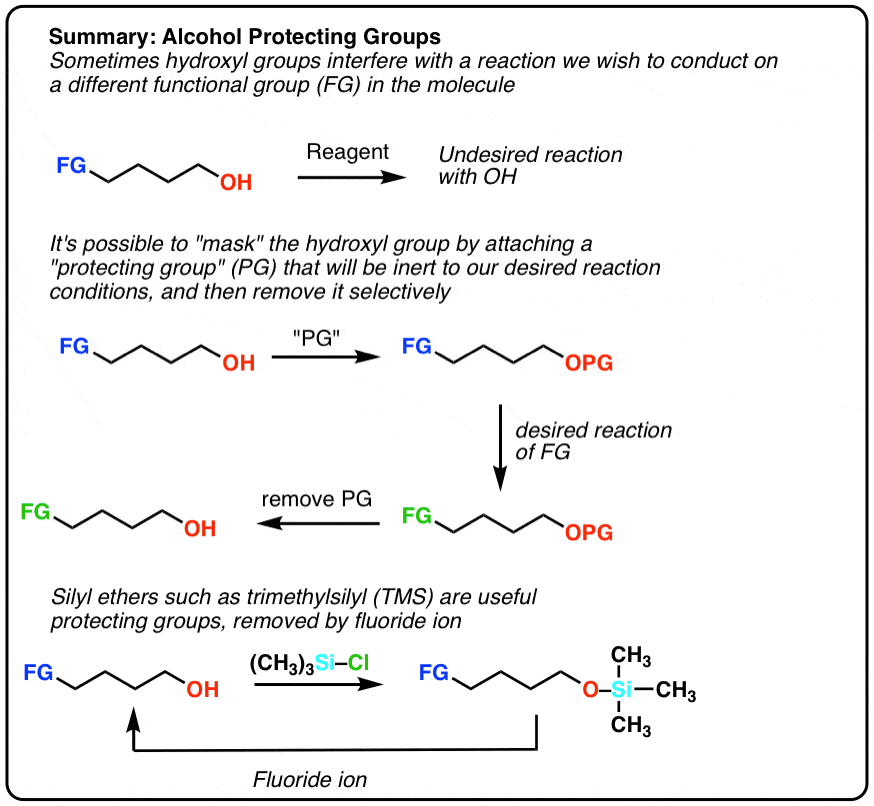
- 很多时候,是有用的面具醇的反应,因为他们的相对较高的酸度干扰强碱性试剂如格氏试剂。
- 最常见的保护组醇甲硅烷基醚。它们很容易由治疗醇与R3SiCl的基地,然后用氟离子的来源很容易移除F(-)由于Si-F债券非常强劲。
- 甲硅烷基醚惰性格氏试剂,强大的基地,氧化剂(尽管与强酸将被删除)。
- Tetrahydropyranyl (THP)醚保护组醇也有用。
- 普通醚一般不用作保护组织因为他们删除需要严厉的条件
表的内容
- 当醇
- 保护组织就像画家的磁带
- 什么是化学相当于“画家的磁带”?
- 一个潜在的解决方案:醚(剧透:他们不是好)
- 一个更好的方法:甲硅烷基醚
- 甲硅烷基保护集团的成功应用策略
- 摘要:保护组醇
- 笔记
- (高级)引用和进一步阅读
1。当醇
正如我们所看到的在本系列以前的文章中,醇用途广泛参与各种官能团的反应。它们可以deprotonated与基础(让他们良好的亲核试剂取代反应),使质子化(使他们好离开组织替代和消除反应),氧化醛或酮,或者转化为更好的离开组(卤代烃,或烷基甲苯磺酸盐)允许的替代和消除反应。
这种多样性也有一个缺点,然而。有时酒精官能团可以妨碍我们可能喜欢做其他的反应。让我告诉你我的意思。
我们看到了一个最有用的碳碳键形成反应你在组织学习1:的亲核取代N2)乙炔化物的卤代烃(共轭碱乙炔)
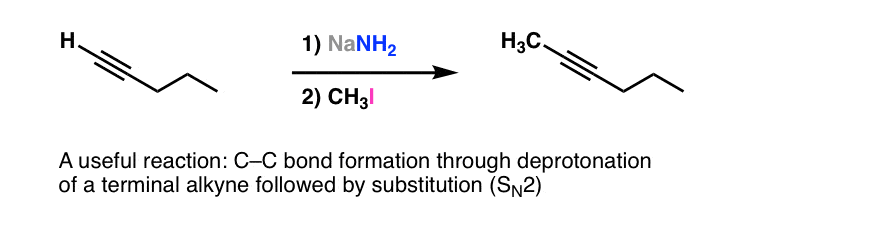
自炔烃就像一个空白的画布,这个反应可以设置许多不同类型的官能团的引入通过加成反应。
现在,让我们修改我们的衬底。我们增加了一个羟基(OH)的分子。现在,让我们看看会发生什么。
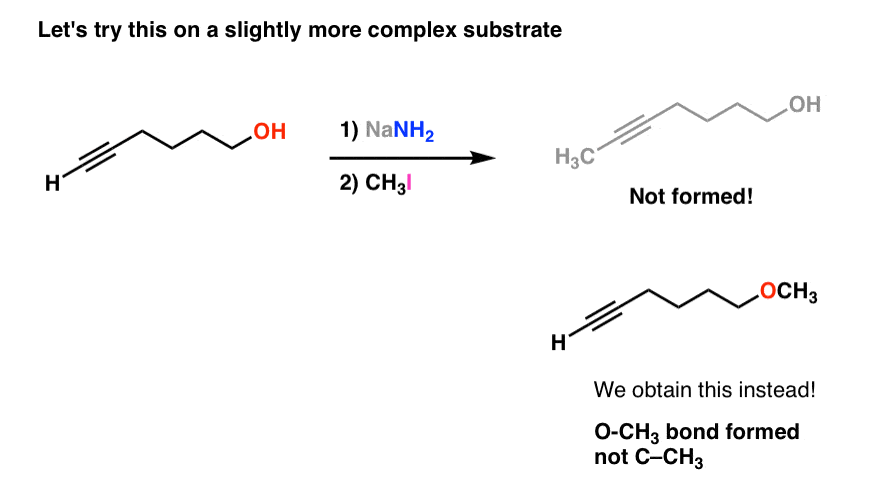
看看发生了什么——我们现在成立了一个新的O-CH3债券而不是碳碳键。到底发生了什么事?
当然,答案是,我们强碱NaNH2deprotonated最强的酸(哦,pK一个16和乙炔化物碳氢键,pK一个25)以及由此产生的醇盐[R-O- - - - - -]然后攻击CH3我,导致取代反应碘离子的位移(注1]
这是另一个例子的原则在起作用。在这里,我们想执行取代反应与碳碳C-Br。那么为什么这个反应不导致一个碳碳键的形成?
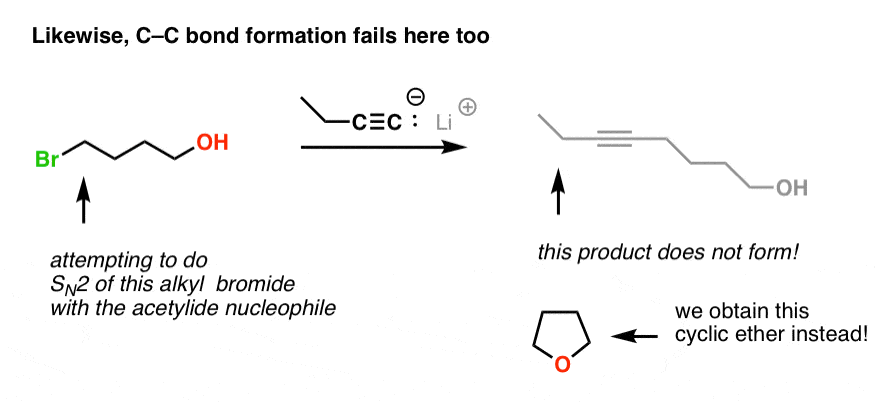
同样的原因!我们的乙炔化物离子是一个强碱deprotonates地组,然后参加一个年代N2反应烷基卤化物4债券(形成五元环)。
这是一个教科书上的例子我们看到在我们的最后后一个分子内的年代N2反应。(为什么不先做替换吗?酸碱反应快,相对于取代反应)。
那么我们如何阻止这发生?
2。保护组织就像画家的磁带
这不禁让人想起一个问题画一个房间的人都能够理解。想象你帮助你的表弟油漆他的房间在一个可怕的黄绿色的阴影完全没把握的在外行人看来,只有一个赶时髦的人可以欣赏它。然后你来那些烦人的墙媒体之一。当然你可以画它。

但现在没用的如果你表哥想插入,1965年smith corona电动打字机在旧货店他发现他使用写他的“小说”。肯定有一个方法不破坏我们的出口。那么你会怎么做?
画家的磁带来拯救!

用画家的磁带,覆盖出口油漆你的心的内容,然后删除录音。然后你可以代入打字机。简单!
3所示。化学相当于画家的磁带
不是很好如果我们有一个“化学当量”的画家醇的磁带。的东西可以
- 面具的反应哦
- 惰性很大的反应条件,和
- 很容易,有选择地删除透露哦组一旦我们完成。
允许我们执行的合成所需的分子(第二方案上面)。这里我使用“PG”代表“保护集团”。
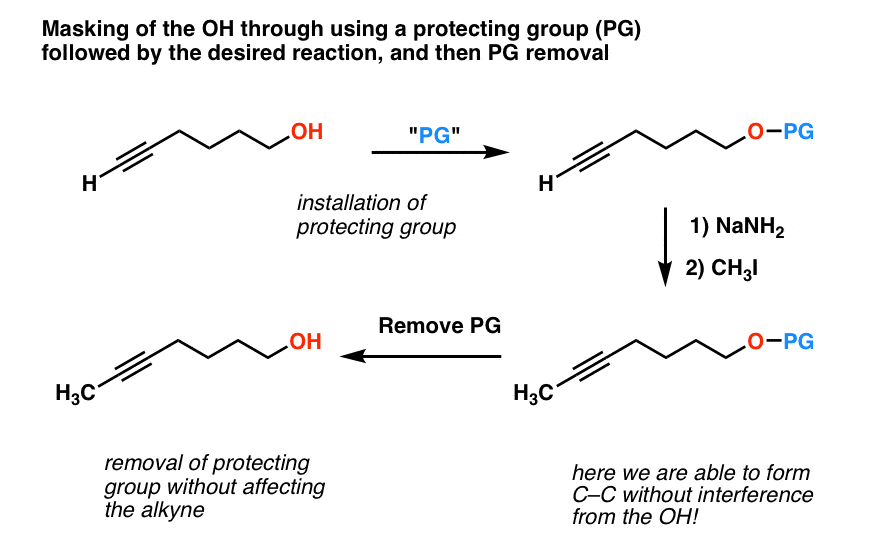
嗯,你可能已经猜到了,进取,化学家们研发出一种解决这个问题。事实上,它很聪明。
4所示。一个潜在的解决方案:醚
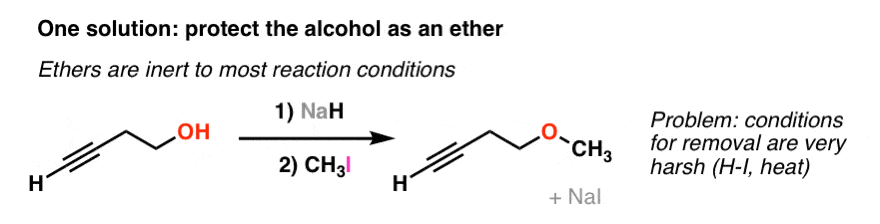
正如我们前面所讨论的,醚类很可能是最无聊的官能团可以遇到。唯一重要的醚反应你在Org 1是封面如何坚持用强酸(如与氢碘酸,你好)。就是这样。除此之外,醚惰性几乎任何其他反应条件可以的名字。
化学当量的“画家的磁带”,无聊的很好!这意味着我们可以“保护”作为一个羟基醚而不用担心受到影响反应我们可能想做其余的分子(如添加一个乙炔化物到一个烷基例如,卤)。
只有一个问题:醚需要非常恶劣的条件为了打破(氢碘酸,嗨)。这就像摧毁村庄为了节省:这种情况可能会火炬其他官能团分子上。
5。一个更好的方法:甲硅烷基醚类
幸运的是一个非常聪明的解决方案设计。相反的典型醚(如形成一个o c键),我们形成一个甲硅烷基醚(即让O-Si债券,而不是一个o c键)。这是更容易比“正常”的形式醚,股票的性质被惰性对许多类型的反应条件。在大多数入门课程中最常见的甲硅烷基醚使用三甲基硅烷基(TMS)虽然有其他人(通常,笨重的硅周围的组织,越难打通O-Si债券)
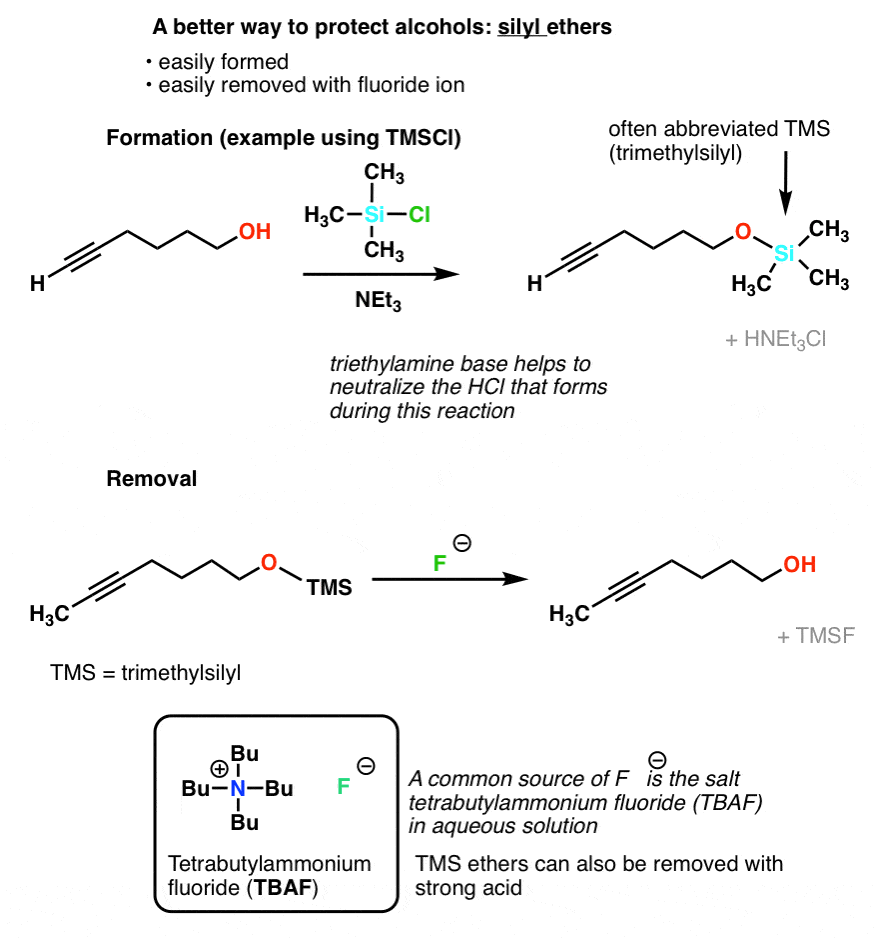
甲硅烷基醚的主要优势是,他们容易劈得开的。Si-F债券比Si-O异常强烈,甚至更强。添加氟离子的来源(F)将导致Si-O债券的乳沟在不影响其他分子。典型的氟化物离子源是氟化盐四丁铵(TBAF)。
还有其他保护组醇吗?那还用说。有关更多信息,请参见注2。
6。甲硅烷基醚保护集团的成功应用策略
让我们回到我们的第二个例子。我们怎么能让这个序列的工作吗?让我们“保护”的自由酒精作为甲硅烷基醚(TMS)并跟进。
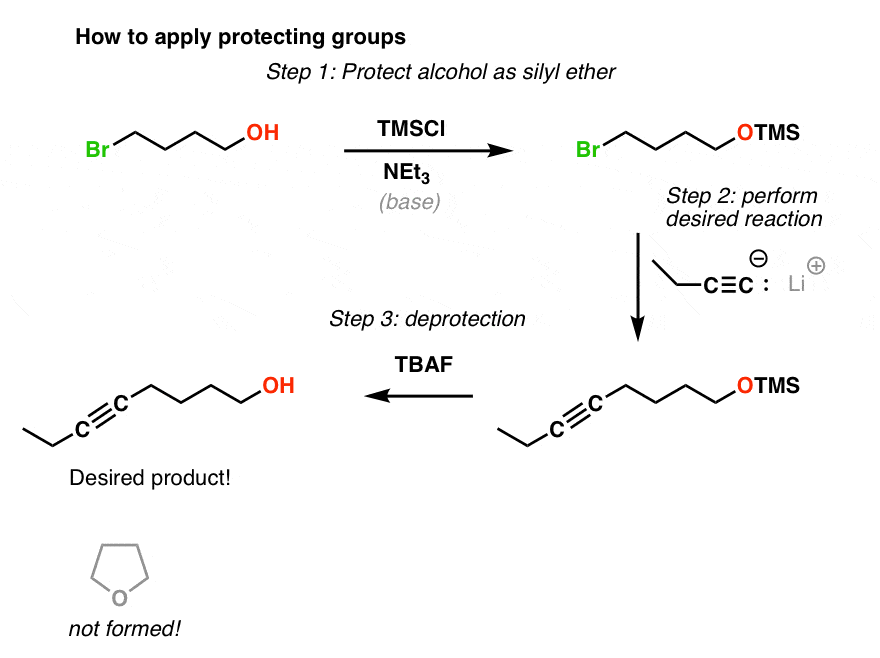
你拥有它。我们需要得到我们预期的反应是一种屏蔽方式哦,直到我们完成执行手术的另一半分子。
7所示。摘要:保护组醇
这篇文章只触及表面的保护组醇。保护组织用于醇在不同的情况下,远远超出了N两个例子我们这里了。例如,当我们谈论格氏试剂,我们会发现他们不能形成于醇的存在,所以我们要保护他们。另一个例子可能是如果你想要不同醇选择性氧化两种分子。我们可以添加更多的关于这个主题的文章。
你会注意到绝大多数分子遇到Org 1和Org 2只有一个重要的官能团。这是非常罕见的,会给你一个取代反应例如,有两个亲核试剂相当的实力。学习如何处理分子官能团有一个以上的关键是,在我看来,组织2结束,组织3开始。
在这一点上,你需要学习了解的相对反应活性不同的官能团,兼容不同的试剂,以及如何计划,只有这样的合成一个关键功能集团将参与反应。
在下一篇文章- - - - - -硫醇和硫醚
笔记
注1。是不是可能NaNH2可能deprotonated一点吗炔烃吗?当然!但请记住,酸碱反应平衡,酒精远强的酸(pK一个~ 16)比炔烃(pk一个25)。即使这乙炔化物形成,它将很快使质子化任何备用酒精R-OH游泳,引起的醇盐。(回篇文章)
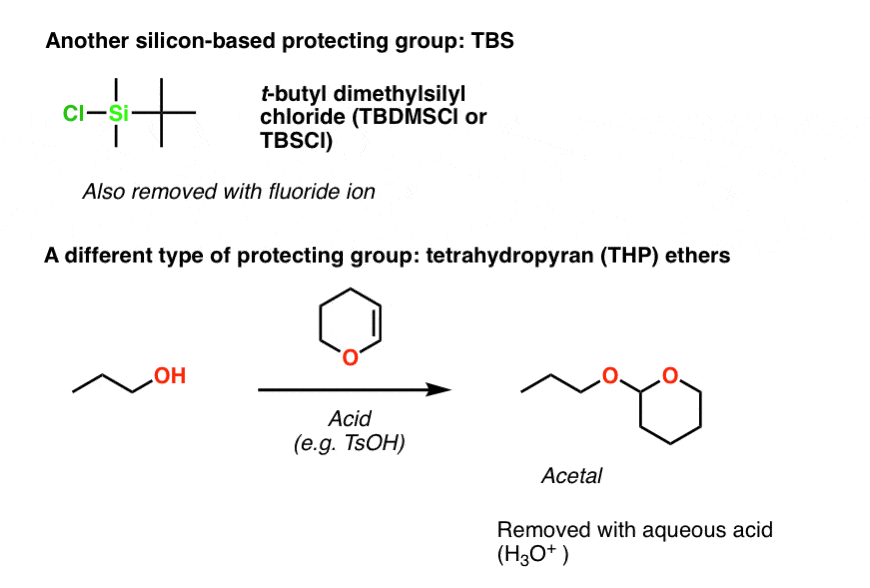
注2。两个保护团体经常是TBS (t-butyldimethylsilyl)和THP (tetrahydropyranyl)醚。TBS TMS安装相同的方式——通过使用TBSCl像网存在的基础3。
THP醚略有不同。他们通过添加dihydropyran安装(一个“烯醇醚在强酸的存在。”)的烯醇醚在碳的强酸使质子化,导致氧鎓离子,然后攻击酒精给醚。这实际上是一种特殊类型的醚两个或两个组在哪里连接到相同的碳。这是一个戴面具的酮,我们称之为一个缩醛。我们谈论缩醛树脂在这篇博客。(回到文章]
更加保护组醇,看到这个群的讲义教授安德鲁·迈尔斯哈佛大学。这是非凡的。
(高级)引用和进一步阅读
保护甲硅烷基醚:
- 保护羟基tert-butyldimethylsilyl衍生品
e·j·科里和Venkateswarlu
美国化学学会杂志》上1972年94年(17),6190 - 6191
DOI:10.1021 / ja00772a043
诺贝尔奖获得者的原始论文教授e·j·科里(哈佛)描述便利的条件(TBS-Cl,DMF咪唑)保护TBS-ethers醇。 - 代NONRACEMIC 2 - (t-BUTYLDIMETHYLSILYLOXY) 3-butynyllithium (S)乳酸乙:4 - (t-BUTYLDIMETHYLSILYLOXY) 2-pentyn-1-ol(年代)
詹姆斯·a·马歇尔,马修·m·Yanik尼古拉斯·d·亚当斯基思·c·埃利斯和哈里·r·Chobanian
Org。Synth。2005年,81年,157年
DOI:10.15227 / orgsyn.081.0157
这个合成的第一步有机合成(来源可靠的和可再生的有机合成实验过程)O甲硅烷基化与TBSCl根据科里的过程。 - 羟基硅烷保护:使用在多肽合成肽的亲油性修饰符
约翰·s·戴维斯克莱门特l . Higginbotham e .约翰郊区故事,查理布朗,Richard c . Treadgold
j .化学。Soc。,Perkin反式。1,1992年,3043 - 3048
DOI:1039 / p19920003043
介绍了易水解的动力学研究各种甲硅烷基醚在酸性和碱性条件下,并有一个方便的表第一页描述结果。 - 对称alkoxysilyl醚。一个新类的酒精保护组。tert-butoxydiphenylsilyl醚的制备
约翰·w·吉拉德Rejean福丁,霍华德·e·莫顿克丽丝汀Yoakim,克劳德·a . Quesnelle Sylvain Daignault, Yvan Guindon
《有机化学》杂志上1988年53(11),2602 - 2608
DOI:1021 / jo00246a038
本文描述了使用-SiPh2OtBu作为醇保护组与F容易去除- - - - - -相比传统-TBDPS醚。 - 选择性去甲硅烷基醚
托德·d·纳尔逊·r·大卫·克劳奇
合成1996年;1996 (9):1031 - 1069
DOI:1055 / s - 1996 - 4350
本文综述了甲硅烷基醚的选择性切除相似或不同的甲硅烷基的存在醚组在相同的分子。在有机合成,去保护策略是保护策略一样重要!醚还可以用于酒精保护。两种常见的醚基于保护团体THP - (tetrahydropyranyl)和妈妈(methoxymethyl)。 - 吡啶p-toluenesulfonate。温和、高效的tetrahydropyranylation醇的催化剂
渡边Miyashita Akira Yoshikoshi, Paul a .格雷科
《有机化学》杂志上1977年,42(23),3772 - 3774
DOI:1021 / jo00443a038
而p亚苄基酸通常是用作tetrahydropyranylation醇,催化剂比率(吡啶盐的p亚苄基酸)可以作为一个更温和的这个反应的催化剂。这是在试图保护的价值酒精与其他一些微妙的官能团的分子。 - 总合成(S) 12-hydroxy-5 8 14 -独联体,-10 -反式-eicosatetraenoic酸(萨缪尔森的HETE)
e·j·科里Haruki丹羽宇一郎,Jochen Knolle
美国化学学会杂志》上1978年,One hundred.(6),1942 - 1943
DOI:10.1021 / ja00474a058
本文演示了一个使用合成策略酒精保护组。基质组之一-哦是受保护的经过醚(后来deprotected条件未提及)ptsa的甲醇,1 h RT, 94%的收益率。 - 总合成的Stigmatellin Diastereo》拆分
迪特尔•恩德斯博士教授Gunter Geibel西蒙·奥斯本博士博士。
欧元。J。2000年,16(8),1302 - 1309
DOI:10.1002 / (SICI) 1521 - 3765 (20000417) 6:8 < 1302:: AID-CHEM1302 > 3.0.CO; 2 j
9- >3涉及到妈妈的保护。有趣的是,这是一个选择性的分子中羟基,因为,正如本文所说,“第二个羟基被一个氢键羰基函数(的)昊图公司-安置”。这表明我们通常的方式画结构并不总是反映的首选构象!
保护与妈妈——集团通常使用MOM-Cl(氯化methoxymethyl)。然而,由于这种化合物的极端毒性(它是一个强大的烷化剂,可以使烷基化蛋白质和核酸在我们的身体),为保护寻求替代方法,以下两篇论文由诺贝尔奖得主教授g . a . Olah给妈妈的替代方法——保护不使用MOM-Cl醇。 - Iodotrimethylsilane-Catalyzed Methoxymethyl醚的制备二甲氧甲烷的初级和二级醇
乔治•a . Olah阿尔塔夫侯赛因,Subhash纳
合成1983年,11,896 - 897
DOI:10.1055 / s - 1983 - 30554 - 的代谢物合成terrein曲霉菌terreus
约瑟夫·奥尔巴赫和史蒂文·m·发现
化学。Soc。化学。通讯。1974年,298 - 299
DOI:10.1039 / C39740000298
本文演示了妈妈的使用,保护总合成。两组-哦是最初由deprotecting保护妈妈醚醇盐与不,MOM-Cl紧随其后DMF在rt,最终合成,保护组被使用”浓盐酸的微量甲醇在62°15分钟”。
我将试试。尽管如此,醛是固体,而不是液体。
溶解在溶剂四氢呋喃或任何你使用的烯醇化物作为稀溶液(例如0.2)
一百万谢谢。你真是个罕见的宝石。
我试过几次用氢氧化钠、KOH MgI2,以及使用盐酸酸催化,但这一切都无济于事(查耳酮醛不deprotonating形式)。我想利用这次不,这就是为什么我关心保护羟基组。
为什么不直接pre-form LDA的烯醇化物四氢呋喃,然后添加你醛一滴一滴地在低温度?哦,可能会使质子化你的烯醇化物,但它是相当位阻。
我用3,5-di-tert-butyl-4-hydroxybenzaldehyde。我想把它与苯乙酮形式(E) 3 - 3, 5-di-tert-butyl-4-hydroxyphenyl 1-phenylprop-2-en-1-one
我用3,5-di-tert-butyl-4-hydroxybenzaldehyde。我想把它与苯乙酮形式(E) 3 - 3, 5-di-tert-butyl-4-hydroxyphenyl 1-phenylprop-2-en-1-one。
在这种情况下,很难保护因为它是夹在那些叔丁基组。
你有试过不管怎样运行反应吗?你pre-form苯乙酮,然后加入醛的烯醇化物吗?很好奇哦,是否会给你的问题。
否则这基本上是一个Claisen-Schmidt反应,其中约十亿例存在条件下,烯醇化物可逆和轻微的基础形式,我可以想象你可以得到这个。
我想做个酚醛使用强碱的醇醛缩合。我怎么能保护羟基的醛吗?
你是哪个个酚醛开始吗?
通常的过程将开始一个甲氧苯甲醛,然后试着去除甲基醇醛后TMSI之类。
温和的方法之一就是把hydroxybenzadehyde与KH和BnBr O-benzylated苯甲醛然后醇醛后,治疗与Pd-C, H2。或paramethoxybenzyl (PMB)和DDQ deprotect。
我在CH2OH面前deprotect ?
渗出性中耳炎Deprotecting从来不是乐趣。这取决于你的分子是稳定的。我会聘用基本条件(RS -极性非质子溶剂),因为可能电离CH2OH酸性条件。不知道其他的分子是什么样子,这很难说。
我想保护脂族噢的芳香,给我建议。
不知道你的分子看起来很难说。很容易有选择地保护芳哦,因为它是相当多的酸性,一旦形成醇盐会更亲核。一个想法是保护两组,然后有选择地deprotect芳香哦。
请告诉酒精与紫外活性基团保护
通常2-nitrobenzyl。看到https://en.wikipedia.org/wiki/Photolabile_protecting_group
我怎么保护氨基基团和东亚峰会期间反应为什么我需要这样做吗?
假设您有一个初级和二级醇分子。经颅磁刺激更喜欢一种吗?为什么?
理论上主要醇的位阻不如二级醇。你会认为经颅磁刺激可能是主要的选择。它是,但是在很小程度上。为了得到很好的选择性小学/中学,你必须使用一个非常庞大的保护组像TBDPSCl TIPSCl或者三苯甲基氯。但就像我说的你必须保护组比经颅磁刺激要大得多。
你好,
我有几个问题,我学习有机合成,
我明白可以倾心silylmethylether R -如果没有一个好的离去基团如(Br, Cl, OTs)是正确的,因为我没有读些什么呢?
非常感谢!
我不知道“R -意味着所吸引”。你能详细吗?
TBDMS-Cl优于TMS-Cl醇基的选择性保护,为什么
多笨重,因此对空间更敏感的因素。然而我更进一步并使用TBDPS。
保护组可以被用来保护哦集团存在的羧基官能团(保护)?
甲硅烷基组好,苄组织好。大量的选项。
我试图保护与氯化三甲基甲硅烷基芳基哦HMDS使用基地。在反应中显示出不同的位置。但当我们做柱层析法。它只返回给开始。甲硅烷基保护优惠在柱层析法吗?
解决方案是什么?请帮助我。
经颅磁刺激组极其不稳定,特别是在一个酚羟基。如果你要去甲硅烷基组,然后选择TBS或更重的东西。
如何添加/删除一个保护组织影响立体化学?例如羟基哦组楔形或破折号保持不变或会改变吗?
不会受到影响。就像去质子化,你只影响O-PG债券。反转stereochem你得反切断债券。
为什么不能叔醇保护tetrahydropyranyl吗
醚?
我不会说这100%的限制,可能存在异常,但如果你教这个,这是至少有两个原因。
1。THP保护涉及使用强酸,强酸会使质子化哦,导致损失的水形成一个叔碳正离子(稳定)。
2。叔醇相当位阻,攻击的速度叔醇的亲电试剂由设计马力的质子化作用可能是缓慢的。
希望这可以帮助!詹姆斯
谢谢你的建议我会考虑更多的细节。
我正在寻找方法来保护骨骼分子上的羟基,羧基最后需要保持活跃。有可能掩盖一个哦在骨头酸链仍“活跃”的尽头?
理查德。
试图使氯化羧基,然后保护羟基,然后添加水分子,生产所需的产品。使用保护代理,不与盐酸溶液反应,将反应产生的水与cocl组的结束你的分子。
谢谢你非常详细的帖子!爱的例子与画家的磁带。