羧酸衍生物
二异丁基氢氧化铝(DIBAL)用于酯类和腈类的部分还原
最后更新:2022年11月2日|
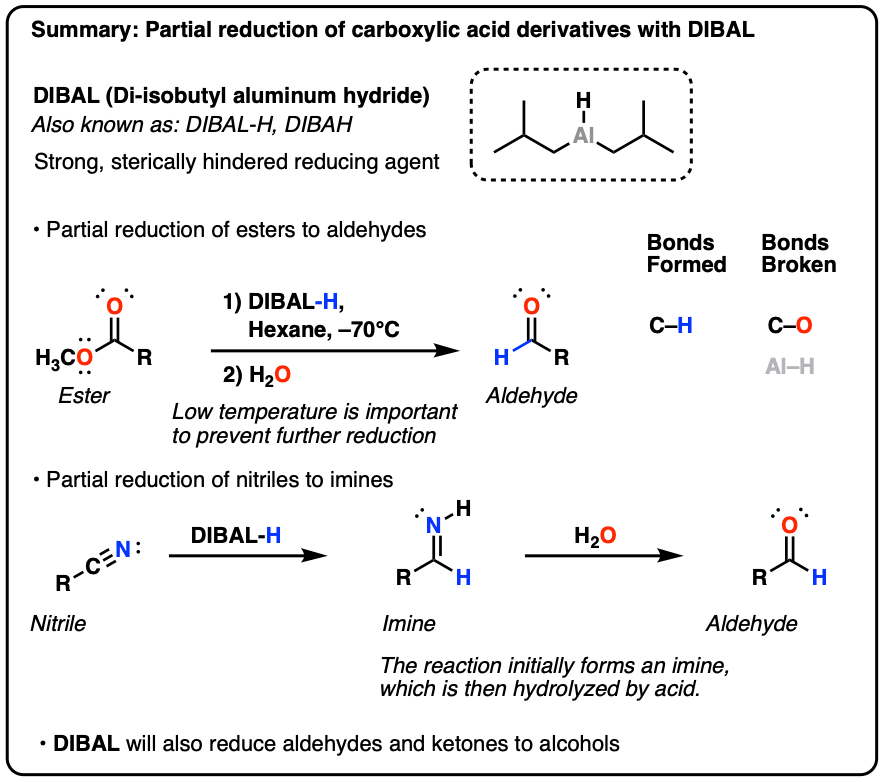
DIBAL(Di -异丁基氢化铝)-体积庞大还原剂的部分还原酯类而且腈
- DIBAL(亦称DIBAL-H或DIBAH)是一种坚固、笨重的还原剂.
- 它对还原是最有用的酯类醛。
- 与氢化铝锂不同,它不会还原醛进一步提供只加入一个等价物,反应混合物保持低温。
- 它也会减少其他羰基化合物如酰胺、醛、酮和腈.
目录
1.二异丁基氢氧化铝的结构
DIBAL是坚固的,笨重的吗还原剂.在反应性方面,它与氢化铝锂有很多相似之处。
不像LiAlH4它(理论上)可以产生四等量的氢化物,DIBAL只有一个Al-H键。
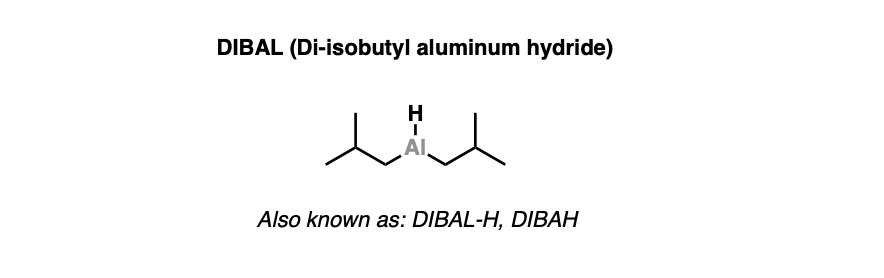
这使得其反应的化学计量学更容易控制。
2.二巴尔还原酯制醛的研究
最引人注目的反应DIBAL是还原酯类醛。不像锂铝氢化物(LiAlH4),以减少酯类到伯醇,还原与DIBAL可以停在醛阶段,如果温度保持很低。
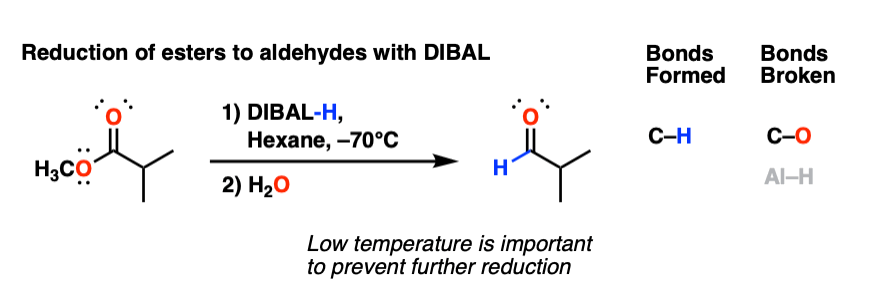
的优势DIBAL这里它更有效率。如果我们用LiAlH4,我们得到a伯醇,然后我们必须氧化到醛使用试剂如PCC, Dess-Martin周烷,或者Swern氧化。(看到帖子:酒精氧化)
3.二异丁基氢氧化铝还原酯制醛的机理
还原的机制酯类变成醛DIBAL大致类似于我们熟悉的亲核酰基取代的加成-消除机制,只是第一步略有修改。(看到帖子:亲核酰基取代)
DIBAL-H是中性的,铝和硼在元素周期表的同一列,有一个空的p轨道。这就是路易斯酸。
的羰基氧气的酯类是一个路易斯碱.第一步是路易斯碱的配位羰基氧向路易斯酸性铝,给一个带负电的物种形式电荷在铝。
然后氢化物(H-)亲核加成羰基碳和C-O键的断裂(形成C-H,破坏C-O键)。(看到帖子:羰基的亲核加成)
这就形成了一个新的四面体中间体本质上是半缩醛与铝相协调。(看到帖子:缩醛和半缩醛)
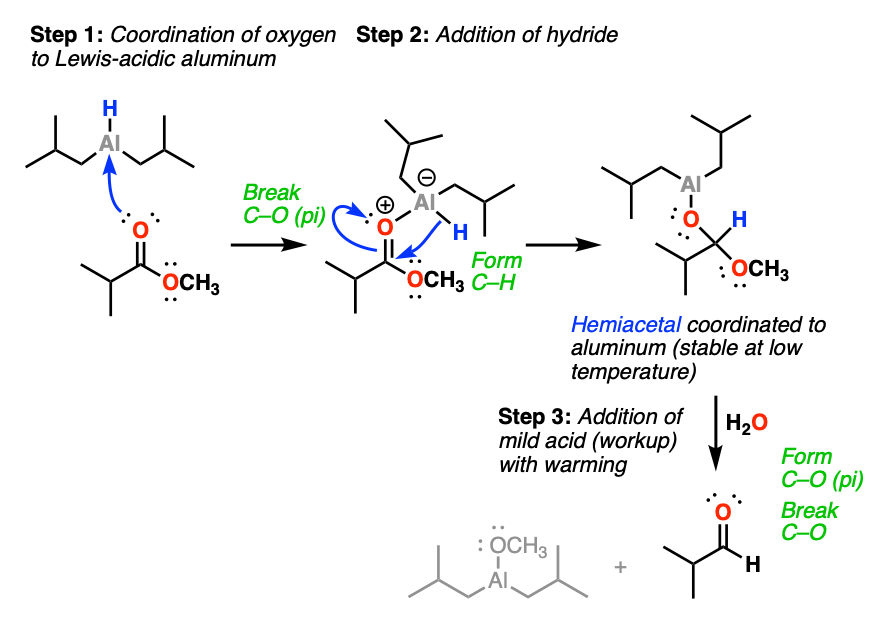
如果保持较低的温度(方便的干冰-丙酮通常引用-78°C的浴),在此阶段用酸淬灭的反应将产生中性半缩醛哪个快丢了卢给一个醛.
(注:得到的反应停止在醛舞台在纸上看起来很棒,但在实践中有时很难实现)
4.DIBAL将腈还原为亚胺(随后水解为醛)
DIBAL还会不会做部分削减腈亚胺。亚胺在加水后水解成醛。(见文章:亚胺-性质,形成和机理)在这方面DIBAL再次不同于LiAlH4,这将减少腈一直到初选胺.
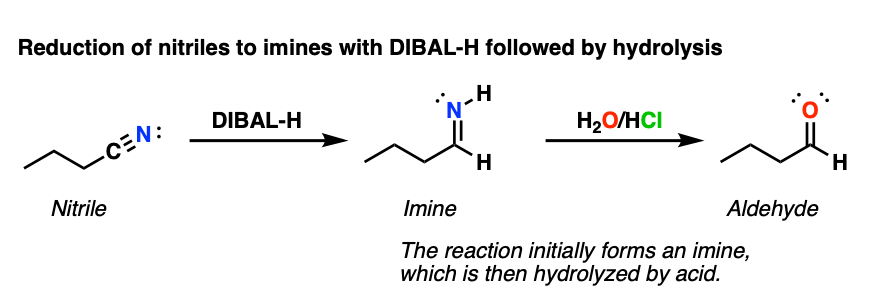
5.腈还原成亚胺:机理
减少腈遵循类似于还原的机制酯类.路易斯基式的配位腈氮到铝,其次是氢化物的交付腈碳(C-H, C-N (pi))。这是加法机制的另一个例子。
从这一点开始,用水猝灭反应导致氮的质子化,然后亚胺水解产生an醛.
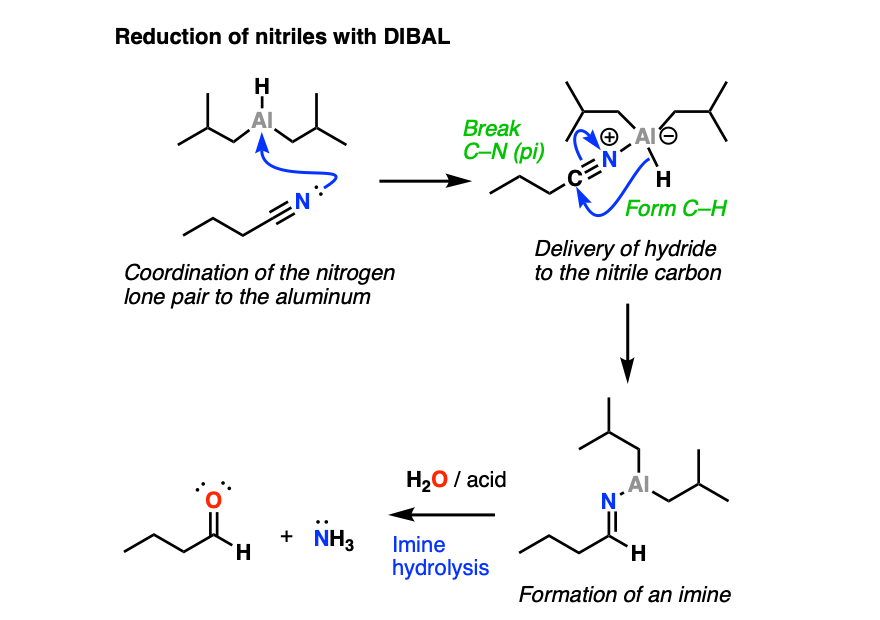
6.二异丁基氢氧化铝(DIBAL)还原酮和醛为醇
虽然不常用这种方式,但值得注意的是DIBAL能做所有的还原吗NaBH4所以酮和醛分别被还原为仲醇和伯醇。
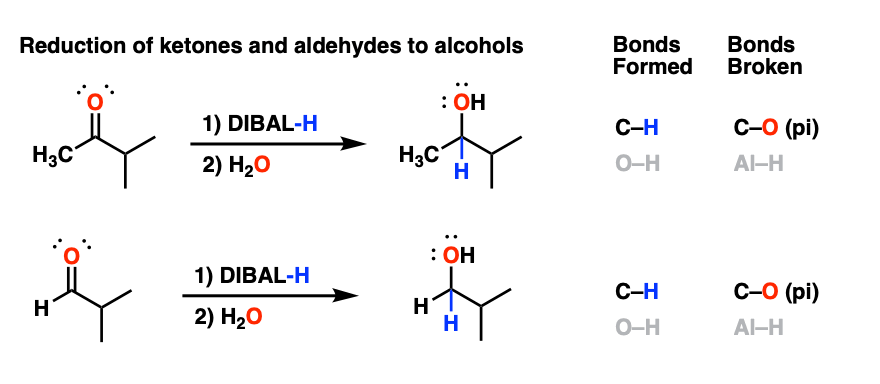
这意味着DIBAL会不会选择性地减少酯在一个没有保护的人面前醛或酮这些群体也会减少。
7.摘要:DIBAL
DIBAL对部分还原是有用的试剂吗羧酸衍生品。一个成功的DIBAL减法酯到一个醛相对于LiAlH4,将节省额外的步骤,然后是氧化。
同样的,DIBAL减少腈为我们提供了一种通过LiAlH4完全还原而无法获得的醛(水解后)的途径腈来胺.
笔记
从这篇文章(摘要可免费获取):
- 醇和硫醇与氢化物反应生成氢2和它们对应的共轭碱
- 共轭醛和酮在C=O时还原得到烯丙基的醇
- 羧酸释放H2生成羧酸
- 烷基卤化物是惰性的。
- 环氧化合物主要在阻碍较少的位置还原生成醇
- 叔酰胺被还原为胺,但伯酰胺只缓慢地减少。
注2.你能读到关于化学的DIBAL以及《有机化学试剂指南》中的80多种本科有机化学试剂,可以在这里下载PDF文件.
测试你自己!
(测试)
(高级)参考资料和进一步阅读
- 金属组织,XXVII铝三烷基和二烷基‐氢氧化铝
齐格勒,k;马丁,h;克虏伯,F。李比希。安。化学196062914 - 19 (1)
DOI:10.1002 / jlac.19606290103
二异丁基氢化铝(DIBAL或DIBAL-H)最初是由诺贝尔奖得主K.齐格勒教授研究作为聚合的辅催化剂烯烃.两篇关于DIBAL-H还原酯类: - 减少酯类将羧酸和二异丁基氢氧化铝反应成醛
路易斯安那州扎哈金;我叫霍丽娜。列托人。1962年,3.(14), 619 - 620
DOI:10.1016 / s0040 - 4039 (00) 70918 - x - 二烷基铝氢化物还原
阿尔弗雷德·e·g·米勒,简·w·比斯,路易斯·h·施瓦兹曼
有机化学杂志195924(5), 627 - 630
DOI:1021 / jo01087a013 - 二异丁基氢化铝与含有代表性官能团的选定有机化合物的反应
Yoon Nung Min和Young Soo Gyoung
有机化学杂志198550(14), 2443 - 2450
DOI:1021 / jo00214a009
本文详尽地介绍了有机化学中基本每一类官能团的还原DIBAL- h。 - 二异丁基氢化铝(DIBAH)和三异丁基铝(TIBA)作为减少代理有机合成
埃克哈德•WINTERFELDT。合成1975;1975(10): 617 - 630
DOI:1055 / s - 1975 - 23856
经典的用法回顾DIBAL-H和三异丁基铝的有机合成。即使这可能是今天的,它仍然是一个有价值的资源。 - 碘化铟原位生成富对映体烯基试剂的合成与利用及其与醛的加成:(2R,3S,4S)-1-(叔丁基二苯基硅基氧基)-2,4-二甲基-5-己烯-3-醇
布莱恩·a·约翰斯,查塞塔·m·格兰特和詹姆斯·a·马歇尔
Org。Synth。2002,79现年59岁
DOI:10.15227 / orgsyn.079.0059
本程序中的C步是硅基保护酒精接着是DIBAL-H还原酯.注意罗谢尔盐(酒石酸钾钠)的特殊工作条件DIBAL减少- h。
回复:现实生活中的免责声明。伙计,那些水解铝盐是我经历过的最恶心的乳液!
根据我的论文,我最大的DIBAL-H还原量是175 mL CH2Cl2中的10.1 g (17.9 mmol)。对我来说,关于这种反应的好消息是双重的。1)原料为明亮的蜡笔黄色,产品无色。2)反应是瞬间的。就像在DIBAL-H中滴定。奇怪的是,它总是需要2当量的DIBAL(仍然不太清楚为什么,只加入了1当量的H-),但只要黄色消失,我就确定反应的转化率是100%。当然,为了确保万无一失,我会做一个TLC检查,而且它总是完整的。
然后用饱和aq淬火反应。罗谢尔的盐(嗯…TIL Rochelle是它被发现的城市,而不是那个家伙的名字)来帮助打破铝乳液。我们实验室还根据经验发现,用大量的Et2O稀释CH2Cl2反应有助于打破乳液。坏消息是你必须让这种双相混合物搅拌大力至少90分钟-2小时后再分离。只要加入足够的Et2O,乳剂就会分解,如果搅拌时间足够长,分离就变得非常容易控制。
(如果你想知道,92%的醛收率和93%的酯的“另一面”回收率(它是一种珍贵的手性助剂,我们想重复使用它!)
今年我做了几次DIBAL还原,经常遇到麻烦——特别是,如果你的产品是水溶性的,并且在检查中喜欢水相(一个人永远无法确定),那么尝试从充满罗谢尔盐的饱和水相中恢复它绝对是一件可怕的工作。
有人向我建议,Fieser工作之后,过滤在Celite应该删除铝盐乳液一样好。从现在开始,我可能会把这种方法作为首选,因为试图从罗谢尔盐溶液中提取我的产品给我带来了很多痛苦!
此外,重新阅读这个网站正确,我现在将总是使用H2O淬灭我的DIBAL腈还原。我之前错误地使用了甲醇,看看上面亚胺水解的机制,这可能解释了为什么当我用甲醇淬亚胺时,我得到了一堆讨厌的垃圾!我想我可以把反应倒在0摄氏度的水中,而不是直接在-70摄氏度下淬火。
我个人不能获得醛在一个场合,我尝试DIBAL。部分问题可能是(旧的)DIBAL的刻度(<25毫克)和滴度,以及没有选择好溶剂(应该使用CH2Cl2而不是乙醚)。所以我用DMP重新氧化了酒精,就搞定了。
铝盐因其令人讨厌的乳剂而臭名昭著。对于DIBAL,我一定要用罗谢尔盐搅拌很长一段时间。对于LiAlH4,我总是使用Fieser检查和过滤固体…不需要提取,感谢上帝。
总之,我还原的不是酯,而是硫酰亚胺。这是一个(OH-protected)利用噻唑烷硫酮的醛醇加合物作为手性助剂。我们在实验室开发了醛醇加成的条件。可以说我们做了非对映选择性的醛醇加成很多.将硫酰亚胺部分还原为醛是常见的下一个转变,所以我们冰箱里总是有一瓶新鲜的DIBAL。我用这种方法还原了5种不同的硫酰亚胺,谁知道我在合成过程中做了多少次谁知道我做了多少次。
我唯一一次还原的酯是0.7 g (2.4 mmol)。醛收率68%,醇收率30%。还用DMP将酒精重新氧化回63%的醛(或87%的酯->醛),这种还原是在fraster - seebach烷基化(这是一个痛苦的过程(-40度,3天),但经历了一个伟大的反应。
不是DIBAH而不是DIBAL吗?
它可以被称为DIBAH、DIBAL或DIBAL- h。有机化学家们在讨论时,通常会称它为DIBAL,因为它比其他两种都更容易从舌头上滚下来。
我们能在-70°C通过DIBAH从酮中获得酒精吗?我知道在室温下可以,但我不知道在-70°C下是否可以。你有什么推荐信吗?
你能证明水解是如何发生的吗?我有点卡住了
在酸性条件下,将铝盐转化为半缩醛。别担心,学生们一直都有这个问题,因为,嗯,他们就是这样。当我们批改小测验时,学生们看到酸条件下的半缩醛时就会抓狂,他们不知道下一步该怎么做。然后学生们继续使用OH-因为记住学生们的说法,OH-在酸性溶液中总是可用的。
我用2,5-3,5当量把酯还原成醇。所以不,它不会在醛处停止,实际上在醛处停止还原比继续还原为醇要困难得多。
那是因为你使用了不止一个eq。
你的DIBAL在与氧协调时是否获得了一个额外的碳原子?
开枪。是的,确实如此。固定
我用了6年的DIBAL来打开我的异丙基环,它工作得很好,但当我使用新的DIBAL时,它产生了不寻常的报告,有人感觉像这样的任何prb吗
DIBAL-H的降解产物是什么?
这也能还原羧酸吗?
不,DIBAL-H不与羧酸反应。你有两个选择:例如,将-COOH酯化为-COOMe,然后使用DIBAL-H,或者你可以直接将-COOH与其他试剂如LiAlH4或NaBH4一起使用。
是的。谢谢克里斯!
通常用几当量的二乙醛将酯还原为乙醛,而不是如上所述的一当量。重要的是保持温度低[<-50],并在低温下淬火(我一直用MeOH而不是水来淬火-水在这个温度下会结冰!)
仅仅使用1eq是没有用的,因为醛比酯更容易还原。
喜欢这个网站,到目前为止,我从中学到了很多:)
迪巴尔还有一个锦囊妙计。如果你得了a,b, unsat。酯或酮,它可以干净地还原而不影响双键。不像NaBH4或LAH。
事实上,我只是在计算时不小心用了2 eq. DIBAL,得到了100%的酒精,没有一丝乙醛,所以我不会这么着急超过1 eq。
在烷基腈制备醛的最后一步中,氨(NH3)是如何形成的——我的意思是,哪里有一个额外的氢质子(H+)可以形成NH3?提前谢谢你。
当加水时,它会在检查步骤中出现。有多余的水。
你好,
我想把酯还原成醛。
我会在DCM中尝试-78°C的DIBAL。
如果不行,我就把它还原成酒精然后用PCC氧化。
我的问题:
1)我认为非极性溶剂会使反应变慢。那么我应该用甲苯代替DCM吗?
2)如果要喝酒,为什么-78°C ?我不能在0°C做吗?
我应该把酯加到迪巴尔还是相反?
3)最后一个问题,如果我去乙醛,可以用甲醇淬火吗?水在-78°C时会结冰。
另外,您对这篇在0℃时将NaOtBu加入到Dibal中还原为醛的文章有什么看法?
非常感谢
我会在网上寻找有人成功地将酯还原为醛的记录。例如,如果你去ACS出版物主页,搜索“酯二酸还原醛全合成”。你会提出一些有信誉的论文和支持信息。利用这些条件。
比如,这样做:http://pubs.acs.org/action/doSearch?text1=baran+ester+reduction+aldehyde+dibal&field1=AllField
如果你想要乙醛,你必须把它保持在-78。非极性溶剂是理想的。避免空灵溶剂(它们倾向于与铝配合,这可能会影响反应性),DCM应该没问题。甲苯可能存在溶解度问题,但在-78度对你来说可能没问题。如果你的目标是酒精,那么加热是可以的。
我还没有看到你最后提到的那篇论文。
在Dibal还原反应机理中,从酯到醛,我们知道OCH3是一个不好的离基,但它还是出去了。请解释一下??我必须在研讨会上解释这个dibal机制
DIBAL还原生成O(-), O(-)本身是强碱。因此,碳氧双键的形成伴随着CH3O(-)的排出并没有伴随巨大的能垒。CH3O(-)不是一个很好的离去基,但仍然比H(-)或大多数碳基离去基好得多。
我还想知道DIBAL-H是否可以用来还原羧酸?!如果是的话,产物会是醛吗就像我们用DIBAL-H还原酯一样?
你真的得打开它。这是有可能的,但你必须用超过3个等价物来加热。它远远优于使用LiAlH4 !
“dibal h”能减少酸氯化物吗?
是的,它应该生成醛。
在芳香族硝基存在的情况下,是否有可能将乙酯还原为醛?
在其中一个评论中提到使用LiAlH4来还原羧酸,为什么会这样?为什么不和迪巴尔在一起
它是低效率的。LiAlH4相当便宜,你必须使用更少的等价物。
所以. .在酯上使用DIBAL-H,得到醛。酯的另一个有机部分呢?[RCOOR ']那R '部分呢?我想我们要一个酒精[OR '] ?
是的,这是正确的。
你可以通过回流甲醇来分解铝络合物。DIBAL 2等在零度时将酯还原为醇。1 Eq DIBAL在-78时将酯还原为醛。这些反应是干净的。产量超过90%。与甲醇回流后,可以进行硅滤,浓缩甲醇提取物,甚至不需要做柱。当然不应该有其他竞争团体。
根据我的经验,让它停在醛上是反复无常的,而且非常依赖溶剂。在甲醇中回流似乎很极端…为什么不像其他人一样使用罗谢尔盐?
U在评论中说,要还原羧酸,可以用NABH4,对吗?
羧酸只容易被LIAlH4和二硼烷还原。
不,NaBH4不能还原羧酸。关于LiAlH4和BH3你是正确的
我不明白这种中间产物怎么有资格被称为半缩醛。我的意思是通式R1HC(OH)OR2的-OH基团在哪里
它本质上是半缩醛的共轭碱,Al和氧配位而不是H。
感谢James的回复