醛和酮
亲核加成,羰基
最后更新:2022年11月30日|
亲核加成,金属羰基合物
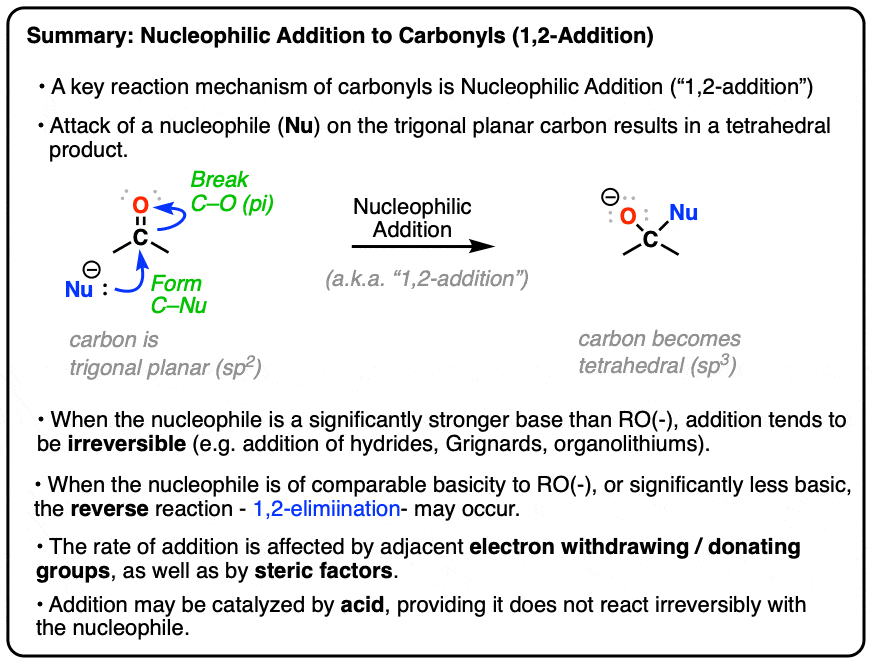
- 最重要的反应羰基集团(C = O)是增加的亲核试剂羰基碳,有时被称为,“加法”。
- 亲核加成改变了杂交从sp的碳2对sp3三角形的几何平面四面体。
- 这取决于的碱度亲核试剂,除了可能是不可逆的(如氢化和烷基组)或可逆的(例如,HO -醇、(- CN)。
- 相反的过程是消除或经常“1,2-elimination”。
- 增加的速度增加了相邻吸电子集团,和减少了相邻electon-donating组。
- 率也降低了空间因素。
表的内容
- 羰基的属性
- 亲核加成羰基(加法)
- 不可逆转的加法,并有很强的基地
- 可逆加成
- 增加的速率影响因素:电子效应
- 增加的速率影响因素:立体效果
- 添加中性的亲核试剂
- 总结
- 笔记
- 测试你自己!
- (高级)引用和进一步阅读
1。羰基(C = O)的属性组
一个C = O债券被称为羰基组。他们发现醛、酮、羧酸及其衍生物。
由于氧的电负性明显高于相对于碳(3.5)(2.5),C = O键的电子高度极化对氧气。
这反映在上发现的部分正电荷部分负电荷的碳和氧。
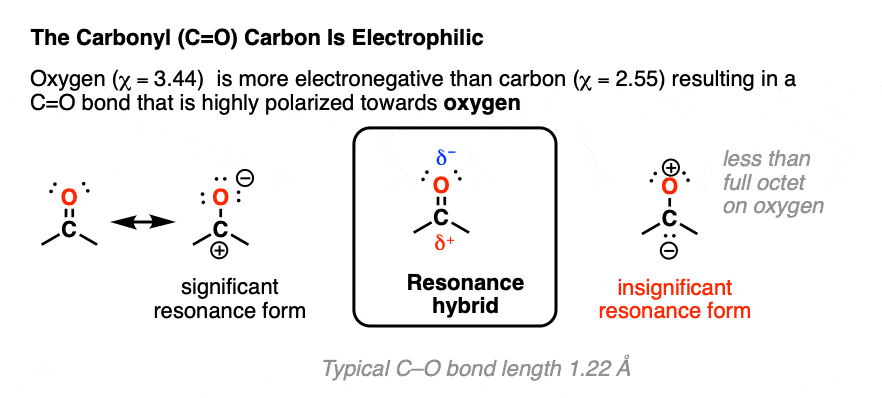
羰基组有明显的共振形成有一个正电荷碳和氧的负电荷。
共振形成碳负电荷和正电荷在氧气从来没有被吸引,因为它代表着不到一个完整的八隅体氧大力这是非常不利的。
2。亲核加成,羰基
这个反应,亲核加成,有时,“加法”。
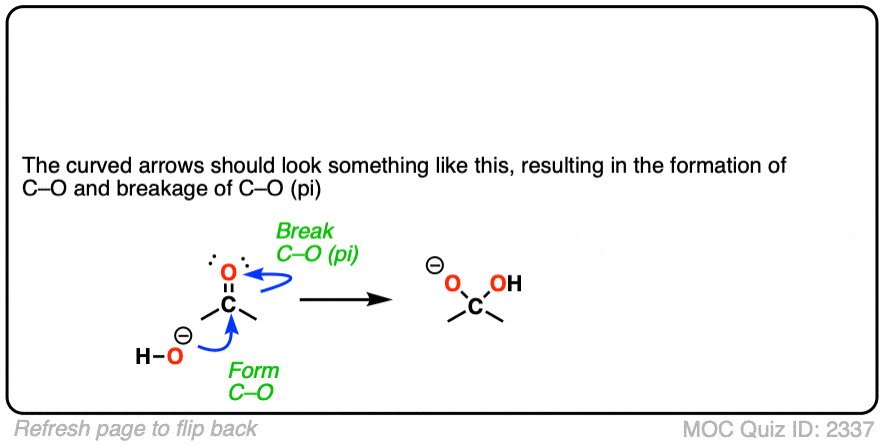
在这个反应形成C-Nu债券和切断π键断裂。碳从三角形的几何平面四面体。后,氧气熊消极形式电荷。
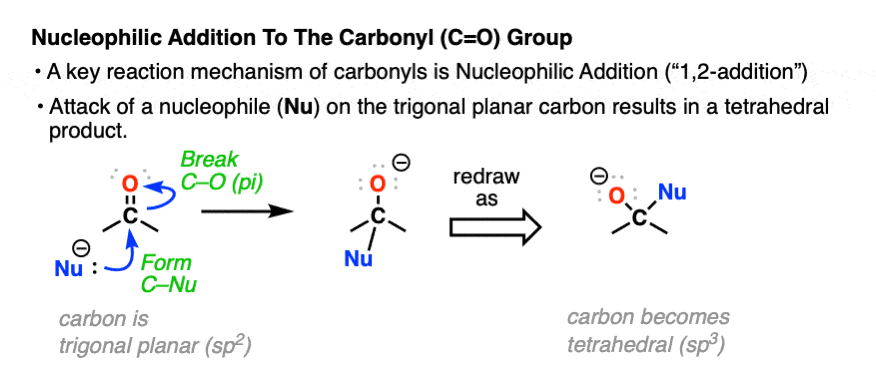
例如醛和酮进行添加与氰根离子给氰醇。
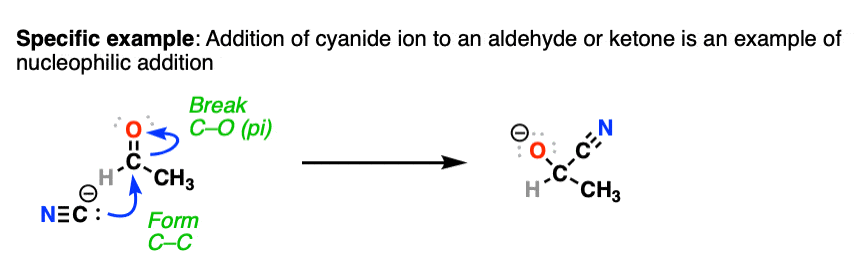
这种机制的重要性羰基化学再强调也不为过。确保你知道如何画这个反应的弯曲的箭头!
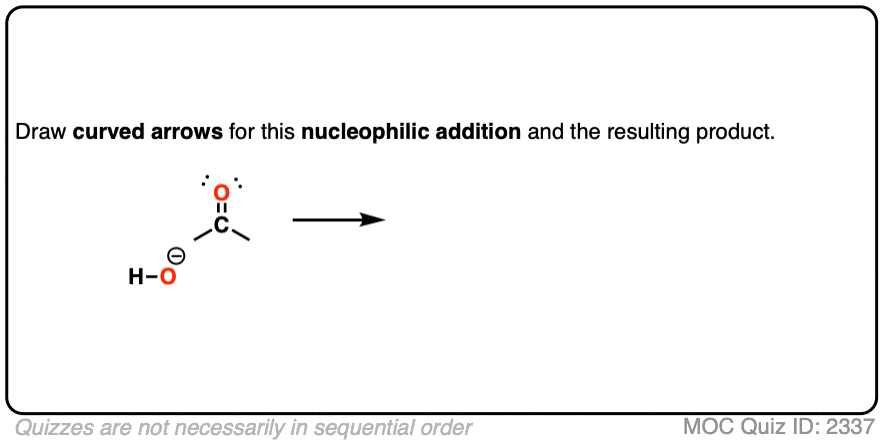 点击翻转
点击翻转
这种逆过程被称为消除,或者“1,2-elimination”。在这个机械的步骤,C-LG债券被打破和切断π键组成。
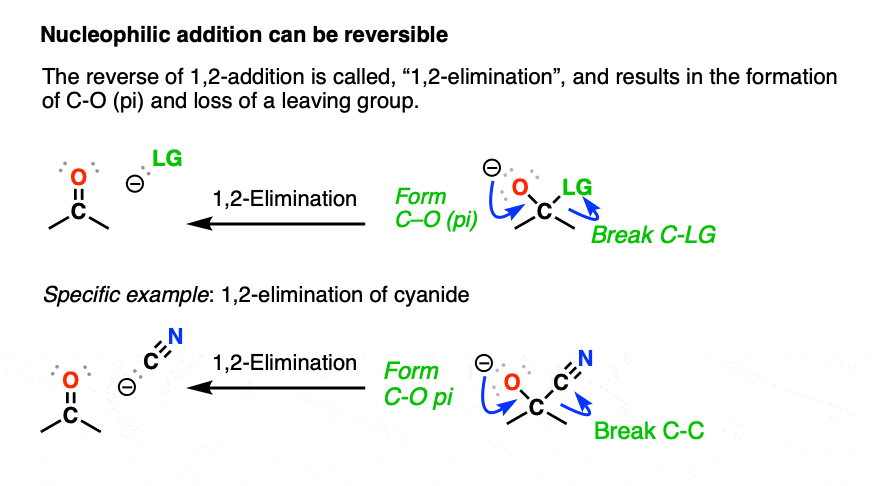
综上所述,1、加法和1 2-elimination是两个最重要的化学机械的步骤羰基集团和他们发现大量的机制。
3所示。不可逆转的亲核加成
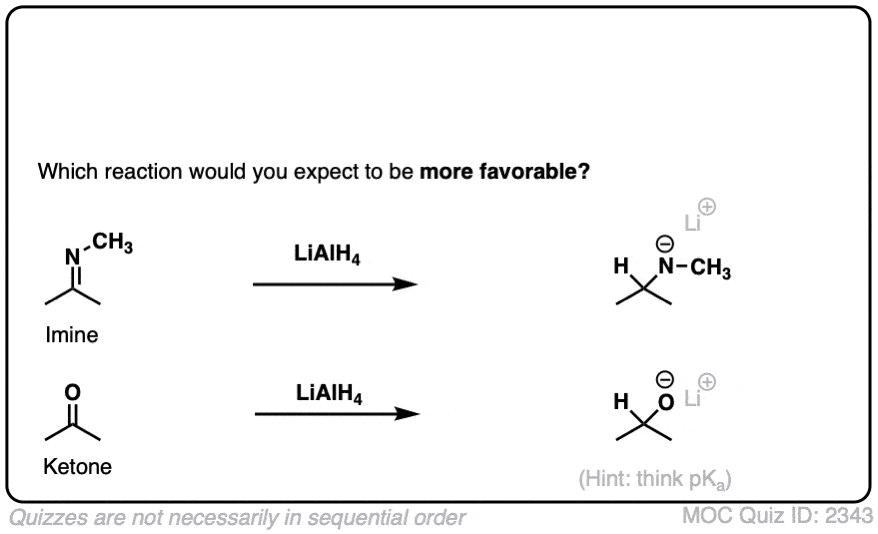
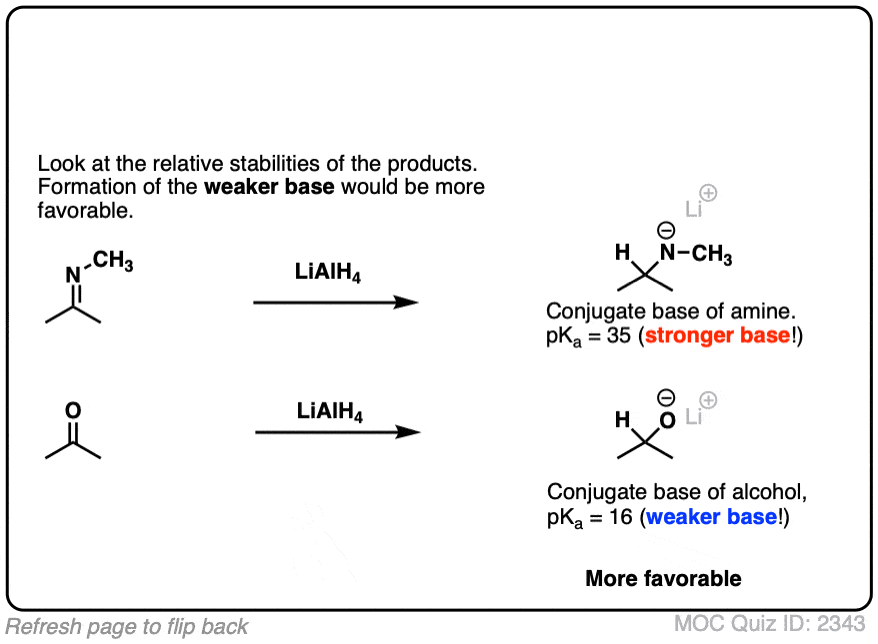
比较的相对碱度的开始亲核试剂ν(-)带负电的氧气产品可以极大的帮助确定平衡的位置。
就像在酸碱反应,有利于平衡是一个更强的酸和给弱酸性和弱碱性强基础亲核加成反应,导致的形成较弱的基础将青睐。
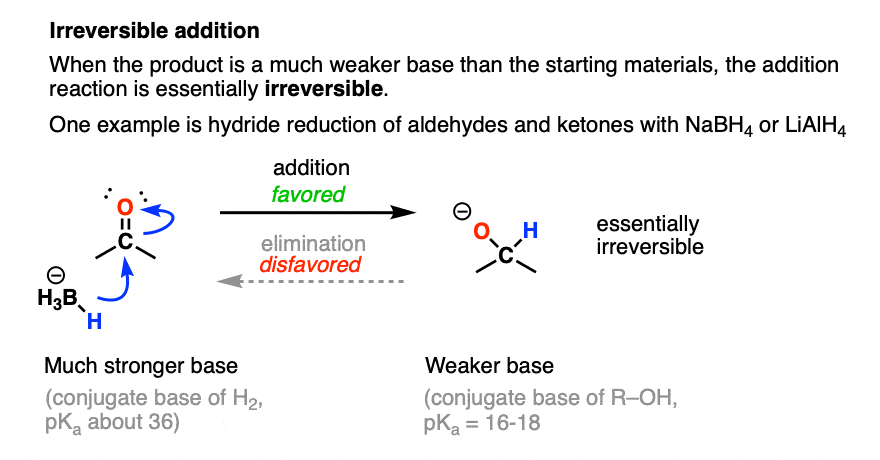
当亲核试剂恰好是一个非常强大的基础,除了反应本质上是不可逆转的。
一个典型的例子是醛和酮的还原硼氢化钠,NaBH4。
的pK一个H的2,共轭酸氢化的离子H(-)是关于36和pK一个卢武铉的共轭酸产生的醇盐大概是16。
从酸碱的角度来看,这个反应是深受20 pK一个单位(1020.)。平衡跑远正确的。(注1]
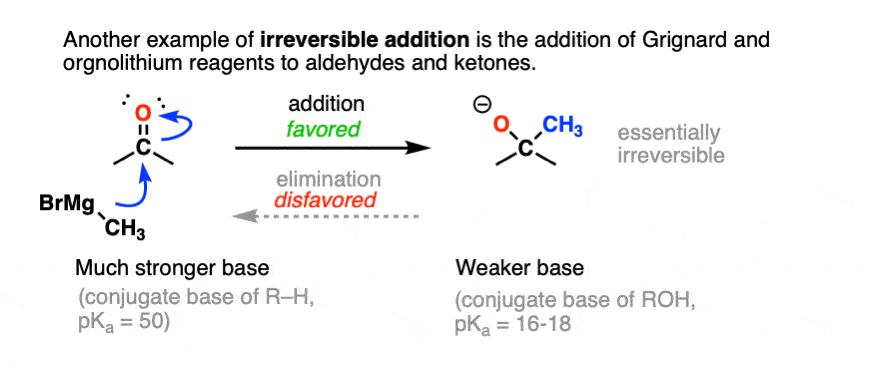
不可逆之外的另一个例子是增加格氏或organolithium试剂对醛和酮。
的pK一个负碳离子约50。所以在这种情况下将不好的逆反应约34 pK一个单位。
4所示。可逆加成
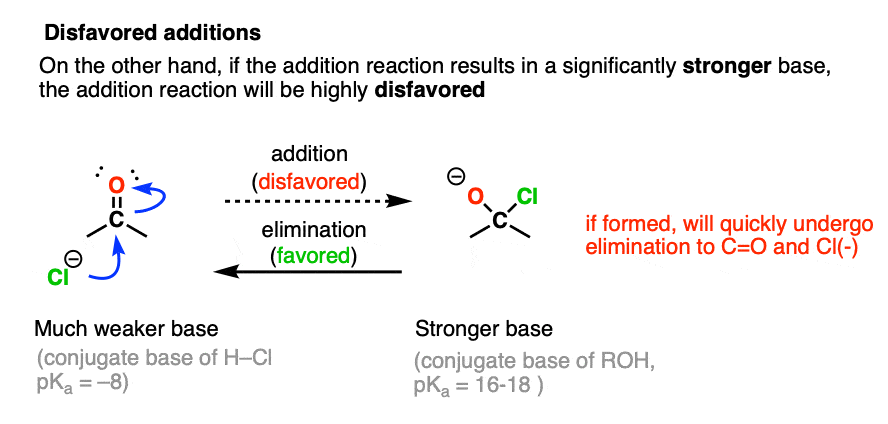
在天平的另一端,卤化物离子如Cl (-)不通常添加到金属羰基合物。我们可以看到通过比较碱度的原因。
的pK一个的盐酸,共轭酸Cl (-) 8。的pK一个一个典型的酒精卢武铉的范围在16日至18日举行。添加卤化物离子会导致的形成强大的基础从一个较弱的基础,这是大力不利。
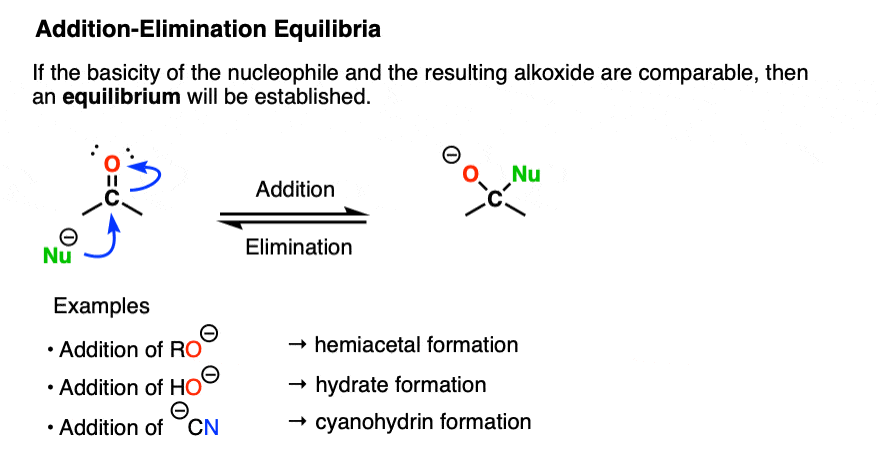
当的碱度亲核试剂可比产品的碱度,一个平衡的结果。
这是添加氢氧化的情况,醇盐氰离子。
可比性是什么意思呢?一个好的经验法则是包含在注2]
5。亲核加成率的影响因素。电子效应
增加的亲核试剂羰基化合物大大影响周边取代基。
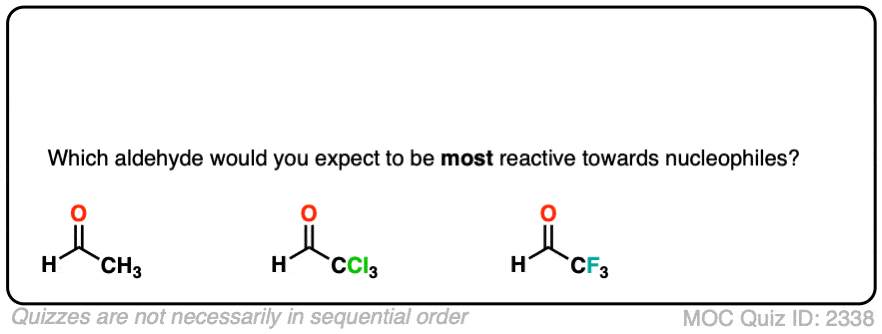
一方面,electron-poor越多羰基碳,将对的亲核试剂的反应。例如,我们应该期待系列乙醛的反应性与三氯乙醛与trifluoroacetaldehyde增加与增加电感取代基的影响。
 点击翻转
点击翻转
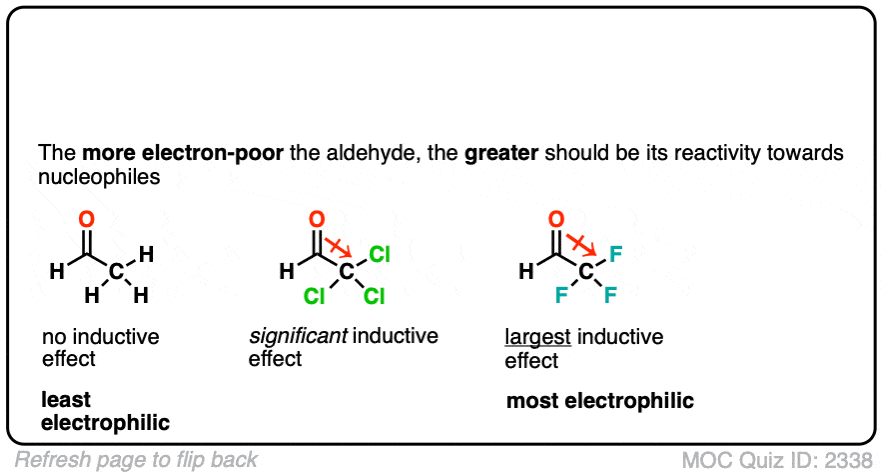
向着相反的方向,我们应该期待electron-releasing取代基产生相反的效果。
您可能还记得,烷基组激活在亲电芳香取代,因为他们稳定相邻碳正离子,相对于氢。
完全基于这种电子效应我们因此希望除了更快醛比可比酮(这是!尽管立体效果也扮演了一定的角色)。
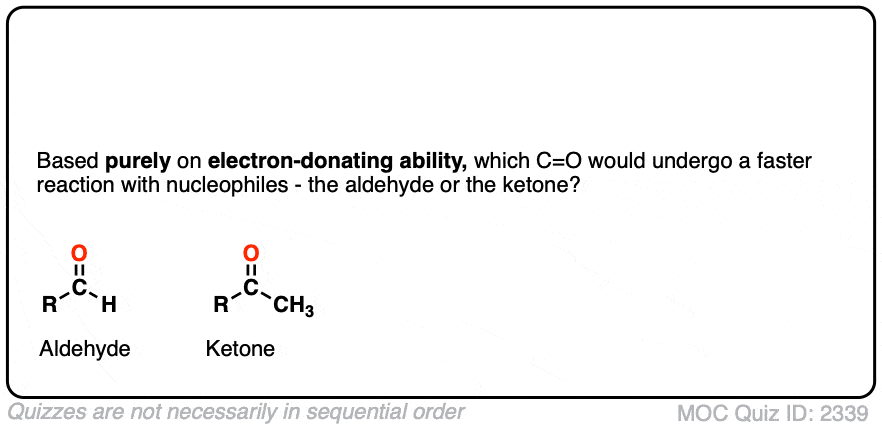 点击翻转
点击翻转
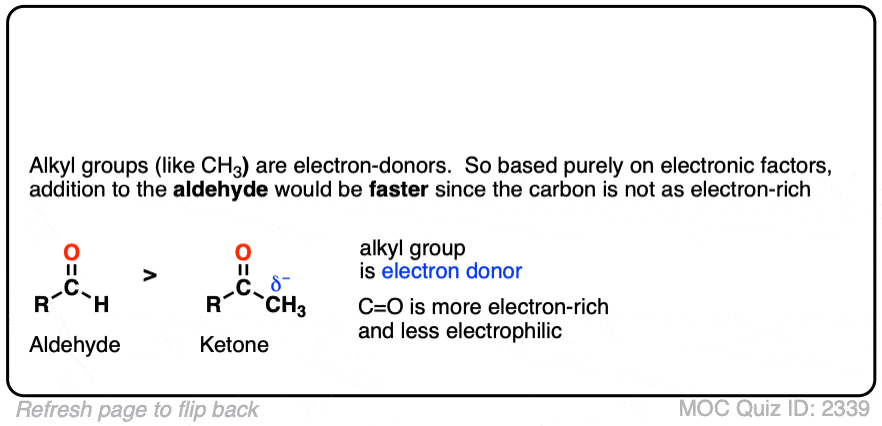
您可以使用类似的推理预测的相对反应活性酯类、酰胺和羧化物。(注3]。
6。亲核加成率影响因素:立体效果
除了金属羰基合物也受到任何团体的存在可以阻止传入的方法吗亲核试剂。这些被称为立体效果。
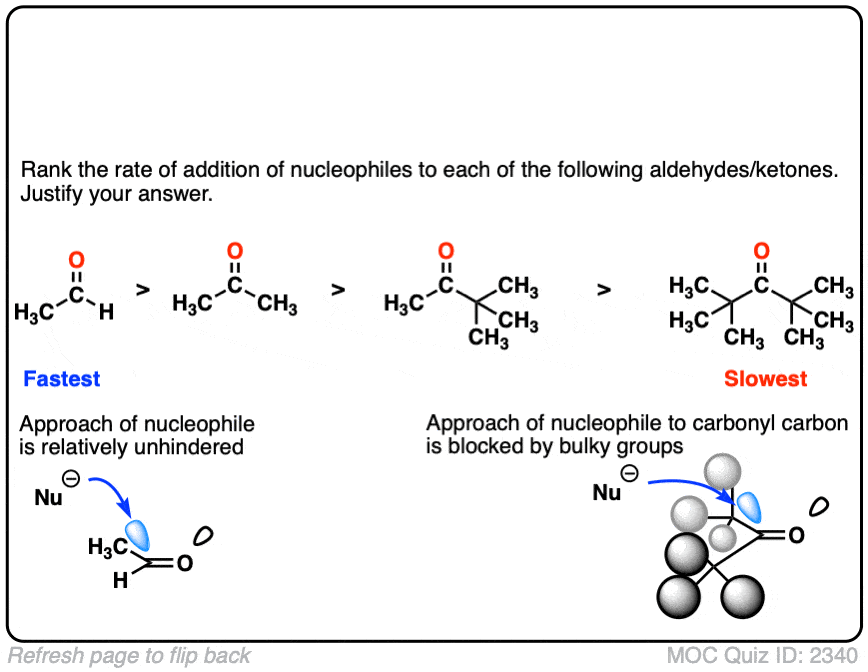
一个著名的例子是醛和酮的加入的亲核试剂。除了酮相当慢。(注意4]
如果我们批量酮更包括,邻叔丁基组,将进一步受到阻碍。(注5]
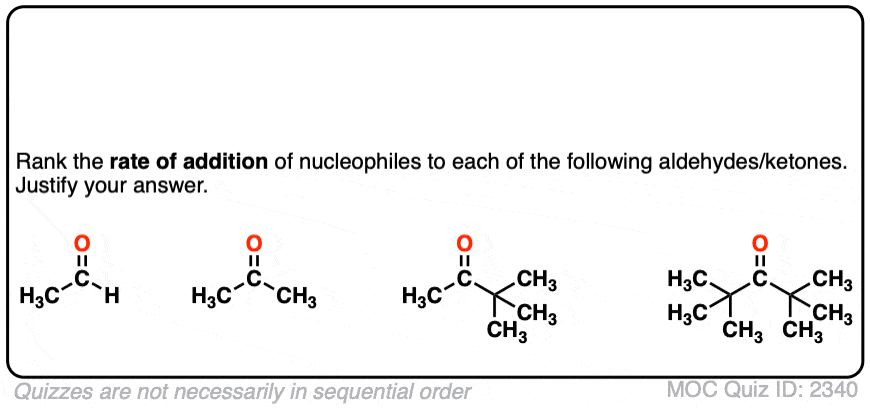 点击翻转
点击翻转
7所示。中性的亲核试剂
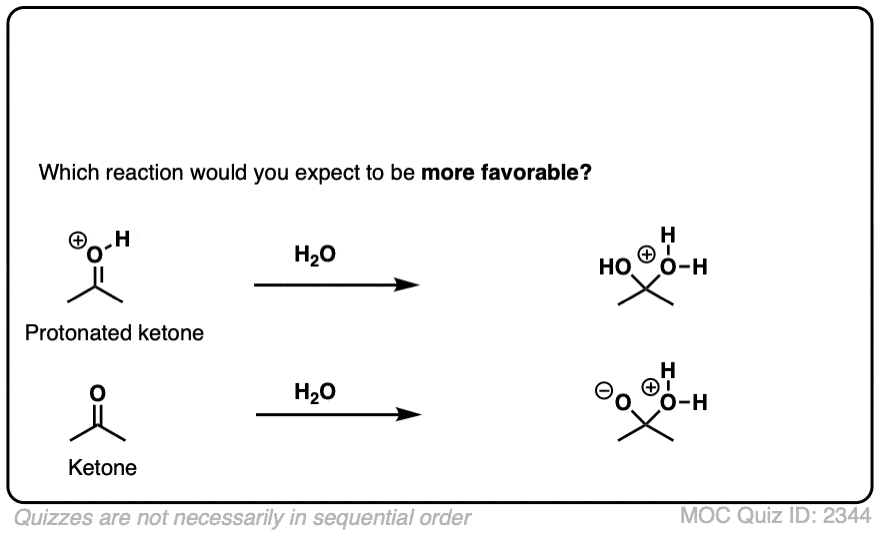
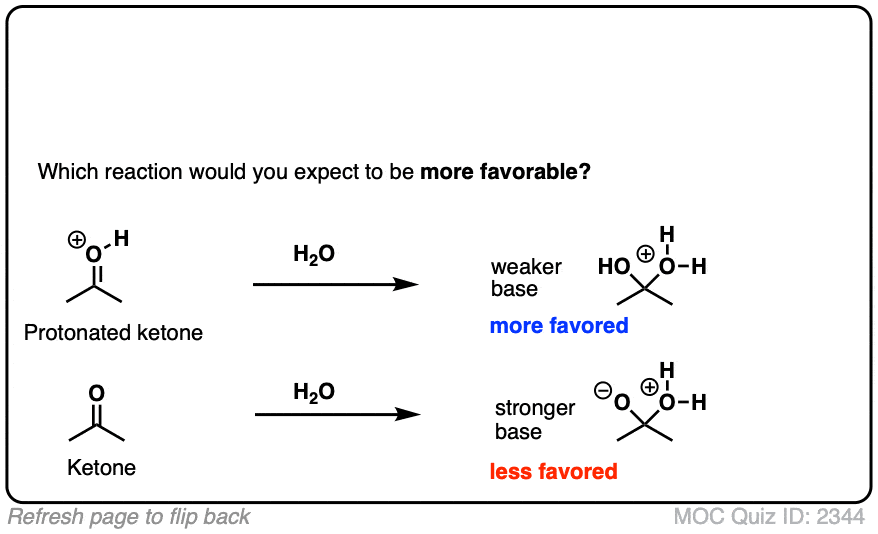
除了金属羰基合物不仅限于带负电的亲核试剂。中性的亲核试剂,如醇类和胺非常能增加吗金属羰基合物。
亲核加成的arrow-pushing机制是相同的。
但是请注意,该产品将承担额外的积极形式电荷。这些反应通常是可逆的,最好被描述为平衡反应。(注6]
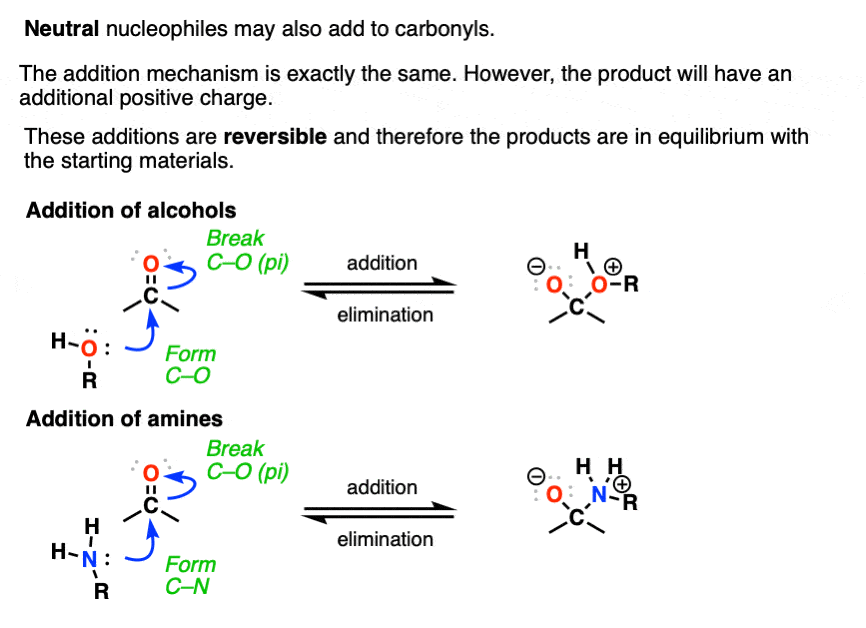
一般来说,中性的物种比他们穷的亲核试剂共轭基地。
除了可以增加的速度通过一种酸催化剂。
否则,除了机制仍然是完全相同的。
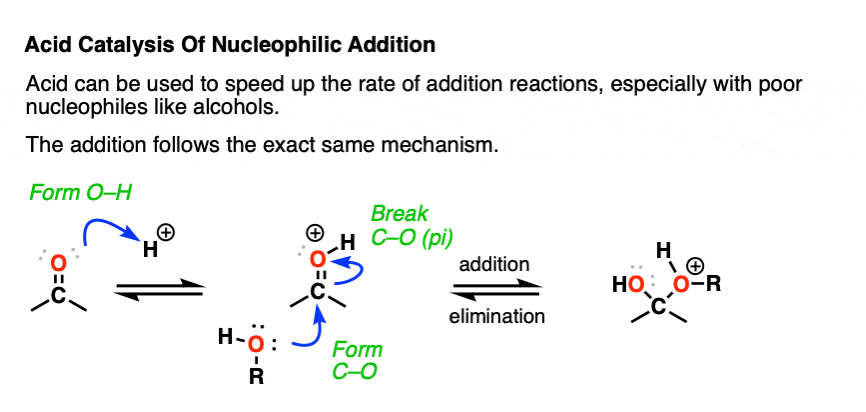
注意,只适用于酸催化的亲核试剂不被酸碱反应!
8。总结
亲核加成反应是最重要的金属羰基合物。不仅仅是醛和酮,但也羧酸衍生品。
- 金属羰基合物接受除了反应大范围的亲核试剂。
- 比较的相对碱度亲核试剂和产品极有帮助在决定如何可逆的加成反应是多少。与格氏反应和氢化物不可逆转的。反应与薄弱的基础卤化物和羧化物通常不会发生。
- 电子效应(电感效应,电子捐赠)对反应有很大的影响。
- 一大群人毗邻羰基将会减慢反应速率。
- 中性的亲核试剂也可以增加金属羰基合物,虽然他们的添加通常较慢的和可逆的。酸催化有时被用来增加的速度。
笔记
注1。这基本上是真实的,但也有一些例外。的机制Cannizarro反应涉及到一个共同氢化转移从一个醛除了产品的混合物酯和一个酒精。
注2。不精确的,但一个不错的经验法则是大约10 pK一个单位的碱度醇盐。的pK一个HCN的9和pK一个醇盐的骤减。另一方面,retro-Claisen已知的反应,和pK一个的酯烯醇化物大约是25。
注3。它看起来很奇怪当你想想,但是如果你犯了排名的列表激活组对于亲电芳香取代:
Cl(激活)< H <烷基<、< NH2NHR, NR2< O(-)(激活)
它与增加的速度反向相关的亲核试剂金属羰基合物电阻-电容- x (O)。
这是
RCOCl H(最快)> >烷基>和> NH2NHR, NR2< O(-)(经历慢之外)。
激活组非常擅长稳定的碳正离子。电子密度就可以捐给碳正离子,electron-poor越少。
想的羰基2 nd-best共振结构的碳正离子与O (-)。更好的组X是在捐赠电子密度,对的亲核试剂反应会越少。
注4。H.C.布朗研究醛和酮的还原反应的相对速度,发现醛更活泼。看到参考。
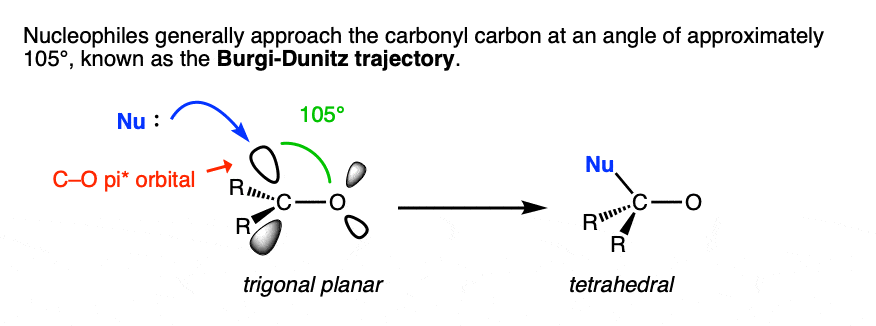
注5。虽然没有明确这里讨论的角度的亲核试剂的方法金属羰基合物值约为105°,现在被称为Burgi丹尼角或轨迹。这正值的位置切断π*轨道,接受的一对电子亲核试剂。
注6。平衡的几个关键因素。bdapp平台一个明显的一个是浓度。被淹没了羰基与亲核试剂,一个可以推动加成反应前进。推动缩合反应的一种方法(如形成亚胺)是隔离H2啊,这是通过使用形成的干燥剂或蒸馏。添加酸增加的速率会影响平衡。是一个微妙的影响分子内的反应,倾向于自发形成5 - 6,自己半缩醛在可能的情况下由于熵的因素。热可以发挥作用。
测试你自己!
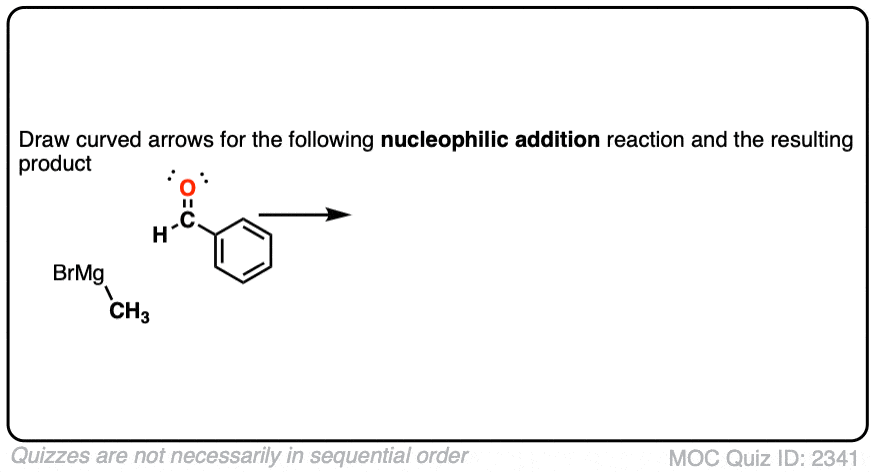 点击翻转
点击翻转
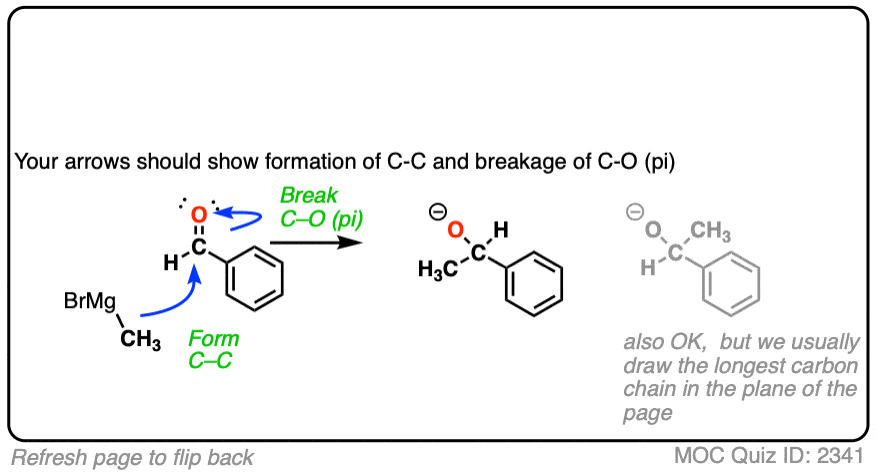
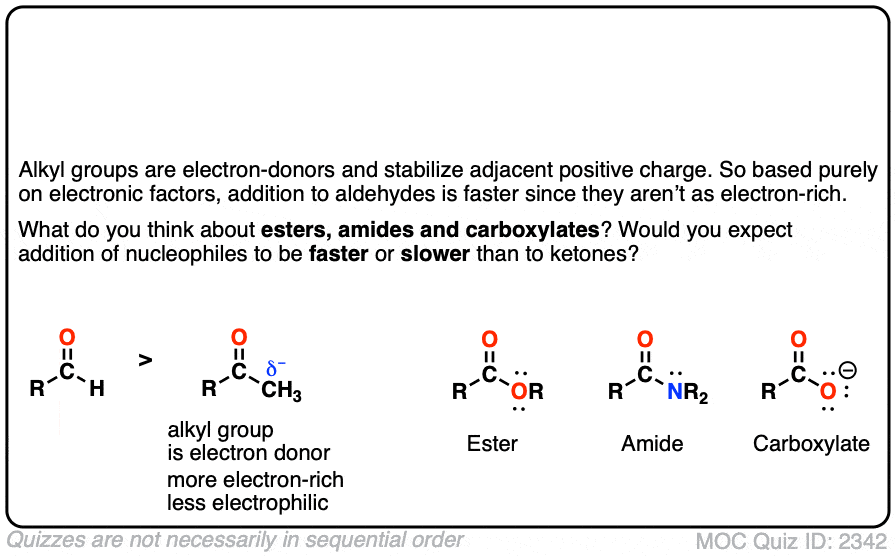 点击翻转
点击翻转
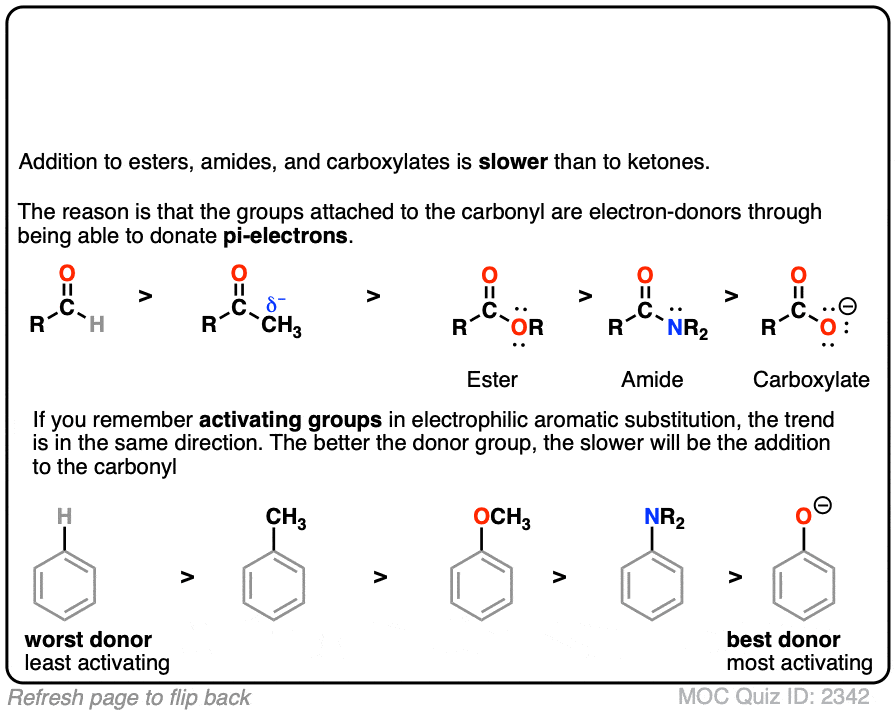
 点击翻转
点击翻转
 点击翻转
点击翻转
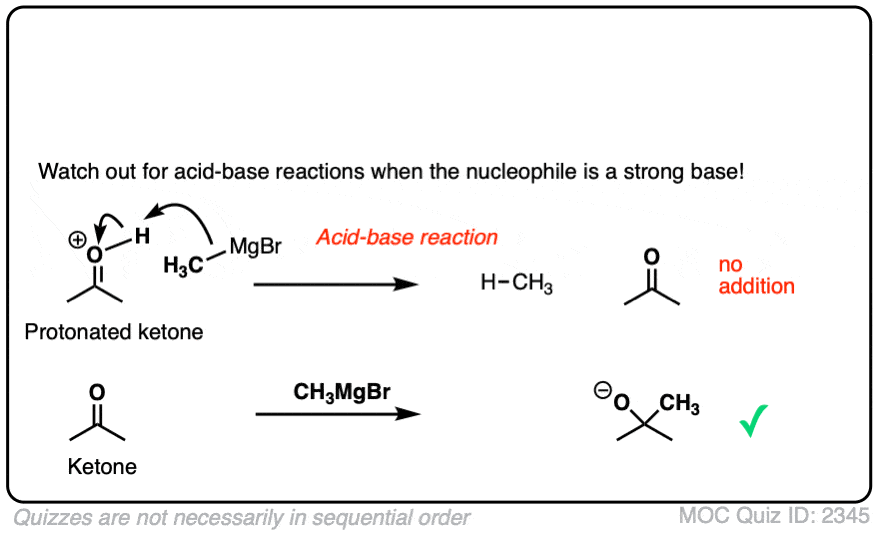
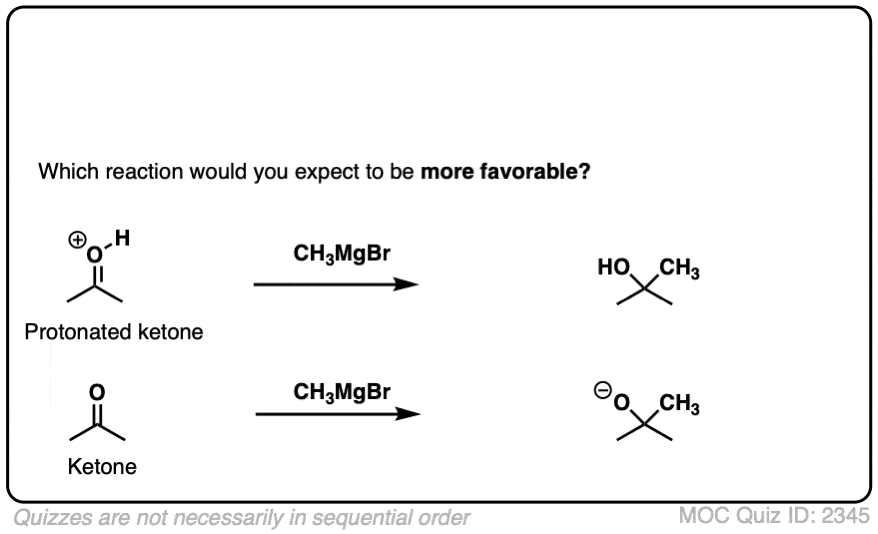 点击翻转
点击翻转
(高级)引用和进一步阅读
1. xcvi。反应涉及的氰化氢碳化合物
亚瑟Lapworth
j .化学。Soc。反式。,1903年,83,995 - 1005
DOI:10.1039 / CT9038300995
2. cxxii。反应涉及的氰化氢碳化合物。第二部分。氰醇被认为是复杂的酸
亚瑟Lapworth
j .化学。Soc。反式。,1904年,85,1206 - 1214
DOI:10.1039 / CT9048501206
Lapworth是最早认识到基地的作用催化的醛和酮HCN,也明白反应是可逆的。
3所示。立体化学的反应路径羰基中心
到了Burgi J.D.丹尼,J.M.黄祖辉,g . Wipff
四面体,30(12)1974年,1563 - 1572。
DOI:10.1016 / s0040 - 4020 (01) 90678 - 7
晶体结构的详细研究了一个趋势的亲核试剂的方法羰基中心约105°角。的轨迹亲核试剂对C = O键,被称为Burgi丹尼轨迹提出了最大化重叠,切断π*债券和允许的放松羰基碳四面体几何。
4所示。化学空间压力的影响
h·c·布朗,o·h·惠勒市川
四面体11957年,214 - 220。
DOI:10.1016 / 0040 - 4020 (57)88041 - 7
研究各种醛和酮的还原反应速率对硼氢化钠。剧透:醛要快得多。
评论
评论部分