有机反应入门
什么是好的离去基?
最后更新:2023年2月1日
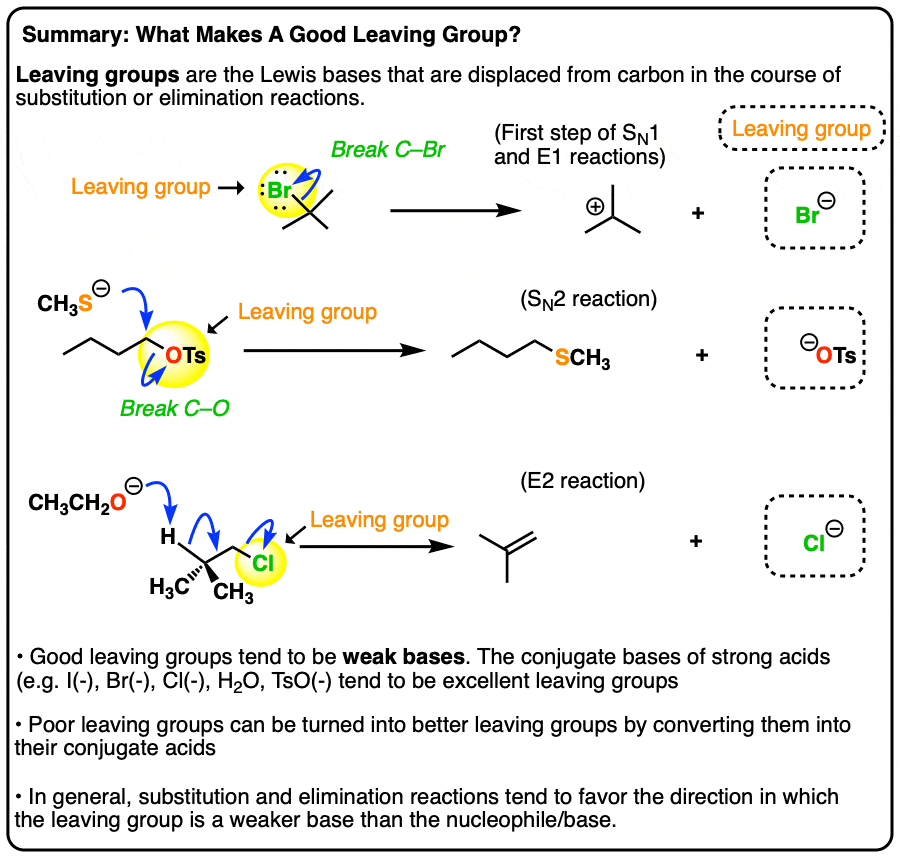
好的离去基是弱碱
- 一个离去基团(也称为“nucleofuge”)是新的路易斯碱它是在各种取代和消除反应中产生的当一个新的碳键形成时。
- 正如酸碱反应倾向于强酸加强碱生成弱酸和弱碱的反应一样,取代和消除反应倾向于强酸加强碱生成弱酸和弱碱的反应离去基团碱比亲核试剂(或碱基,在消除反应的情况下)
- 用pK一个因此,可以很好地预测各种取代反应或消除反应是否有利。好的离去基薄弱的基础即强酸的共轭碱(I- - - - - -、溴- - - - - -, Cl- - - - - -, TsO- - - - - -H2O)
- 差的离去基(往往是强碱)可以通过加入强酸(或路易斯酸)而变成较好的离去基。例如,醇可以转化为烷基氯化物通过添加盐酸。
- 虽然相对碱度亲核试剂/离去基团是一个很好的指导,一个突出的例外是氟化物(F-),它是一个弱碱,但往往不作为离去基团这是因为碳氟键非常强(约130千卡/摩尔)。
- 当碱性的时候亲核试剂而且离去基团具有可比性(即在约5-10 pK一个单位),则可以建立平衡。
目录
- 什么是离去基?
- 酸碱平庸原则,再认识
- 用pKa表评价离队能力
- 共轭酸是一个更好的离去基
- 共轭碱是A更糟糕的是离去基团
- 例外情况-氟
- 最佳离去基团(N2)
- 总结
- 笔记
- 测试你自己!
- (高级)参考资料和进一步阅读
1.离去基就是一个反方向的亲核试剂
很多反应包括的亲核试剂而且基地结果形成了一个离去基团(也称为“nucleofuge”)。
a是什么离去基团呢?
也就是说,而a亲核试剂是路易斯碱那形式一个和碳的新键离去基团是路易斯碱结果是打破一个和碳的键。
这是一个反应产生a的例子离去基团.这是亲核试剂取代反应-特别是亲核试剂取代反应在一个烷基碳与双分子速率决定步骤(SN2).
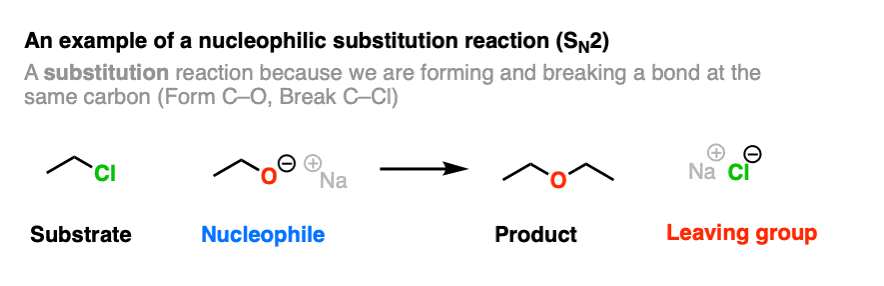
注意这个反应四个组件。
碳氧键形成,碳氯键断裂。
为了看到更多导致离开基团的反应的例子,我们将在下面介绍,悬停在这里可以看到弹出的图像或者点击这个链接.
没有什么能阻止我们把上面画的这个反应翻转过来得到一个相反的反应。我们把它画出来
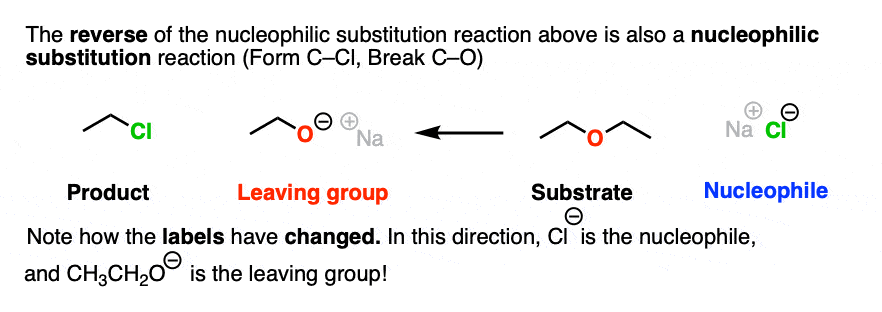
注意,我不说这两个反应是相等的可能.因为我们可以画这两个反应可以不意思是他们是同样在反应容器中有利的。
然而,它是真正的,像画这两个反应都是亲核取代反应,因为我们在同一个碳上形成和断开一个键。
话虽如此,你认为哪种反应更受欢迎?
换句话说,如果我们做实验,你会预测继续完成?
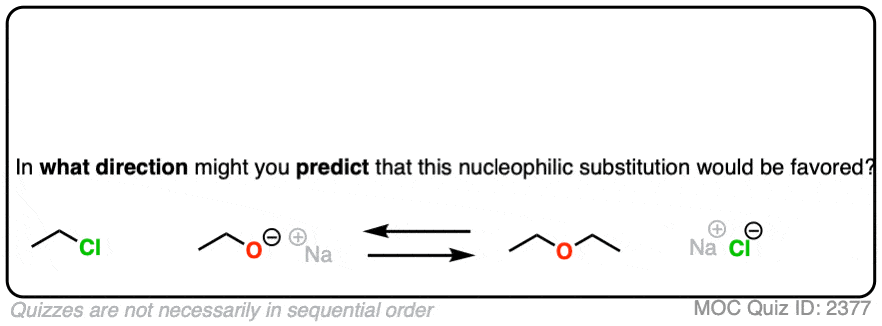 点击翻转
点击翻转
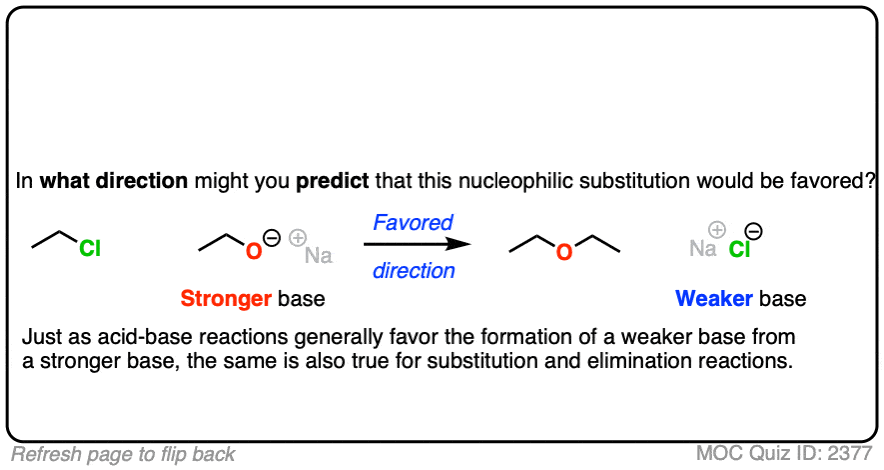
如果你说的是上面那个,恭喜你。
为什么?
2.取代和消除反应只是酸碱反应的延伸吗?
让我们改变一下上面那个反应,看看这个是不是看起来更熟悉。
在H-Cl和NaOCH的酸碱反应中2CH3.给CH3.CH2OH和NaCl,哪个方向更有利?
你们可能还记得酸碱平庸原则:强酸加强碱得到的是弱酸和弱碱。(看到帖子:如何使用pK一个表格).
所以这个酸碱反应的有利方向是生成较弱的基地(Cl)
就像从强碱到弱碱,酸碱反应更容易发生一样,取代和消除反应也往往被青睐的时候离去基团碱比亲核试剂(或基础)。
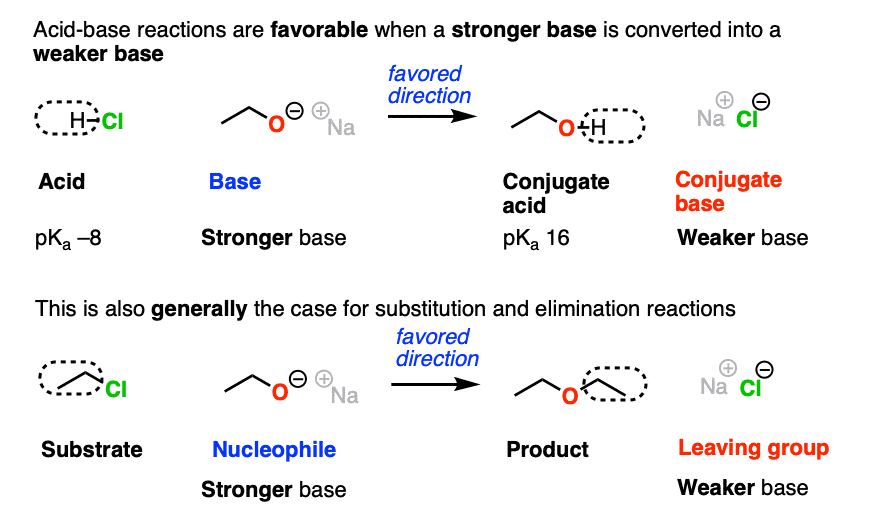
事实上,酸碱反应的四个组分很好地映射到上面亲核取代反应的四个组分上。
上述取代也有利于由强碱(CH)形成弱碱(Cl-)3.CH2O -)
就此而言,这个也一样消去反应
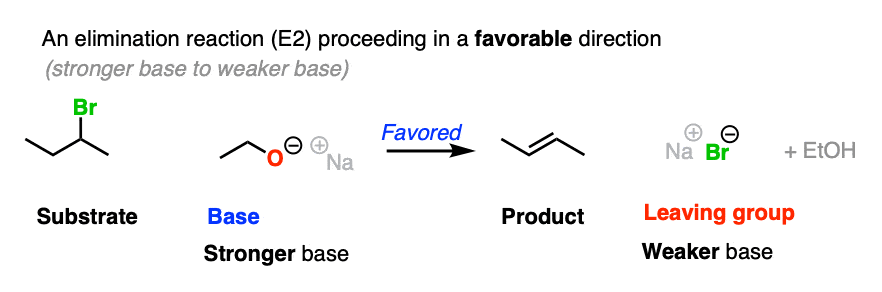
如果离去基团碱被翻转,反应就不那么顺利了。为了观察这种“翻转”反应,悬停在这里可以看到弹出的图像或者点击这个链接.
这也是损失的情况离去基团在这个SN1反应:
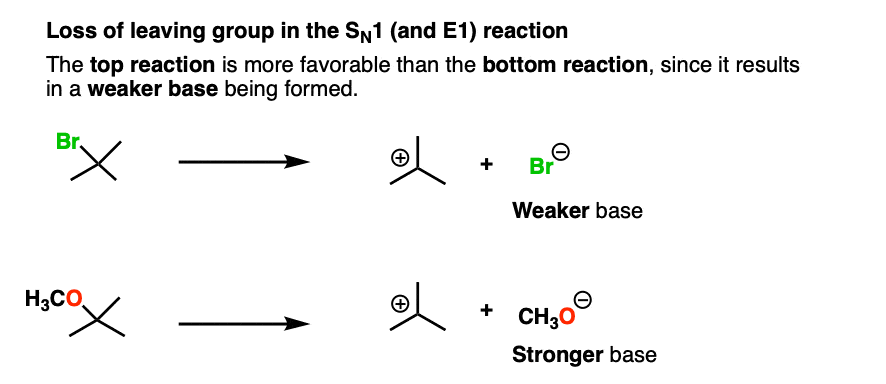
还有很多例子,比如Org 2中的亲核酰基取代反应。举个例子,悬停在这里可以看到弹出的图像或者点击这个链接.
一般而言,碱变弱,的更好的离去基团.
我们可以反过来说碱越强,效果越差离去基团.
3.使用pK一个确定离队能力表
如果基础强度决定离去基团能力,那么pK一个表格应该是一个很好的决定指南离去基团能力。
在之前的文章中(看到的:如何使用pK一个表格)我们相当详细地讨论了这个问题。
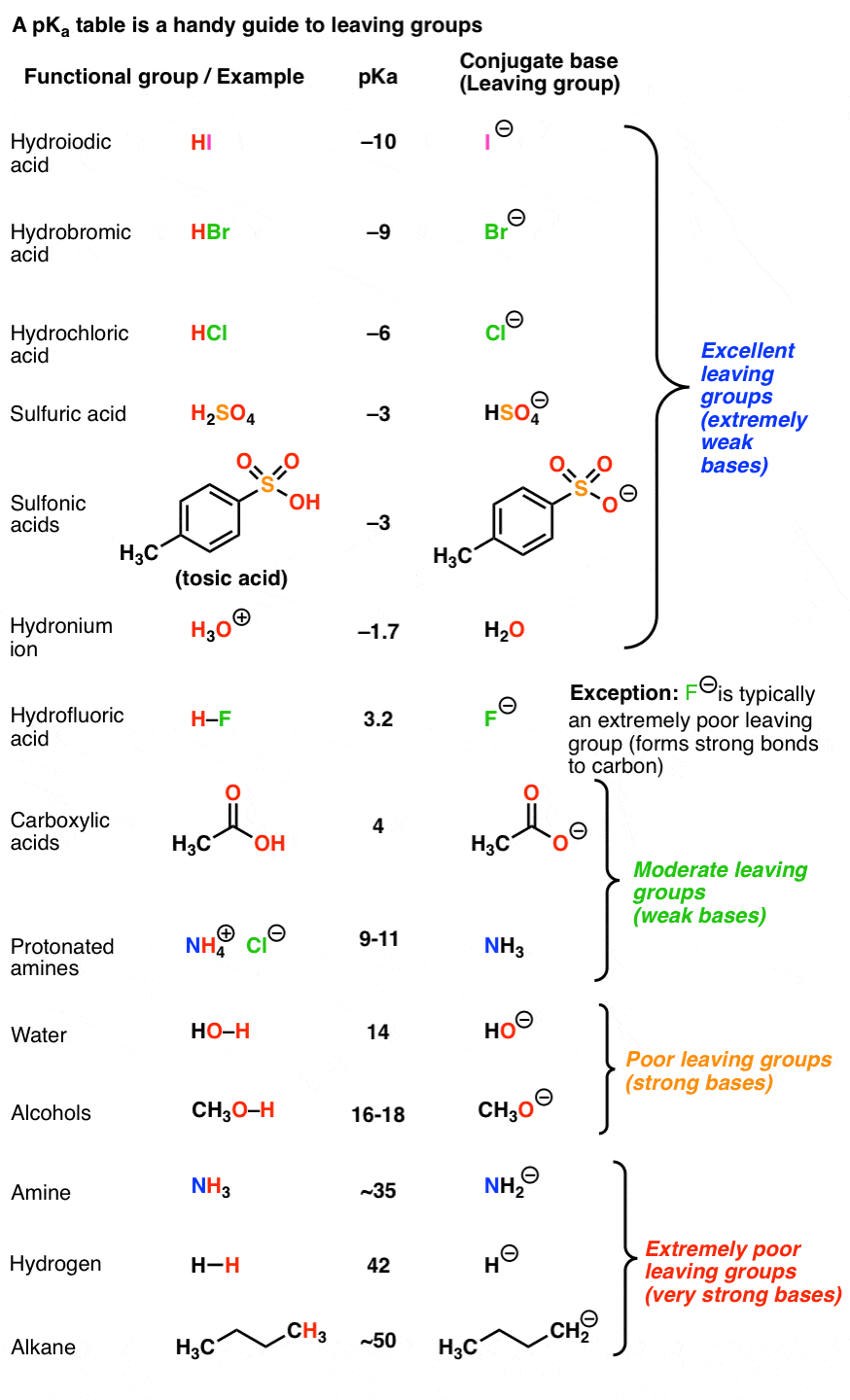
回想一下更强的的酸,较弱的的共轭碱意思是pK的顶部部分一个表应该是一个优秀的指南,最好的离开组。强酸的共轭碱,如I(-), Br(-), Cl(-), HOSO3.(-), TsO(-), H2哦,其他的都是薄弱的基础而且伟大的离开组织。
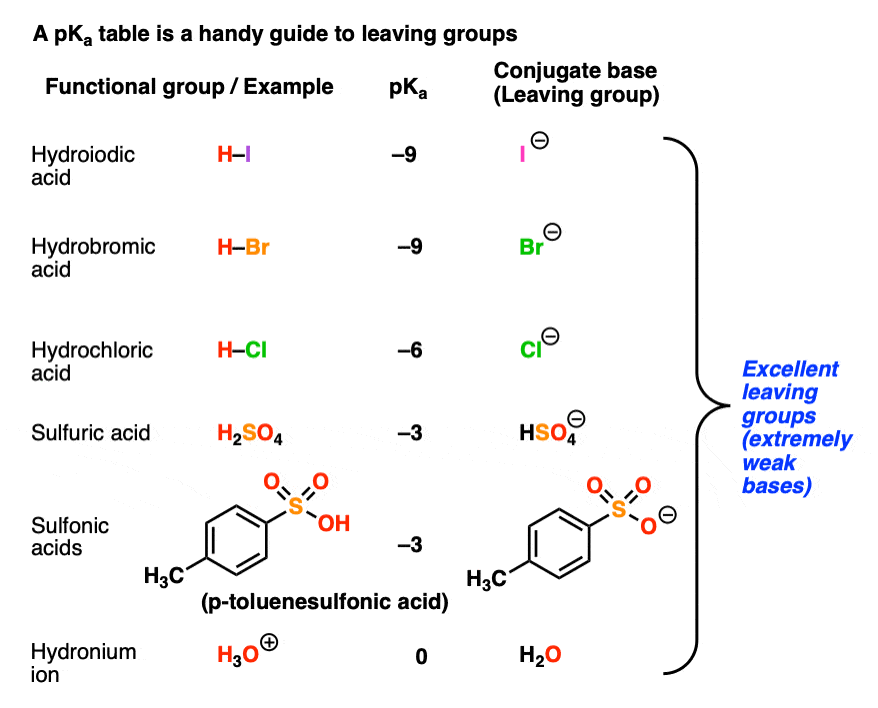
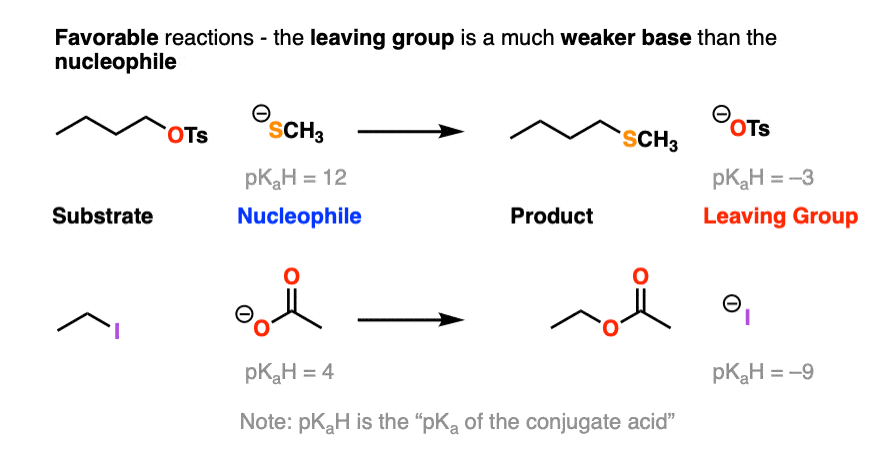
注意pK一个H是“pK”的缩写一个的共轭酸”。
另一方面,pK的底部一个该表应该是一个指南最糟糕的离去基-弱酸的共轭碱,如H(-)和H3.C(-)是极强碱。
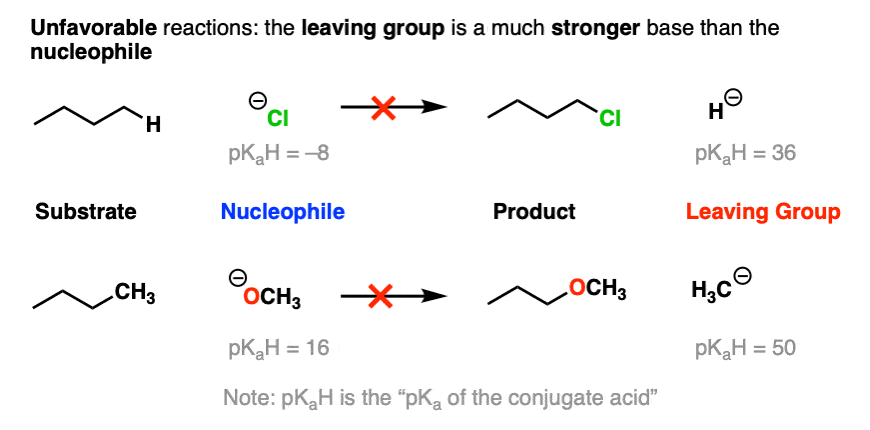
这就是为什么我们看不到烷基基团或氢化物离子作为离去基团。
我应该强调比较碱度亲核试剂而且离去基团是一个好的开始,但是是吗不是唯一的变量.化学键断裂和形成的相对强度也是一个因素,这在氟原子中表现得最为突出异常下面)。
当亲核试剂而且离去基团的类似的碱度(即约5-10 pK一个,取代反应是潜在的可逆的,平衡可以被推向一边或另一边,这取决于我们选择什么条件。[注1]
此外,重要的是要记住酸性和碱性(即pK)一个的位置平衡(想想“能量的差异”)而亲核性是由反应速率因为很多亲核试剂的反应都是不可逆的。所以尽管相关性很好,但并不完美。
同时,要注意酸碱反应。一个好的经验法则是,相对于取代和消除反应,酸碱反应是快速的。看到帖子:酸碱反应很快)
4.共轭酸是一个更好的离去基
氢氧根离子可怜的离开基团,因为它们是强碱。
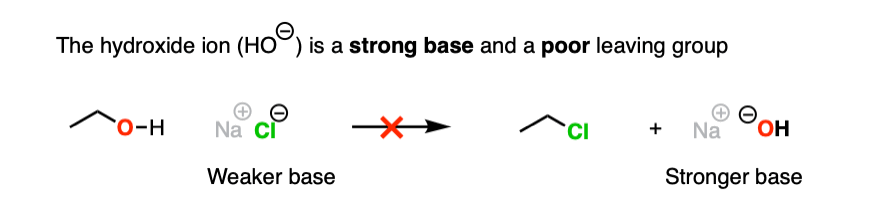
我们可能会问自己:有没有办法修改所以当碳氧键断裂时离去基团是一个较弱的基地吗?这样就更有利了。
是的,有一种简单有效的方法可以让OH变得更好离去基团.
如果我们加strong酸,然后我们做共轭酸也就是R-OH2(+)。
现在,如果Cl(-)攻击,我们离去基团就是弱碱H2这是10的倍数14不如HO(-)基本。
所以在酸存在的情况下,这个反应变成多更有利的。的共轭酸是一个更好的离去基团!(这是的主要应用之一酸催化在有机化学中。)
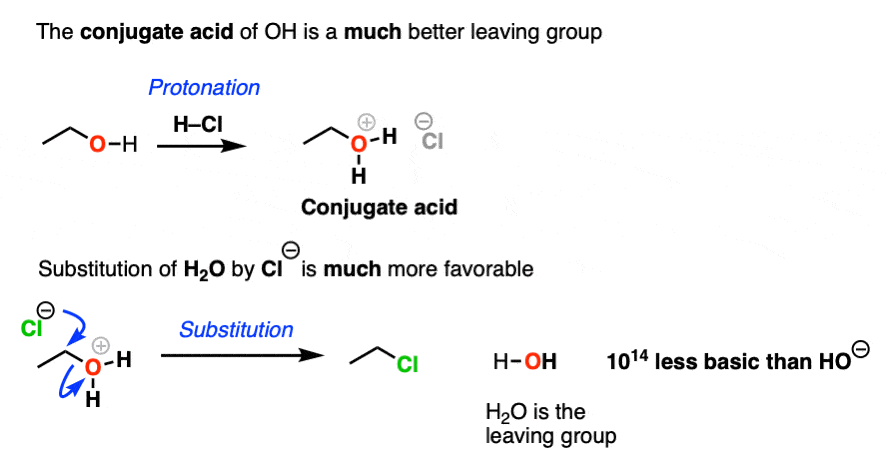
在关于醇的那一章,我们会看到很多醇的取代和消除反应需要为了让羟基离开。
路易斯酸也可以用于此目的。[注2]在亲电性芳香族取代的章节中,我们会看到很多这样的例子(例如,在Friedel-Crafts反应中,Lewis酸如AlCl3.用来使Cl变成更好的离去基(见post:Friedel Crafts烷基化和酰基化反应).
其他方法修改-OH,使其成为更好的离去基团包括将它们转化为比HO(-)弱得多的磺酸盐。[看到帖子:Tosylates和Mesylates] [注3]
5.共轭碱是一个较差的离去基
这是真的共轭酸是更好的离去基团.同样值得注意的是共轭基地是一个更糟糕的是离去基团.
酸碱反应也是快一般来说,取代反应和消除反应。
如果把强碱加到带有酸性质子的物质上,酸碱反应就会先发生。这会给共轭碱,这将拥有一个更糟糕的离去基团而不是中性物种。
举个例子。你可能会认为离去基团这是HO(-)。它不是。的离去基团应该是O(2-)
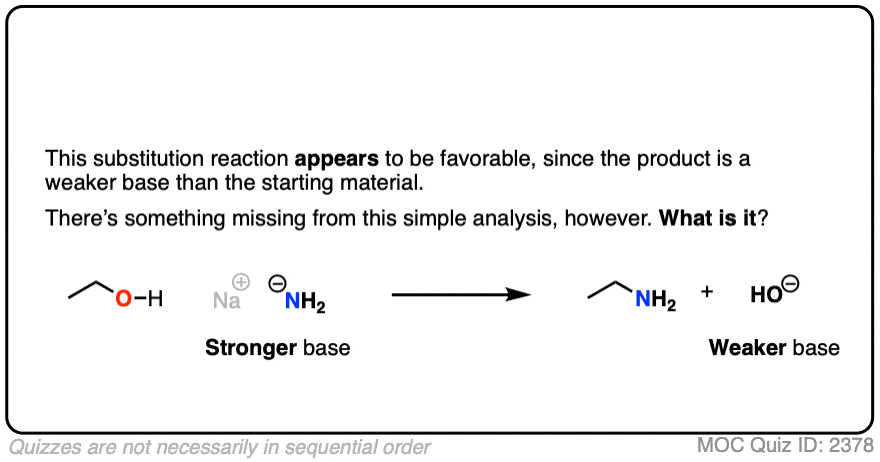 点击翻转
点击翻转
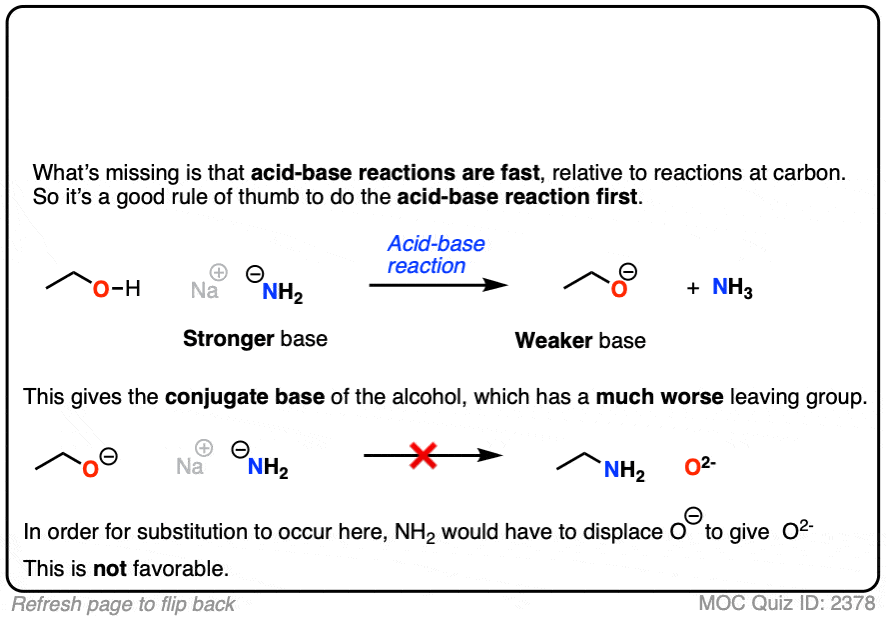
那就糟多了离去基团.
同样的,不要忘记羧酸....酸!
6.异常
就这么简单吗?只要应用酸碱平庸原则,我们就搞定了?
不完全是。如果我们不提到一些例外就不是有机化学了。
一个突出的例外是氟.氟离子(F-)是弱碱(pK -)一个HF的含量为3.8),但总体上较差离去基团在取代反应中。[注意4]
一个关键原因是C-F键的强度(约130千卡/摩尔)。
到目前为止,我们只考虑了稳定性离去基团相对于亲核试剂.但是稳定性产品也很重要。
由于C-F键如此强,反向反应(破坏C-F键,使F(-)变成a离去基团)会有一个极高的活化能,非常不利。
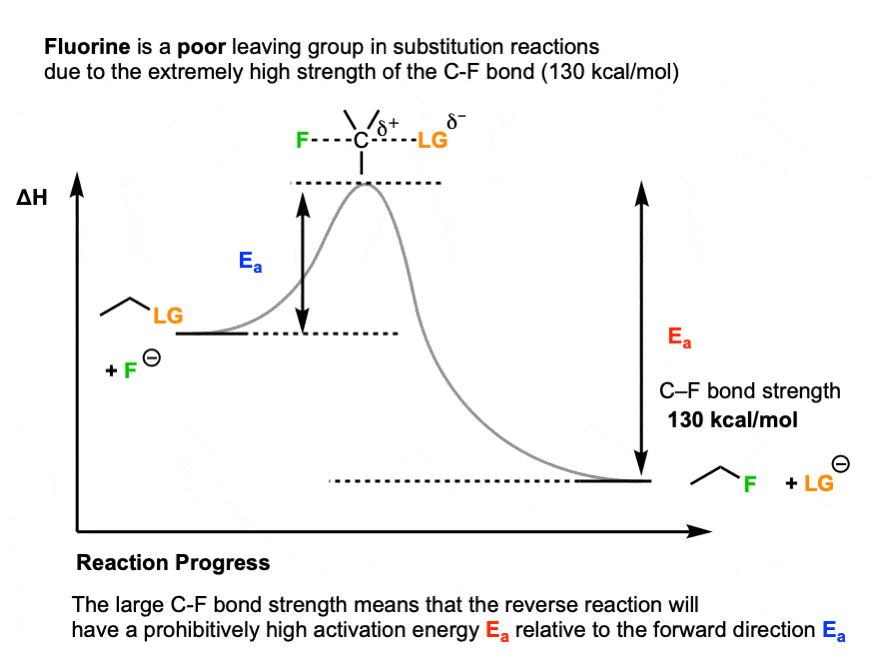
所以关键的变量不仅仅是相对的稳定性亲核试剂相对于碱基,还包括形成和断开的键的强度。
另一个氟是a的反应离去基团是亲核芳烃取代,但C-F的断裂在这种情况下不是决定速率的步骤(见Post:亲核芳香族取代)
7.最好的离去基团
可能是最好的离去基团是氮(N2).氮不仅非常稳定——毕竟,它占我们大气的79%,基本上是惰性的——它是一种气体,这意味着任何有机反应都需要氮2会导致它从溶液中冒出来,使反应基本上不可逆(有时是爆炸性的!)
胺(R-NH2)可与亚硝酸(HONO)通过“重氮化”过程转化为重氮盐R-N≡N(+)。
然而,氮是一个很好的离去基团, sp3.-杂化碳原子与氮成键2它们非常不稳定并且不会停留足够长的时间来参与与亲核试剂的反应;一旦形成,N2只是叶子,导致碳正离子(和并不罕见的,破碎的玻璃器皿)在它的尾流。
重氮盐2-杂化碳更稳定,用于有机反应;有关更多信息,请参阅这篇文章(看到帖子:重氮盐反应)
8.总结
让我们来回顾一下。
- 离去基是作用相反的亲核试剂,即它们是由碳键断裂形成的路易斯碱。
- 正如酸碱反应倾向于由强碱形成弱碱的方向一样,涉及离去基团的反应也倾向于产生弱碱的方向。
- 强酸的共轭碱(如I-、Br-、Cl-、TsO-、H2O)是很好的离去基。
- 的共轭碱弱酸(H-, H3C(-),烷基阴离子)是不好的离去基。
- 的共轭酸是一个更好的离去基团.一个常见的例子是醇,它可以在HO被质子化后发生取代和消除反应。
- 的共轭碱是一个更糟糕的是离去基团.一个好的经验法则是做首先是酸碱反应.
- 氟离子(F-)是弱碱,但碱性差离去基团这是由于碳氟键的强度。
如果你不确定反应会发生在分子上的什么地方,那就找一个好的离去基团.那通常是行动的地方!
笔记
注1。当碱性的时候亲核试剂和离去基团具有可比性(即在约5-10 pK一个单位)那么反应就有可能是可逆的.(关于这5-10 pK的更多信息一个单位编号,见酸碱反应的简便经验法则)
在这种情况下,它是一个平衡,平衡的位置可以影响勒夏特列原理。例如,有可能使反应从一个较弱的碱到一个较强的碱通过使用大量过量的亲核试剂,或通过去除较强的碱。
一个有趣的例子是基于不同溶解性.芬克尔斯坦反应是一种烷基碘化的烷基氯化物。两者之间没有太大的区别离去基团氯离子或碘离子的能力。然而,两者之间存在着显著的差异溶解度NaCl(或NaBr)和NaI的含量丙酮.NaI可溶于丙酮;NaCl不是。因此,当氯化钠形成时,它从溶液中析出,使反应向右。勒夏特列原理的另一个例子!
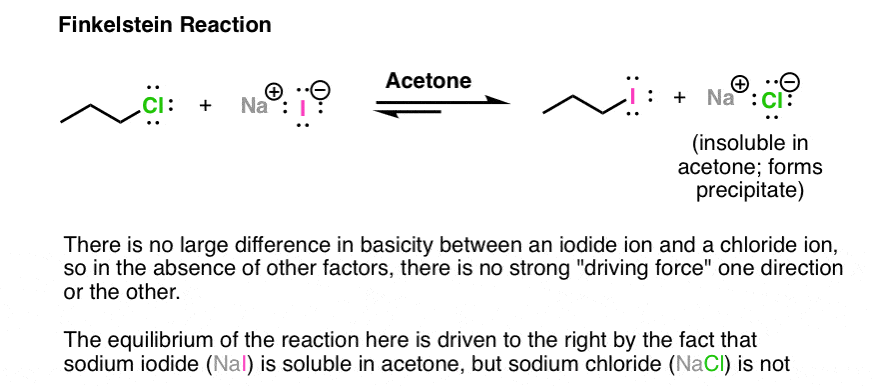
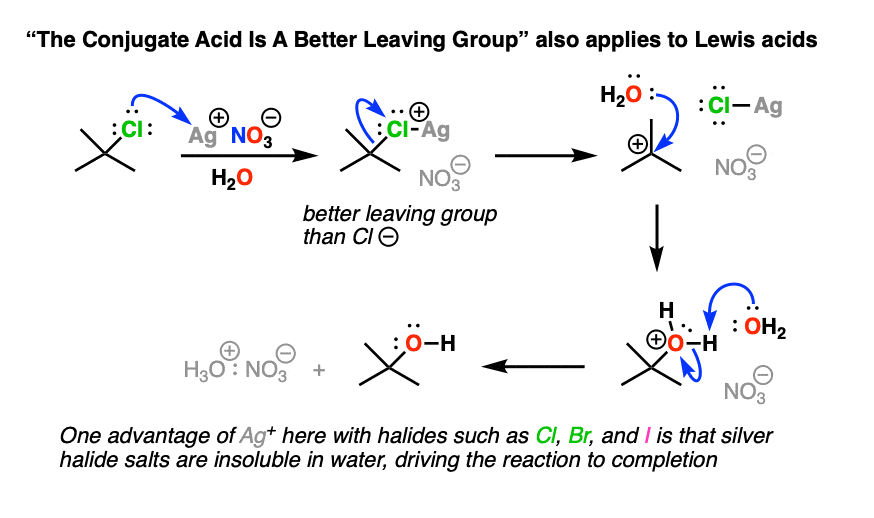
注2-也可以使用路易斯酸。与烷基卤化物,有时是银盐,如AgNO3.或AgBF4是用来协助Cl或Br基团的流失(反离子NO3.(-)或BF4(-)在这里只是一个旁观者).Ag(+)与Cl或Br配合,形成更好的离去基团(卤化银盐)
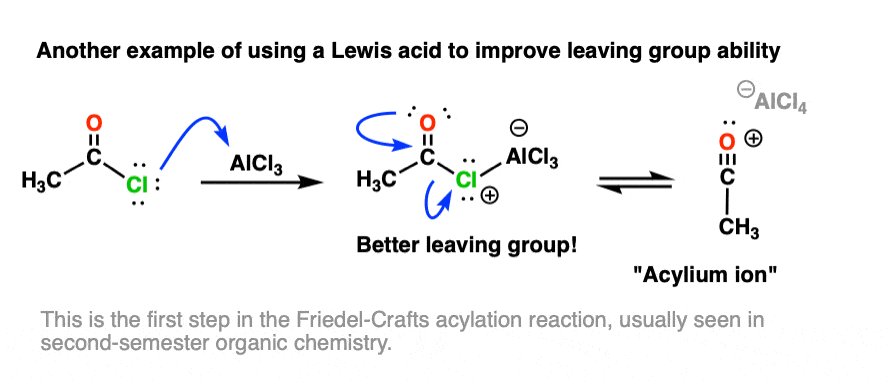
路易斯酸用于增加离开基能力的其他例子见于芳香族化合物的几个反应中,如Friedel-Crafts酰基化反应,其中路易斯酸(如AlCl3.)有助于从酸卤化物中流失氯:
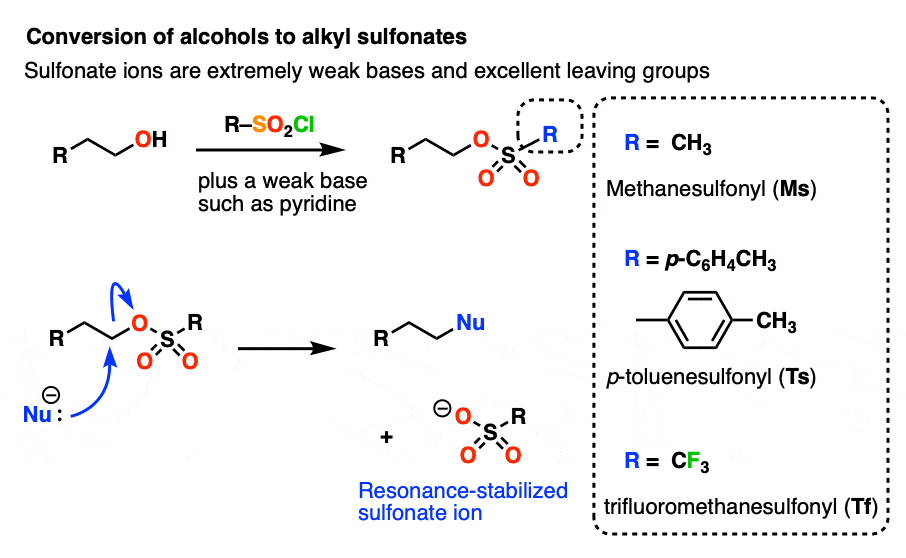
注3-酒精可以转化成烷基通过使用磺化试剂等p-甲苯磺酰氯(TsCl)或甲磺酰氯(MsCl).由于氧上的负电荷可以通过共振而离域,因此磺酸盐是很好的离去基。一个更好的离去基团比(-)OMs或(-)OTs为三氟甲基磺酰基(-)OSO2CF3.“三氟化”基团,其中OMs上的氢原子被吸电子的氟取代。
注意4氟是一种劣质离去基团在亲核取代反应中,但在某些情况下,是a离去基团在各种消除反应中。一个例子是E1cb机制,其中第一步是形成a共轭碱,然后(决定速率的)消除a离去基团.
另一个氟原子的例子离去基团是亲核芳烃吗取代反应在这里,吸电子的F实际上有助于使碳更亲电。用于测定胰岛素中多肽序列的Sanger试剂是促进具有氟化物离去基的亲核芳香族取代试剂的一个有用示例。
注5-一个物种是有可能的这两个一个好的亲核试剂一个很好的离去基团.亲核性定义为率的反应亲核试剂在给定的基底上。然而,碳碘键相当弱(约50千卡/摩尔),很容易发生裂解。
注7。我个人对“最佳”的投票离去基团Of all time "在这个反应中出现。
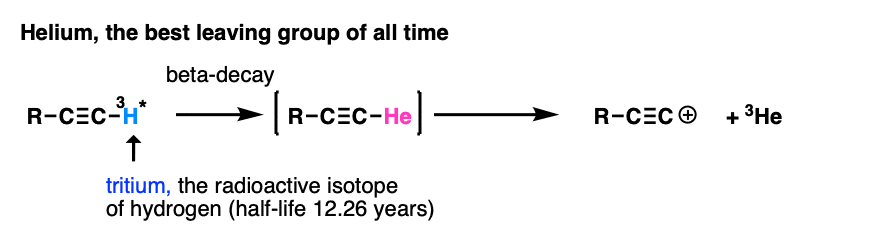
研究人员想要研究炔基阳离子,非常不稳定,寿命很短。然而,通过在末端碳上放置一个放射性氚原子,少量的β衰变产生了一个氦原子,氦原子迅速离开,产生了一个炔基阳离子(与溶剂苯反应)。他们当然不会等上12年才达到50%的完工率:-)[裁判- - - - - -j。化学。社科学报1988,110,1298]
测试你自己!
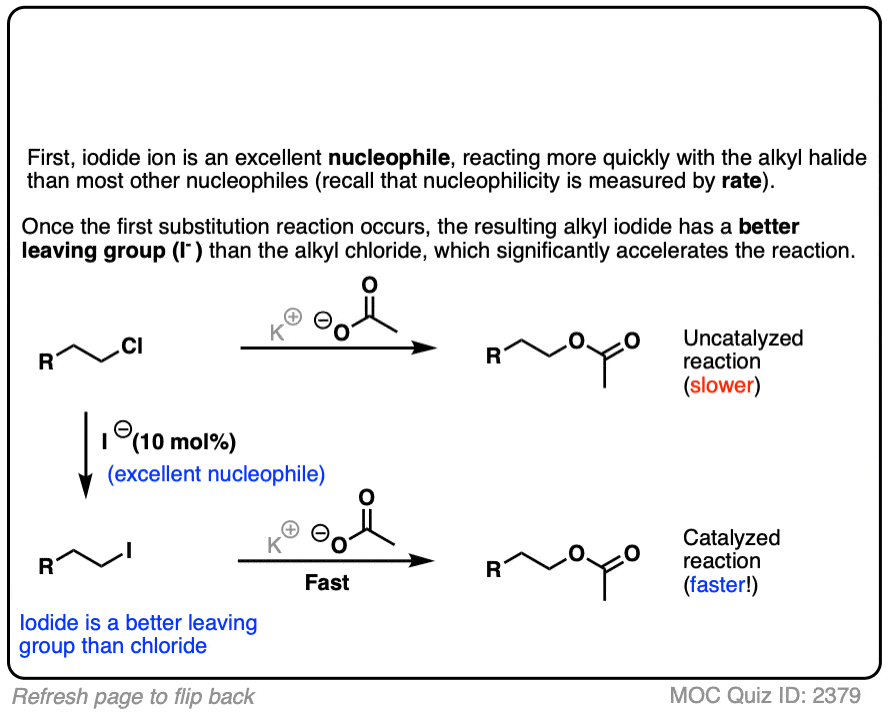
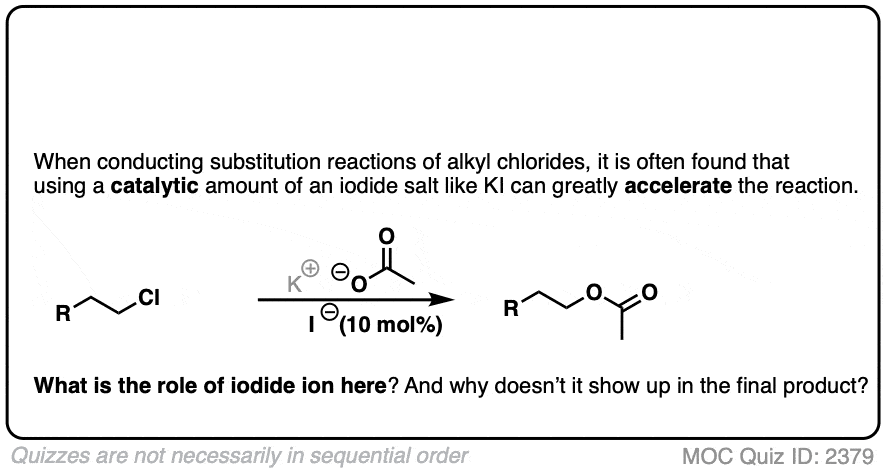 点击翻转
点击翻转
(高级)参考资料和进一步阅读
- 的生成和捕获炔基阳离子
吉安卡洛。Angelini,迈克尔。Hanack, Jan. Vermehren和Maurizio。一般颤抖
美国化学学会杂志1988110 (4), 1298-1299
DOI:10.1021 / ja00212a052 - 的影响羰基卤化物反应性的相关组SN2反应
f·g·博德威尔和w·t·布兰宁
美国化学学会杂志196486 (21), 4645-4650
DOI:10.1021 / ja01075a025
这是金子!!谢谢
谢谢!
太棒了!这澄清了很多!谢谢! !
很高兴你发现它有用!
我爱你的网站!!我花在这上面的时间比我的课本还多,提高了我的测验分数。
非常感谢!
很高兴你觉得它有用!
这太清楚了!
你太棒了,太棒了!
哪个是好生命基苯氧基(PhO)还是氯(Cl)?
什么是弱碱?
哪个是好的离去基苯氧基(PhO)还是氯Cl?
你自己算出来的方法是:找到pKa表,算出苯酚(PhOH)和盐酸的pKa。哪个酸更强?现在,酸越强,共轭碱就越弱。那么哪一个的共轭碱更弱呢?碱越弱,离去基越好。
苯酚的pKa约为16,盐酸的pKa约为-5,所以“强酸弱共轭碱”意味着Cl-是更好的离去基。
谁都知道盐酸是强酸!!愚蠢的
HCL是强酸,它是较好的离去基
你连这都不知道怎么上普通化学课!
苯酚在10 pka左右,盐酸在-7 pka左右。所以盐酸是更强的酸=更弱的共轭碱=作为阴离子更稳定=更好的离去基。我的思路正确吗?
这是我见过的最容易理解的方式!非常感谢,请再接再厉。
很高兴你觉得它有帮助,伊凡娜!谢谢
非常感谢。非常清晰和信息丰富。请保持下去。
非常棒的博客!
我有我的MCAT考试在2天,(好吧,1.5天,如果你从现在开始计算),希望我无意中发现你的博客3个月前!还剩下1.5 x 12个小时!:)
很高兴你觉得有用。当你完成后,告诉你的朋友:-)
是的,请讨论您提到的关于a-e rxns中的F-的额外因素。
非常感谢你总是让它清晰有趣!
如果离去基带正电,使碳上的电荷变成中性,比如S+(CH3)2?
离去基应该是S(CH3)2它是一个非常弱的碱,也是一个很好的离去基!(很像OH2(+))]
这正是我所需要的。有机化学一直是化学中似乎不可能理解的一部分。但在你解释的帮助下,我看到我自己会得到一个全a,毫无疑问。多亏了你,詹姆斯。
这是一个伟大的网站,非常有用,比我的文本或教授更清楚。谢谢你!
感谢这个神奇的资源帮助我通过orgo。像你这样的人需要在大学里教学生,因为任何人都可以从你做的这个网站上看到,你实际上关心人们的学习和理解,或者....谢谢你!
只是想说声谢谢。真希望我几个月前就能找到这个网站。所有的信息都很容易获取,而且组织得很好。继续这项巨大的工作。你的网站获得了一个忠实的访问者。我下学期也会回来上有机第二课。
这个网站很有用!非常感谢!
我认为第二段有个错误。原子不可能同时是中性的和带电的。中性原子的原子序数(质子数)与电子数相同。我建议你说一个原子变成一个离子(带负电),以达到完整的八极。
不,他的意思是当电子移动到离去基上时它就带电了。我不认为有什么错误。
继续你的好工作。你的网站真的帮助我和我的朋友了解了有机化学的大部分概念。
太有帮助了!你做得很简单。除了PKa,还有其他因素吗?如果一个羟基gp连接到碳上,那么化学键强度的影响呢?
谢谢詹姆斯
CN-是一个好的离去基吗
不,它是个很差的离去基
为什么?
谢谢!但是你能解释一下为什么弱碱是更好的离去基吗?
离去基越稳定就越容易离去,对吧?所以,如果碱很弱,它就不会急于接受质子并进行反应。因此,由于碱不容易反应,所以它是稳定的,是一个很好的离去基。
弱碱在溶液中作为阴离子是非常稳定的。弱碱有一个强共轭酸(例如HCl是弱碱Cl-的强共轭酸)。在酸中,你可以把碱想象成一个“离去基”,它允许H+自己离开(就像Cl-在水溶液中迅速离开H+)。因为酸很强,我们知道碱很容易离开。
相反,如果酸很弱(比如CH3COOH),我们就知道它能把H+束缚得比较紧。碱(CH3COO-)在溶液中相对不稳定,所以它不愿意离开H+。当相同的碱基附着在碳骨架上时,情况非常相似。氯会很容易离开碳骨架因为它很喜欢Cl-在溶液中,而CH3COO-不太喜欢这样。中等强碱,比如NH3是很差的离去基,而像OH这样的强碱是很差的离去基。如果你拿一个很强碱,比如CHC-(乙酰基)它永远不会离开,所以我们甚至不认为它是离去基。
氧- ph作为离去基排在什么位置?它比卤化物好吗?
这个网站很棒,非常感谢你,你解决了我在有机化学方面的大部分问题。
这是迄今为止我所见过的关于亲核试剂和离去基团最连贯的解释。在这方面,比Youtube和大多数教科书都要好!
如果分子的不同部分有两个相同的离去基呢?比如说,两个溴。那么选择离去基的时候要考虑哪些因素呢?
然后你要检查一下这些离去基所连着的碳。小学、中学还是大学?然后再看反应条件(比如有什么亲核试剂?)这就导致了SN1/SN2/E1/E2的决定。你可能想要查看我的“SN1/SN2/E1/E2快速N ' Dirty指南”以获得更多信息,因为在博客评论中可以总结很多内容。
我见过醇氧化合物在sn2th反应中被去除(与羰基有关)。我在混乱中,在这样的反应中哽咽。请帮助
非常感谢!
第一张图需要小修正:反应物一侧为中性,生成物一侧为正电荷(需要给Nu加上一个负形式电荷,或者从L上取下负形式电荷)。
你能解释一下为什么F能在羰基碳或芳香环上成为离去基吗?
是的,F-在这种情况下是可以的离去基(亲核芳香族取代)因为速率限制步骤是芳香族环的破坏(破坏芳香族)离去基的损失比这一步慢。而且,因为F-能吸收电子,F实际上有助于加速反应,因为它能消除环上的电子密度,使环更容易被攻击。
詹姆斯,有人提到了F-在质子溶剂和非质子溶剂之间的区别,你介意解释一下吗?
先谢谢你
问题在这里得到了一个全面的回答:https://forums.studentdoctor.net/threads/nucleophiles.752905/
“在极性质子溶剂中,亲核试剂,通常是阴离子,被氢键溶剂强溶剂化。虽然你确实希望整个反应在一种溶液中发生,但你不希望有这么强的溶剂化反应,因为这会阻碍阴离子与亲电试剂快速反应。氟化物的这种影响最大,因为它们很小,不容易极化。在极性非质子溶剂中,这种阴离子溶剂化作用不会发生到同样的程度,因此比碘化物(考虑碱度)反应性更强的氟化物将是一个更强的亲核试剂。”
很好的阅读,如果有人需要的话。
在亲核取代和消除反应中,无论溶剂是什么,F都是一个较差的离去基。
这个网站对我的考试很有帮助,很好地澄清了我对有机化学的疑惑你能告诉我为什么氟是一个例外在羰基碳或芳香环中,与其他卤素相比,它是一个很好的离去基
在非质子溶剂中,I-比F-是BLG。
在质子溶剂中,F-比I-是BLG。
如果是弱亲核试剂那一定是BLG。
我是对的,对吧?
问这个问题是因为我读到差的碱是BLG,我接受,但我认为它应该在溶剂中有所不同。
(例如:F- in质子比I- due h键稳定得多。)
谁能告诉我我说得对不对?
F -
为什么碘既是好的离去基又是好的亲核试剂
非常感谢!
这些文章真的很有用。继续做好工作。来自印度的欢呼!
+NR3是最好的离去基。
你能解释一下氟离子的例外情况吗?
哦。我的。善良。这真是太神奇了。我永远不知道该如何感谢你,也不知道该如何表达这对我的帮助。说真的,你现在在我眼里就是神。
离去基依赖于溶剂效应吗?
了不起的网站,解释任何主题与轻松。每当我有任何疑问时,我就会参考MOC,它帮助了我很多。詹姆斯先生,谢谢你的卓越努力。你通过这个网站使学习有机化学变得有趣。
最好的解释可以在这里找到,非常感谢
好的,谢谢ankit!
中性基团比带负电荷的离去基团更好吗?
共轭酸总是一个更好的离去基。所以H2O是比HO-更好的离去基,HOR比RO-更好,NH3比NH2(-)更好。如果综合考虑多个因素,就很难得出结论。例如Cl-是比NH3更好的离去基。
这就是为什么有一个pKa表很有用。
哪种溶剂是给定的pka表。
Q.离开的倾向是否取决于溶剂,例如,如果F-在极性质子介质中离开,它会通过氢键来稳定电荷,这在极性非质子介质中是不可能的
碳氟键非常强,不管用什么溶剂,它都不太可能是取代基或消去基。
为什么留基是弱碱,有什么解释吗?
想想反应中离去基的生成。你需要打破一个键,形成一个相对稳定的物种。所以如果键太强(比如C-F)或者离去基本身不太稳定(强碱性)那么这个过程的活化能就会太高,不可能发生。
我搞不懂HF和它的共轭碱。F-是一个很好的离去基吗?所以对于E2反应它会离开?
不,F-是一个很糟糕的离去基。部分原因是C-F非常强。
它肯定不会发生E2反应。
氮气和水,哪个更好?
你很难找到比N2更好的离去基。
这可能与LG有关,也可能与LG无关,但您能否回答:
氯仿与乙醇的反应。KOH和对甲苯胺的形式?
可能……https://en.wikipedia.org/wiki/Reimer%E2%80%93Tiemann_reaction
如果一个物种是好的亲核试剂,那么它是否有必要是好的离去基
不。氟离子是很好的亲核试剂,但不是很好的离去基。
感谢上帝,我在2020年找到了这个网站!你可能真的救了我一年。干杯!
你能告诉我更多关于氟的加成消除反应吗?
是的,看看这个亲核芳香族取代。
//m.deriinvest.com/2018/08/20/nucleophilic-aromatic-substitution-nas/
这真是太神奇了。2年来,我一直在努力理解这一点。谢谢你!
谢谢你!这对我很有帮助,我正在努力学习有机化学1,这对我很有帮助。
如果NH3比H2O更碱那么它是一个比H2O更好的离去基
你能解释一下为什么氢是强碱吗
我猜它是惰性气体构型所以不会给出电子
请澄清。
我查了很多资料,这真的很有用!!谢谢! !
H是电负性最小的元素。求它的有效核电荷。它是阴离子吗?
我以前很困惑为什么I-能同时成为最好的亲核试剂和最好的离去基
谢谢你的解释!
很高兴你觉得有用。谢谢你!