碳水化合物
Ruff降解和Kiliani-Fischer合成
最后更新:2022年9月19日|
Kiliani-Fischer合成和Ruff降解
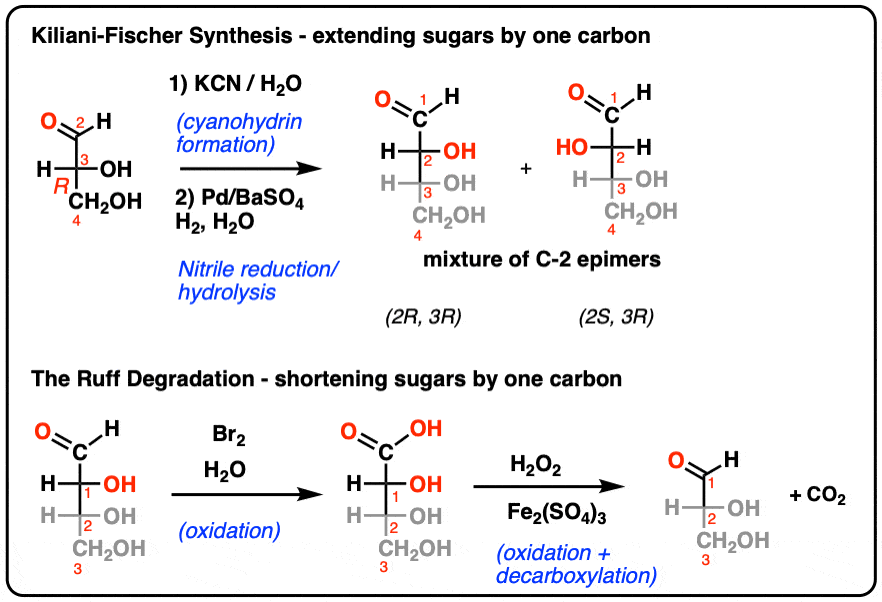
- 的Kiliani-Fischer合成是一种方法扩展碳水化合物链单碳.
- 的拉夫退化是一种方法缩短碳水化合物链单一碳.
- Kiliani-Fischer合成涉及到加成氰根离子到开链醛(在醛糖的情况下),然后是部分减少然后水解得到新的醛.在没有手性试剂的情况下,会产生非对映体(外映体)的混合物。
- Ruff降解法是一种进行反反应的方法。A糖被氧化成A羧酸然后与硫酸铁和氧气氧化,释放出CO2.
目录
1.氰化物离子有助于延长碳链
氰化物离子(CN- - - - - -)是一个非常有用的工具,可以通过单个碳来延长碳链。
一个常见的例子是氰化物离子与原酸的反应烷基亲核试剂中的卤化物取代反应(年代N2).结果腈然后可以与酸水溶液水解得到羧酸(反过来又可以发生许多进一步的反应)。
在下面的例子中,一个四碳原子烷基卤化物延伸到一个五碳链上羧酸:
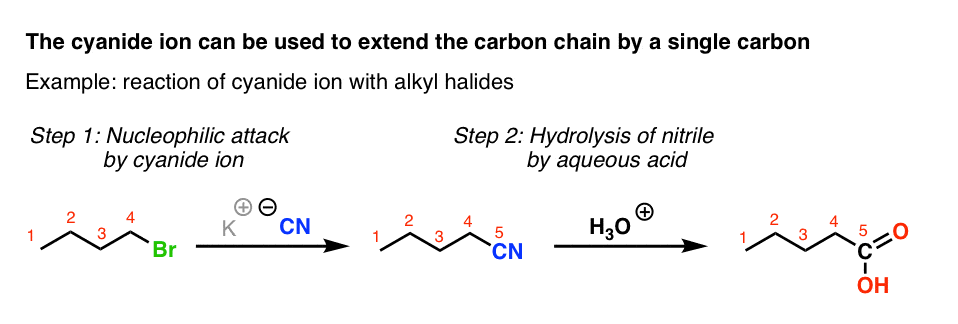
该方法还可推广到其他亲电试剂烷基卤化物。例如,氰化物离子与醛的反应氰醇:
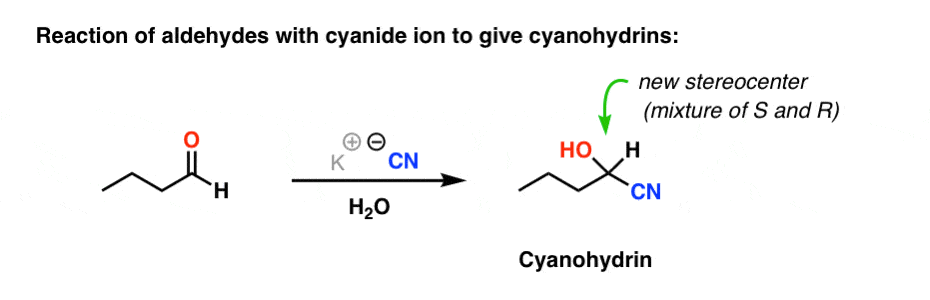
在这种情况下,以及几乎所有其他情况下,创建一个新的手性中心.在没有任何手性试剂的情况下,其结果将是两种构型的混合物(R而且年代)在氰醇碳。
2.Kiliani-Fischer合成
同样的反应可以用来延长一类非常重要的醛的碳链:醛糖(即碳水化合物中含有醛).(参见:关于糖命名法的大帖子]
醛糖中氰醇的形成
以最简单的糖为例,三碳醛糖甘油醛(下面是d -甘油醛)。
与上面的例子一样,氰化物离子对醛结果为氰醇将最长碳链的长度从3个延长到4个。它还创建了一个新的立体中心,产生了具有(R)而且(年代)配置。
因为C-3碳的立体中心(R)在此过程中保持不变,在没有任何手性试剂的情况下,此过程会产生非对映体的混合物:(2 r, 3 r)及(2, 3 r).
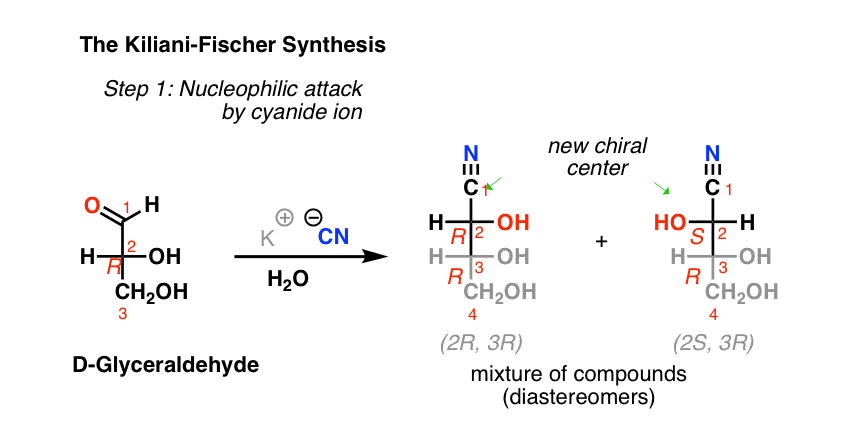
虽然这些氰醇可以水解成羧酸(与水基酸),但通常更有用的方法是采用这种方法来生成新的醛糖。
使用一个中毒催化剂(Pd /贝索4)在氢气(H2)可减低腈到一个亚胺.在水的存在下,亚胺会迅速水解成氨醛.
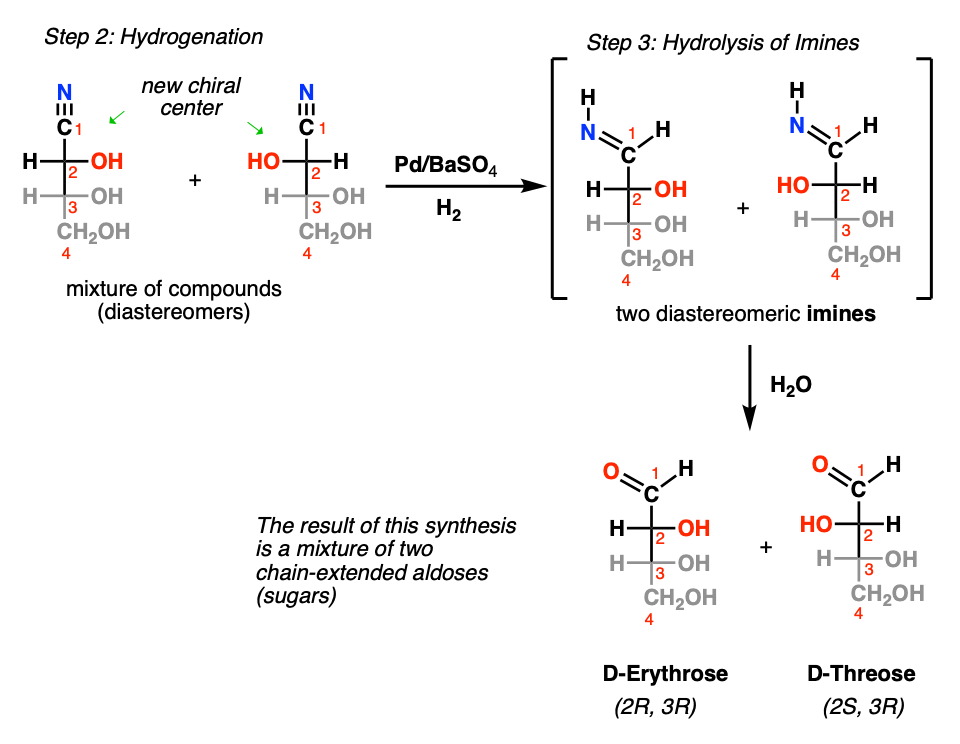
其结果是一个糖延伸了一个碳(作为混合物)。例如,将此程序应用于d -甘油醛,可得到两种非对映体d -红糖(2 r, 3 r)和d -苏糖(2, 3 r).(因为这两种非对映体只在一个碳上的构型不同,所以它们通常被称为“外映体”。
3.褶边退化
也可以进入反向方向,醛糖所在的位置减少长度除以一个碳。
朝着这个方向前进的过程被称为拉夫退化,这一过程可以追溯到19世纪90年代末。
在第一步,醛被选择性氧化成a羧酸由溴(Br2)和水。注意,仲醇和伯醇在这里没有被氧化!
下一步是加入铁(III)盐[Fe2(所以4)3.过氧化氢,这涉及到二氧化碳的损失和相邻的C的氧化2-哎呀醛:
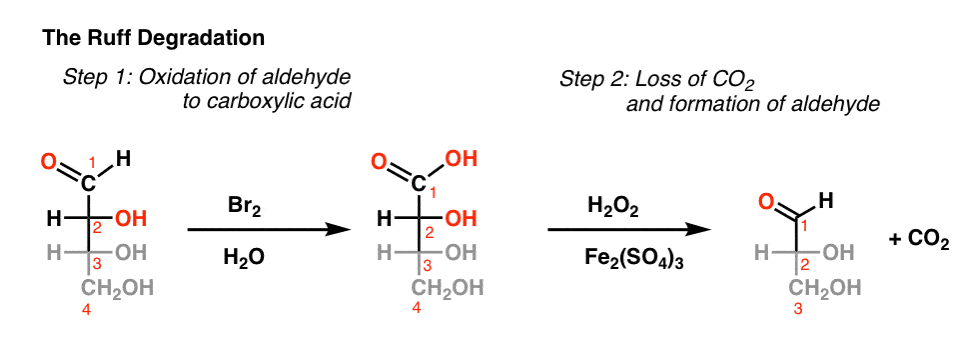
大多数课程一般不会深入到机械细节的杂草,但我们将尝试在Br2/小时2下面的O反应注1.
那么为什么这很重要呢?
我很难告诉你,Kiliani-Fischer和Ruff降解反应是现代有机化学的前沿。他们不是。[不过,公平地说,拆分用手性催化剂从醛生成氰醇是重要而有用。例子.]
然而,它们确实具有重要的历史意义,因为它们是埃米尔·费舍尔用来确定葡萄糖和其他醛已糖结构的两个重要工具,这一努力为他赢得了诺贝尔奖1902年诺贝尔化学奖.
只是为了让你感受一下,Fischer能够证明d -葡萄糖和d -甘露糖在Ruff降解时形成相同的产物(d -阿拉伯糖),这表明它们在C-2(外聚物)上具有相反的配置。进一步的Ruff降解得到d -甘油醛,建立了C-5手性中心的立体化学。
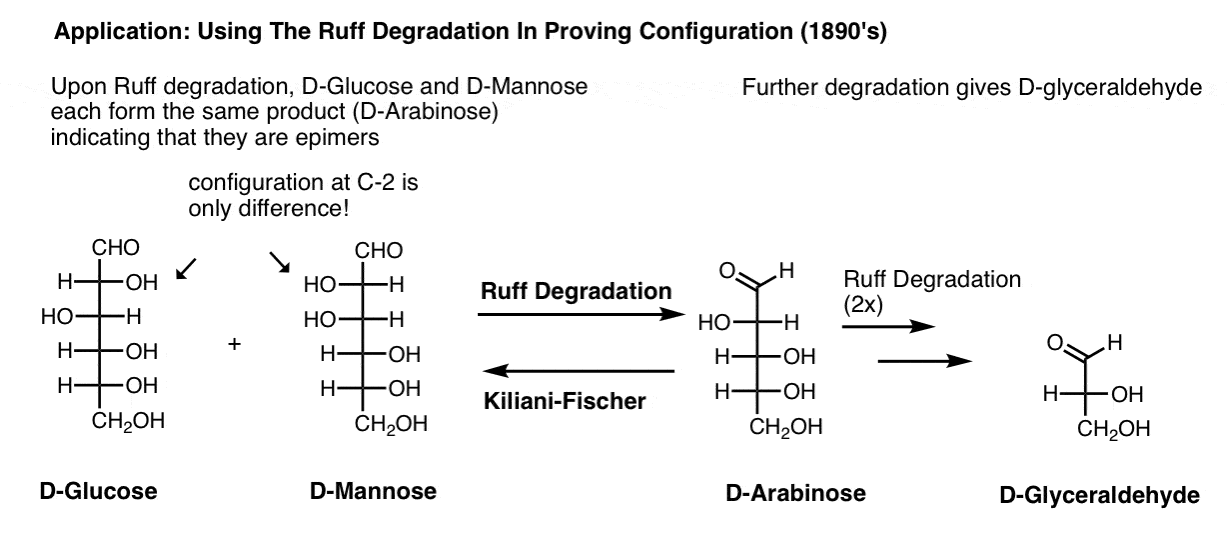
在某些时候,我们将深入讨论当我们研究费舍尔的证据葡萄糖的结构。
笔记
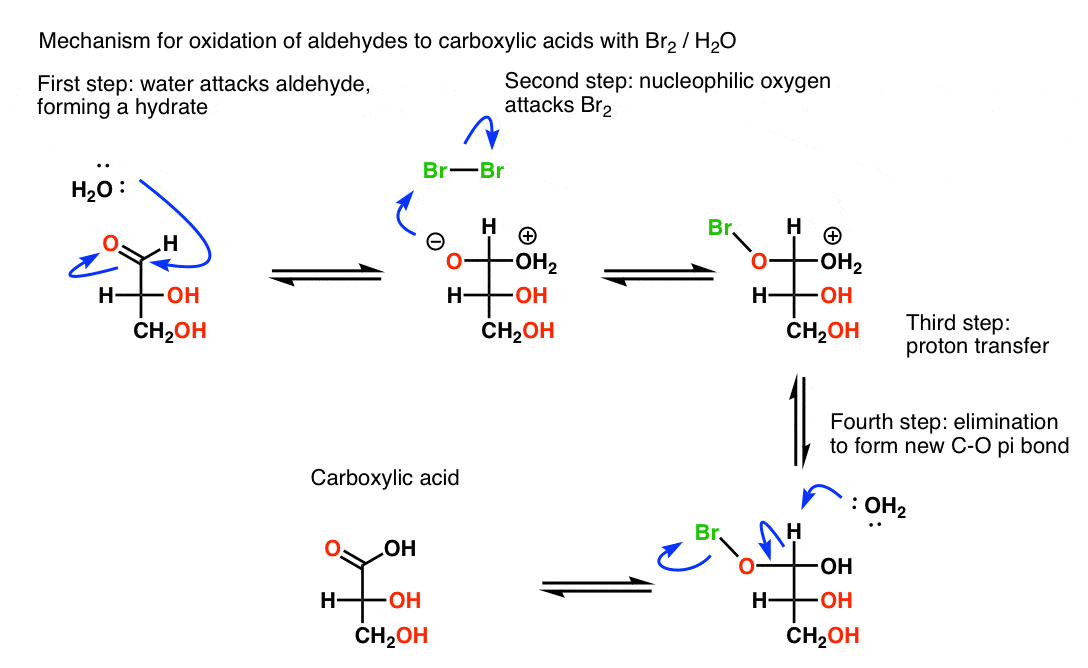
第一步是a的形成水合物从加水到醛.的两性离子O-的形式比中性的形式更亲核,所以这里它表现为亲核试剂攻击Br2.在某一点上,OH2+被中和;这里显示的是攻击Br后发生的2,但它可能发生得更早。
注意,现在有一个好离去基团在氧(Br)上。弱碱(H2O)然后去质子化C-H,形成一个新的C-O π键,失去Br(-)导致形成羧酸.
注2。这里我们不讨论拉夫降解的机理,但我要指出铁和氢2O2成分是什么芬顿反应这个过程会产生羟基自由基。
(高级)参考资料和进一步阅读
- Ueber das Cyanhydrin der Lävulose
海因里希·基连尼
的误码率。1885,18(2), 3066 - 3072
DOI:10.1002 / cber.188501802249 - 还原von Säuren der Zuckergruppe
埃米尔费舍尔
的误码率。1889,22(2), 2204 - 2205
DOI:10.1002 / cber.18890220291
第19届德国化学家海因里希·基里亚尼和埃米尔·费舍尔首次发表了两篇关于糖用氰化物进行1-碳同源的论文th世纪。 - 2-Deoxy-D-ribose。六、1 3-脱氧- d -核糖己酸及其衍生物的制备。关于Kiliani合成的一些观察
小哈里·b·伍德和小休伊特·g·弗莱彻。
有机化学杂志1961年,26(6), 1969 - 1973
DOI:1021 / jo01065a068
本文探讨了通过Kiliani-Fischer合成各种碳水化合物的方法。 - 立体控制可扩展合成l-硬糖醛酸衍生物氰醇肝素相关双糖的合成反应Steen Uldall Hansen, Marek Baráth, Bader A. B. Salameh, Robin G. Pritchard, William T. Stimpson, John M. Gardiner, Gordon C. Jayson
有机的信2009,11(20), 4528 - 4531
DOI:10.1021 / ol901723m
这篇论文展示了Kiliani-Fischer反应在现代有机化学中的效用,使一些不能用其他方法合成的双糖的合成成为可能。
在基里亚尼-费歇尔合成中,我们不考虑循环形式的H键。
我不太明白你的问题,因为氢键不应该影响反应。如果你指的是糖以线性和循环形式的混合物存在的事实,这只对五碳及以上的糖开始变得重要,即使在那时,开链和闭链形式之间也存在平衡。请看这篇关于环链互变异构的文章://m.deriinvest.com/2017/07/13/pyranoses-and-furanoses-ring-chain-tautomerism-in-sugars/
你能解释一下FeSO4 + H2O2的作用吗?它是氧化剂吗?
H2O2将铁氧化为一种非常不稳定的Fe(IV)物种,它反过来从羧酸盐中夺走一个氧的电子。然后二氧化碳的损失,导致碳基自由基,它又被铁氧化一次,产生一个新的碳正离子。碳正离子的共振形式是质子化醛,然后去质子化得到中性醛。我认为在Kiliani-Fischer合成段落的结尾有个错误。D线应该是2S-3R,而不是2R-3S
开枪。你说得对。谢谢你指出来,我会改正的。
我有一个问题,当葡萄糖被强氧化剂氧化时(比如用conc HNO3),为什么中间的2度醇不被氧化??
你确定你得到了Fe(IV)种吗?我认为Fe3+与H2O2反应生成H+和*O-OH自由基。形成的Fe2+然后将另一等量的H2O2还原为-OH(与先前形成的H+反应生成水)和HO*自由基。HO-O*从-COOH中抽出一个质子,生成-COO*,然后失去二氧化碳和一个新的碳中心自由基。然后与HO*反应生成水合物。在最后一步中,也可能有其他几种途径,尽管它们都导致相同的结果。
抢手货。我相信你是对的。会解决这个问题。