酸碱反应
酸碱反应:引入Ka和pKa
最后更新:2022年12月29日|
酸度常数K一个(及其负对数pK一个)是一种非常有用的酸度测量方法
所以上节课我们讲了所有影响酸度的不同趋势.底线是任何稳定共轭碱会导致酸度增加。
现在,了解趋势是很好的。事实上,这非常重要。(见文章:有机化学学习技巧-了解趋势)
但是,当你想比较两个没有趋势相连的分子的酸度时,你该怎么办呢?
例如,共振会增加醇的酸度,但增加多少呢?比把OH变成SH来增加酸度还要多?如果加一个吸电子基团呢?
用这种方法不可能把所有相反的变量都整理出来。趋势只是定性本主题的指南。
为了回答这个问题,我们需要一些确凿的数据,而在有机化学中只有一种方法——通过测量。
这就是酸度常数K一个(和它的负对数pK一个)。
目录
- 酸度常数K一个表示酸解离成共轭碱和质子的平衡常数
- 酸解离常数的例子一个对于强酸(HI),弱酸(CH)3.OH)和一种极弱酸(CH4)
- K的负对数一个,“pK一个是一种比K更方便的酸度测量方法一个
- 的pK一个规模涵盖超过60个数量级
- 笔记
1.酸度常数K一个表示酸解离成共轭碱和质子的平衡常数
我们来看看氢碘酸H-I。在溶液中(我们用水)H - i会质子化水得到H3.O(+)和I(-)。逆反应也有作用。[I(-)与H反应3.O(+)把H-I还给我们。所以这个反应是an平衡。
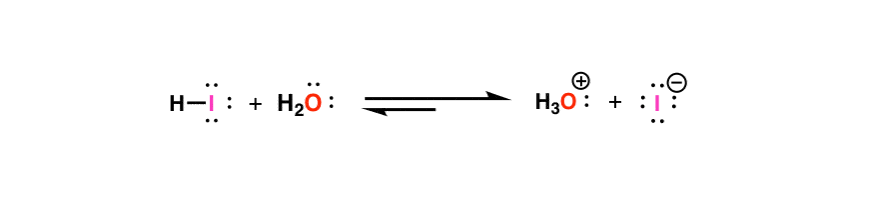
这是有用的部分。我们可以测量这个反应的平衡常数,它会告诉我们H-I的相对酸度。具体如何测量是另一回事了,但为了我们的目的,我向你们保证这些类型的平衡常数是可以精确测量的。
对于H-I,这个反应的平衡常数大约是100亿。这意味着对于每个HI分子,有100亿个I(-)分子。换句话说,H-I很容易就能给出它的质子共轭碱这是强酸的一个主要例子。
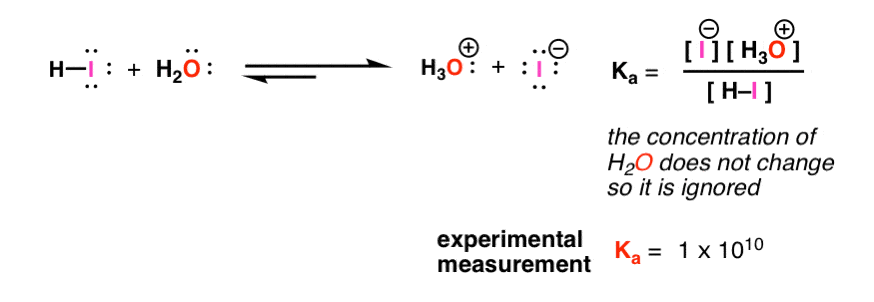
那又怎样?好了,我们不仅可以对氢- i这样做,还可以对任何带氢的物质。这个平衡是我们用来测量任何酸的“标尺”——通过它的平衡常数。[注1]
我们称这个平衡常数为K一个-“酸度常数”。
2.酸解离常数的例子一个对于强酸(HI),弱酸(CH)3.OH)和一种极弱酸(CH4)
让我们来看3个例子。注意,这些有些过于简化了,因为溶剂被省略了
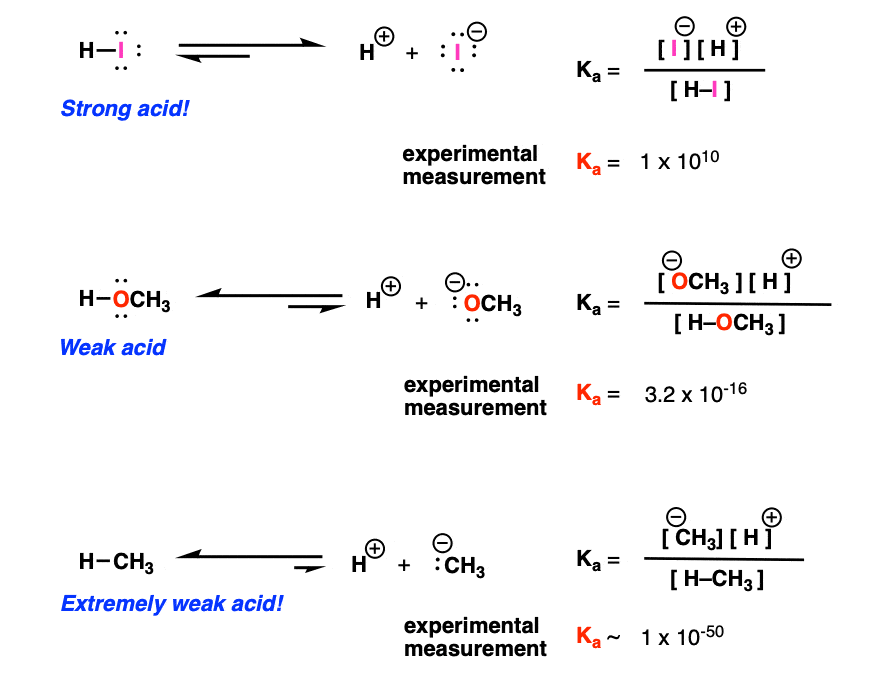
现在比较后面有很多指数的数字之间的酸度不是最方便的方法。所以,我们开始使用对数刻度。这些都是常见的——里氏震级是对数级,例如,8.0级地震的威力是7.0级地震的10倍。
3.K的负对数一个,“pK一个是一种比K更方便的酸度测量方法一个
对于酸度,我们用的数字叫做“pK”一个”。它是通过取对数酸度常数Ka,我们任意地将它乘以- 1K的绝大多数一个数值小于1,我们通常更喜欢处理正数]。

对于H-I, pK一个是-10(表示非常强酸),甲醇是15(弱酸),甲烷是50(极弱酸)。
4.的pK一个规模涵盖超过60个数量级
这个尺度包括60个数量级。这是一个巨大的数字!!!!!
让你们对pK的规模有个概念一个,这是长度(普朗克长度,10)最小值的范围-35年米),到已知宇宙的宽度(大约10米)26米)。(见文章:pKa值跨越60个数量级)
不管怎样,这些测量已经对成千上万种不同的分子进行了。结果是一个大表格,让我们可以比较各种不同官能团的酸度。这里有一个pK的例子一个表来自前一篇文章。
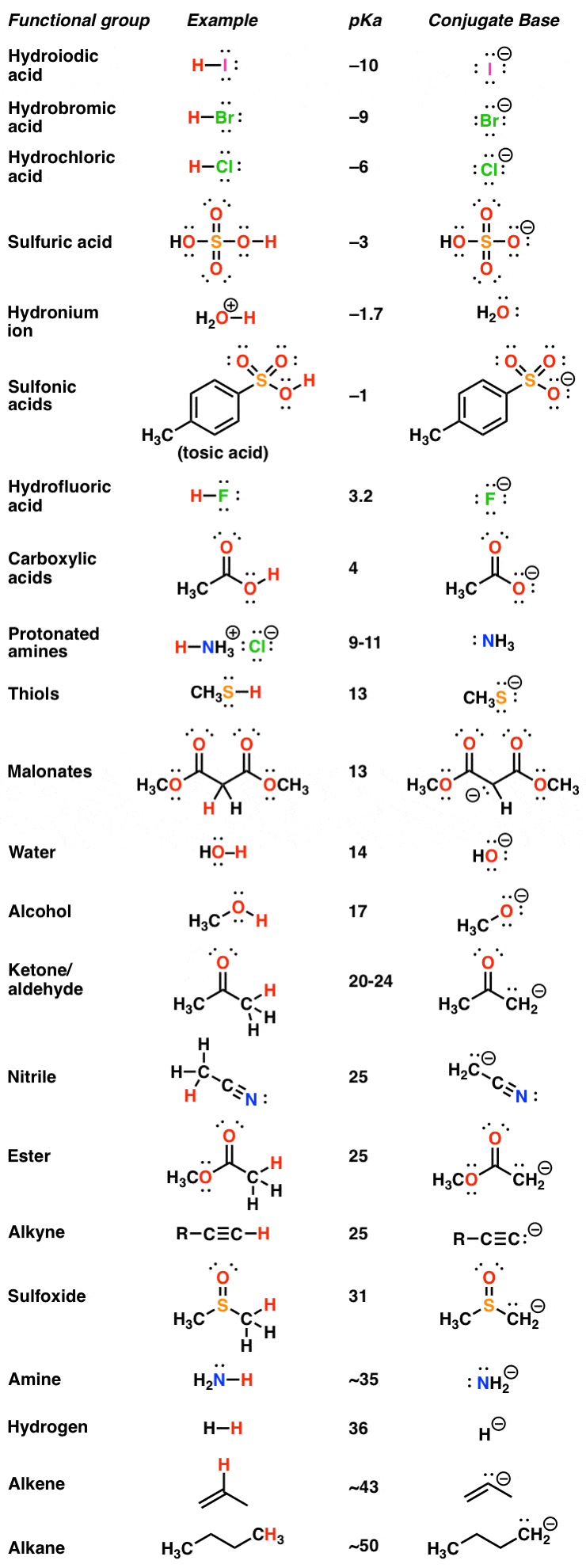
的pK一个桌子是你的朋友。在一份文件中,它给了你关于各种化学行为的范围和程度的信息——强酸中最强的,弱酸中最弱的。因为酸越强,就越弱共轭碱,它还提供了关于碱度的信息。
在下一篇文章:如何使用pKa表
笔记
注1由于“水平效应”,这些测量的溶剂的选择很重要。例如,水通常用作具有pK的分子的溶剂一个值小于零且不大于约14,因为水中不可能有比H更强的酸3.O(+)没有比HO(-)更强的碱。
为了得到一些更极端的值,必须使用其他溶剂,如二甲亚砜(DMSO溶液).如果你最终选择了一门更高级的有机化学课程,你可以用更严格的眼光来看待这些数值。〇强烈推荐埃文斯的pKa表给出H的值2O和DMSO溶液.还有汉斯·赖克在威斯康辛州的英勇努力编译pKa值.
好文章!看起来当你说“这个网站有一个惊人的动画”时,你忘记放链接了。
HI给I-的反应中有一点我不太明白。
如果Ka值是10^10,那么这是否意味着对于每个HI分子,浓度[I-]和[H3O+]的乘积,而不仅仅是[I-]?所以不应该有根号下10^10分子的I-吗?
Evan的pka表的链接不再存在。我搜索了一下,我认为这是你现在想要的链接:http://evans.rc.fas.harvard.edu/pdf/evans_pKa_table.pdf
好的,谢谢!
同样的原则适用于pkb和pka吗?也就是说,低pkb是否意味着碱比高pkb的碱反应性更强?还有pkb表吗?
我建议不要处理pKb。相反,我建议考虑pKaH,即共轭酸的pKa。例如,氧基离子CH3CH2O(-)的pKaH是16。
在许多网站和教科书中,我发现H2的pka小于NH3的pka,或者可以说胺在氢之前,那么哪一个是正确的?
修正*小于
它们差不多。
我有一个疑问:
当极性质子溶剂用作共轭碱的溶剂时,共轭碱会是溶剂中最强的碱/亲核试剂吗?
谢谢!
是的,这就是所谓的“水平效应”。溶剂中可能最强的碱是该溶剂的共轭碱。因此,H2O中最强的碱是HO-(水的共轭碱),因为如果添加一个更强的碱(例如NaNH2),碱会立即使溶剂脱质子,生成它的共轭酸(NH3)和溶剂的共轭碱(HO-)。
啊,Ohkay !
非常感谢!
先生,我认为有毒酸在水中是-2.3,对吗?它不应该高于水合氢离子,对吗?
这个数字差不多。
在强酸,弱酸,非常弱酸的反应中。我认为反向反应的箭头方向是错误的。
感谢这个网站,我有考试在2个月的PCM,这是一个救星。
你是正确的,固定的!
嗨!我想知道项目要点2中的平衡箭头,强酸(HI)、弱酸(CH3OH)和极弱酸(CH4)的酸解离常数Ka的例子。在这个例子中,对于弱酸和极弱酸,箭头表示平衡在右边而不是左边。我想知道这是一个错误,还是我忽略了一些东西为什么平衡会转移到碳阴离子而不是烷烃?非常感谢!
伟大的发现。谢谢你!我修复了图像,并上传了一张替换的图片。谢谢! !
我有一个开放式的问题,我很困惑。为什么酯的酸度比酮低?它们不应该有两个作用吗,氧的共振和来自另一个氧的感应效应?
我的猜测是,感应效应可能只对卤素起作用,因为它们具有很强的电负性。或者,键上的电子对已经与另一个单键氧发生共振,这意味着在酯中共振的影响比在酮中要小。还是两个?我会感谢任何比我更有知识的人来帮助我,每天我都觉得我发现了一些与我以为我知道的一切相悖的东西
非常好的问题。简而言之,“实验告诉我们,共振对O和N更重要”。
酸性与共轭碱的稳定性有关,对于酯类和酮类来说,这种共轭碱会形成一种被称为“烯酸酯”的物质。
C=O键的电子越少,碳上的孤对(即共轭碱的负电荷)就越能转移到碳上,形成一个新的π键,并导致氧上的负电荷(更稳定)。
氧和氮的取代基有两种相反方向的作用。
一方面,这些原子具有电负性,这意味着它们会通过单键吸收电子密度。另一方面,它们能够通过共振与相邻的电子受体(例如C=O)形成π键来“捐赠”电子密度,这种效应被称为π捐赠。
那么哪种效果会胜出呢?这是一个很容易问的问题,但仅凭基本原理很难预测。我们从实验中观察到,对于氧和氮,π赋值效应大于感应效应。
这意味着C=O在酯类和(特别是)酰胺类中由于邻近氧和氮的贡献而缺少*少*电子。这意味着这些物种的烯醇化物不太稳定,这反映在它们的酸性较弱。
类似的效应也解释了为什么O和N取代基在亲电芳香族取代反应中被“激活”——O和N的π给能大于电子抽离效应。
(对于氯,吸电子效应大于给电子效应)。
我很乐意详细说明-文本是一个很难解释这些事情的媒介:-)