芳香分子的反应
亲核芳香替代(2)-苯炔机制
最后更新:2022年9月28日|
在本帖里,我们将讨论亲核芳香取代,但与一个新的转折;一个亲核芳香替换,通过一个叫做一个奇怪的中间芳炔(一个通用术语,包括家庭的分子苯炔)。
表的内容
- 亲核性芳香取代——一个快速回顾
- “亲核芳香取代”的名字,但由不同机制
- “苯炔”中间
- 取代苯炔的反应——“芳炔”
- 苯炔经历Diels-Alder反应
- 苯炔的结构
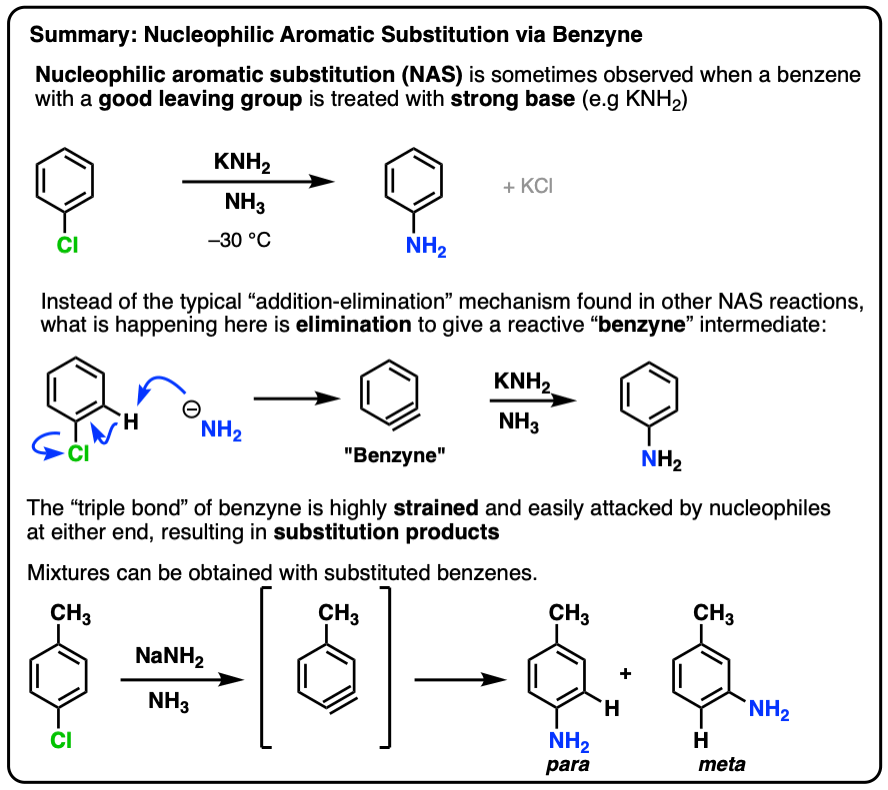
- 摘要:通过苯炔亲核芳香取代
- 笔记
- 测试你自己!
- (高级)引用和进一步阅读
1。快速回顾:亲核芳香取代反应
之前(看到的:亲核性芳香取代]我们看到包含一个electron-poor芳香环离去基团可以接受替换负电子的亲核试剂吗。我们发现通过添加收益的机制亲核试剂芳环(通过一个电子的中间)其次是亏损的离去基团,这一过程有时被称为“addition-elimination”。
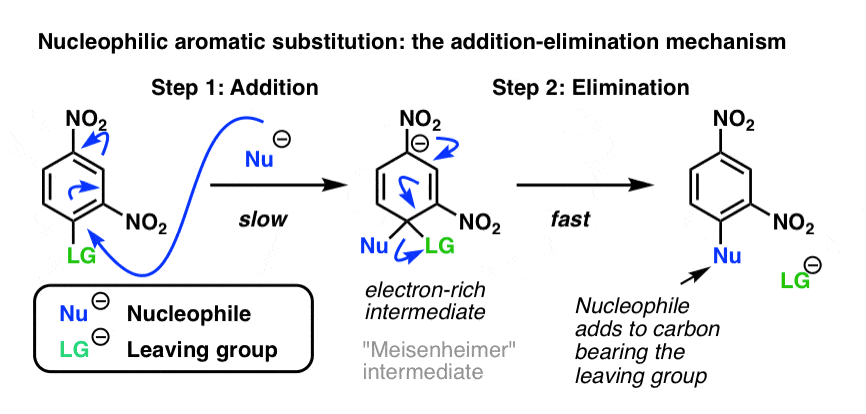
重要的是,唯一的替代产品的一个亲核试剂最终连接到相同的碳,轴承离去基团。(这就有别于亲电芳香取代,的混合物昊图公司- - - - - -,帕拉- - -元- - - - - -产品可以获得)。
2。“亲核芳香取代”的名字,但由不同机制
虽然“addition-elimination”机制对亲核芳香取代已知至少从1902年开始,越来越清楚上半年的20世纪,某些反应分为“亲核芳香替代”似乎进入一个完全不同的机制。
例如,它发现治疗氯苯氨基钠(NaNH2)在液氨(沸点= -33°C)导致的快速形成氨基苯(苯胺):
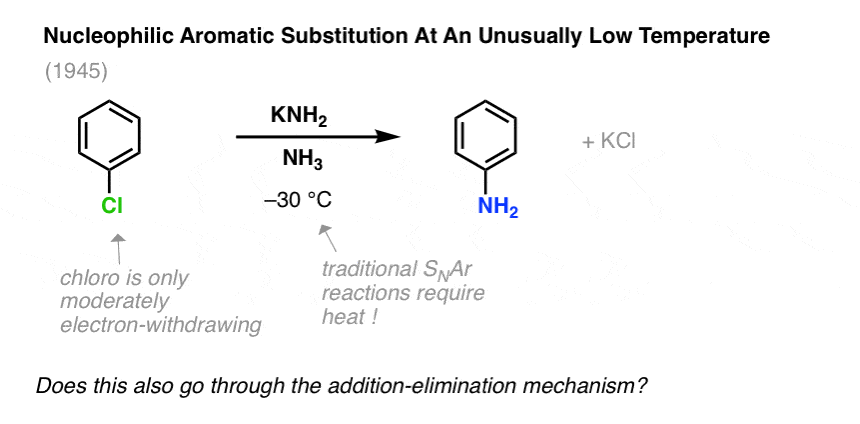
addition-elimination机制在这里似乎不正确,考虑到亲核芳香取代反应与远强电子撤回团体(例如没有2,而不是Cl)需要较高的温度和较长的反应时间。
另一个观察是没有反应发生时,在这种情况下昊图公司- - - - - -职位是附加到烷基组。氢是必要的在这些位置的反应继续进行。
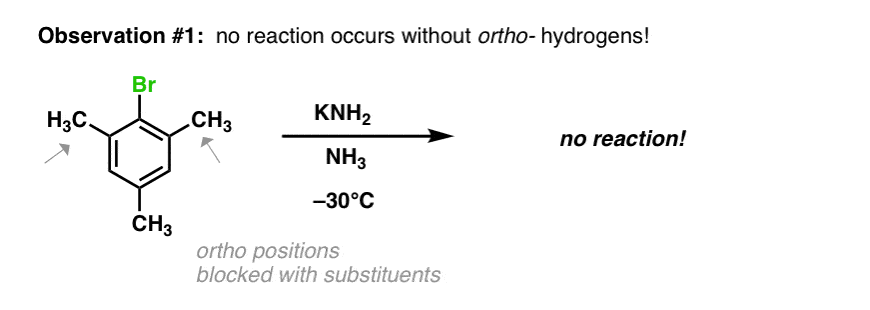
(注意- NaNH2和KNH2可以被认为是基本相同的对于我们的目的)
第二个观察是只在以下情况下昊图公司- - - - - -和元- - - - - -产品形成,从来没有的帕拉-。
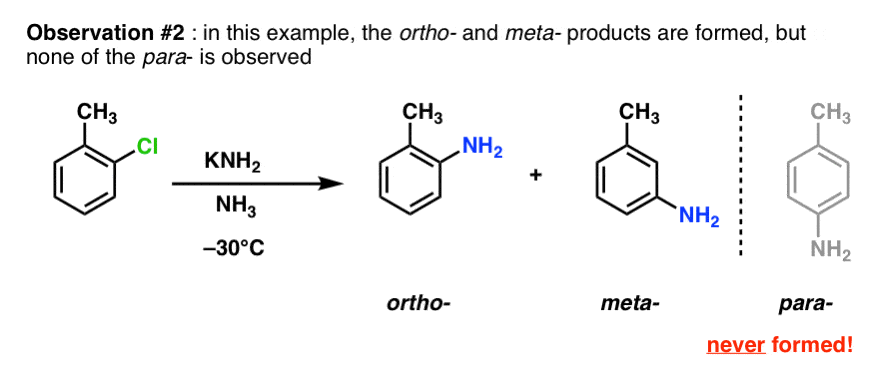
3所示。苯炔的中间
提出了各种中间体来解释这些结果,然后在1953年约翰·d·罗伯茨(麻省理工学院)钉它通过发布最优雅的化学实验所有的时间。
他和他的团队合成氯苯但是特别的区别:碳附着在氯的放射性同位素碳(14碳(C),而不是12C)。
这种放射性碳原子作为一个原子“标签”,只允许他们最终确定替换发生的碳轴承离去基团。(如何?(注意4])
罗伯茨集团此前报告的条件下进行反应,并发现约50%的产品以北半球结束2附着在碳标签,另50%北半球2在碳相邻的标签。
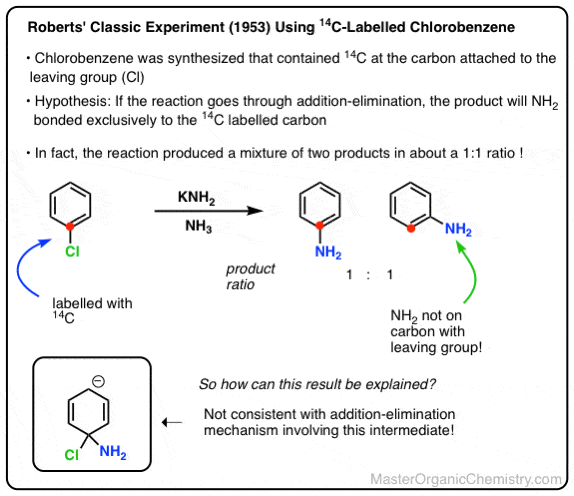
这是不符合一个addition-elimination机制!
事实上,大约50:50的比例的产品意味着的参与对称的中间是攻击同样两侧。
罗伯茨的提议——已经经受住了时间的考验——短暂的中间轴承的参与是一个碳碳三键:“苯炔”!
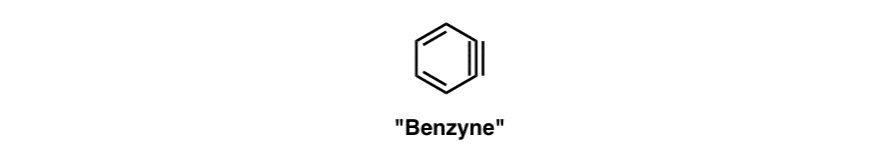
乍一看,这似乎是疯了。一个三键的芳环吗?
它不是一个真正的三键的方式(即我们熟悉的炔烃)。而不是一个两个重叠2 p轨道(如在一个炔烃)“三键”是通过重叠形成的两个相邻sp2轨道平面上的戒指(即成直角,完全独立于,芳香pi系统)。
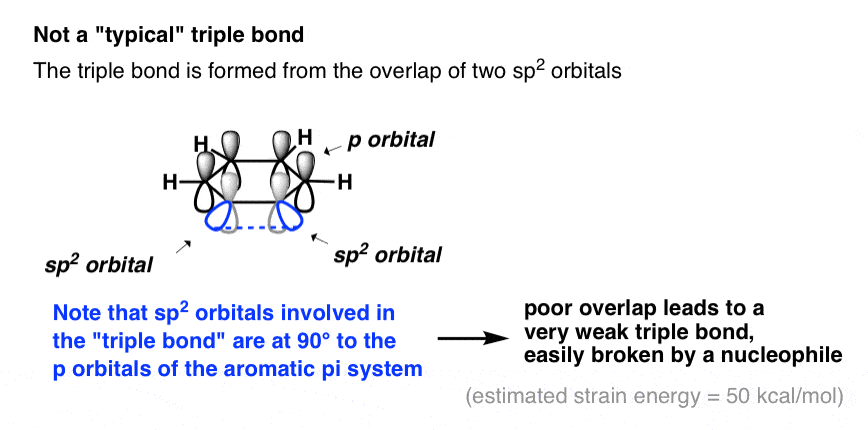
因为这些轨道点远离彼此,他们是穷人之间的重叠,导致“三键”,其实是很弱的。
苯炔的应变能,据估计大约50千卡每摩尔——更紧张比环丙烷(28千卡每摩尔),紧张,仅略低于cyclopropene(54千卡每摩尔)。
想想一个直观的方法就是想象的参与两个共振结构(左,右,下面),使强(平等)贡献整体共振混合,这样两个碳可以被认为是“亲”。
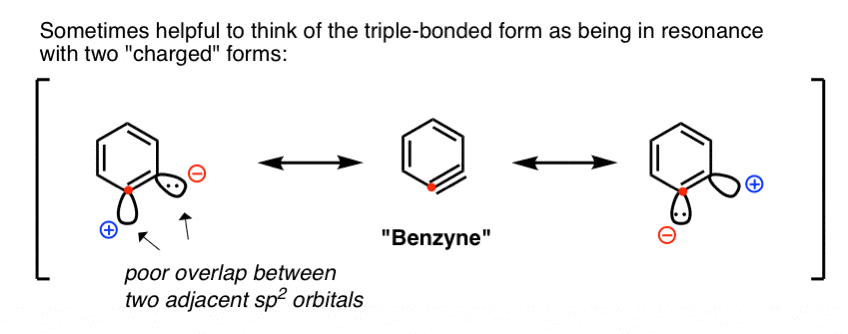
(更严格的方法把它从一个分子轨道的角度——弱键导致一个低能LUMO,攻击的亲核试剂,因此较低的能量障碍)。
然而它可能看起来奇怪,苯炔中间解释所有这些重要的观测,以及更多。
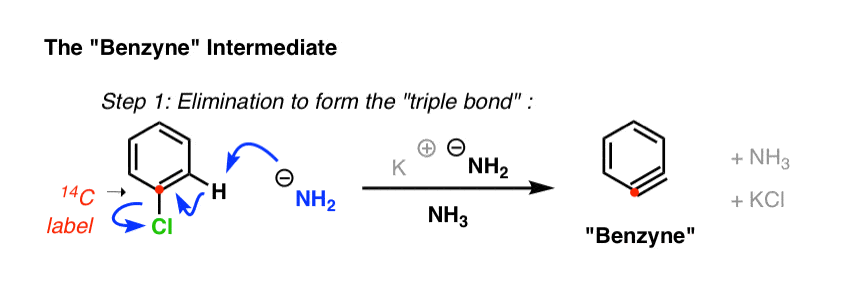
- 在第二步中(除了),能来的攻击要么一边的三键,导致与NH约1:1混合的产品2附着在碳标签(一个)和NH2毗邻贴上碳(B)。
虽然它很容易使用- - - - - -NH2作为亲核试剂,就越有可能亲核试剂这里是溶剂,NH3,容易与极其被动的苯炔反应中间体。NH攻击后3导致发生质子转移,中性产品。(注意,尽管分子内质子转移如下所示,它也可以显示它通过分子间发生机制)
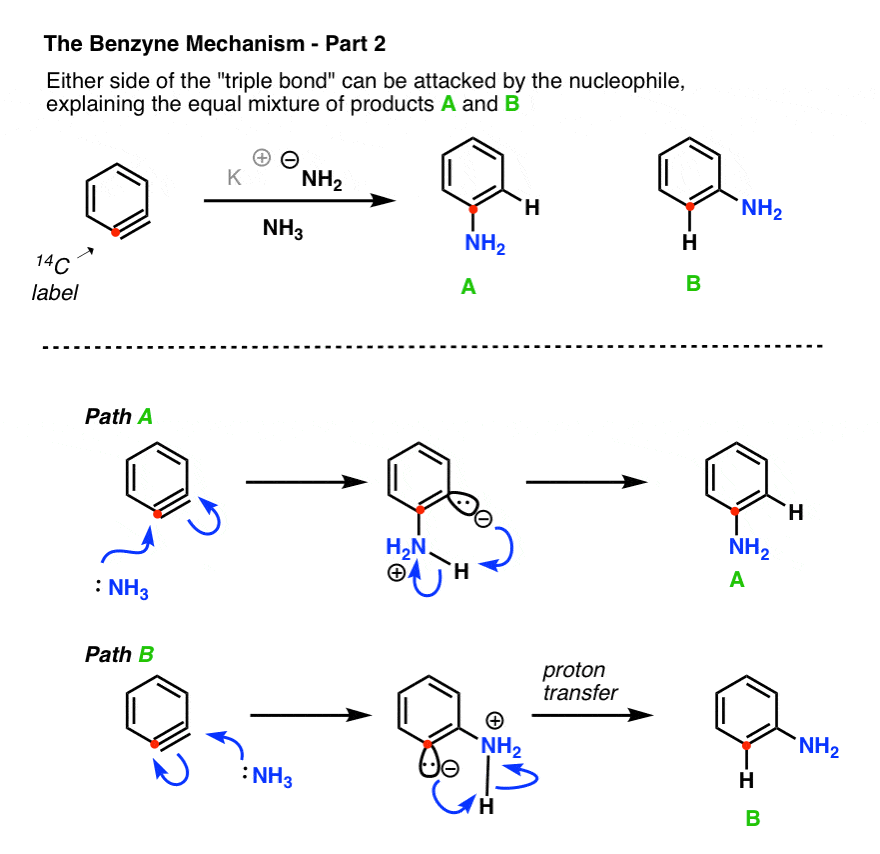
4所示。取代苯炔的反应(“芳炔”)
当一个取代基存在苯炔发生了什么?【注:就像苯取代化合物被称为“粗砂”,取代苯炔被称为“芳炔”。]
当取代基存在时,就会形成不对称芳炔,至少两个产品(有时三)可能形式。在下面的示例中,NH的攻击3在碳的结果昊图公司产品,和北半球的攻击3在碳B的结果元产品。
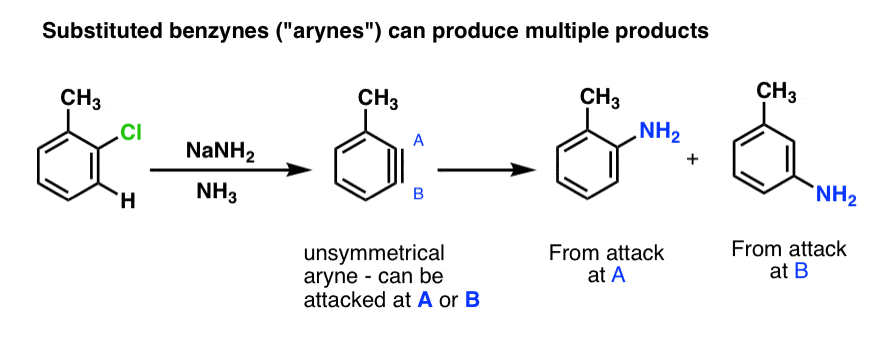
环上的取代基如何影响除了三键?
由于芳香pi-system成直角三键,无关的是捐赠的能力一个孤对环(如哟3),或者接受孤对(如没有2)。
然而,归纳影响仍然是适用的(即通过单键)发生的吸电子效应。
为什么?除了碳三键创建一个负电荷,和吸电子集团稳定负电荷:越近越好。
所以一个关键原则的芳炔的亲核试剂是还会发生,将负电荷接近一个吸电子取代基。
两个关键的例子。
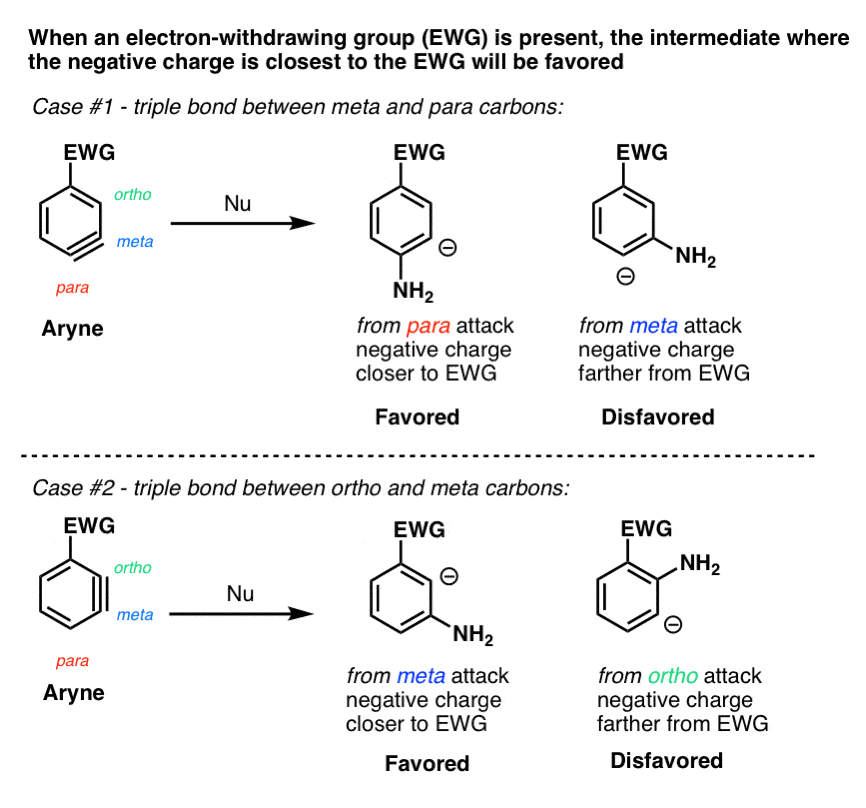
请注意,这仅适用于吸电子集团像CF3,而不是像CH电子基组3或烷基。有趣的是,哟3像一个吸电子集团在这些例子中,因为氧孤不能与三键交互。
看到[注1一些更多的例子)。
5。苯炔经过一昼夜的桤木的反应
苯炔也可以与二烯烃反应Diels-Alder反应。三键的苯炔充当亲二烯体:
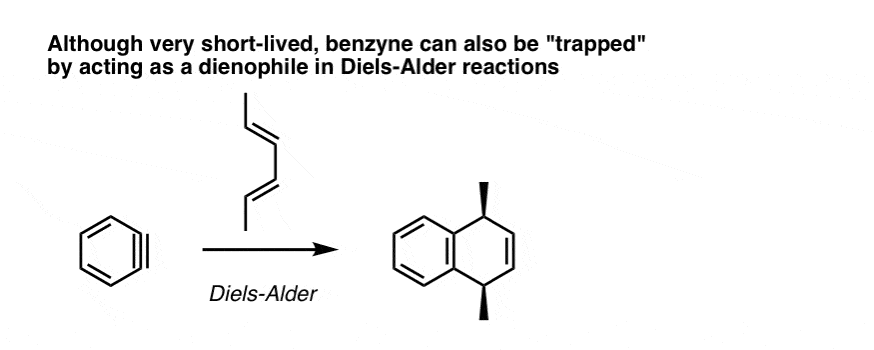
6。苯炔的结构
多年苯炔违抗尝试隔离和表征,其存在推断通过捕获实验的亲核试剂或二烯烃。它生活快,年轻的死去。
最终,苯炔被困在6 k(即六度高于绝对零度)在冷冻氩和通过各种光谱方法研究。三键约为1.26,再比乙炔(弱)(1.20)和相邻的碳碳键大约是1.38,略短于苯。
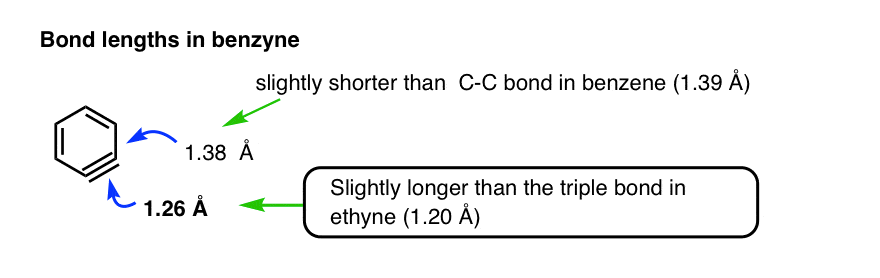
(见参考)。0.01中的所有其他碳碳键的键长在苯。
7所示。摘要:通过苯炔亲核取代反应
最后一个类型的芳香取代反应为我们考虑,一个家庭的反应称为桑德迈尔反应,使用氮气(N2)作为离去基团。下次。
在下一篇文章:重氮盐的反应和桑德迈尔反应
笔记
- 其他一些替换的例子
- 方法生成苯炔
- 罗伯茨的降解研究
其他代替苯炔的例子
当一个吸电子取代基如CF3是用来代替CH3,更多的帕拉形成——大约比例,支持帕拉。(统计数据支持元2:1)。
这是因为攻击的帕拉位置的地方负电荷接近电子集团撤军。
有趣的是,哟3给相同的比例作为CF3(比例)。这意味着氧表演纯粹作为吸电子集团,不是pi-donor。(进一步证明氧孤对不能与三键交互。)
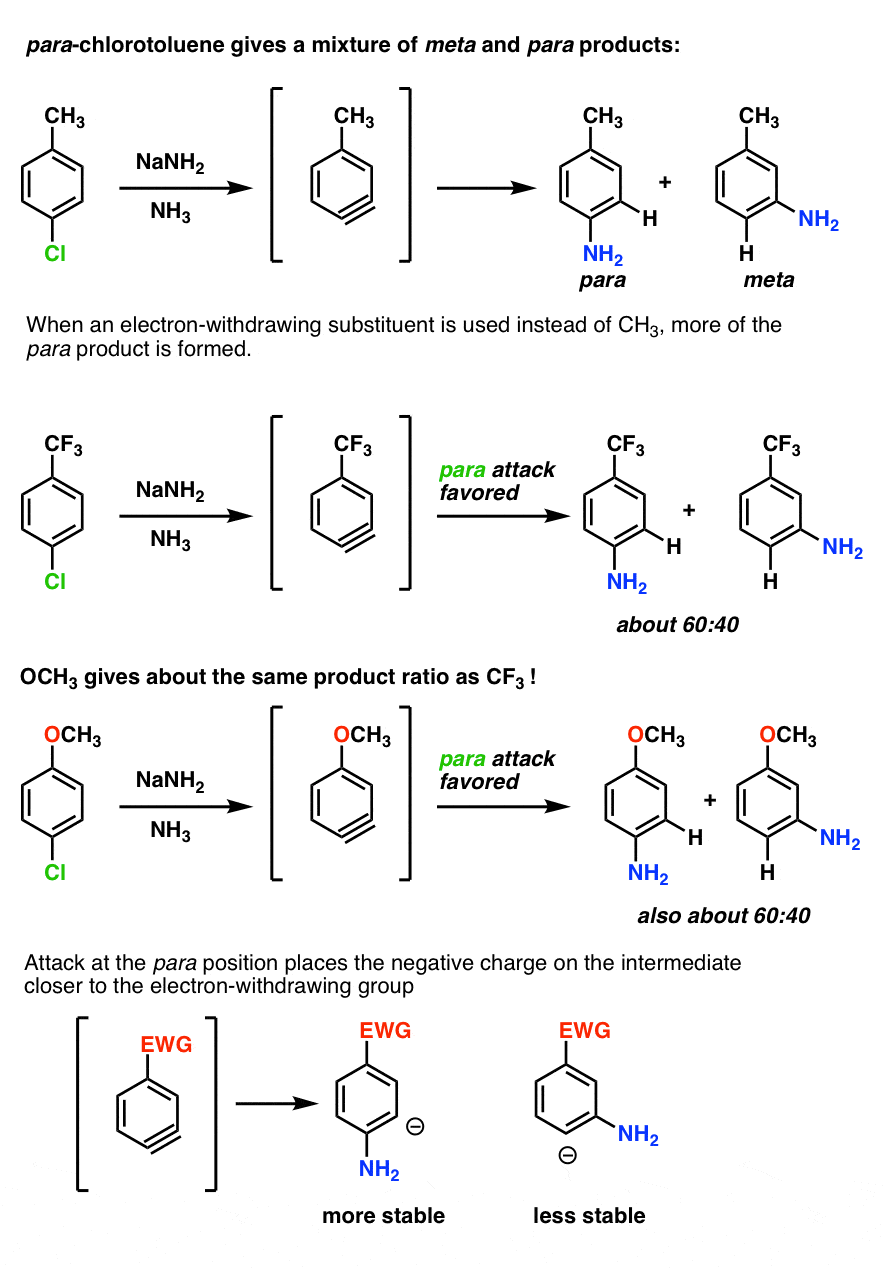
与昊图公司- - - - - -系列,结果是更大的。与CH3,大约同等的混合物昊图公司和元产品。与CF3和哟3,只有元是观察到的。
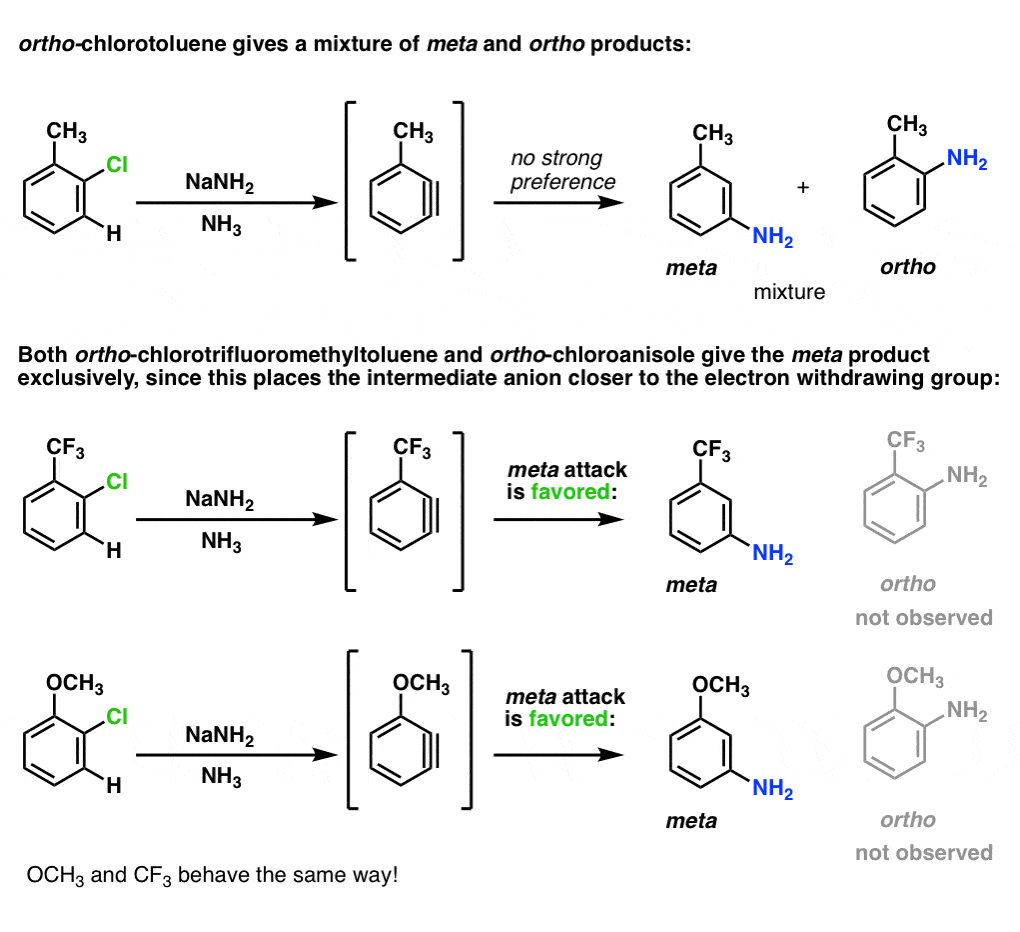
生成苯炔的某些方面
苯炔可以在其他方面除了生成强碱如NaNH去质子化2或KNH2。
格氏试剂的行为很像负碳离子。所以一条不同的道路苯炔与dihalobenzene开始形成o-bromofluorobenzene用镁金属和治疗它。格氏形式,然后这个“负离子”甚至可以取代一个好的离去基团像氟给三键:
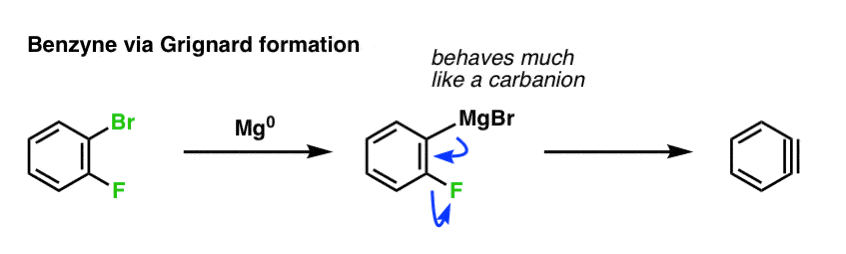
另一个路径是生成一个离去基团可以离开不可逆气体,像有限公司2或者N2。
下面的第一反应,紫外线打破了o - o键,弱然后均裂分离导致两个公司的损失2分子苯炔。
在第二个例子中,商用(廉价)邻氨基苯甲酸与HNO转换成重氮离子2和盐酸。热导致公司的损失2和N2:
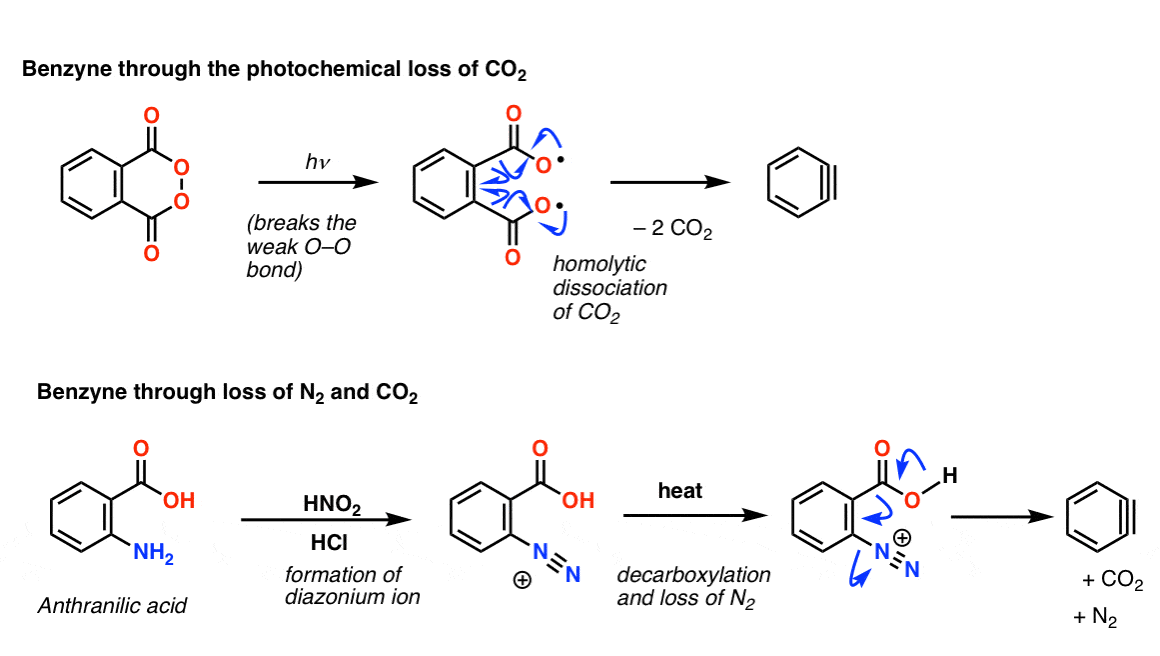
这仅仅是冰山的一角。更多的阅读,这个演讲对芳炔普林斯顿大学的Eric Welin Macmilllan集团是一个很好的介绍。
降解研究。
今天,罗伯茨的结果可以确定标签的实验在大约5分钟通过核磁共振技术,或核磁共振。
但在1954年,这种技术不存在。这是必要的,以确定的比例把产品分解成更简单的组件通过理解化学反应,这种技术被称为“退化”。
苯胺转化为酚通过重氮盐与水形成和替换。加氢与兰尼镍在高压力下给环己醇,氧化和铬酸环己酮。施密特反应环己酮转换为内酰胺,自由酸水解。第二个施密特反应然后解放有限公司2与氢氧化钡,被困。的放射性物质有限公司2和二胺产品被发现是大致相等(和每个大约一半的总酸前体)的反应性,从而确认攻击发生在两个不同的碳氮。
化学祖先不得不执行本职工作只是为了得到一个结构。
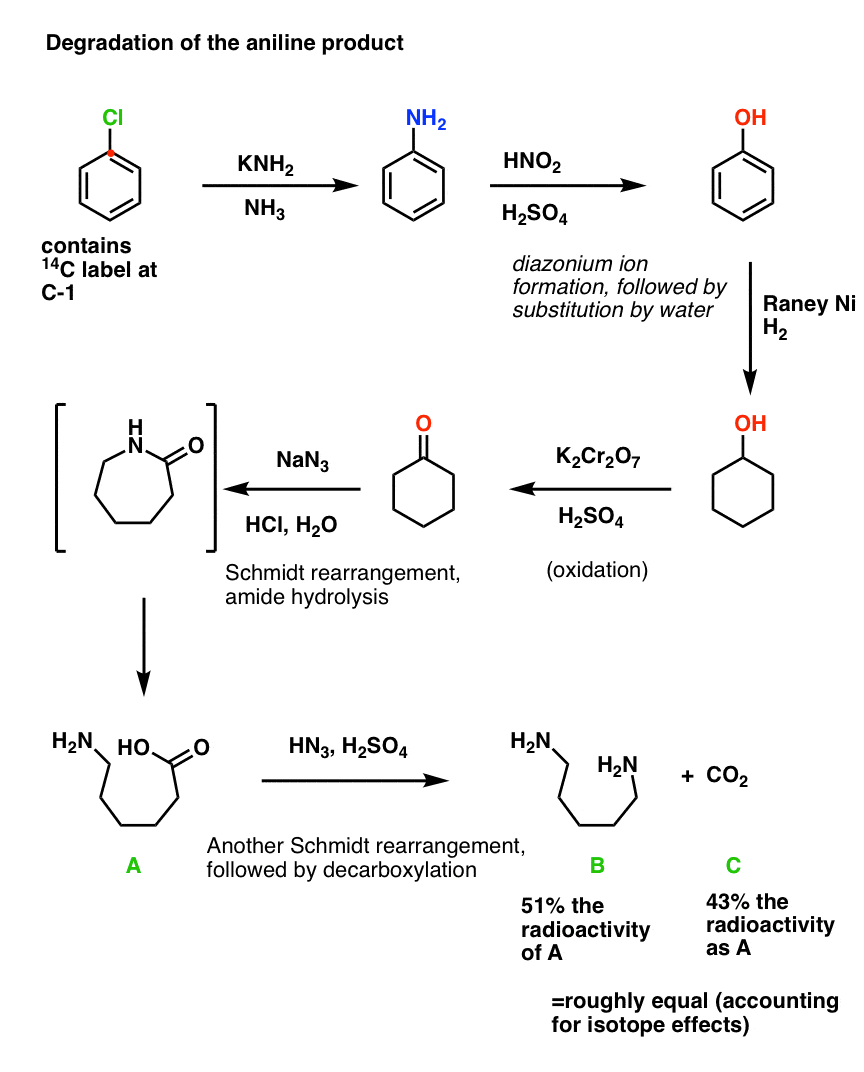
的人比其他人更开发和推广使用核磁共振技术进行结构测定有机化合物,从而让我们从这个痛苦?
约翰·罗伯茨开始这苯炔的研究发表后不久。
测试你自己!
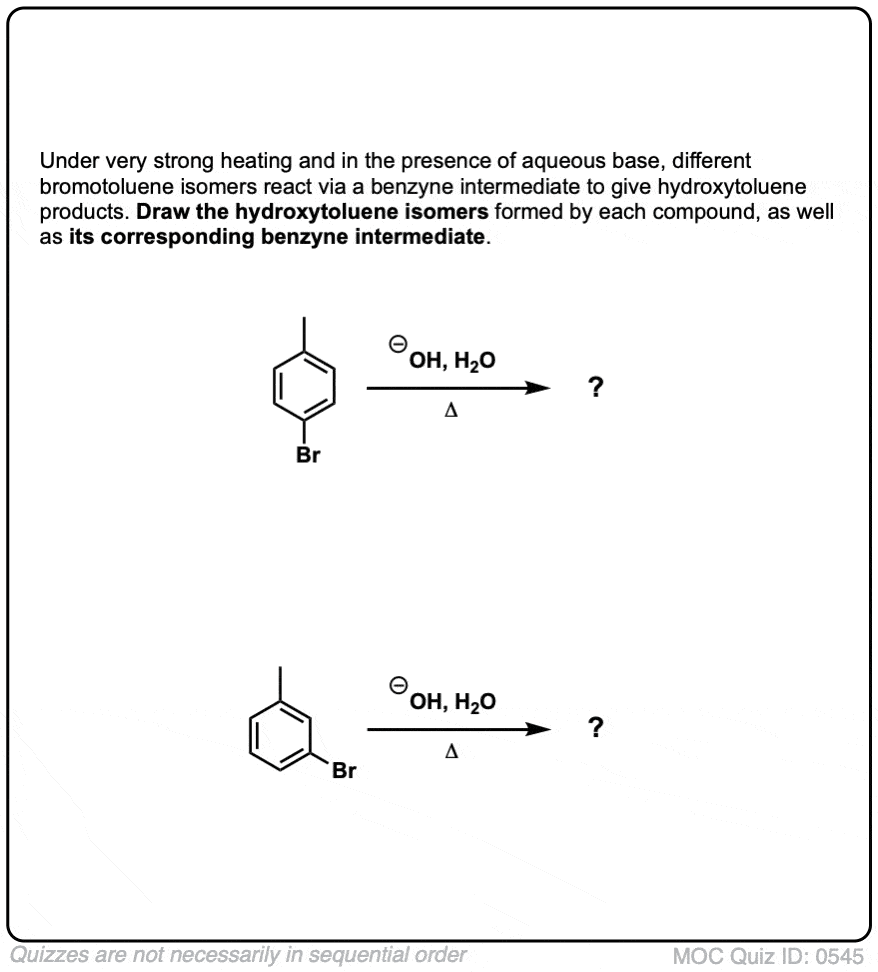 点击翻转
点击翻转
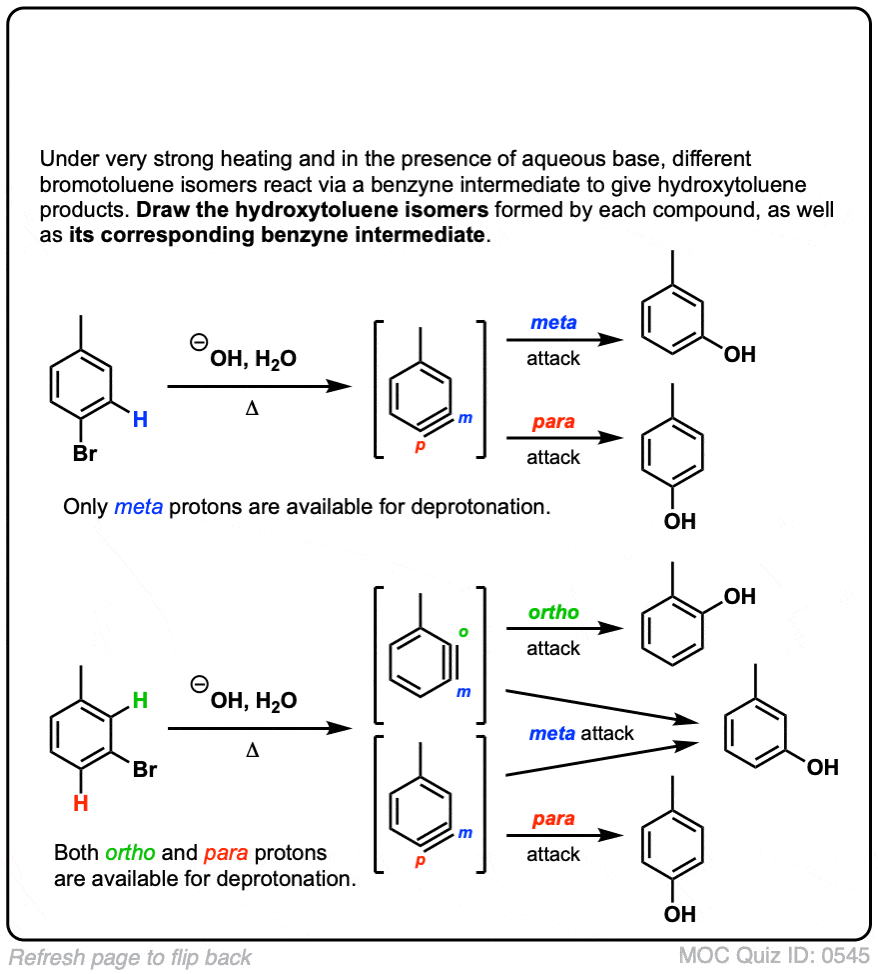
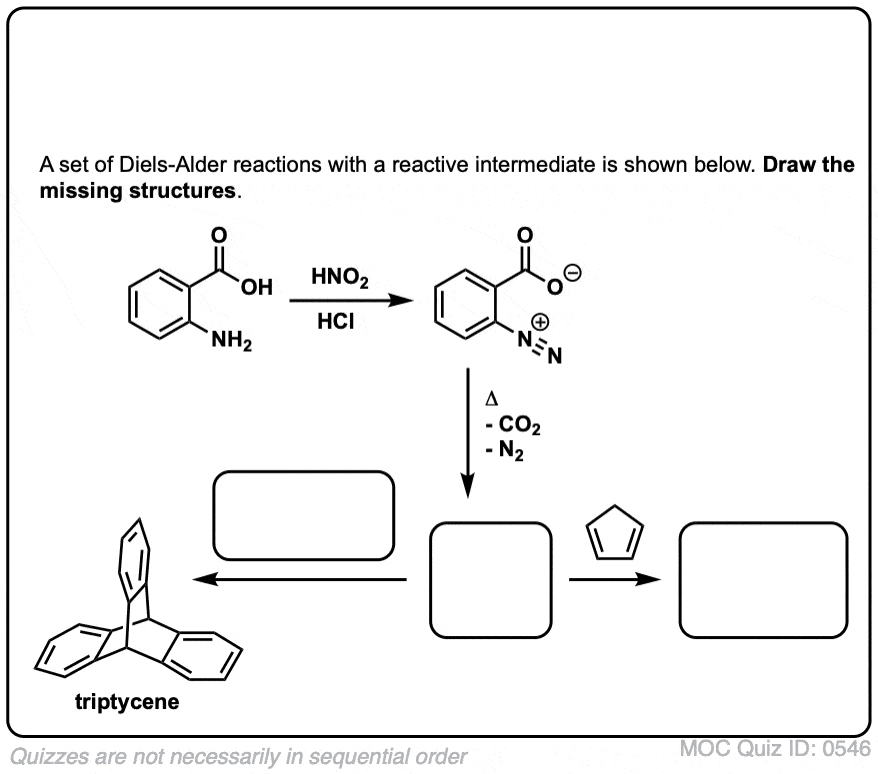 点击翻转
点击翻转
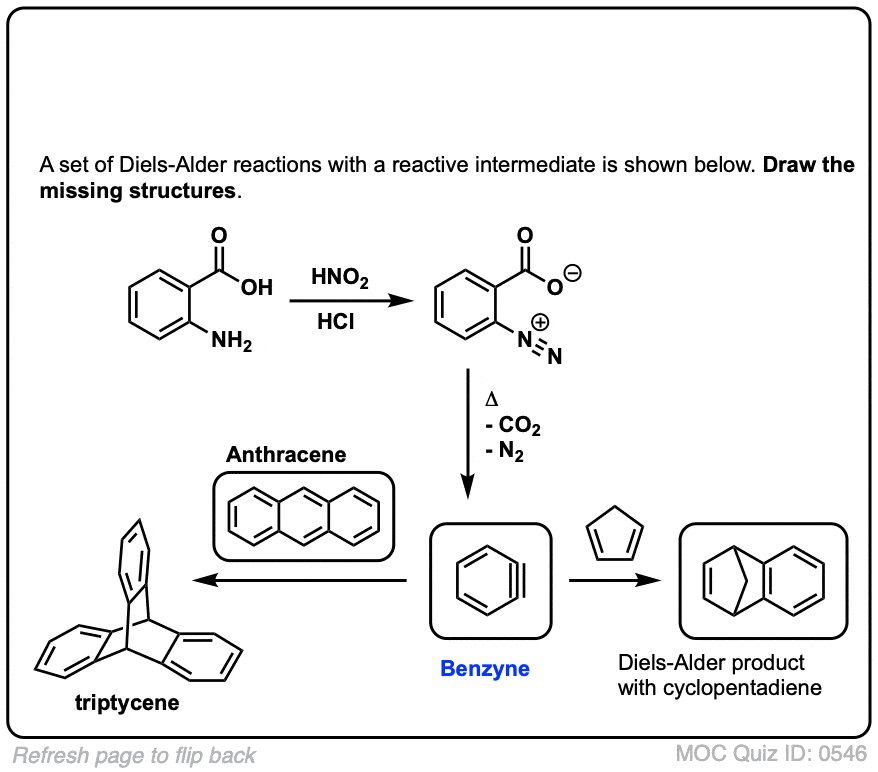
(高级)引用和进一步阅读
在前两篇文章中,诺贝尔奖得主Georg维蒂希反应的描述o-fluorophenyllithium并提出了他们的经历两性离子中间纸2中(尽管他也使用三重键结构o -苯炔)。
- 超级陶冶冯二苯来自Fluorbenzol和死亡苯基锂(IV。Mitteil。超级Austauschreaktionen麻省理工学院苯基量锂)
Georg维蒂希,古斯塔夫皮珀尔,格哈德•福尔曼
的误码率。1940年,73年(11),1193 - 1197
DOI:10.1002 / cber.19400731113 - 苯基锂,der Schlussel祖茂堂静脉neuen化学metallorganischer Verbindungen
Georg维蒂希
自然科学期刊1942年11月,卷30日46-47问题,页696 - 703
DOI:1007 / BF01489519这些文件是经典教授j·d·罗伯茨,他使用14C-labeled氯苯和KNH2证明由于匆忙的苯炔的独到14C标签后的反应。 - 重排反应的CHLOROBENZENE-1-C14钾酰胺
约翰·d·罗伯茨,霍华德·e·西蒙斯Jr .)洛杉矶Carlsmith和c·惠顿沃恩
美国化学学会杂志》上1953年75年(13),3290 - 3291
DOI:1021 / ja01109a523 - Halobenzenes的氨基化机制
约翰·d·罗伯茨,多萝西a . Semenow霍华德·e·西蒙斯Jr .)和洛杉矶Carlsmith
美国化学学会杂志》上1956年78年(3),601 - 611
DOI:1021 / ja01584a024 - TRIPTYCENE
Georg维蒂希
Org。Syn。1959年,39岁,75年
DOI:10.15227 / orgsyn.039.0075
这个过程在有机合成,独立的来源可靠,测试实验合成有机化学过程,也是从Georg维蒂希和准备苯炔是一个经典的方法。 - FLUORIDE-INDUCED 1, 2-ELIMINATION O-TRIMETHYLSILYLPHENYL TRIFLATE在温和条件下苯炔
Yoshio Himeshima Sonoda高明,小林宽司
列托人。1983年,1211 - 1214
DOI:10.1246 / cl.1983.1211
在有机化学中,这是一个非常有影响力的论文,因为这化学使苯炔的一代极温和的条件(室温或以下)。 - 芳炔的直接ACYL-ALKYLATION[制备甲基2 -乙酸(2-ACETYLPHENYL)]
David c . it Uttam k . Tambar和布莱恩·m·Stoltz
Org。Syn。2009年,86年,161年
DOI:10.15227 / orgsyn.086.0161
现代涉及苯炔的合成过程的一个例子,使用化学由小林(ref。6)。教授Brian Stoltz(加州理工学院)发展和继续发展许多有趣的使用苯炔的合成方法。 - Indolyne实验和计算研究:合成亲核添加应用程序和选择性的起源
G-Yoon j . Im莎拉·m·布朗,亚当·e·Goetz,罗伯特·s·佩顿,保罗H.-Y。畅,k·n·胡克和尼尔·k·加戈
美国化学学会杂志》上2010年132年(50),17933 - 17944
DOI:10.1021 / ja1086485
教授尼尔·加戈(UCLA)与Stoltz教授和博士学位将苯炔的概念扩展到其他杂环化合物,如吲哚、特别是发展中基于“indolyne”化学。 - 一个世纪的芳炔化学
汉斯·亨宁温克博士,迈克尔·温克勒该化学。博士,Wolfram桑德教授。
化学。Int。。2003年,42(5),502 - 528
DOI:10.1002 / anie.200390151
好的综述芳炔化学。
所以wellexplained和帮助!你的明确和清晰的语言真的帮助我很多在理解许多重要的话题。每当我寻找怀疑间隙对有机化学,我发现你的帖子,我知道他们会很好地照顾。吨的谢谢,来自印度。
谢谢你!
谢谢这么多。在这个网站所有的内容是非常丰富的
谢谢sir.It帮助我理解这个概念是非常重要的对印度竞争考试。
优秀的. .的way you divided & explained the concept
做好教学☺☺
信息发布. .只是一个小问题…我们如何决定如果在正常加成消除反应收益机制或苯炔机制. .任何参数如温度/试剂等?
寻找存在的强碱(NaNH2)芳炔的形成。
神奇的内容!谢谢你!
我有一些困惑;在抽认卡提出的问题(“测验自己!”)第二种情况处理一个取代基元位置。解决了两个可能的苯炔中间体;m p之间的三键和一个o, p。我们如何决定/预计将主要的哪一个?
由于一吨.Amazing一如既往。最好的几页苯炔。先生向你致敬
好文章! !但我有一个疑问…
为什么不共振发生在苯炔吗?因为它失去了芳香性吗?
是为什么我们不考虑共振效应的取代基而决定产品?
“三键”在苯炔轨道在90°的芳香π体系。他们无法与芳环的轨道组成。
来自印度的爱. .
在我们的文化中教师是神给我们. .
你肯定是一个!
我不明白为什么所有的教科书(Clayden、Yurkanis Vollhardt)表明,NH2 - NH3的亲核试剂,从不!这么多有意义的NH3和你解释。甚至我的教授教——它与氨基。现在我不知道我将把它写在我的测试中。你有什么书谈论这个吗?
感谢这样一个伟大的网站的方式!来自德国的问候
只是可以肯定的是,第二个速率决定步骤,与亲核试剂的进攻芳炔中间体,对吧?我找不到一个提到的职位。
不,速率决定步骤形成的芳炔(去质子化)。这次袭击是快。
优秀的我总是使用这些有用的帖子,把它推荐给我的朋友,所有的文章都不错,非常感谢
优秀的文章,如预期。一个小事情,但:
“苯炔经过一昼夜的桤木的反应
二烯烃在Diels-Alder反应。三键的苯炔充当亲二烯体:“
它看起来像第一第一词缺失的一部分。
开枪。谢谢你!固定的。
好的文章,詹姆斯!
我只是想指出什么可能是一个复制/粘贴错误在你的讨论取代芳炔的区域选择性。案例# 2(当三键之间的邻位的和元碳),你画两种产品具有相同的结构,以及随之而来的ChemDraw中的文本是不正确的。
同样,你可能感兴趣的这个漂亮的文章杰克·罗伯茨:https://onlinelibrary.wiley.com/doi/abs/10.1002/anie.201612152
哦亲爱的。谢谢你指出,哈罗德!固定的。
嘿!错误仍然存在,你知道。
不过谢谢你的帖子!他们被一个巨大的帮助!
固定(最后)。谢谢你唠叨我!