胺
烷基化的胺(糟透了!)
最后更新:2022年11月1日|
- 做一个取代基更多胺从less-substituted胺通过与一个治疗烷基卤化物经常失败,因为该产品胺是更多的亲核比开始的胺。
- 在某些情况下,这是理想的,如的形成烷基铵盐过量的烷基卤化物(例如CH3我)
- 在其他情况下,最好的方法做出更多的替代胺从更少的代替胺通常是还原胺化作用。
表的内容
- “威廉逊醚合成,但胺”:为什么这个反应吸?
- 胺烷基化的失控的列车,步骤1:SN2
- 步骤2:烷基化是紧随其后的是酸碱反应…
- …解放胺,是一种更好的亲核试剂:第三步:第二个SN2
- 步骤4:另一个酸碱反应使一个更好的亲核试剂
- 失控的火车仍在继续
- 反应往往停留在叔胺。通常。
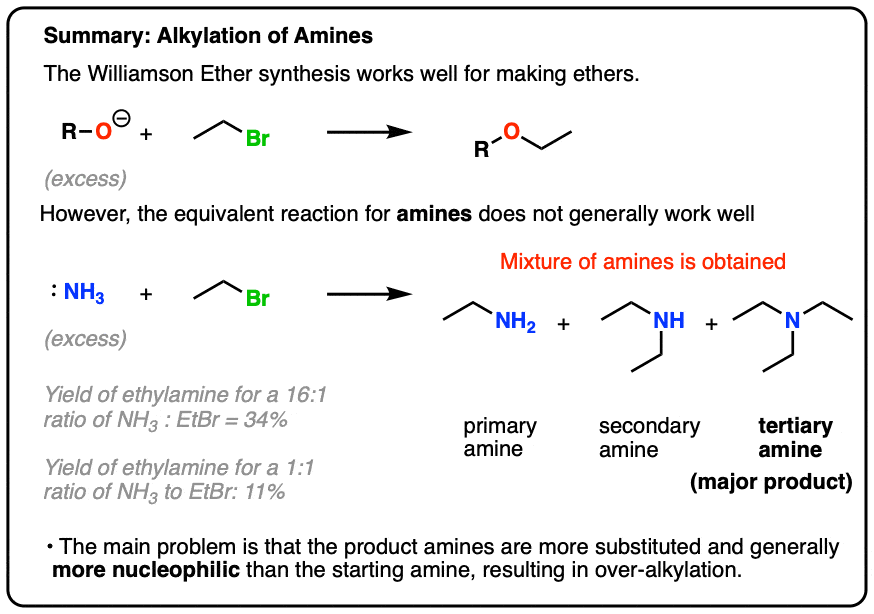
- 摘要:烷基化的胺通常很糟糕。这里有一些解决方法
- 笔记,加上“彻底甲基化”
- (高级)引用和进一步阅读
1。为什么这个反应吸?
趋势的碱度胺提供一个典型的例子为什么化学是有趣的;解密的微妙的权衡各种综合因素在特定的情况下使化学家。奇迹开始明显。
- - - - - -好奇的波函数(灰Jogalekar)
今天,我们来谈谈如何使胺。它不是像你想象的那样简单。
看看你能不能填入空白在以下测试问题:
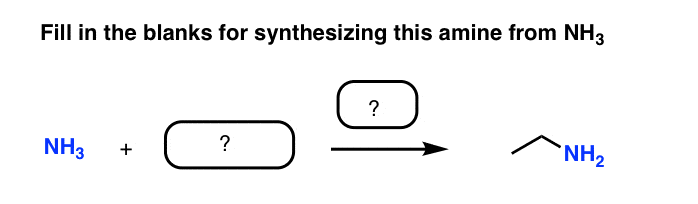
让我们走过的思维过程。我们需要形成一个碳氮键。NH的N3有一个孤对一个好吗亲核试剂。所以,很像威廉姆森醚合成,也许我们可以使用一个烷基卤化物等溴乙烷(CH3CH2Br)和繁荣!完成。
它不完全这样。科学家调查了这个彻底的话说:
“乙基溴化和氨的交互…主要三乙胺的形成相辅相成”。
(裁判:沃纳,j .化学。Soc。1918年,p . 899]
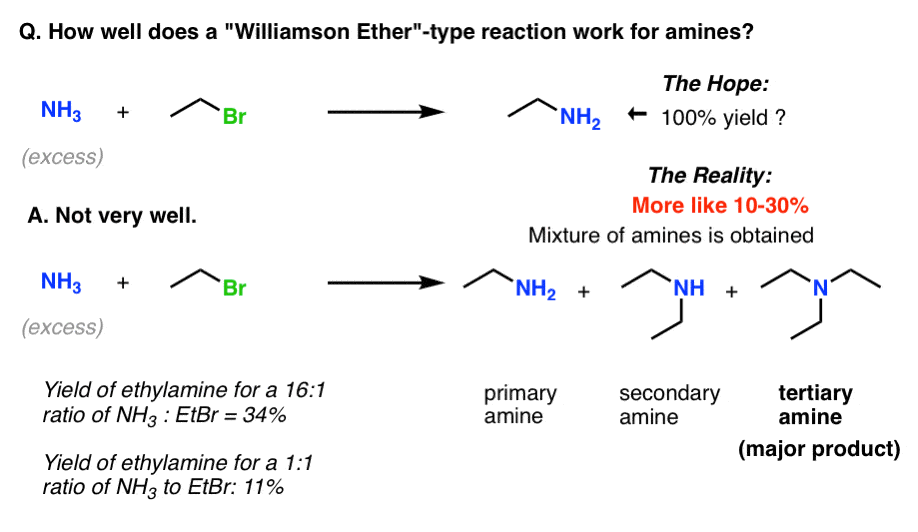
形成的主胺通过烷基化的氨是一个相当低的反应。(的原因经济we通常要使用反应形成一个主导产品的高收益,避免繁琐的分离:这并不符合)。
这是乐趣的一部分学习有机化学的*。就在你认为你可能会发现,一个弧线球。
为什么这个反应。因为没有更好的词,吸?
2。胺烷基化的失控的列车,步骤1:SN2
让我们看看第一反应会发生氨的时刻,一个解决方案是结合溴化乙:亲核取代(通过N2机制)
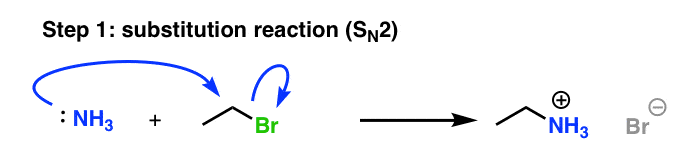
3所示。步骤2:烷基化是紧随其后的是一种酸碱反应
目前为止一切都很顺利。我们形成了碳氮键。因为过量的氨的反应是,酸碱中和反应可以导致的至少一些铵盐,产生我们中性的主胺。
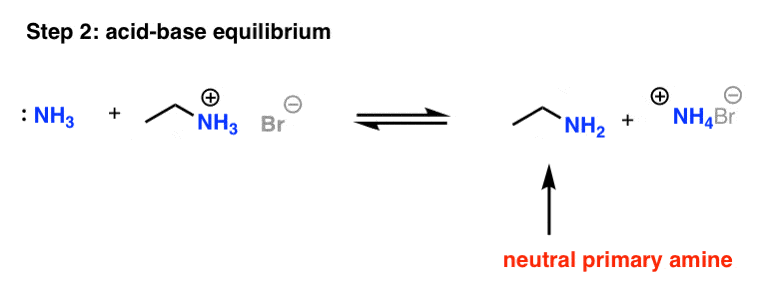
现在我们有主胺。我们做完了,对吧?
没有那么快。看,相对于置换反应,酸碱反应快这事件将发生之前第一个去质子化取代反应剩余的溴乙烷焚烧殆尽了。
这意味着乙胺将出现在同一瓶与乙基溴化。
所以呢?
4所示。步骤3:酸碱反应释放胺亲核试剂,甚至比开始的胺
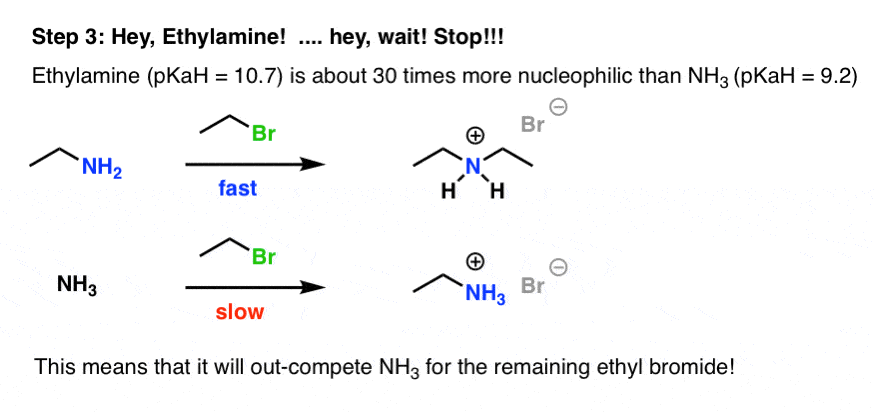
嗯,乙胺本身就是一个好亲核试剂。事实上,它是一个更好的亲核试剂比氨本身,因为电子基烷基集团[链接:5个因素影响胺的碱度]
更好的多少?如果我们使用pK一个H作为一个代理亲核性(合理的,因为位阻不是一个因素在这里)pK一个H为NH乙胺的10.7和9.23。这是大约101。5=亲核的30倍。
乙胺由第一N2将开始吞噬溴乙烷代替NH…3!
我们已经创建了一个怪物!
即使我们尝试堆栈甲板NH(比方说)一个15倍过量3,乙胺的反应仍会更快(30/15)= 2倍。(沃纳所做的,上面;EtNH的产量2在这些条件下,34%和11%的1枚NH吗3。]
5。步骤4:另一个酸碱反应使一个更好的亲核试剂
现在我们有diethylammonium产品过剩的存在基础,这将导致至少有一些二乙胺的形成。
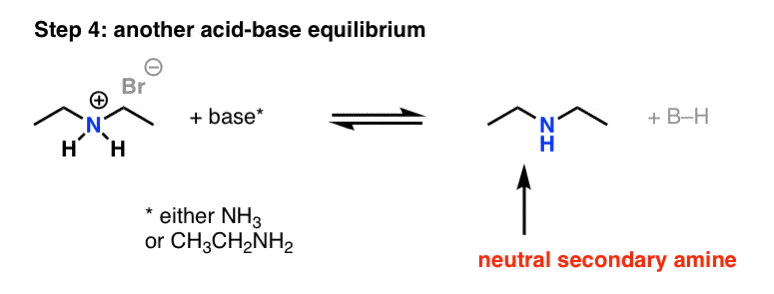
你知道这意味着什么吗?另一个亲核试剂已经生产,与NH竞争吗3剩下的溴乙烷。
如何亲核性与氨和乙胺吗?
的pK一个H(二乙胺约为11.0,比乙胺稍微亲核!
6。失控的火车仍在继续
二乙胺,成为一个更强亲核试剂比氨和乙胺反应更快剩下的溴乙烷比那两种物种。这将形成triethylammonium溴化,然后可以deprotonated(使用的任何一个胺基地解决方案),形成中性三乙胺。
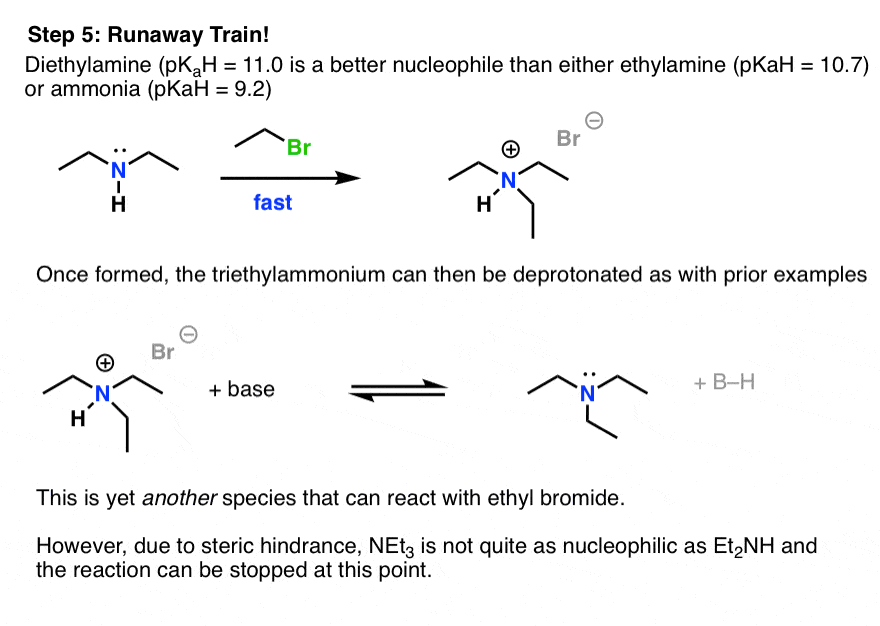
现在我们有三个亲核胺物种都在解决方案同时,游泳之前我们所有的溴化乙被消耗。
这汤包含多个胺产品的反应我的朋友杰夫将在他的实验室笔记本上描述为一个“BFM”。(“B”是“大”,“M”是“混乱”…。)
7所示。反应往往停留在三级胺…
“失控的火车”通常在第三站胺阶段。在这个特定的例子中,pK一个H(三乙胺为10.75,略低于二乙胺。(回想一下,pK一个H指碱度,不是亲核性:净的碱度3是由于降低溶解度的减毒吗共轭酸在水里。(更多的在这里]。]
的亲核性三乙胺的小于二乙酯胺很大程度上是因为三乙胺氮三级,这将增加空间位阻和减缓反应速度。
出于这个原因,形成三级胺从二次胺通过烷基化是因此,在大多数情况下,免除我们的广泛的”胺烷基化是垃圾”声明。
8。摘要:烷基化的胺通常很糟糕。这里有一些解决方法
否则,必须使用工作区。有很多。叠氮化良好的亲核试剂例如,他们可以没有事故和减少烷基化胺之后。的加布里埃尔Synthesi年代是另一个解决方案。
我们的技能鉴定问题的文章吗?
这里有一个反应,大多数有机化学家认为是最好的方法胺:反应叫还原胺化作用。
这里有一个小的预演。
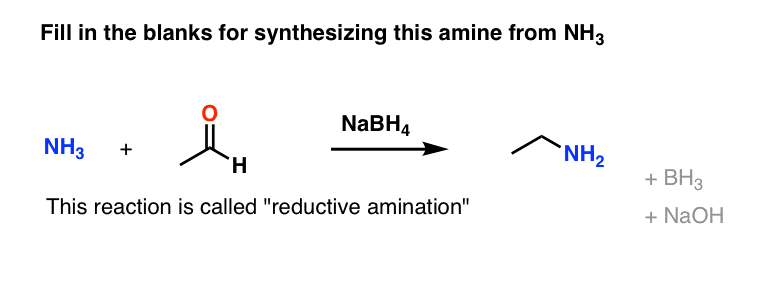
我们将讨论在接下来的帖子,这个反应是如何工作的还原胺化反应。
笔记
注1。烷基化的氨气主要停在第三胺阶段。
虽然高等胺往往比二级亲核性较弱胺,他们仍然的亲核试剂,当处理过度烷基卤化物强制条件下可以被转换成第四纪铵盐。
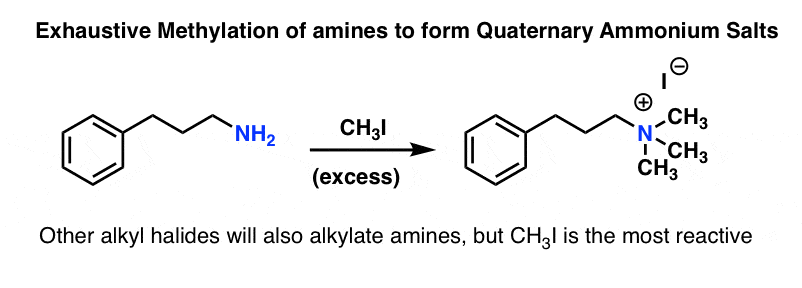
最好的例子是与碘甲烷的反应详尽的甲基化。回想一下,甲基卤化物反应最快烷基卤化物的年代N2反应由于其较低的位阻。
治疗胺拥有大量过剩甲基碘会导致他们的第四纪铵盐。我们将在以后的帖子中看到,这些第四纪铵盐能像优秀的离开组织消除反应(很少,取代反应)烯烃,特别是在霍夫曼消除。
(高级)引用和进一步阅读
- ——乙胺和二乙胺的准备
埃米尔阿方斯沃纳
j .化学。Soc。反式。1918年,113年,899 - 902
DOI:10.1039 / CT9181300899
早期报道的合成烷基胺的烷基化与乙基溴化氨,和第二段开头”这是一个错误的过程,因为它在很大程度上减少的形成相辅相成有用的三乙胺,收益率随之损失的主要和次要的基地”。 - 在直接N-Alkylation Chemoselectivity铯效应:高胺
拉尔夫·尼古拉斯·塞尔瓦托Advait美国纳格尔,Kyung Woon荣格
《有机化学》杂志上2002年,67年(3),674 - 683
DOI:1021 / jo010643c
的选择性monoalkylation胺是可能的,只要你知道如何去做。 - 效率和选择性的N-alkylation胺与醇类催化了锰螯复合物
让-巴蒂斯特·Sortais Saravanakumar Elangovan雅各布·诺伊曼,凯瑟琳Junge,克利斯朵夫Darcel & Matthias贝尔
自然通讯2016年,7:12641
DOI:10.1038 / ncomms12641 - 选择性合成二、三级胺通过还原N烷基化等腈N烷基化等胺和铵甲酸由钌催化的复杂
Iryna d . Alshakova Georgii。尼克诺夫博士
ChemCatChem2019年,11(21),5370 - 5378
DOI:10.1002 / cctc.201900561
这两篇论文在本质上是相同的反应。这些反应的机理表明,它基本上是一个“锅”还原胺化作用。的酒精原位氧化和过度的酒精作为还原剂。 - 水的N-alkylation胺使用烷基卤化物:直接代叔胺在微波辐照下
宇鸿Jua Rajender Varma。
绿色化学,2004年,6,219 - 221
DOI:10.1039 / B401620C
本文表明,烷基化的次要的胺收益率三级胺,很明显。但更重要的是,第四纪铵盐只有形成困难;本文不报告任何第四纪铵盐形成即使延长微波加热的次要的胺过剩的烷基卤化物。
我这边Dr.James问候。我读过很多关于不同话题的文章,你的有机化学,我真的很感激你让学生了解有机化学像微风。
我也把你的博客我的学生当他们坚持一些非常困难的话题复杂机制的反应和其他话题。
谢谢
非常感谢,这是只有通过这篇文章我明白了上述反应。
这(网站)(https://www.chemguide.co.uk/organicprops/haloalkanes/nh3.html说伯胺的主要产品多余的氨气。是错误的吗?
维尔纳,j .化学。比率Soc。1918年,p . 899尝试16:1 NH3比乙胺和胺的有34%的收益率。如果你使用50:1或100:1比氨烷基卤化物,那么它将有更高的收益率。但这是开始一个相当不切实际的过程。
亲爱的Ashenhurst博士,
我想知道是否你添加的链接为什么叔胺基本低于二级胺描绘了一幅完整的形成季铵盐。而人能正确地主张,三乙胺是基本略低于二乙胺在水介质,执行的SN2反应可以使用极性溶剂,没有水,对吗?所以不能的相对极性性质pentacoordinate过渡态和随后的盐的离子性质稳定足够的极性溶剂,不是水?我问这个,因为我学会了在我的第二年的本科生n-Pr3N +梅的反应速率(SN2)可以通过增加使用的溶剂极性增加由于极性的增加TS的原因而反应物。
亲切的问候,
Vignesh