烯烃的反应
第四种烯烃加成模式-自由基加成
最后更新:2022年11月28日|
HBr的自由基加成烯烃与ROOR(过氧化物)
我们已经看到有三个主要的烯烃反应模式[碳正离子,三元环,协调一致的],但也有两个次要的途径。这篇文章讨论了其中之一:自由基添加HBr烯烃,显示相反的区域选择性(anti-Markovnikov)而不是“正常”添加的HBr烯烃(马氏),它遵循“碳正离子”途径。
目录
- HBr自由基加在烯烃上可生成“抗马氏尼科夫”产物
- 过氧化物存在下HBr与烯烃加成的自由基机制概述
- 通过热或光对过氧化物的均裂引发自由基过程
- 醇氧自由基和HBr形成溴自由基的研究
- 繁殖步骤#1:将溴自由基添加到烯烃中,从而产生最稳定的碳自由基
- 繁殖步骤#2:生成的碳自由基从H-Br中去除一个氢原子,重新生成溴自由基
- 终止步骤
- 摘要:羟基溴自由基加成烯烃的研究
- 笔记
- (高级)参考资料和进一步阅读
1.HBr自由基加在烯烃上可生成“抗马氏尼科夫”产物
如前所述,烯烃通常与HBr反应生成马氏“除了;溴在取代度最高的碳上烯烃,而氢最终在取代最少的碳上。然而,当同样的反应在过氧化物和热/光的存在下进行时,有趣的事情发生了:添加的模式改变了!
而不是Br在大多数取代碳烯烃,它最终是最小的。[然而,反应的立体化学没有改变:它仍然会产生“syn”和“anti”产物的混合物。]
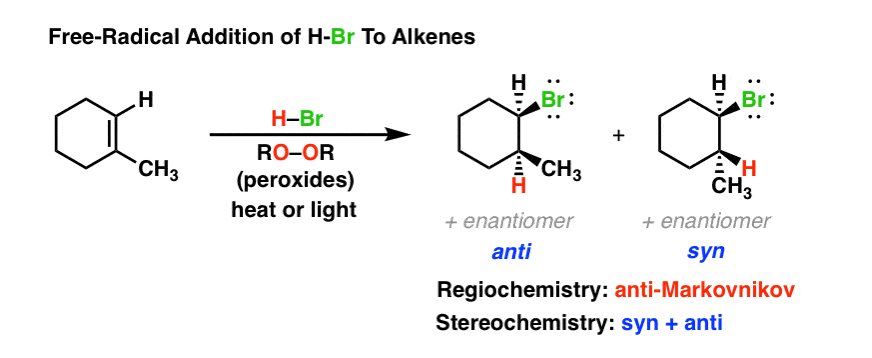
这个所谓的“anti-Markovnikov加法很有趣。过氧化物的存在以及热(或光)会对这个反应产生什么影响?
2.过氧化物存在下烯烃加成HBr的自由基机制概述
这个反应通过a发生自由基的过程.(对于自由基化学的入门知识,你可能想看看这篇介绍性文章自由基反应).以下是该机制的概述:
- 过氧化物含有弱氧-氧键[约35千卡/摩尔;相对于C-H约100千卡/摩尔]
- 加热导致均裂键的断裂,也就是说,键的断裂使得每个原子上只留下一个未配对的电子。强光源[例如泛光灯或其他接近紫外线的光辐射源]也可以切断这种结合。
- 生成的高活性烷氧基可以从H-Br中抽象出一个氢,从而得到溴激进。溴自由基是加入到烯烃.
- 除了烯烃将会以这样一种方式发生,即最稳定的自由基形成了[在上面的例子中是叔自由基]。这就是为什么溴会在取代最少的碳上烯烃.(见:稳定自由基的3个因素)
- 然后这个叔自由基从H-Br中去除氢,释放出一个溴自由基,循环继续。
3.通过热或光对ROOR(过氧化物)的均裂引起自由基过程
只需要微量的过氧化氢(催化)量就可以使反应开始,当然,至少需要一摩尔当量的HBr才能使HBr完全加入烯烃.
在第一步中,能量的加入(以热或光的形式)导致弱O-O键的均溶断裂,产生两个新的自由基。“均溶”指的是键被破坏,以至于每个原子都能得到相同的("细数=希腊语“相同”)电子数。
(我们在有机化学中看到的大多数键断裂都是杂溶的,即键断裂不均匀。)
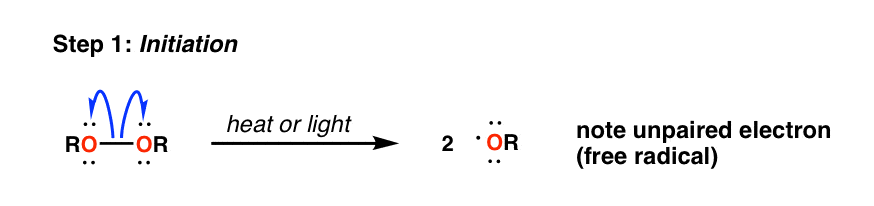
的单刺箭头描述单个电子的运动;生成了两个烷氧基。由于自由基的数量有净增加(0→2)这是一个初始化的一步。
用于此目的的常见“过氧化物”是过氧化t丁基或过氧化苯甲酰。[注1].或者其他自由基“引发剂”,如AIBN也可以用。
仅使用催化量的过氧化物来启动该反应(通常为10-20摩尔%,尽管可以使用更多,特别是分批添加时)。
4.醇氧自由基和HBr形成溴自由基的研究
在下一步中,步骤1中的一个氧自由基在另一个均溶过程中从H-Br中除去一个氢。
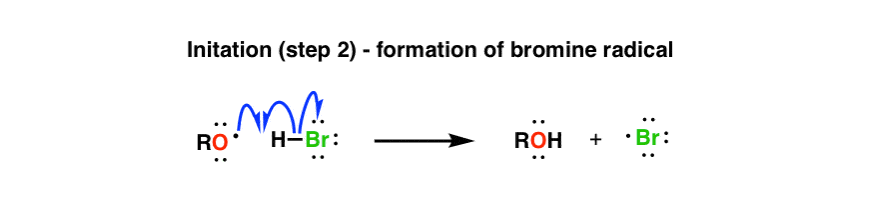
这里,我们正在形成一个氢氧键(CH中氢氧键的离解能为102千卡/摩尔3.OH)和H-Br键的断裂(键解离能为87千卡/摩尔),因此大约15千卡/摩尔的能量差使这个过程基本上不可逆。
(注:由于这一过程不改变自由基的数量,它在技术上是一个传播步骤)
5.繁殖步骤#1:将溴自由基添加到烯烃中,从而产生最稳定的碳自由基
一旦形成,溴自由基就可以加入烯烃.
在一个相对“平坦”的地方烯烃如1-甲基环己烯,自由基的加成将以相同的概率从两边发生。
问题是,哪一个双键上的原子自由基会攻击吗?毕竟,这种纽带可能以两种不同的方式断裂。
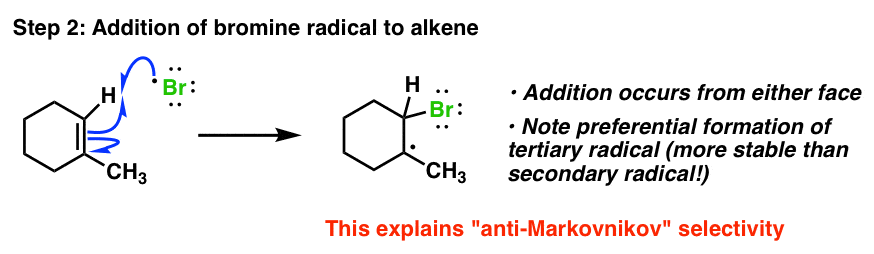
- 溴自由基对取代较多的碳的攻击会导致在a上产生一个新的自由基二次碳。
- 溴自由基对取代量较少的碳的攻击会导致a上产生一个新的自由基三级碳。
自由基是缺乏电子的物质,由邻近的电子供体稳定。更稳定的自由基中间体是三级自由基,这就是为什么加成主要发生在取代量较少的碳上(即连接在最少碳上的碳)。
这就解释了anti-Markovnikov反应的选择性。
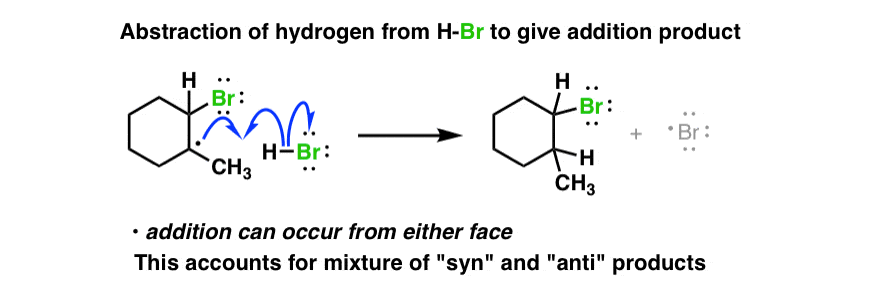
6.繁殖步骤#2:生成的碳自由基从H-Br中去除一个氢原子,重新生成溴自由基
等一下传播步骤在主序列中,生成的碳自由基从另一等价物H-Br中除去一个氢,形成最终的加成产物。
烷基自由基是2-杂交,并且是容易反转的浅金字塔。
因此,H-Br可以在自由基的任何一面反应[注2].如果它攻击与Br相同的面,那么我们得到一个"syn”产品。如果它攻击Br的反面,那么产物就是“反”。
两者的混合物将得到。该反应没有立体选择性。
通过这个过程生成一个溴自由基,然后它可以添加到另一个等价的烯烃(传播步骤# 1)。
7.终止步骤
当HBr的浓度和烯烃相对于自由基的浓度变得较低,则会发生终止(看到帖子:起始,传播,终止).这可以通过各种特定的途径(未显示)发生,包括两个自由基的重组,以产生一个新的键。
8.摘要:羟基溴自由基加成烯烃的研究
这种反应途径最常被观察到(在Org 1和Org 2中),用于HBr的加成,尽管有丰富的化学自由基加成反应烯烃存在(特别是对于有机锡烷)。
在下一篇文章:烯烃的臭氧分解
笔记
注1.过氧化苯甲酰是一种常见的家庭使用的痤疮清洁剂,甚至使外观Oxy护肤品的经典广告(Oxycute’Em).)
注2.自由基碳的几何结构是一个浅金字塔,具有较低的反转势垒,允许在任何一面进行反应。例外情况是在非常不受欢迎的奇怪情况下,例如在桥头堡(看到双环分子及其命名方法).
(高级)参考资料和进一步阅读
Lowry & Richardson的化学键解离能有机化学的机理与理论“,, Harper & Row, 1987年,第161-162页
- 不饱和化合物加试剂和重排反应中的过氧化物效应。
Frank R. Mayo和Cheves Walling
化学评论1940年,27 (2), 351-412
DOI:10.1021 / cr60087a003
f·r·梅奥是著名化学家m·s·卡拉施的学生,他们在1960年首次描述了“过氧化物效应”anti-MarkovnikovHBr的加入烯烃,将其归因于自由基机制。 - 向4,4-二甲基戊烯-1中加入溴化氢
卡拉施先生,切斯特·汉纳姆先生,格莱斯顿先生
美国化学学会杂志1934年,56(1), 244 - 244
DOI:10.1021 / ja01316a504
本通讯除标题外,还描述了从HBr中获得的两种产品烯烃通过亲电和自由基机制。 - 溴化氢与烯烃键的光加成反应
威廉·e·沃恩,弗雷德里克·f·鲁斯特和西奥多·w·埃文斯
有机化学杂志1942年,07(6), 477 - 490
DOI:10.1021 / jo01200a005
正如本文所述,HBr的自由基加成不仅可以由过氧化物引发,还可以由光引发。 - 不饱和物质中加入试剂的过氧化物效应。第二十二。三甲基乙烯、苯乙烯、巴豆酸和巴豆酸乙酯中溴化氢的添加
Cheves Walling, M. S. Kharasch和F. R. Mayo
美国化学学会杂志1939年,61(10) 2693 - 2696
DOI:10.1021 / ja01265a034
Kharasch和他的同事报告了苯乙烯在稀戊烷溶液中与过氧化二苯甲酰的氢溴化反应,得到了80:20的比例,有利于一次溴化反应。不幸的是,没有提供详细的条件。 - 可伸缩的anti-Markovnikov脂肪族和芳香族的氢溴化烯烃
Marzia Galli, Catherine J. Fletcher, Marc del Pozo和Stephen M. Goldup
Org。Biomol。化学,2016,14, 5622 - 5626
DOI:10.1039 / C6OB00692B
这是一篇有趣的论文,展示了这种化学在现代有机合成中的相关性;它描述了在“无引发剂”条件下合成初级溴化物的简单可扩展条件的重新发现烷基和芳基烯烃.
倒数第二段:“这种反应途径最常被观察到(至少在Org 1和Org 2中)”-未完成的句子。
像往常一样,干得好。
固定的。谢谢你提醒我简短地介绍一下有机锡烷化学。
这方面有视频教程吗?我通过听和做比阅读学得更好:)
目前没有,对不起!
为什么氢自由基不先加入烯烃,而先加入溴自由基
因为它还没有形成!请参阅下面的评论以澄清(或至少试图澄清)它。
为什么叔基更倾向于从HBr上脱去氢而不是溴?
不知道你是什么意思-你是说和溴自由基反应?
任何时刻溴自由基的浓度都远小于HBr的浓度。
如果它与溴自由基反应,那就是终止步骤!
不,事实上他问的是"氢在氢溴中的抽象"的步骤,为什么我们不得到二溴环产物。这个反应在热力学上是不利的(+39千卡对-23千卡)。这在《有机化学基本原理》一书的第387页中有讨论(谷歌,太迷人了!)我希望这能有所帮助。
谢谢你!
在步骤2中,为什么溴自由基没有抽象出烯丙基氢(就像NBS卤化反应一样)?我认为烯丙基自由基几乎和叔基一样稳定。
我认为这是因为C-C π键强度约为60-65千卡/摩尔,而C-H烯丙基键强度约为80-85千卡/摩尔。换句话说就是更高的活化能
会不会是烯丙基氢的提取确实发生了,但所产生的烯丙基自由基除了与氢氧根br反应外没有其他东西可与之反应?烯丙基自由基可以从H-Br中重新抽象出一个氢,从而重整烯烃,最终加入一个溴基。如果发生这种情况,烯烃可能会发生异构,我不知道有没有观察到。只是一个想法……
谢谢你,布鲁斯,我认为这就是正在发生的事情。
你有关于HBr自由基加成的帖子吗当没有过氧化物的时候,换句话说,另一种途径?
自由基途径需要过氧化物。“离子”途径涉及碳正离子,在这里涵盖://m.deriinvest.com/2013/02/22/addition-pattern-1-the-carbocation-pathway/
你能评价一下这个反应产生的立体异构体的稳定性吗?谢谢你!
立体异构体的稳定性?它是一种构型的混合物。很难一概而论。
你如何确定一个自由基反应是由热还是光引起的?
两者都可以。举个例子,看这里(二甲苯的苄基溴化)http://www.orgsyn.org/demo.aspx?prep=CV4P0984
在HBr溶液中加入烯烃之前先加入锌粉会发生什么?
你能举个具体的例子吗?
在本科学习中是否有必要学习键能值....
我想是的。有必要学习扑克牌中手牌的价值吗?
我的课本上说反马氏加成只发生在HBr上,而不是HCl上。你能告诉我为什么吗?
HCL不会形成氯自由基,因为氯具有很强的电负性,它只会形成阳离子。
这是不正确的。
在最后一步,为什么叔基与H-Br中的H反应而不是与H-Br中的Br反应?(产物是1,2-二溴-2-甲基环己烷)
与Br反应会生成氢自由基H•,它比溴自由基稳定得多。碳溴键的形成要比碳氢键弱得多。