炔的反应
炔卤化:炔的溴化、氯化和碘化
最后更新:2022年11月14日|
卤化的炔烃与氯2、溴2,而我2
在这篇文章中,我们将对“三元环路径”做同样的事情。
如果你回想一下关于烯烃的系列文章,烯烃与某些亲电试剂(如卤素等)反应生成带正电的桥式中间体.常见的例子有bromonium离子和“汞鎓离子”。这些中间体然后遭受a的背后攻击亲核试剂,为产品提供反式立体化学。
所以,我们可能也会这样想炔烃如此相似烯烃,也应该以类似的方式作出反应。[当然,学过有机化学的人会告诉你,我们“期望”发生的事情并不总是那样做实际发生!]。
目录
1.炔烃与氯的卤化反应2、溴2,而我2
烯烃与氯等二卤化物发生卤化反应2、溴2,而我2.这些反应通过带正电的桥接中间体进行,如“溴”和“氯”离子。这些中间体然后遭受a的背后攻击亲核试剂,为产品提供反式立体化学。(看到帖子:烯烃的卤化)
令人高兴的是,的反应炔烃如Cl等亲电试剂2、溴2,而我2做给出与观察到的结果非常相似的结果烯烃.例如,an的处理炔烃等于1个Cl2提供二氯烯烃两个氯相对,得到反式-dihalides
如果第二个氯的当量2加入四氯,就会形成四氯衍生物。[注1]
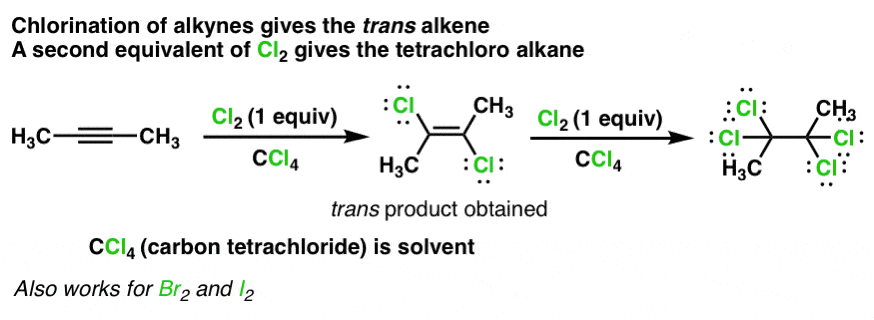
那么这个反应是如何发生的呢?我有个提议。
2.炔的卤化也通过桥离子中间体进行,提供反式产品
就像烯烃的π键炔烃可以作为亲核试剂,攻击氯2生成桥接的中间产物(卤鎓离子)
在下一步,氯离子从背面攻击碳,导致反式产品。
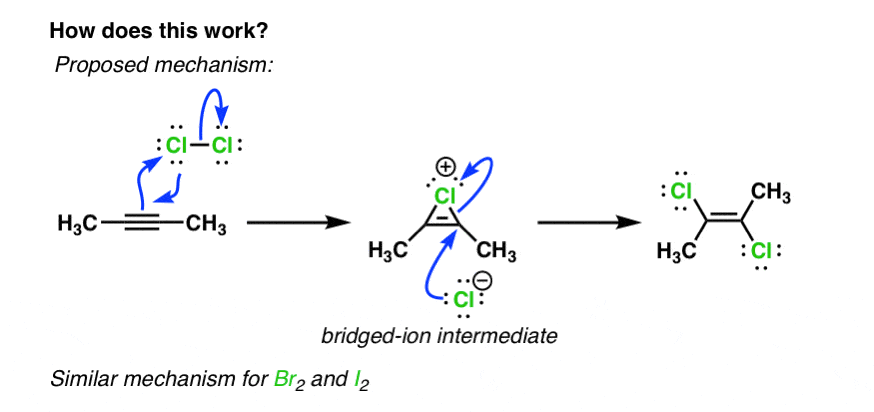
实际上有一个非常这里要指出的是一个有趣的观察,但我将把它留给下面的“注释”部分,因为它对大多数读者来说并不是绝对必要的。下面是预告片:炔烃要慢反应比烯烃是这样的。[注2]。
是的,氧汞化反应炔烃通过三元环途径进行,但正如前面文章中所讨论的(看到帖子:炔的硼氢化和氧汞化反应)处理炔烃与汞(II)和酸性水[和酸]通常生成酮在酮-烯醇的互变异构烯醇中间。(看到帖子:Keto-Enol互变现象)
3.烯烃与炔烃卤化的“三元环”途径比较
在这一点上,有必要总结一下三元环路径之间的关键相似点和不同点炔烃而且烯烃.

在下一篇文章:炔烃-“协同”途径
笔记
注1。分离二氯不是问题烯烃这里,两个吸电子的氯使它更弱亲核试剂而不是开始炔烃.这意味着可以添加不同的亲电试剂到烯烃例如。所以如果你想要氯化,然后溴化,这是一个可行的选择(仍然得到四卤化物产物)
注2.为什么会有这样的反应炔烃要比这个慢烯烃?毕竟,不应该炔烃要比别人更“暴露”烯烃,空间受阻较少?这个三元环中间体是由炔烃卤素有两个特性,使它比相应的三元环中间体更不稳定烯烃.首先,多出来的双键会产生更多环应变;sp2杂化碳(理想角为120°)被约束成三角形(内角为60°)时比杂化碳更不稳定3.杂化碳[理想角度109°]将是。
还有一点,大多数学生直到有机化学第二学期才会发现。中间体形成了三元环antiaromatic的性格。(看到帖子:Antiaromaticity)
也就是说,有4个π电子被约束在一个共轭环中,类似于[从未孤立]环氧乙烯.因此,这种中间体应该具有特别高的能量,并且具有更高的生成激活屏障。
请注意,在机制上存在一些分歧;有人提出,这种反应可以继续进行下去亲核攻击炔烃,至少对于Br的第一个等价物2[根据我的3月5日版。- Sinn, H. et. al.,蒙塔什化学。1965,96, 1036]
注3。那么氯生成卤丙烷呢2和H2哦,就像我们对烯烃?嗯,这个反应也可以,但就像氧汞反应一样,它很复杂:我们得到一个卤化的烯醇中间产物,也要经过酮烯醇互变异构形成羰基.因为互变异构通常是2nd这个学期的主题,大多数教科书认为不值得在这个时候详细讨论这个反应,这个主题通常在章节中缺席炔烃.
对于那些超级好奇的人,这里有一个建议:
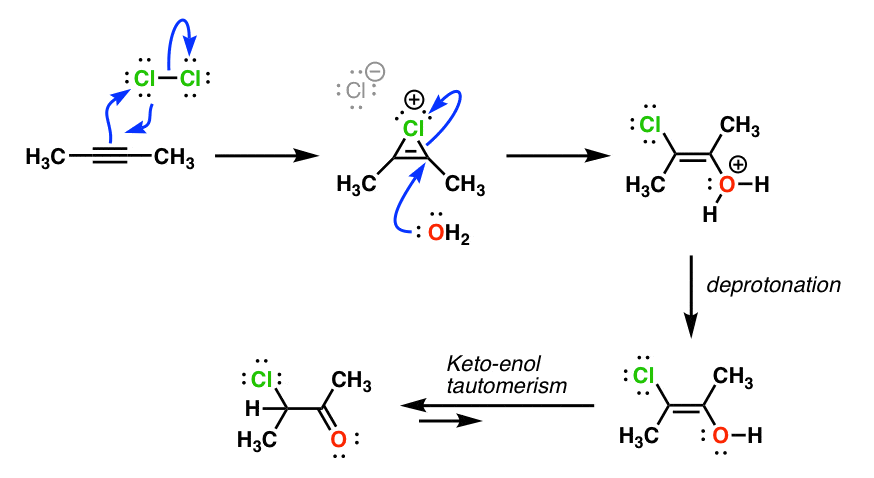
在下一篇文章:炔烃-“协同”途径
(高级)参考资料和进一步阅读
- Untersuchungen über异构体。2
阿瑟·迈克尔
j . Prakt。化学。1892年,46 (1), 209-210
DOI:10.1002 / prac.18920460115
一篇关于溴化的早期论文炔烃.本文提到了二羧基乙炔溴化反应的70%反式同分异构体。 - 溴加法和对称取代基二苯乙烯和托兰衍生物
Sinn, H., Hopperdietzel, S. & Sauermann, D.;
Monatshefte für Chemie1965,96, 1036 - 1055
DOI:1007 / BF00919180
在添加的机制上存在一些分歧炔烃本文为溴的亲核攻击提供了一些依据2. - 亲电加成的立体化学烯烃和乙炔
罗伯特·c·费伊
立体化学专题1968,3., 237 - 342
DOI:1002/9780470147122.ch4
这篇评论比较偏重于烯烃反应,但确实有关于Cl2和Br2加到乙炔的章节。在第291页,作者说:“[…]乙炔的溴加成物[…]在醋酸中,遵循与醋酸相似的动力学烯烃但乙炔的活性比相应的乙炔低100- 5万倍烯烃”。 - 乙炔亲电溴化反应动力学及机理研究
詹姆斯·a·平科克,基思·耶茨
加拿大化学杂志, 1970年,48(21): 3332 - 3348
DOI:1139 / v70 - 561
立体选择反3-己炔的溴化有加成,但两者都有加成独联体而且反式在苯乙炔的腐蚀过程中得到了产物。 - 磺酰卤化物及其衍生物的反应。14.的影响乙炔4-氯苯磺酰氯的添加速率和产物的结构
George H. Schmid, Agnieszka Modro, Fred Lenz, Dennis G. Garratt和Keith Yates
有机化学杂志1976年,41(13), 2331 - 2336
DOI:1021 / jo00875a025
当亲电加成涉及桥离子中间体时,由三键产生的反应比由烯烃.这可能是为什么亲电试剂如Br, I, SR等的亲电添加反应在三键时比在双键时慢。 - 原子分裂的电子传输研究p*角度应变环乙炔的分子轨道:对亲电性的影响炔烃
Lily Ng, Kenneth D. Jordan, Adolf Krebs和Wolfgang Rueger
美国化学学会杂志1982,104(26), 7414 - 7416
DOI:1021 / ja00390a005
的低反应性的另一种可能解释炔烃相对于烯烃和轨道中未填满轨道的可用性有关炔烃.已证明p*轨道是弯曲的炔烃(如环辛)的能量比的p*轨道低烯烃,有人认为线性炔烃能在它们的过渡态中产生弯曲结构亲电试剂.
形成的三元环中间体具有抗芳香性。也就是说,有4个π电子被约束在一个共轭环上,"这是否意味着Cl的两个孤对中的一个是抗芳系的一部分?
是的,完全正确!
错了,卤丙烷rxn和炔
两个晕原子连接在一起
我在什么地方见过,你甚至可以得到一个cis产物,通过什么其他机制你可以得到一个it
谢谢你!