消除反应
消除(E1)反应与重组
最后更新:2022年12月2日|
哪里有碳正离子(见最后发表),重排反应是从不落后。我们的老朋友为一个短期旅行回来在本章消除反应。
表的内容
1。这有什么奇怪的消除反应吗?
最后一个(奇怪的)反应给你们关于消除反应。你能看到有什么奇怪的吗?
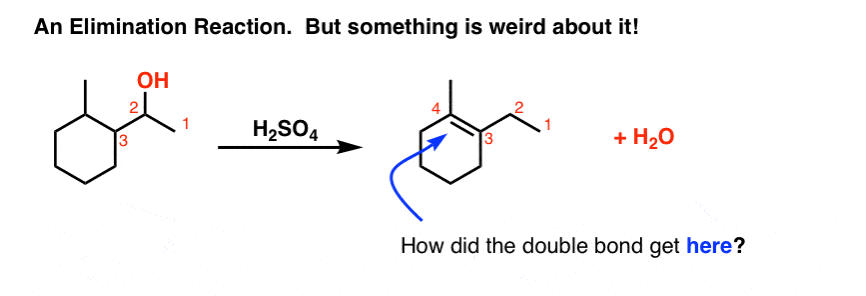
,双键怎么结束了吗在吗?通常当发生消除时,我们把氢从碳毗邻离去基团。但在这里,一些额外的发生。
2。消除(E1)与重排:氢化物转移
让我们看看所有形式的债券和债券打破我们可以追踪完全发生了什么:
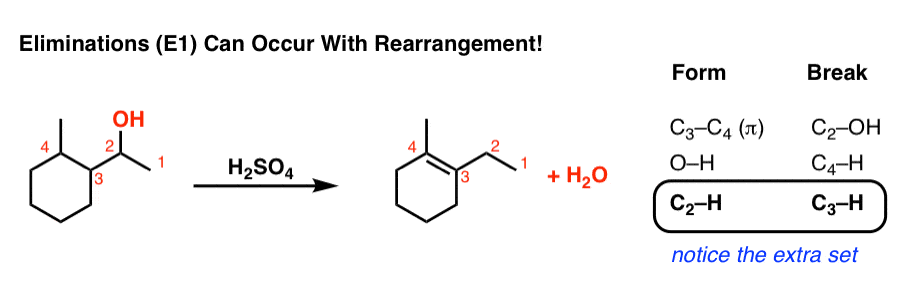
注意它如何不同于一个典型消去反应吗?当然,我们形成碳碳(π),打破碳氢键和c哦,但我们有一个额外的碳氢键,形式和一个额外的碳氢键,休息时间。
这是一个肯定的迹象重排一步!
这里发生了什么?
我们首先使质子化酒精。这允许对水离开在下一步,也就是形成碳正离子。
事情是这样的:碳正离子是二次,我们毗邻三级碳。如果氢(及其对电子)迁移从C3 c - 2在我们的示例中,我们现在有一个叔碳正离子,更稳定的。
之后,一个基地(水在这个例子中)可以去除碳氢键,形成更多的替代烯烃(扎伊采夫的产品在这种情况下)。这是怎样的烯烃最终在那里。
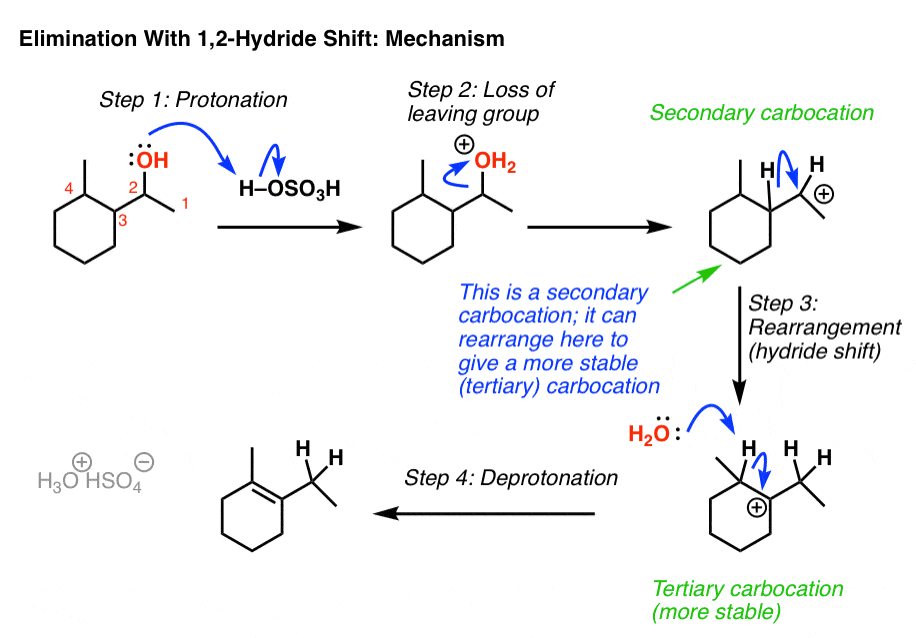
好的。这是一个神秘的解决。
3所示。消除(E1)与重排:烷基转移
你可能会记住这些类型的重组可能发生SN1反应了。如果你读过那篇文章,您可能还记得,除了氢的转移(“氢化”,因为有一对电子我们也可以有烷基转变。这是最后一个例子。
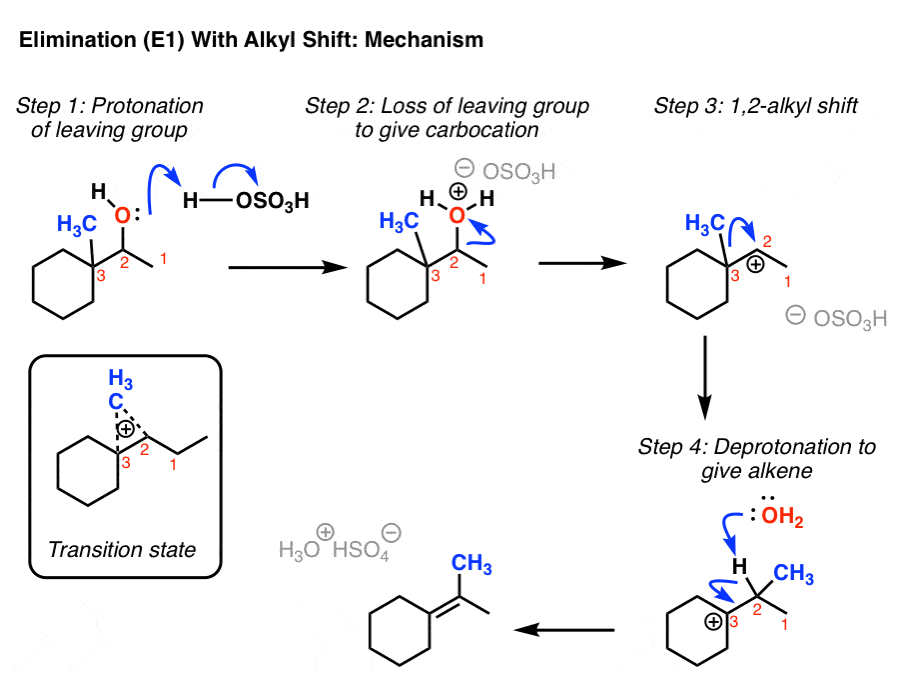
这几乎消除反应。
在接下来的系列文章,让我们去学生斗争虽然最大的一个问题。
既然我们已经经历了替换和消除反应,我们如何决定哪些人会发生在每一个情况?
好问题。这是下一个。
下一个系列中,职位1:SN1 SN2 / E1 / E2的决定(1)-底物
笔记
(高级)引用和进一步阅读
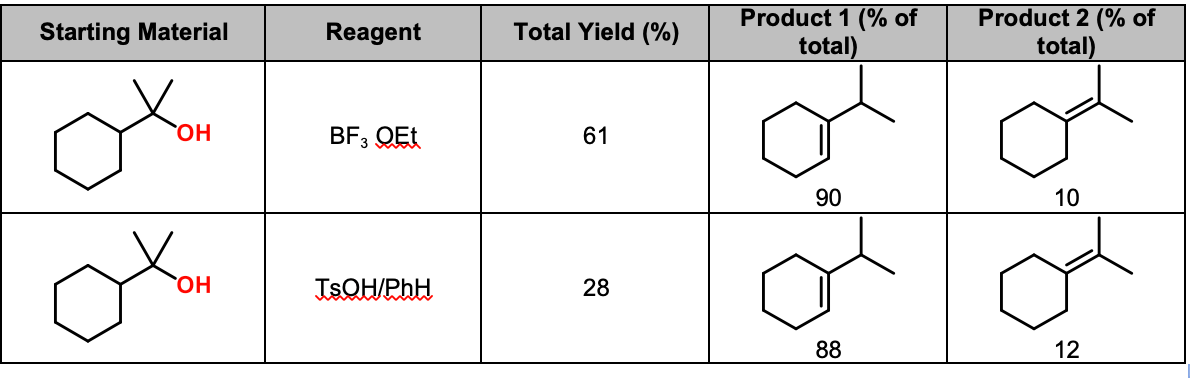
- 看看本文对于一些非常干净,脱水的经典例子烷基转变。作者把1-cyclohexyl-1-methylethanol和治疗用TsOH /苯或BF3•诗人2。你可能会认为他们会得到tetrasubstituted烯烃,但占主导地位的产品是三代的烯烃(挺)。原因是更多的酸度轴向碳氢键与中间的碳正离子。
男朋友3·诗人2促进快速、温和、清洁和特定选择的叔醇的脱水。
波斯纳,g . h .;Shulman-Roskes e . m .;哦,c·h·;携带、J.-C;绿色,j .诉;克拉克,a b;戴,h;Anjeh, t . e . N。
四面体。1991年,32(45),6489 - 6492。
DOI:10.1016 / 0040 - 4039 (91)80200 - p
- 相邻的氢同位素效应构象在溶剂分解3-methyl-2-butyl p-toluenesulfonate
s . Winstein j .高桥
四面体1958年,2(3 - 4),316 - 321
DOI:10.1016 / 0040 - 4020 (58)88053 - 9
3-methyl-2-butyl-tosylate是一个系统,将容易溶剂分解下,见表3。 - 消除反应的机制。十三。基础的影响,溶剂和结构产品比率在消除反应的一些次要的甲苯磺酸盐
欧文·n·费特和威廉·h·桑德斯
美国化学学会杂志》上1970年,92年(6),1630 - 1634
DOI:1021 / ja00709a035
最后,本文指出的那样,“一个有趣的趣闻E1的反应是烯烃导致氢化物转移和2-methyl-3-pentyl 3-methyl-2-butyl甲苯磺酸盐,2 -甲基- 1戊烯,2-methyl-l-butene,分别在越来越多沿< s-BuOH < t-BuOH系列溶剂正丁醇层。” - 与C重组研究14:第九。的FORMOLYSIS METHYL-C14-ISOPROPYLCARBINYL p-TOLUENESULPHONATE
Finlayson和c·c·李
可以。j .化学。1960年,38,787 - 792
DOI:10.1139 / v60 - 114
另一项研究来自Ref。1相同的系统,它使用C14标签研究的重组- pg。700。 - 超级死Pinakolinumlagerung cyclischer Verbindungen
汉斯•Meerwein沃尔特Unkel
Lieb。安。化学。1910年,376年(2),152 - 163
DOI:10.1002 / jlac.19103760203
本文由汉斯Meerwein碳正离子的早期研究的先驱和催化重组,在频哪醇,semipinacolic重组。在这篇文章中,他表明,2,2-dimethylcyclohexanol是通过酸转化成isopropylidenecyclopentane和1,2-dimethylcyclohexene。 - 超级Ringveranderungen贝der Wasserabspaltung来自alicyclischen Alkoholen
汉斯Meerwein
Lieb。安。化学。1918年,417年(2 - 3),255 - 257
DOI:10.1002 / jlac.19184170205 - 分子内重排的共同基础。. 1 Di-tert-butylcarbinol的脱水和转换产生的壬烯Trimethylethylene和异丁烯
弗兰克·c·惠特莫尔和e·e·斯塔尔
美国化学学会杂志》上1933年,55(10)4153 - 4157
DOI:1021 / ja01337a042
f·c·惠特莫尔教授是评论中提到碳正离子化学的历史,他是第一个表明碳正离子可以用一个“开放六重奏”表示的电子和吸引他们。 - 饱和碳原子的替代机制。第29一部分。位阻的作用。(D)部分的机制与水乙新戊基溴的反应酒精
即Dostrovsky和e·d·休斯
j .化学。Soc。1946年,166 - 169
DOI:10.1039 / JR9460000166
这里使用条件下(含水乙醇和氢氧化钠),约36%的重新安排烯烃(trimethylethylene)是获得新戊基溴离子。可能的更高的收益烯烃可能,如果有酸性条件有利于形成碳正离子。 - Lanostane Cucurbitane转换。
爱德华兹,o . e .;Kolt, r . j .。
可以。j .化学。1987年,65年(3),595 - 612。
DOI:10.1139 / v87 - 104
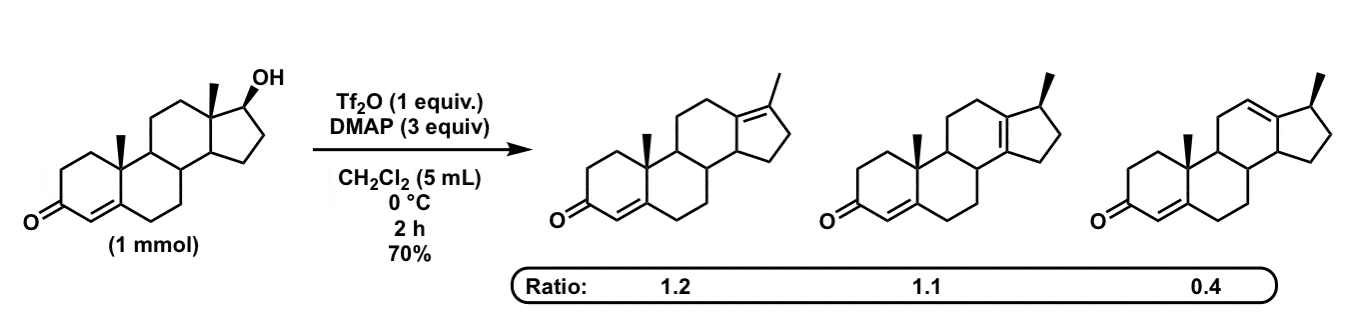
作者以一个非常严格的系统包含一个叔(类固醇lanostane)酒精并观察会发生什么当脱水与强酸(H2所以4-乙酸-交流2啊,所谓“Westphalen条件”)。后损失的水,从邻甲基转移观察到季碳(不是氢化物转移,有趣的是!)和作者的比率进行比较烯烃(三代的vs tetrasubstituted)。比率大大受到微妙的电子远程组的影响。 - 轻微的锅方法各种甾族的二级醇转化为相应的烯烃。
库马尔,r . r .;Haveli s d;卡根,h . B。
Synlett2011年,2011年(12),1709 - 1712。
DOI:10.1055 / s - 0030 - 1260803
稍微不同的激素系统,给重排+消除产品的混合物。
你好,谢谢你的好的文章,我16岁,但我喜欢化学和我要在IChO参赛。但是一个问题,如果两个烷基和氢化物转移是可能的,会发生什么?
氢化物转移,一般来说,将执行1 2变化比烷基转移快得多。首先,思考的动力1、2的转变。少替换的驱动力是形成碳正离子。如果你有一个中等碳正离子邻叔碳,和叔碳氢键迁移,您获得一个更稳定的三级碳正离子。然而如果一个烷基迁移,你获得一个(同样稳定)二级碳正离子。
可能会发生异常。在实验室里,有1的情况下,优先2 -烷基会发生变化,特别是在刚性循环系统。在刚性,循环系统包含一个免费的碳正离子组最有可能迁移是那些有债券与空的p轨道;轴组,换句话说。看到帖子的末尾的引用一些例子。