化学概论
化学平衡
最后更新:2022年10月28日|
化学平衡
在化学领域,不可逆反应得到了所有媒体的关注:人们熟悉的火灾和爆炸在YouTube上有很好的表现。问题是,不是所有的反应都能完成。有时候,一个反应的产物可以一起反应再生起始材料,从而建立一个可逆的的反应。这些类型的反应在我们周围都在发生,我们从来没有注意到。在任何给定的时刻,我的健怡可乐(pH值3.39)中都有数量惊人的质子在与水分子交换,但由于没有净变化,这个过程实际上是看不见的。
在“从普通化学到组织化学”bdapp平台的最后一课中,我们将讨论化学平衡,这是一个巨大的有机化学主题。你要学习的很多反应都是平衡反应,这个概念超出了化学反应,延伸到了很多过程,比如底物如何与酶结合,甚至分子如何可逆地改变它们的三维结构。
那么什么是化学平衡呢?为什么它很重要?化学平衡是什么意思?
让我们从最基本的开始:
- 化学平衡只会发生在有显著反向的反应。
- 当化学平衡建立时,反应物和生成物的浓度随时间没有变化。
- 在平衡时,过程的G等于零。没有驱动力。
《Gen Chem》中引入平衡的最重要方法可能是酸碱反应。强酸盐酸(HCl)与水反应生成H3O(+),这本质上是一个不可逆的反应。相反,弱酸乙酸(CH3COOH)与H2O反应生成H3O(+)和CH3COO(-),但是反向反应也会发生。
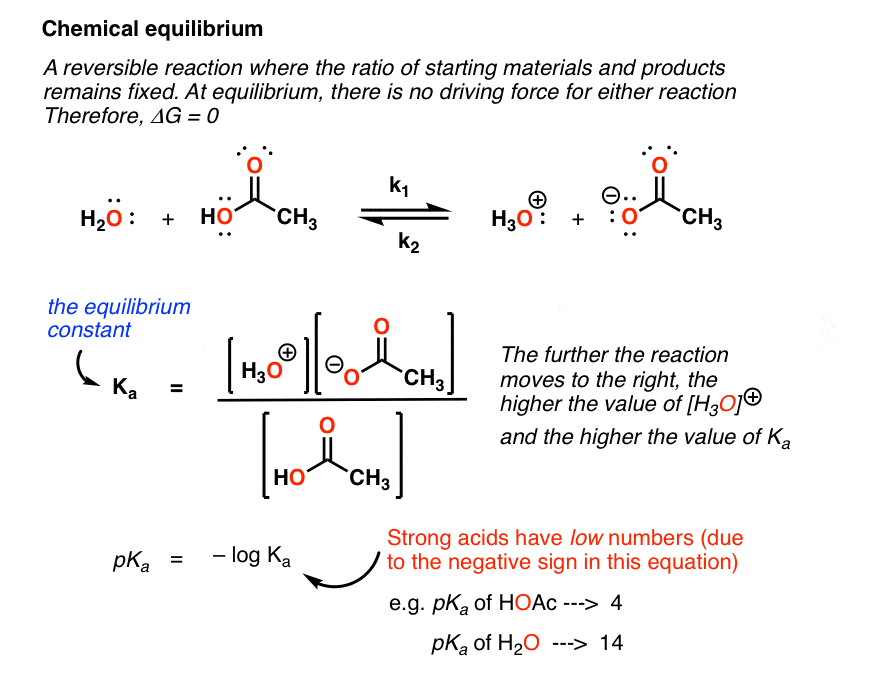
注意这一点很重要酸的相对强度由这个平衡常数的值来衡量。这为我们提供了一种非常有用的测量方法pKa等于这个反应的Ka的负对数。pKa是比较不同分子相对酸度的好方法。随着分子酸度的增加,这种平衡会越来越向右进行。结果是强酸的pKas低(就像强酸溶解在水中会导致低pH值)和弱酸有很高的pKas。]
你可能想都没想过,但是平衡状态下的化学反应一直在你周围以如此微妙的方式发生,你甚至都没有注意到。例如,在你附近的汽水机的每个罐子里,水和(加压的)溶解在溶液中的二氧化碳之间已经建立了平衡,从而形成碳酸;同时,碳酸分子解离,提供二氧化碳和水。
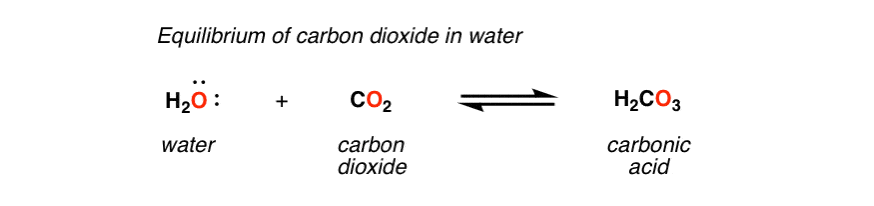
二氧化碳、水和碳酸浓度的净变化:零
平衡常数可用来确定Δ G。
在平衡状态下没有驱动力。反应的Δ G为零。在平衡常数和Δ G之间有一个非常有用的数值关系,叫做吉布斯自由能等温线方程我们可以用它来解Δ G(如果我们知道平衡常数)或者平衡常数(如果我们知道Δ G)
吉布斯方程:Δ G = -RT lnK
在有机化学课上你会看到很多可逆反应生成混合物的例子。一个具体的例子是在研究构象,它们是通过键的可逆旋转形成的分子的三维状态]。如果你知道K,你可以用这个方程求出Δ G:

你甚至可以把这个方程代入图形形式来查看关系(如果你能原谅蹩脚的Excel技能)
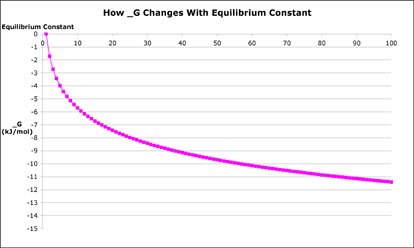
看看这条曲线的开始部分有多陡峭!一个反应的能量差是如此之小这让人很惊讶对于9:1的反应物来说。想想看,5.4 kJ/mol并不算多——例如,与430 kJ/mol的C-H键的强度相比。对于一个99:1的反应,差值必须只有11.4 kJ/mol。
Lé Châtelier的原理
这是关于平衡的最后一个关键概念。有机化学是一门实用科学。我们经常关心的是将一种化合物转化为另一种化合物。我们经常想要停止逆反应来提高产物的收率。
我们通常可以找到一种方法来操纵平衡,提供我们想要的产品。你经常会听到这样的描述推动反应向前。这是通过去除正向反应的一个副产物来实现的,因此防止了反向反应的发生。
举个例子。对待一个醛与一个胺生成一种叫做an的化合物亚胺还有一个水分子。这个反应是可逆的;水可以和亚胺反应得到产物。
这是关键。如果你能找到一种方法去除掉这里的水,你实际上就关闭了k2(逆反应)这对整个反应有什么影响?它将继续向前(向右)方向,直到重新建立平衡。永远不会,因为我们加了干燥剂。结果:一种产品,而不是混合物。
实际上,除去水有几种方法,其中一种方法是加入一种物质(称为甲酯)干燥剂)会与水发生不可逆的反应,从而将其从方程中去除。硫酸镁(MgSO4)只是一个例子-它形成一种水合物.
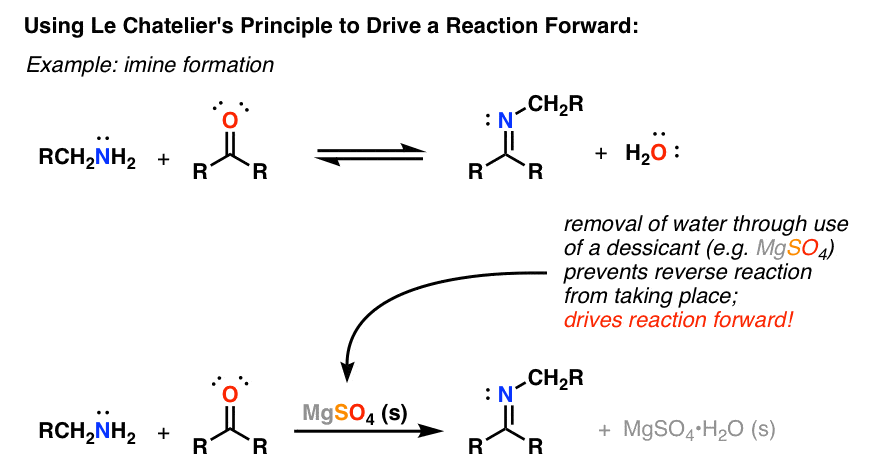
这个概念的名字你应该很熟悉:它叫勒夏特列原理。
在有机化学中你会遇到很多关于勒夏特列原理的例子,因为你会遇到很多可逆反应(一些在Org 1中,但很多在Org 2中)。
底线:如果你了解一个反应和它的产物,你可以选择条件,允许去除产物,从而阻止平衡的建立,并推动反应向你想要的产物方向发展。
如果平衡时G为零,为什么要计算平衡反应的G呢?有什么好计算的?
这是一个非常棒的问题。
差值是*体系*的G与各组分的G°(生成能)之间的差值。
对于处于平衡状态的系统,G为零。没有能量的净变化。
如果平衡常数为1(生成物的浓度=反应物的浓度),那么我们也可以说生成物的G°(生成的G)等于反应物的G°。
但大多数时候,平衡常数大于(或小于)1(取决于你画方程的方向)。这意味着一种组分比另一种组分更稳定,我们可以用吉布斯自由能方程G°= RT ln k将它们的相对稳定性与平衡联系起来。如果我们知道在给定温度下的平衡常数,我们可以重新排列方程来求解能量差。
明白吗?
这让我明白了这一点。谢谢你!
在将吉布斯自由能与平衡常数联系起来的表达式中,G到底是什么,它是生成物还是反应物,它不可能是系统的,因为在平衡状态下G是0
我认为表达式中应该是标准吉布斯自由能而不是吉布斯自由能.....标准吉布斯自由能是生成物和反应物吉布斯自由能之差吗