烯醇、烯醇化物
迈克尔加成反应和共轭加成
最后更新:2023年6月16日|
迈克尔•加成反应(和共轭加成)
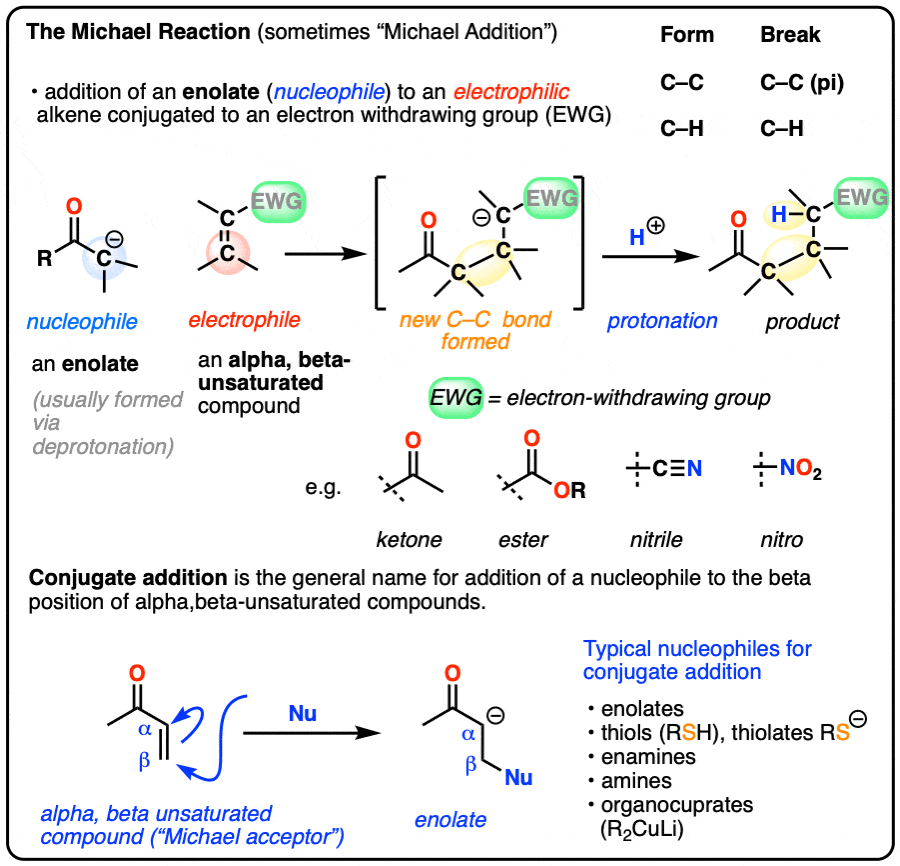
- 的迈克尔反应(有时“迈克尔加成”)的一个烯醇化物一个亲电烯烃,比如一个α-β不饱和酮,腈,或酯
- 的主要驱动力是形成碳碳(单一)债券(80千卡每摩尔)和碳碳π键的断裂(60千卡每摩尔)
- 迈克尔反应机制是1)去质子化形成一个烯醇化物,2)共轭加成的烯醇化物到烯烃,3)质子化作用产生的(新)烯醇化物
- 共轭加成(或“1,4-addition”)就是一个反应的通用名称亲核试剂亲电的β碳补充道烯烃在共轭吸电子集团
- 的亲核试剂,可以参与共轭加成包括烯醇化物,胺,硫醇盐(RS(-)),烯胺和dialkylcuprates(“吉尔曼试剂”)
- 格氏试剂做不执行共轭加成;他们添加羰基碳(“加法”),而是organolithium试剂和LiAlH4。
表的内容
- 迈克尔反应——一些例子
- 迈克尔反应的一般模式
- 迈克尔反应机制
- 为什么不亲核试剂添加到“正常”烯烃吗?
- 共轭加成(“1,4-Addition”)
- 1、加法和1,4-Addition
- 分子内的迈克尔反应
- 工作从迈克尔加成的产品
- 总结
- 笔记
- 测试你自己!
- (高级)引用和进一步阅读
1。迈克尔反应——几个例子
烯醇化物可以添加到贝塔(β)α-β碳羰基化合物,形成新的碳碳键和碳碳π键。这就是所谓的“迈克尔反应”亚瑟为了纪念迈克尔的最初的反应(1887)报告(裁判]。(见文章-烯醇化物,形成稳定和反应)
由于碳碳π键被打破,形成两个新单键的碳,迈克尔反应的一个例子除了的反应。(见文章-加成反应,消除相反)
这是迈克尔反应之间的一个例子烯醇化物丙二酸的酯和一个α,beta-unsaturated酮(又名“enone”)(NaOCH打下坚实的基础3在这种情况下)是用于形式烯醇化物:(pK一个丙二酸的酯类通常约13,这是相当有利的酸碱反应)
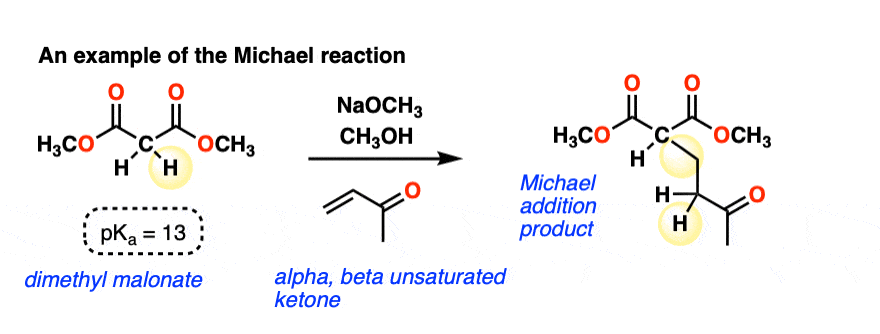
形成新的碳碳单键,所以是一个新的碳氢键上α碳α,β不饱和酮。上的碳氢键α碳丙二酸的酯坏了,所以是碳碳π键。
的亲核试剂还可以添加α,beta-unsaturated吗腈,比如在这个例子:
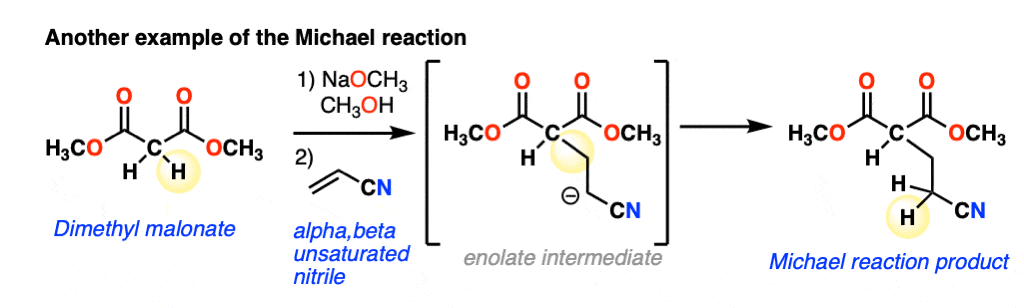
超出范围α,β不饱和酮和α,β不饱和腈包括α,β不饱和酯类、硝基化合物、磺酸酯类和更多。因为它能让漫长的这些名字写出来,“迈克尔受体”常被用来指烯烃(注1)连接到一个或多个电子组可以作为撤军pi-acceptors。(见文章:探索共振:π受体)
这是迈克尔反应之间的一个例子酮烯醇化物(通过选择性less-substituted的去质子化α碳与庞大的基地di-isopropyl锂酰胺(乔治。),ee的文章,动力学和热力学烯醇化物)和一个α,β不饱和酮。
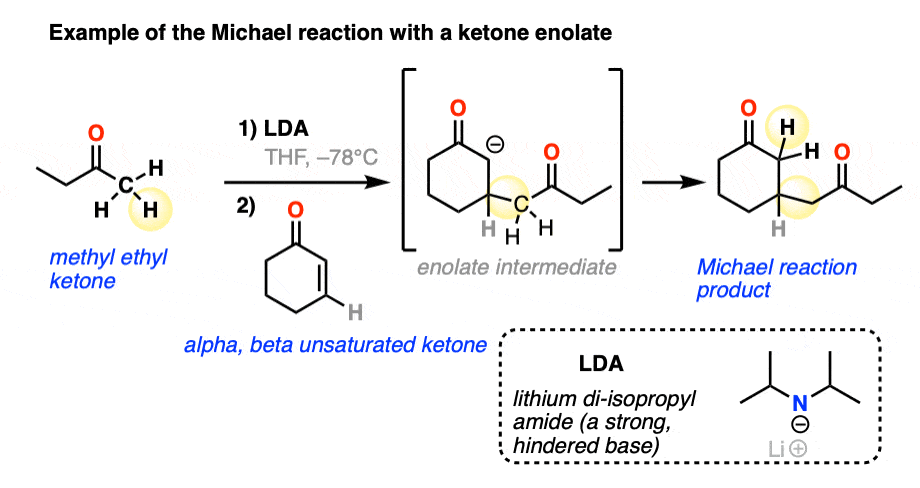
记住这三个例子,让我们画出总体方案!
2。迈克尔反应的一般模式
迈克尔反应的一般模式是这样的:
- 一个烯醇化物(通过治疗的形成酮,酯,腈或类似的物种基地)增加了β碳一个亲电烯烃如α,beta-unsaturated酮,腈或硝基化合物(“迈克尔受体”)
- …给一个新的碳碳单键和碳碳π键
- …导致新烯醇化物,然后使质子化给最终产品。
电子集团在撤军烯烃通常是一个羰基化合物如酮或酯,但也可以是腈、硝基或磺酰等等。
迈克尔的驱动力的交换是一个相对较弱的碳碳π键(约60千卡每摩尔)相对强劲的碳碳单键(约80千卡每摩尔)。
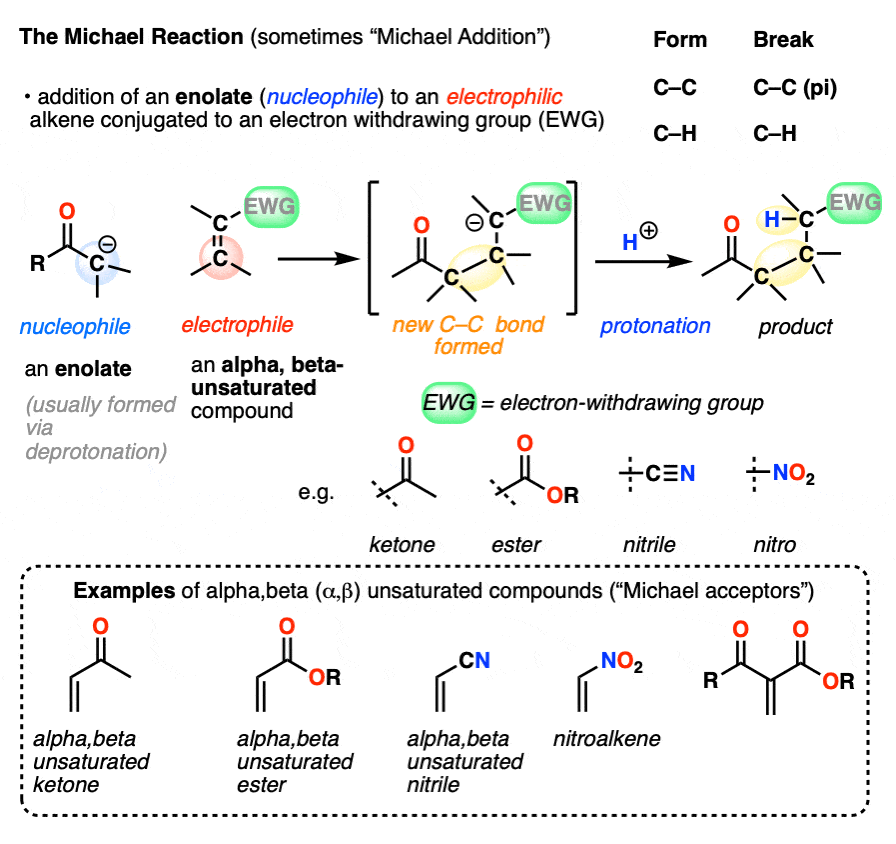
一个典型的产品迈克尔反应有两个羰基组由3个碳。(一般的名字这是一个“1,5-dicarbonyl”,虽然在某些情况下,硝基,青紫或磺酰组站在一个或多个的羰基碳原子。)
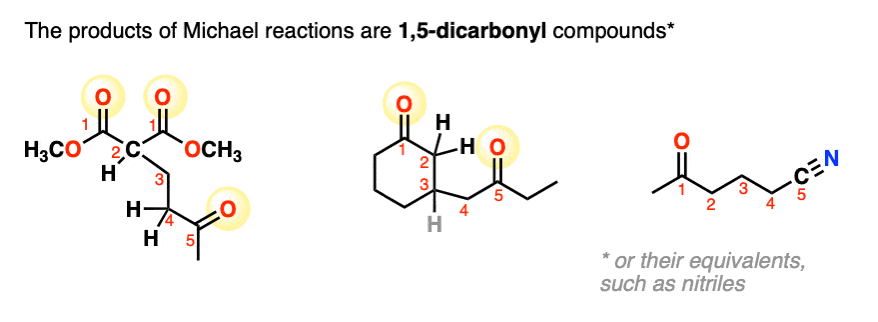
3所示。迈克尔反应机制
迈克尔反应涉及三个关键步骤:
让我们看看与丙二酸的第一步酯在本文的第一个例子。
在第一步中,甲醇钠(NaOCH3)中的一个质子α碳,导致一个新的烯醇化物。
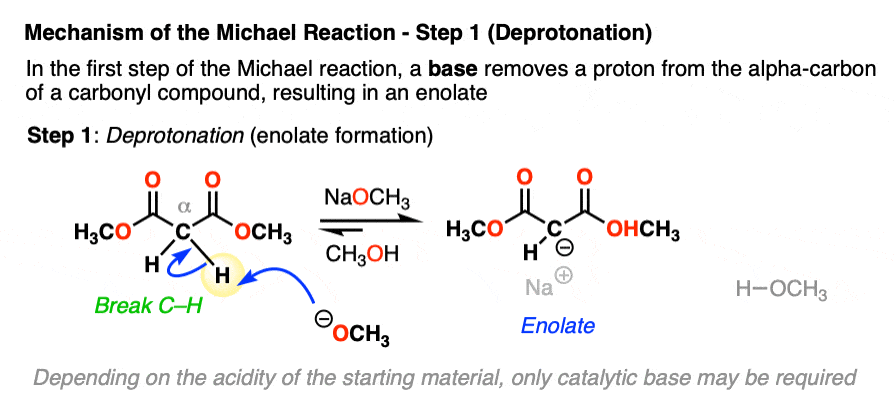
烯醇化物非常棒的亲核试剂。在第二步中,烯醇化物增加了β碳的α,β不饱和酮,其结果新烯醇化物。这种机械的步骤通常被称为共轭加成或(有时)1,4-addition。
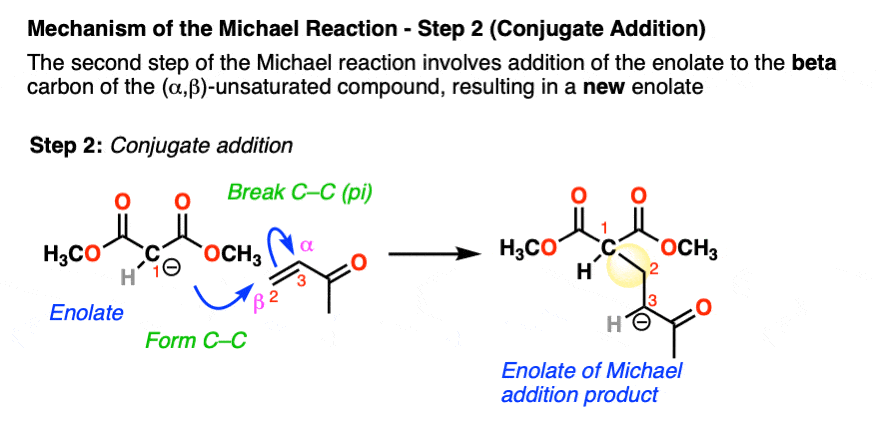
最后一步是质子化作用产生的烯醇化物中性的迈克尔加成产物。
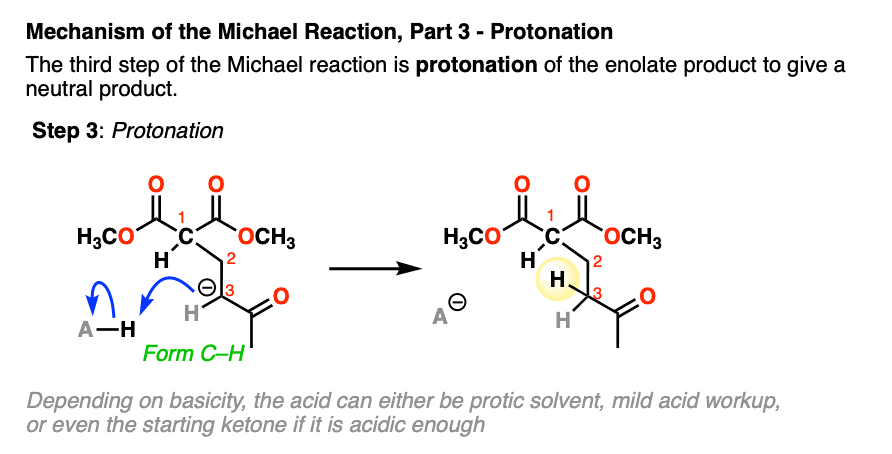
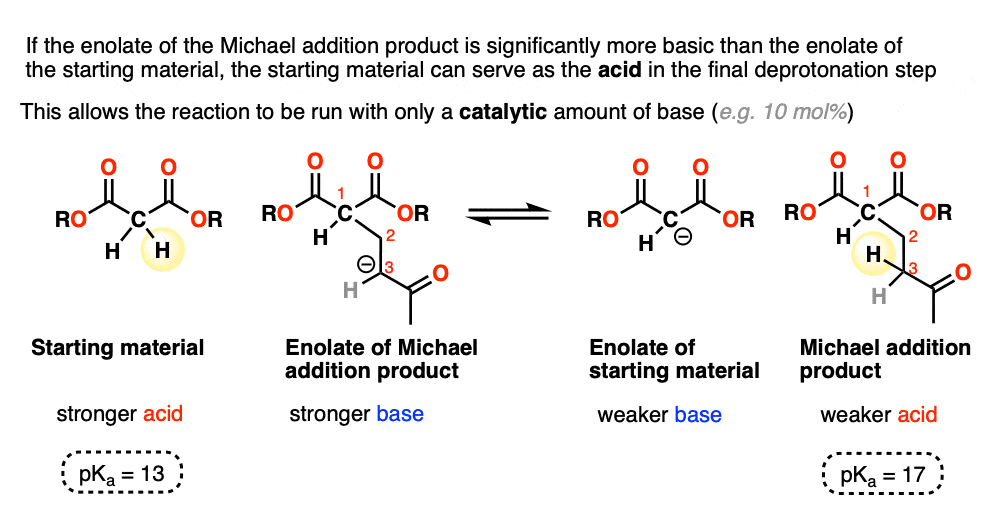
当烯醇化物的产品是更基本的比烯醇化物起始物料的反应可以使用一个运行催化数量的基础。
4所示。为什么不亲核试剂添加到“正常”烯烃吗?
如果你退一步,第二个迈克尔反应似乎有点不同寻常。
毕竟,早在一天,你可能整个Org 1单位的反应烯烃——我打赌不是其中的一个例子涉及添加一个亲核试剂到一个烯烃。(大部分的烯烃我们看到参与反应的反应亲电试剂与烯烃,如酸、卤素m-CPBA,OsO4阿,3等等)
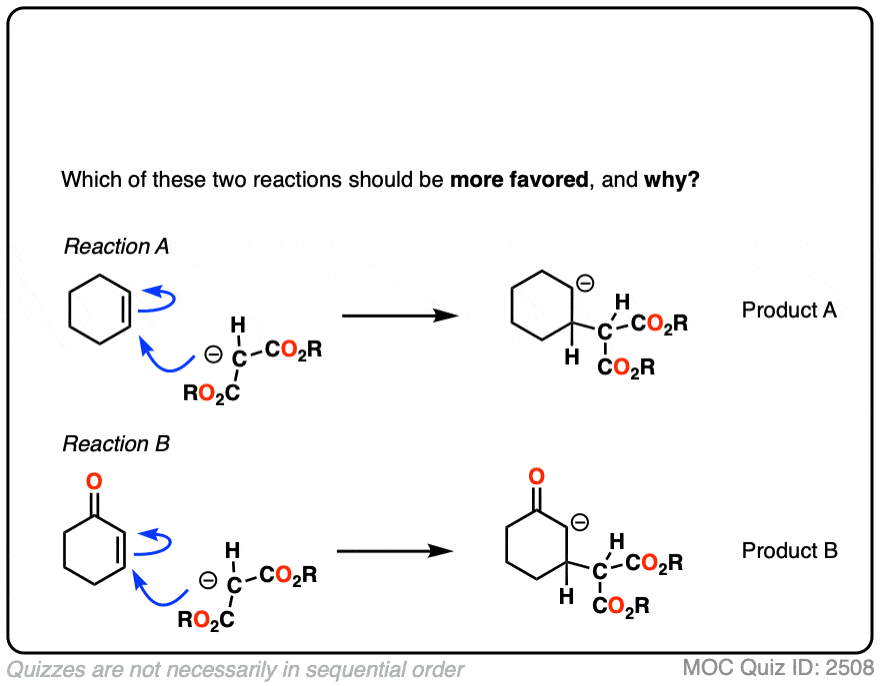
为什么一个烯烃有利的当烯烃是相邻的酮,酯或其他electr0n-withdrawing集团,但是不利的为“正常”烯烃比如说,环己烯吗?
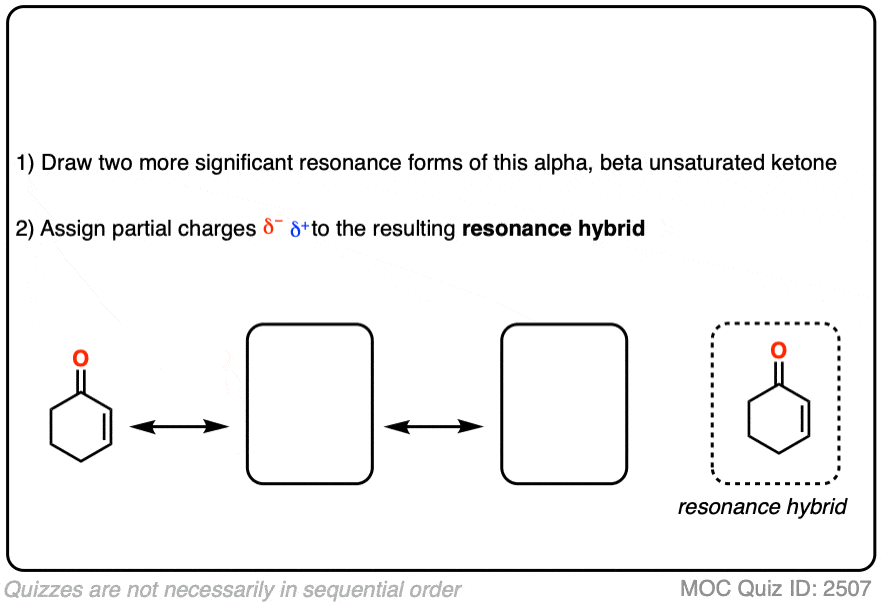
这可能是有用的画出重要的共振形式的α,beta-unsaturated酮连同它的共振杂化。
 点击翻转
点击翻转
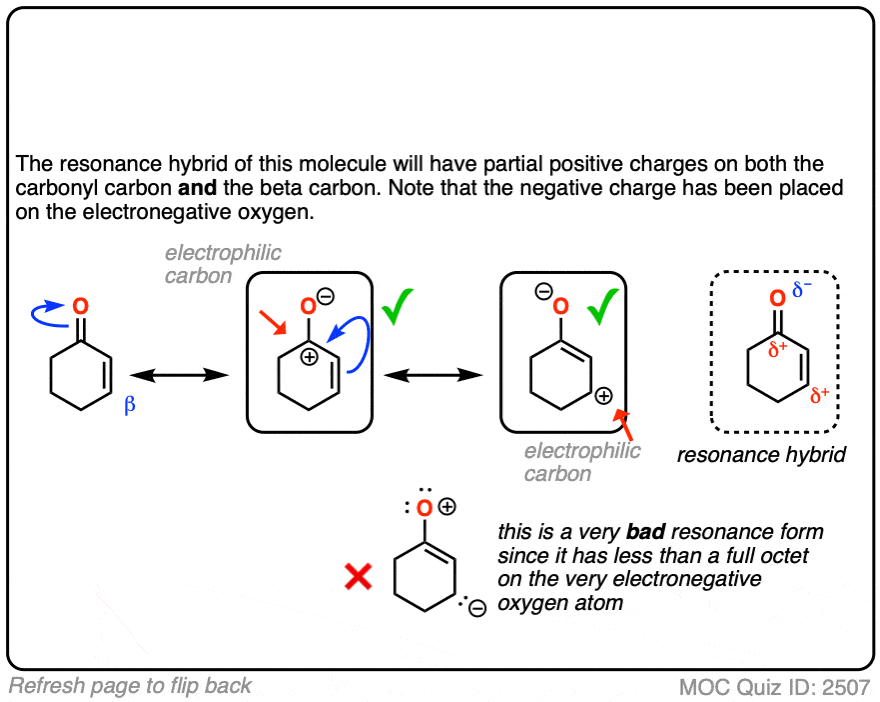
当你画出共振的关键形式,你会注意到有一个β碳正电荷和负电荷的氧气。β碳亲电,换句话说,羰基氧作为电子“下沉”电子在碳碳π键。
反应性的α,β不饱和系统是有意义的,当你考虑稳定负电荷的结果的亲核试剂β碳。(看到后7因素稳定负电荷)
 点击翻转
点击翻转
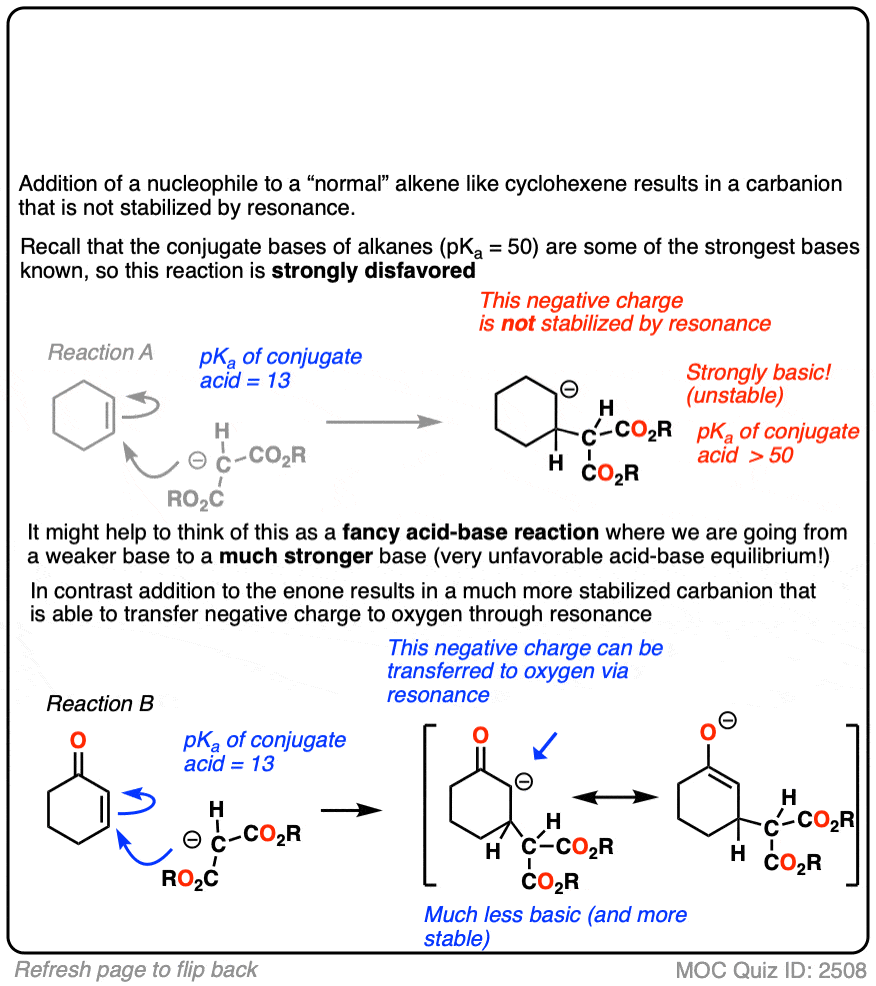
添加亲核试剂到一个烯烃结果在一个新的碳负电荷(也称为“负碳离子”)
除了普通的亲核试剂烯烃强烈冷宫以来产生的负碳离子是一个极其吗强碱(回想一下,pK一个烷烃> 50名左右)。(注2]
另一方面,当一个酮,腈,酯或其他pi-acceptor是相邻的烯烃,由此产生的负电荷可以离域共振氧或氮。
原子的电负性比碳,这些能更好地稳定负电荷。这就是一个典型的原因酮有一个pK一个17日左右(30个数量级比一个普通的烷烃酸性更强!)
或国家更短暂,除了这些烯烃结果在一个烯醇化物,比普通的烯醇化物更稳定负碳离子由于负电荷可以转移到氧气。
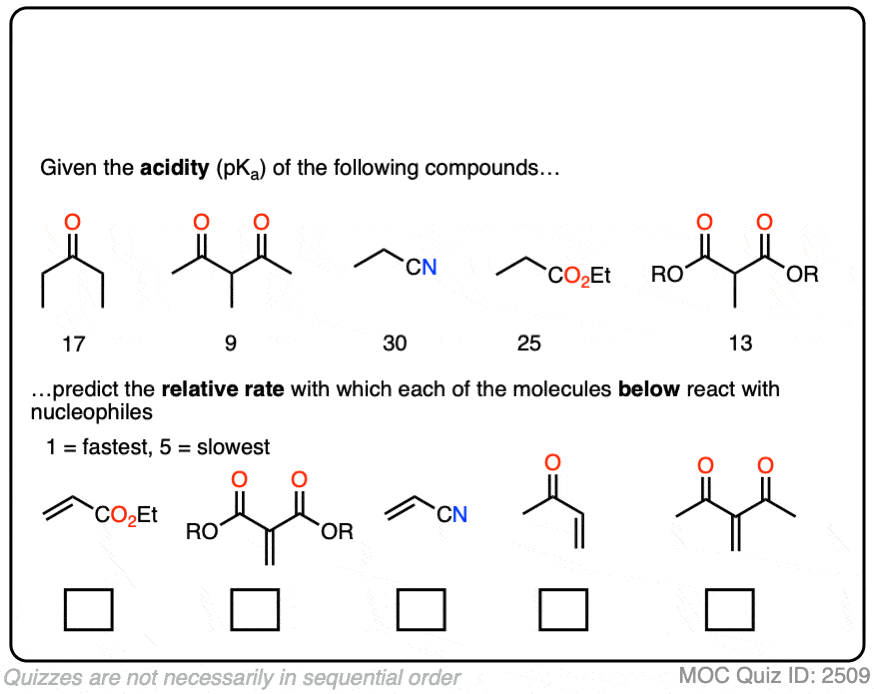
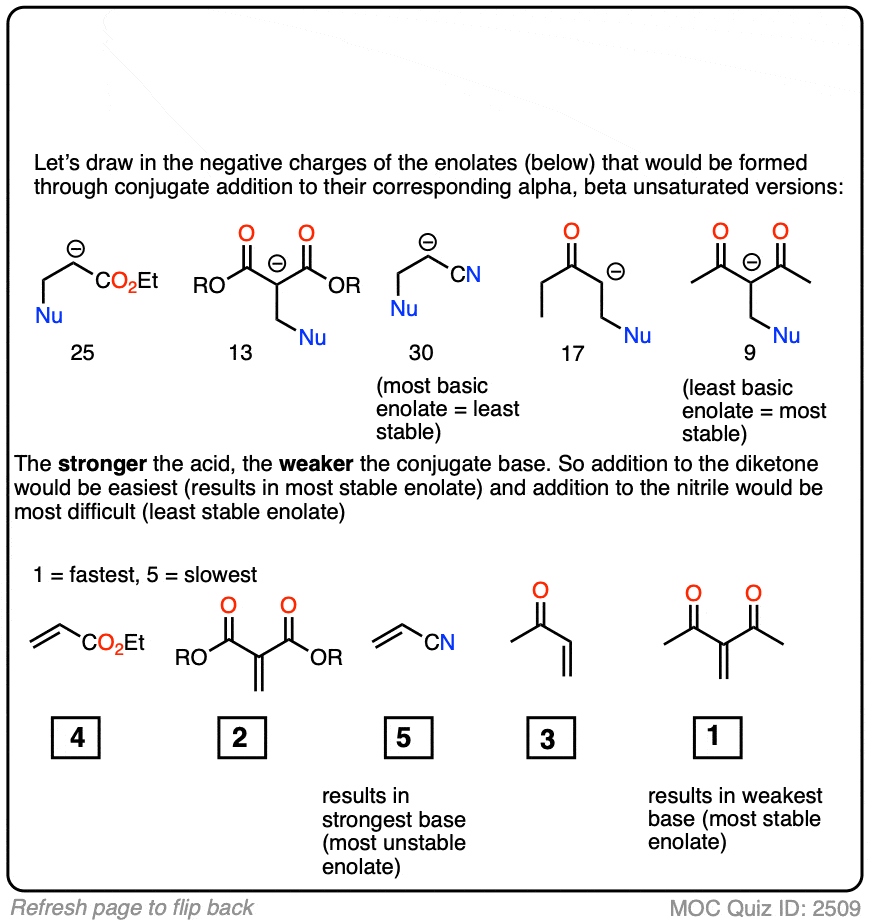
事实上,易于共轭加成的稳定性结果的关联非常好烯醇化物。试试这个练习,例如:
 点击翻转
点击翻转
5。共轭加成(“1,4-Addition”)
迈克尔反应是一个更一般的类的反应共轭加成。
共轭加成的亲核试剂到一个烯烃这是在接合羰基(C = O),含氰基的(CN)、硝基(没有2)或其他官能团可以作为“π受体”。
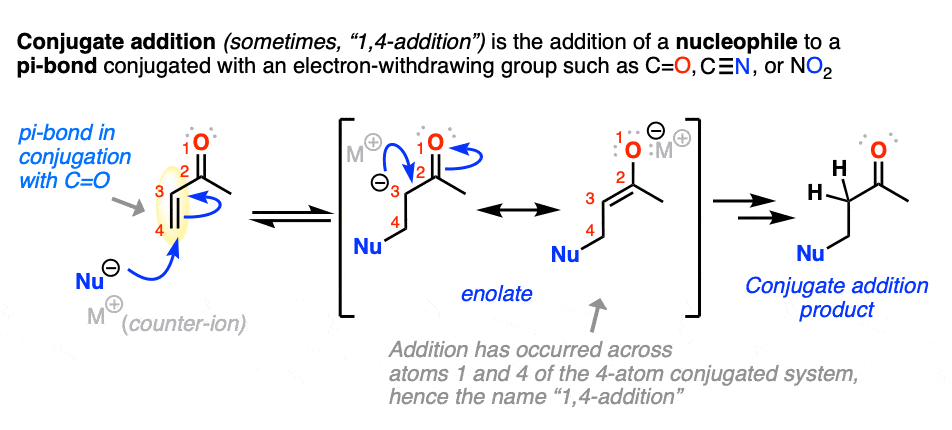
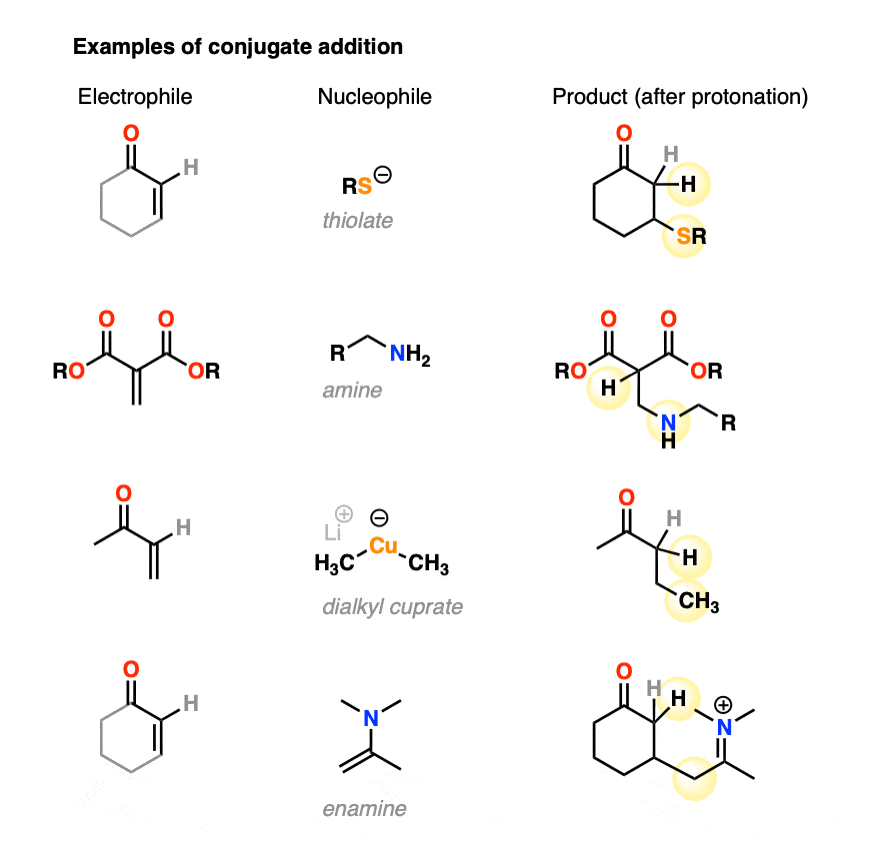
共轭加成可以用很多不同的亲核试剂发生,如胺硫醇盐(RS(-)、烯胺和dialkylcuprates,许多其他人。这里有一些代表性的例子。
6。1、加法和1,4-Addition
好吧。到目前为止还好。很遗憾地告诉你,时间已经到来,让我们的讨论更加复杂。
迈克尔受体如α,beta-unsaturated酮没有就一个亲电子碳。它有两个:β碳(我们一直在关注吗)除了羰基碳。
共轭加成,有时被称为“1,4-addition”对比“加法”,这是另一个名称为亲核加成羰基(C = O) (见文章:亲核加成,羰基)
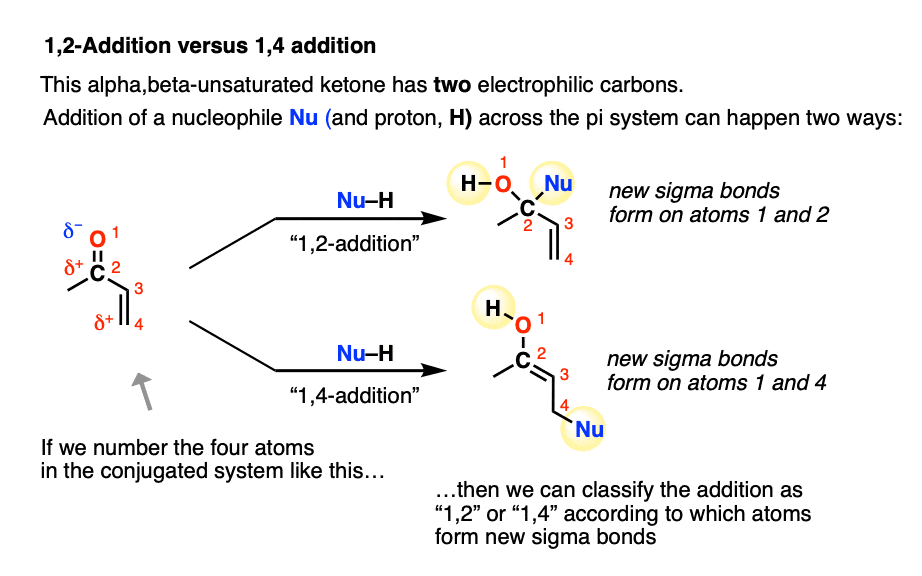
在分子enones, 1, 2 - 1, 4 -可能发生。(迈克尔用更少的亲电子受体羧酸衍生品如酰胺和腈将有更少的竞争1,2-pathway)。
- 往往是“1,加法”快由于这一事实羰基碳,直接连接到氧气更大的部分正电荷β碳。当添加不可逆转的,因为它是与许多强碱性的亲核试剂(或通过保持低温反应动力学控制)1、两种产品通常会占主导地位。
- 往往是“1,4-addition”产品更多的热稳定因为它们涉及到打破了碳碳π键(60千卡每摩尔),而不是切断π键(80千卡每摩尔)。当反应是可逆的,或加热,这样一个平衡建立了(热力学控制)1、4-products往往会占主导地位。
与我们之前讨论的动力学和热力学控制,然而,(见文章-动力学和热力学控制)温度不是万能的。的身份亲核试剂起着关键作用。
一个经典的例子对比反应是通过比较发现格氏试剂的反应(RMgBr)和organocuprates(吉尔曼试剂,R2CuLi)与α,β不饱和酮(“enones”)。都是强碱性的亲核试剂,添加不可逆转。然而…
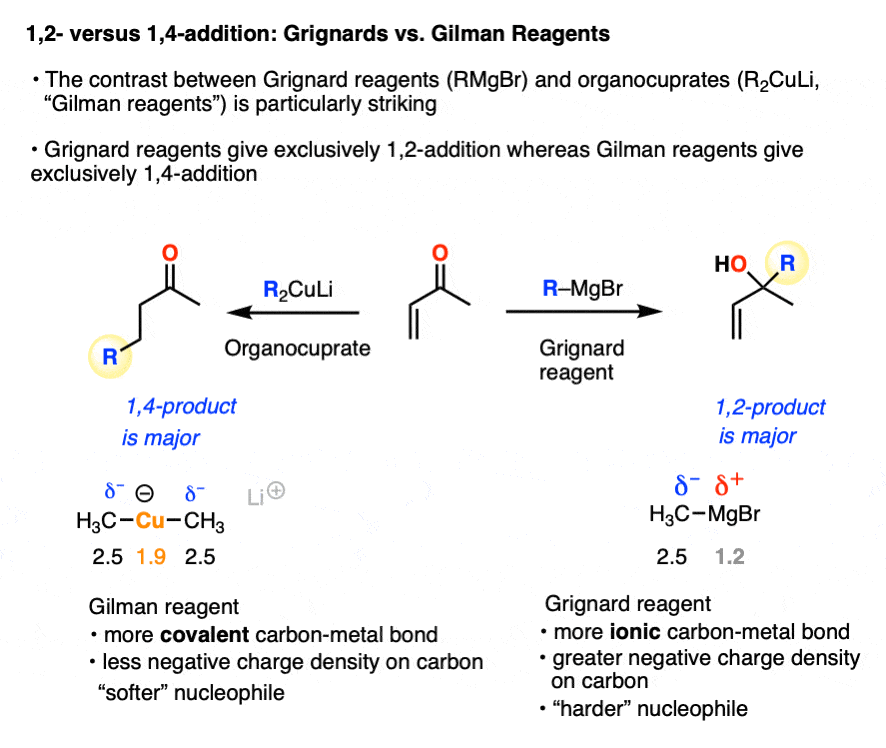
- 格氏试剂会优先给加法(LiAlH等organolithium试剂和氢化物4)
- Organocuprates倾向于优先给4-addition (硫醇烯醇化物一样,烯醇化物,胺和烯胺)
那么发生了什么?这是一个伟大的的问题。
一个工作模型来解释这些不同的模式被称为硬软酸碱理论(HSAB)。在HSAB,倾向于“硬”亲核试剂与“硬”亲电试剂反应,和“软”的亲核试剂与“软”亲电试剂反应。(注3]
(更多HSAB和总结的因素促进1,2 -和1,4-addition,请参阅注意4]
7所示。分子内的迈克尔反应
34有机化学的规则是:“如果一个反应存在,有一个分子内的变体”。
迈克尔和共轭加成反应不同。
关键的分子内反应,你可能会看到我说过很多次在这个网站,是一个教师的角度来看,他们涉及到没有新概念但提供了惊喜的感觉。因此,他们成为伟大的考试问题。
看看你是否能画出这种分子内迈克尔反应的机制。记得你的碳数量,首先画丑陋的版本如果它是不清楚,这样你可以得到正确的键形成/键断裂。你总会有时间去画一个漂亮的版本。
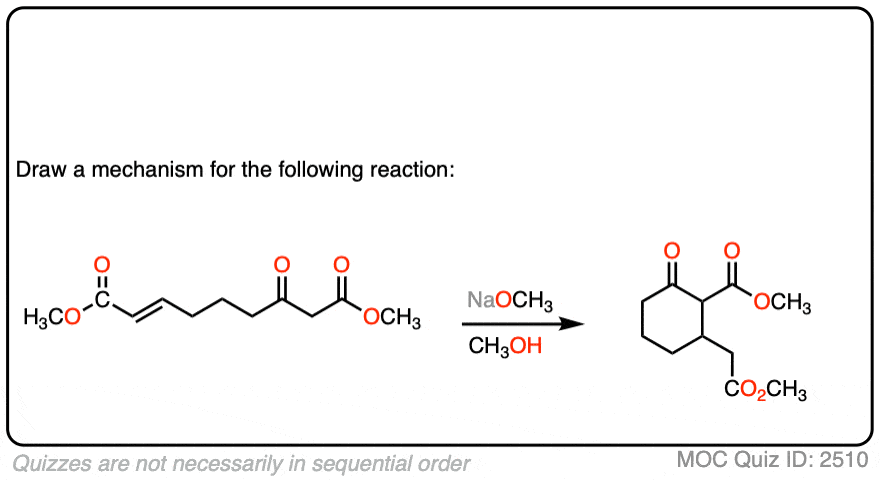 点击翻转
点击翻转
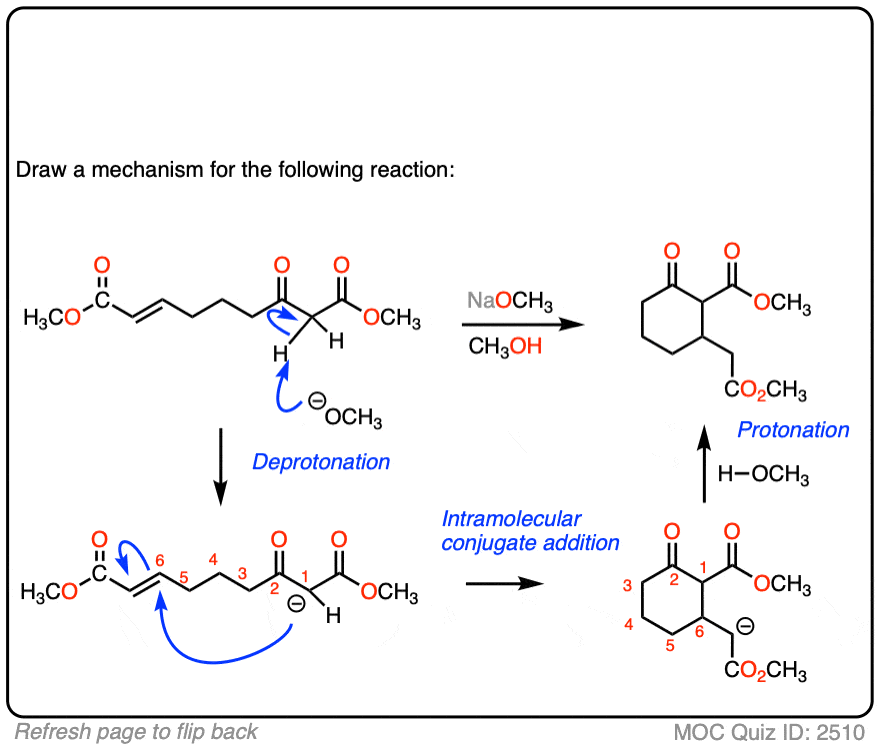
这是另一个测试。在这种情况下,画这种分子内迈克尔反应的产物。
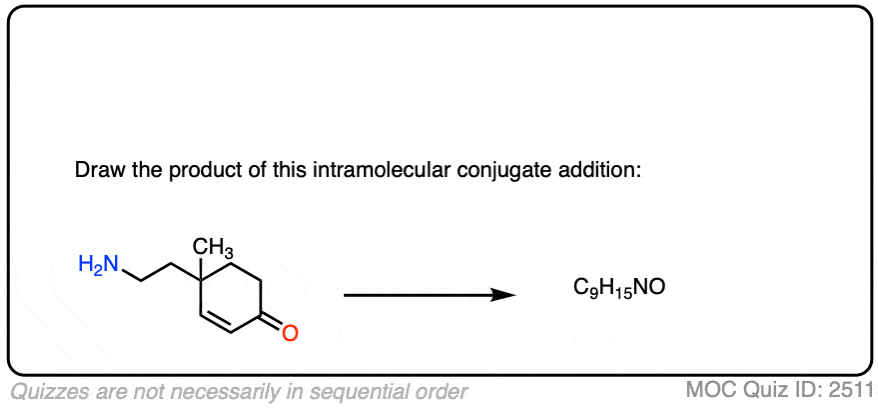 点击翻转
点击翻转
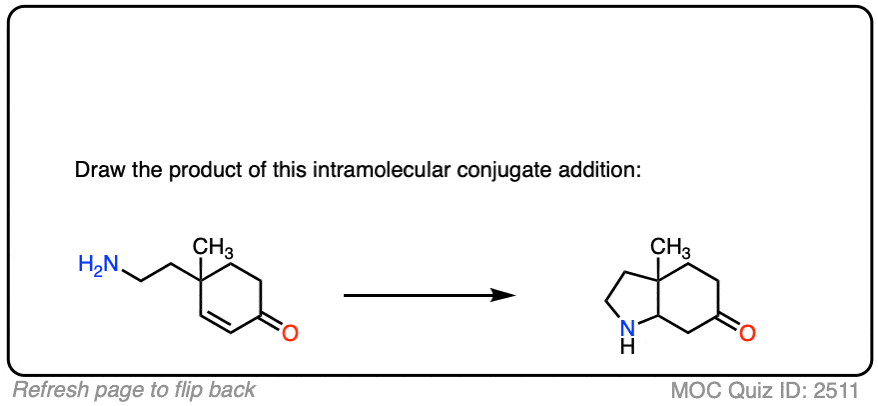
8。迈克尔增加和合成:向后工作
我不知道规则这个数量,但任何时候你学习一种新的反应,你可以把它在一个合成的问题。这意味着能够工作向后从产品合理的起始原料。
看看你能不能断开这些迈克尔加成/共轭加成产品回到适当的起始原料。
提示:回想一下,在迈克尔反应模式的关键是形成1,5-dicarbonyl。
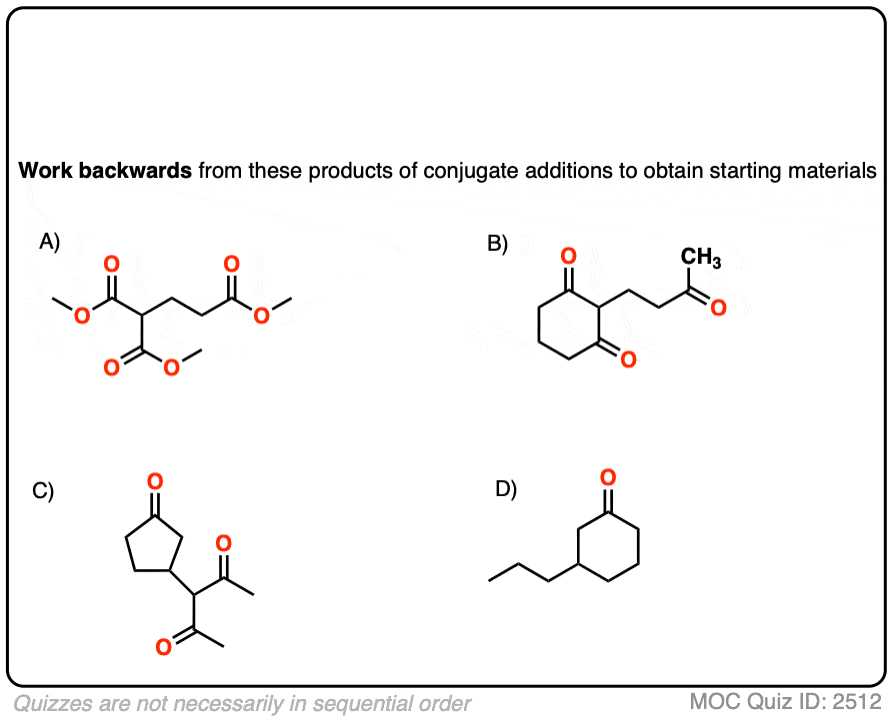 点击翻转
点击翻转
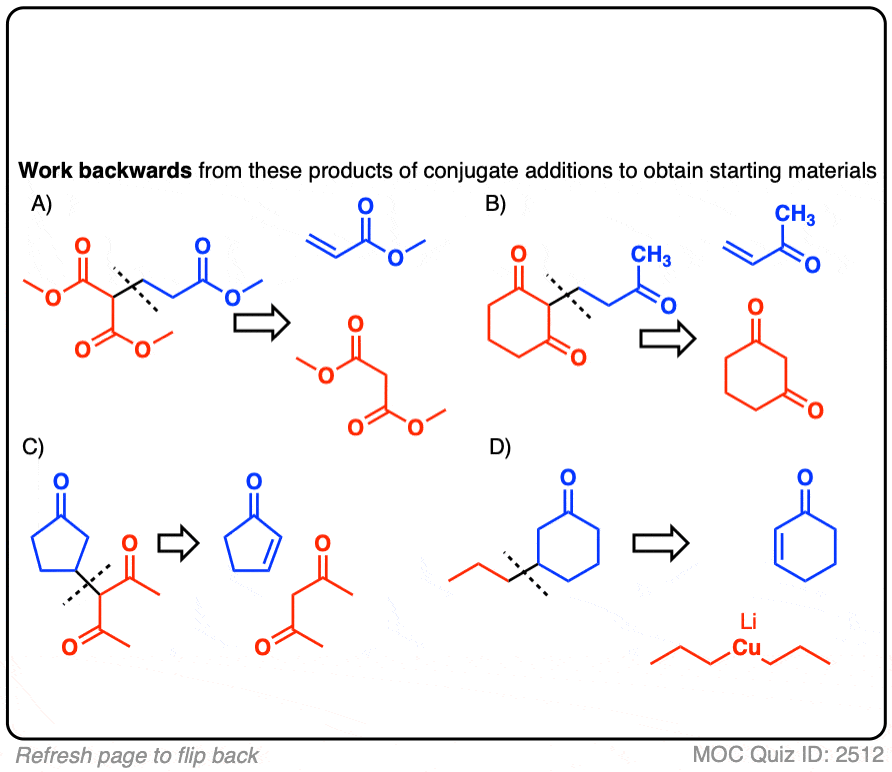
可能会有不止一个正确答案;酸性更强的起始物料每个案例所示。
9。总结
- 我们已经见过迈克尔加成是关键的一步共轭加成一个烯醇化物一个亲电烯烃。
- 反应所得的三个步骤:1)去质子化2)共轭,和3)质子化作用
- 烯烃与pi-acceptor如接合羰基,腈、硝基酯(和其他人)有一个重要的共振形成的β碳熊一个正电荷。与普通烯烃这个碳亲核加成,是有可能的,因为pi-acceptor能够接受孤对从一个π键和稳定的负电荷比碳原子的电负性。
- 共轭加成可以发生在各种亲核试剂如烯醇化物、organocuprates,硫醇,胺、烯胺等等。
- 当两个1,2 - 1,4 -是可逆的,平衡倾向于形成的产品由于破损较弱的碳碳(pi)债券。
- 强碱性离子的亲核试剂,添加不可逆(格氏和organolithium试剂等)往往会给产品的加法选择性超过4-addition。
- Organocuprates倾向于给1 4-addition产品只做硫醇,膦类化合物、烯胺等。
迈克尔反应的一个关键应用在罗宾逊环状结构,其中包括迈克尔加成醇醛缩合紧随其后。(见文章:罗宾逊的环状结构)
笔记
注1。虽然我写了“烯烃“在这里,Michael-type与亲电反应也会发生炔烃。
注2。如果这听起来像是我们沸腾的酸碱反应…你没有错!很多反应可以判断他们是否有利或不利取决于产品是否比开始更不稳定的(基本)材料。它是方便的认为“碱性”只是一个花哨的名字为“孤对电子不稳定”。
注3。软硬酸碱理论的蒸馏Klopman-Salem方程反应性的两个关键方面:1)静电吸引的贡献,和2)轨道重叠的贡献,这是最高的HOMO和LUMO能量很近。(维基百科文章Klopman-Salem非常糟糕——看到弗莱明的经典前沿轨道和有机化学反应为一个更好的讨论)
在一个模式下的反应(“努力交互”),反应产品驱动静电吸引高度富(δ- - - - - -)亲核试剂对高度阳性(δ+)亲电试剂。这是相对较小,最有效的极化原子电荷密度高,叫做“硬”在这个模型中(像一个带电小台球,质子H +是典型的“硬”亲电试剂)。
这使我们能够合理化倾向于1,格氏的加法和organolithiums之间的交互”硬”亲电试剂和“硬”亲核试剂。
- 的羰基碳是更多的阳性比β碳(“困难”)因为它是直接与氧的电负性
- 格里纳和organolithium试剂有更多离子李carbon-metal债券由于电负性较低(1.0)和Mg相对于铜(1.9)(1.2)。这意味着碳将有更大的电子密度(δ- - - - - -= "困难"),而不是在organocuprates C-Cu债券在哪里更共价(2.5 C)的电负性
由于静电原因,1,加法也快4-addition。
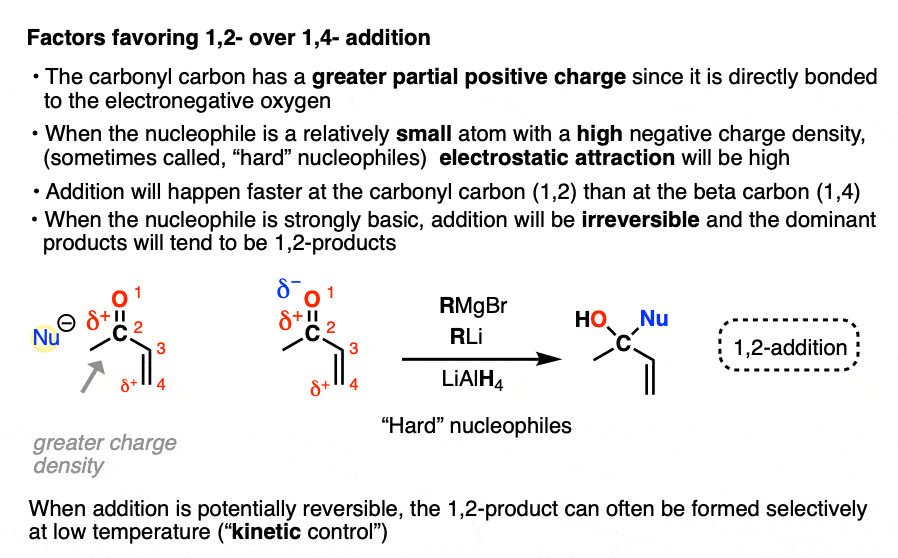
在其他模式下的反应(“软软的交互”)产品分布是来自由轨道重叠孤对之间的亲核试剂和最低未占据分子轨道(LUMO)enone。
“软”的亲核试剂与亲电试剂被认为是相对较大的,可极化的原子电荷密度较低,像一个大的削弱球的,很容易挤压和变形。典型的“软”的亲核试剂包括烯烃、硫醇和碘。“软”亲电试剂包括缺电子烯烃像enones。Pericyclic反应像Diels-Alder完全是基于“软软的”互动。
由于复杂的原因,并不是所有的原子的LUMO有效尺寸相同。(注5在的LUMO]enone,β碳更有效比大小羰基碳。没有电荷的影响,最大的反应将会发生在网站可以发生人类之间的重叠亲核试剂的LUMO亲电试剂。
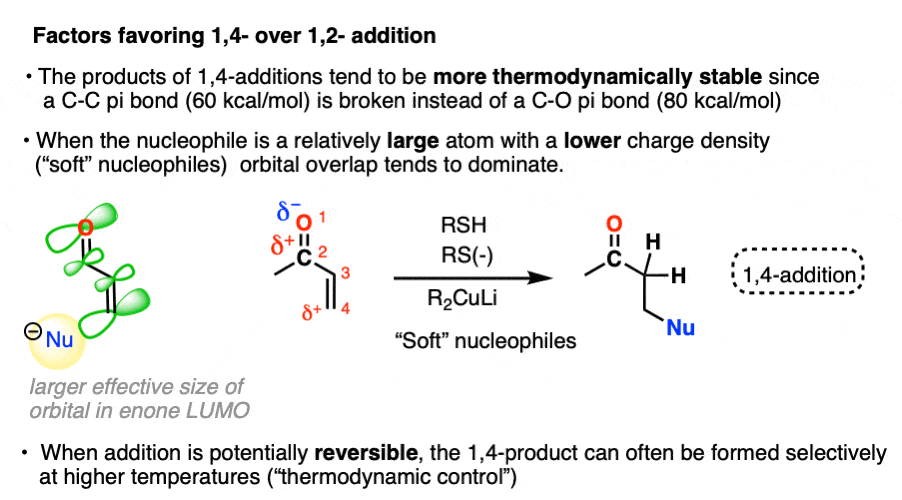
注5。在Huckel分子轨道理论,每个π分子轨道被描述为一个2 p在碳原子轨道的线性组合,相关系数c在每个碳贡献的大小。(每一个碳不等于)
测试你自己!
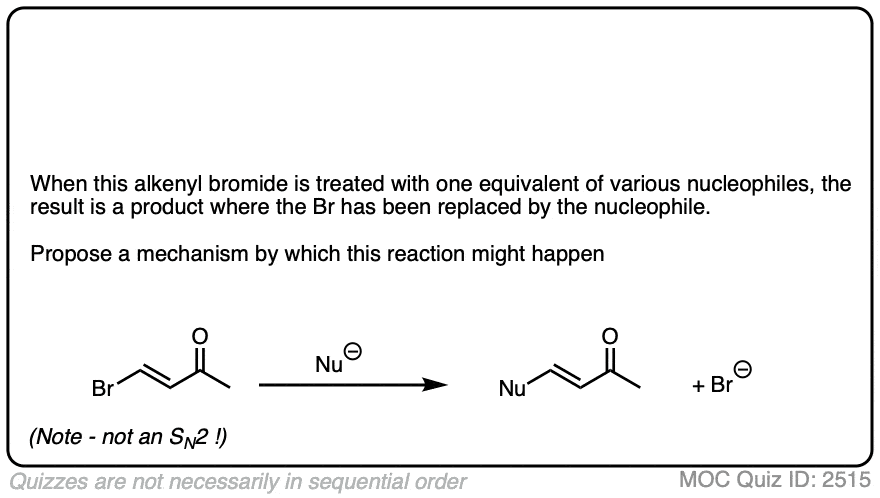 点击翻转
点击翻转
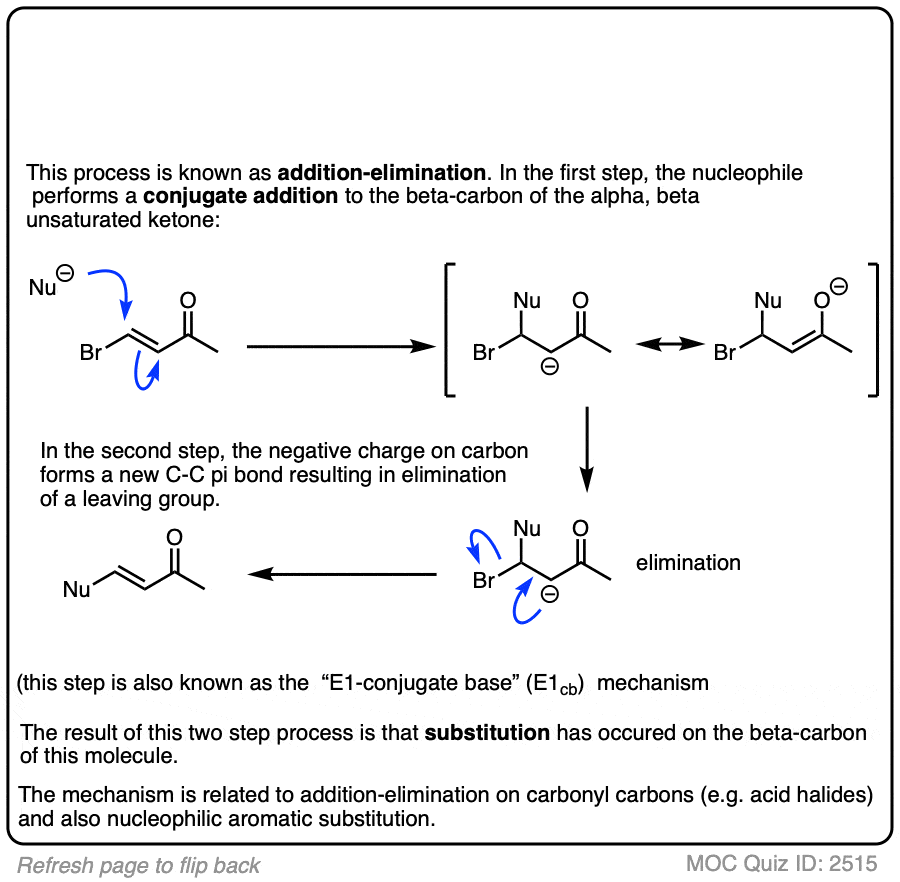
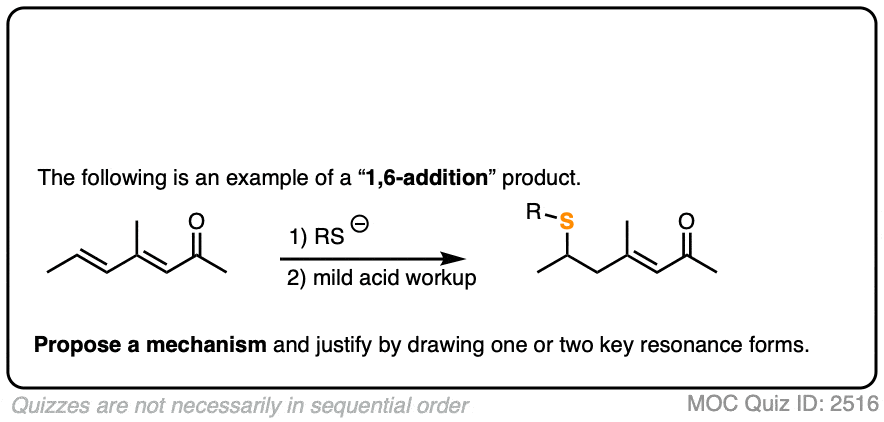 点击翻转
点击翻转
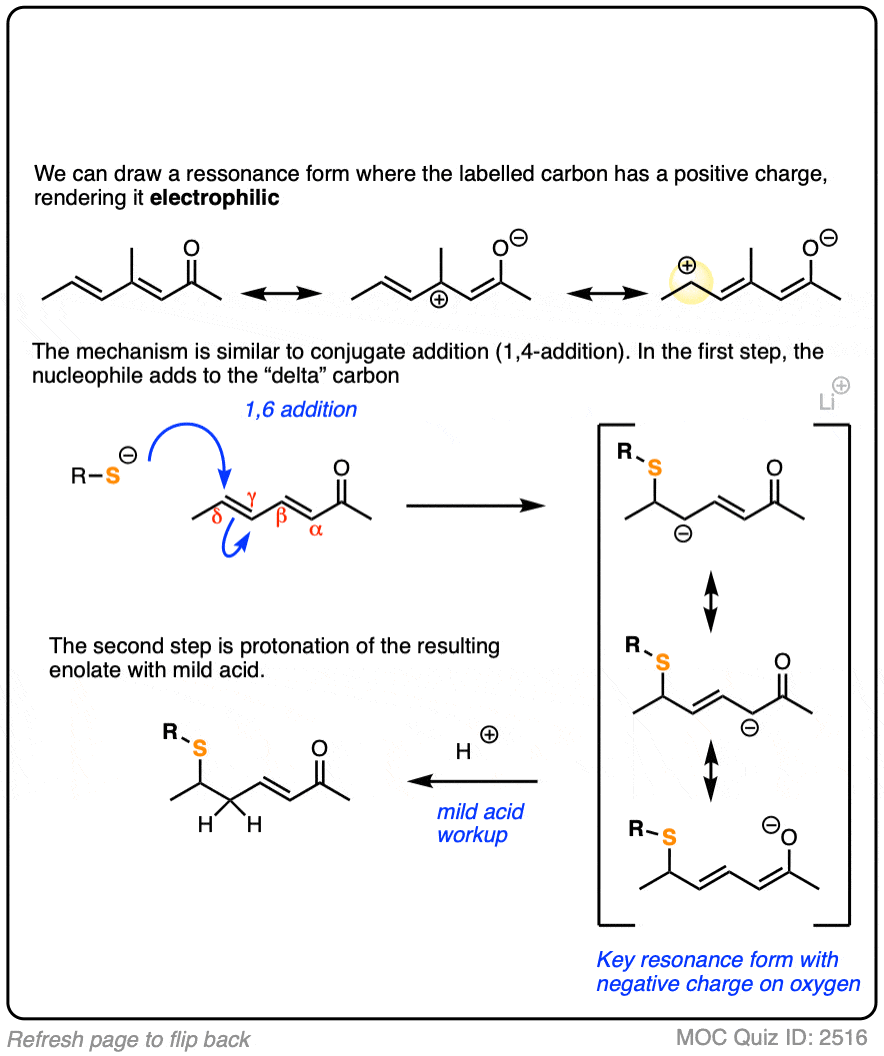
(高级)引用和进一步阅读
- Ueber死除了冯Natriumacetessig量和Natriummalonsaureathern吧台Aethern ungesattigter Sauren
答:迈克尔,j . Prakt。化学。1887年35(1),349 - 356
DOI:10.1002 / prac.18870350136
原始论文亚瑟迈克尔的碳亲核试剂,b-unsaturated系统。注意,即使迈克尔是美国塔夫茨大学的化学家(见论文的结尾),这仍然是用德语写的,发表在德国自德国化学期刊》杂志上是最好的。 - 迈克尔反应
伯格曼,e d;金斯伯格,d;Pappo, R。反应。1959年,10,179年
DOI:10.1002/0471264180. or010.03
经典回顾迈克尔反应。这个年底也有详细的实验程序,类似于您可能会发现什么有机合成。 - (R) 3-phenylcyclohexanone
Makoto Takahashi, Tamio Hayashi Takaya义明和小笠原群岛山正
Org。Synth。2002年,79年,84年
DOI:10.15227 / orgsyn.079.0084
如果使用手性路易斯酸,然后不对称1,4-additions也是可能的。的的或y underlying why certain nucleophiles or Lewis acids prefer 1,4 or 1,2 addition is “硬软酸碱理论”或HSAB。这是由r·g·皮尔森在1960年和非常有用,因为它允许化学家快速和定性确定基于其分子或离子的反应极化率。 - 硬链接和软酸和碱
拉尔夫·g·皮尔森
美国化学学会杂志》上1963年,85年(22),3533 - 3539
DOI:10.1021 / ja00905a001 - 酸和碱
拉尔夫·g·皮尔森
科学1月14日1966年:卷。151年问题3707年,页172 - 177
DOI:10.1126 / science.151.3707.172 - 硬和软酸和碱,HSAB,第1部分:基本原则
拉尔夫·g·皮尔森
《化学教育1968年,45(9),581年
DOI:10.1021 / ed045p581 - 硬和软酸和碱,HSAB,第二部分:基础理论
拉尔夫·g·皮尔森
《化学教育1968年,45(10),643年
DOI:10.1021 / ed045p643 - 硬软酸基地(HSAB)原理和有机化学
Tse-Lok何
化学评论1975年,75年(1),1 - 20
DOI:10.1021 / cr60293a001 - Chemoselectivity有机金属反应:HSAB评价
Tse-Lok何
四面体1985年,41(1)、3 - 86
DOI:10.1016 / s0040 - 4020 (01) 83470 - 0
引用# 6和# 7覆盖HSAB理论有机化学的特定应用程序,展示了特定的反应机制的基础上可以解释这一理论。 - 从头开始研究导致更大的理解HSAB原则
Pratim k Chattaraj和保罗v . r . Schleyer
美国化学学会杂志》上1994年,116年(3),1067 - 1071
DOI:10.1021 / ja00082a031 - 告别HSAB治疗两可的反应
博士教授。赫伯特·迈尔,马丁Breugst,阿明r . Ofial博士
《应用化学国际版英文2011年,50(29),6470 - 6505
反对意见HSAB教授娃:“两可的反应的预测软硬酸和碱的概念失败在大多数情况下,必须抛弃。本文提出另一种方法是合理化的区域选择性两可的系统区分之间的动力学和热力学产品控制以及反应继续进行,没有活化能。马库斯定性理论的预测能力。” - 使用手性亚胺不对称的迈克尔加成反应
吉恩·德安杰洛,迪迪埃Desmaele,弗朗索瓦丝杜马斯,Andre Guingant Vedejs E。
四面体不对称1992年,3(4),459年
DOI:10.1016 / s0957 - 4166 (00) 80251 - 7
迈克尔反应也可以是不对称的;如果你有一个手性亚胺代替羰基,那么立体选择1,4-addition是可能的。 - 的拆分Organocatalytic 1, 4-Addition富苯α,β-Unsaturated醛
尼克·a·帕拉斯和大卫·w·c·麦克米伦
美国化学学会杂志》上2002年,124年(27),7894 - 7895
DOI:10.1021 / ja025981p
这是一个现代转折之前由麦克米伦教授引用,有机化学作出了重要贡献。本文表明,不对称迈克尔增加可以通过手性亚胺中间体生成手性亚胺原位使用手性胺催化剂。这个概念很简单和优雅。
评论
评论部分