醇盐的SN2反应与烷基卤化物离子给醚(威廉森合成)
描述:烷基卤化物(或甲苯磺酸盐)与烷氧基离子反应形成醚。这个反应叫做威廉森醚合成。
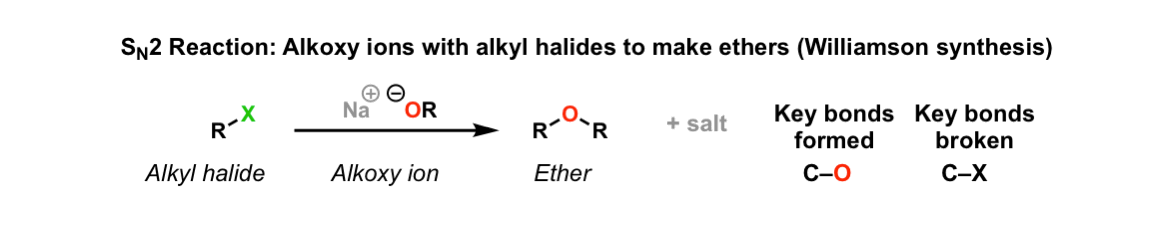
注:X是一个卤化物(Cl, Br)或磺酸盐(OTs OMs)。烷氧基上的抗衡离子离子可以是任何碱金属(例如Li Na, K)
例子:
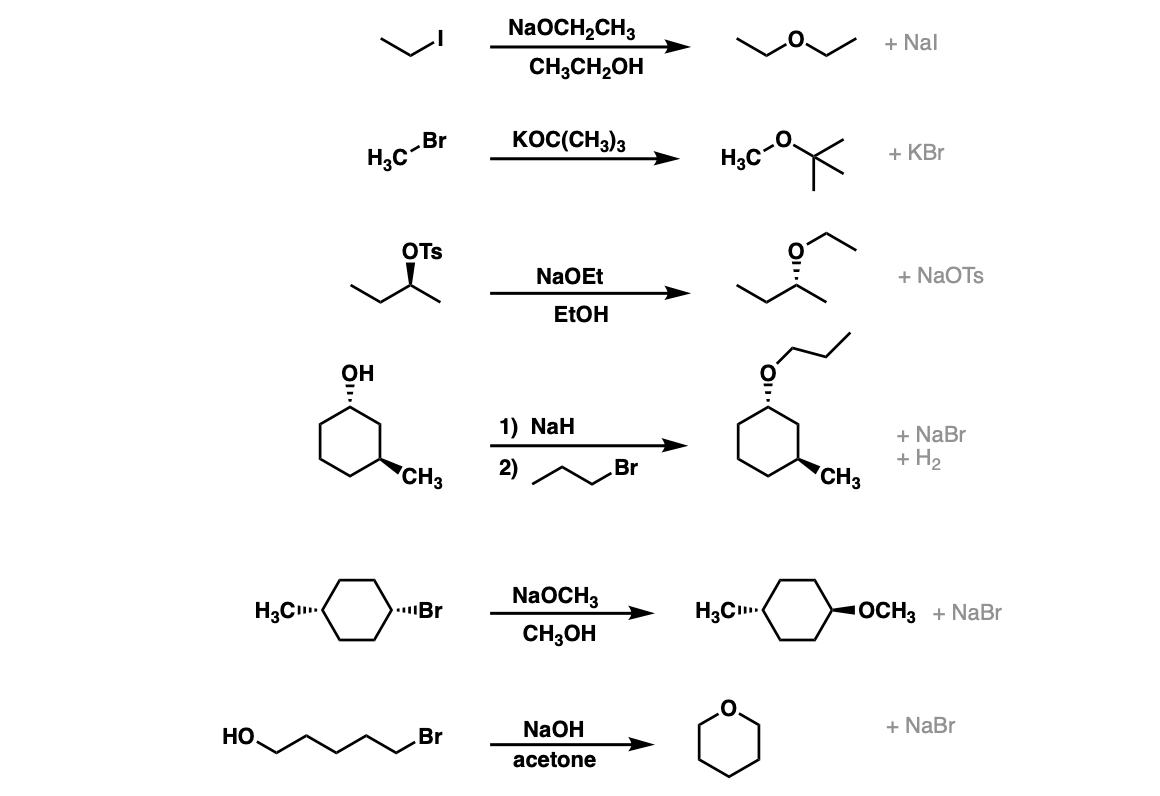
注:注意,因为这是一个SN2反应和收益通过背后攻击,会有反转的配置碳(注意最后两个例子)。溶剂通常是最好的选择共轭酸的醇盐。
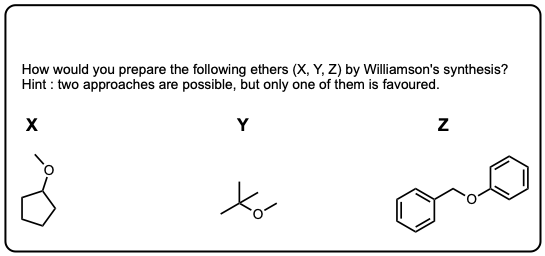
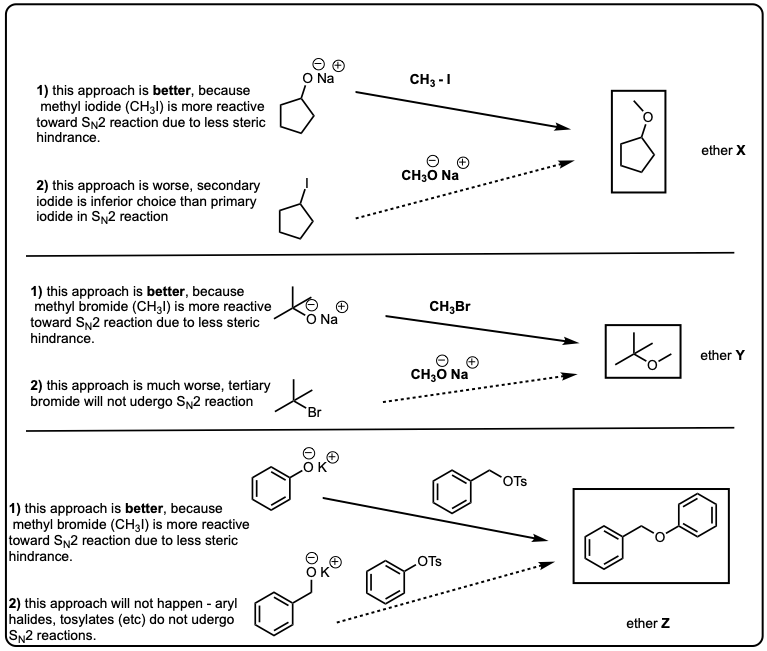
注意,在这第二个例子醚很难使相反的方向(CH3O——攻击三级烷基溴化)SN2反应不工作在高等教育中心。
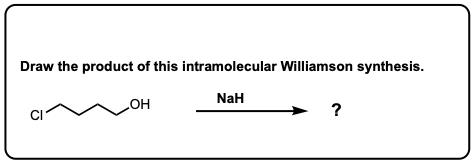
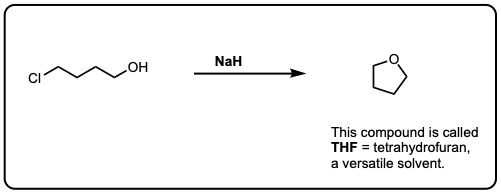
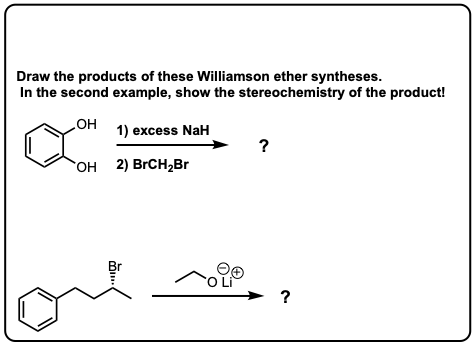
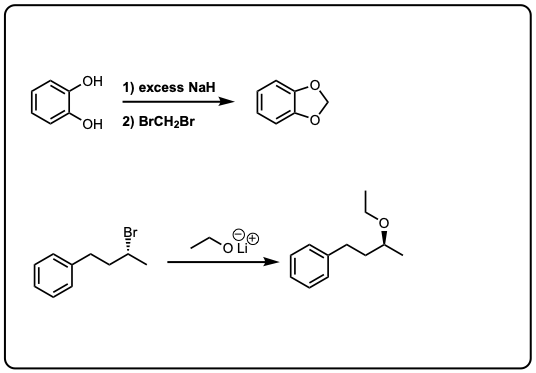
4显示了一个例子与不给去质子化醇盐其次是增加的烷基卤化物。第六是一个例子分子内的威廉姆森醚合成!当心这些类型的例子是很常见的考试问题。
机制:在SN2反应的亲核试剂(RO)攻击的碳好离去基团,形成一个切断债券和打破C-Br债券(步骤1,箭头a和B)。
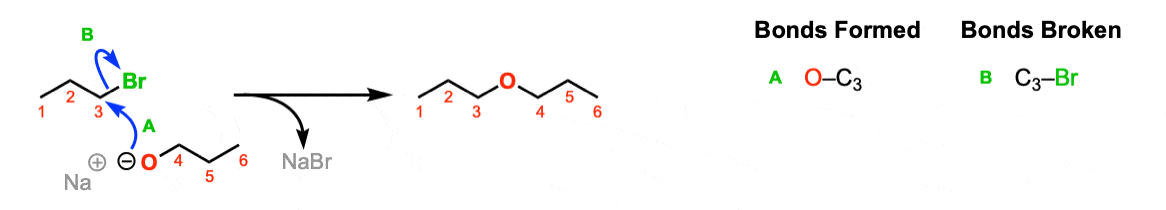
注:同样,Na(+)并不重要,它只是一个旁观者。
测试你自己!
 点击翻转
点击翻转
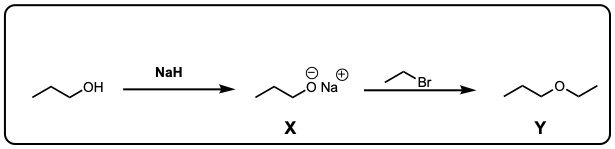
 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
(高级)引用和进一步阅读:
- XLV。ætherification理论。
亚历山大·威廉姆森(1850),伦敦,爱丁堡和都柏林哲学杂志,和科学期刊,37:251,350 - 356,
DOI:1080/14786445008646627
原来的威廉姆森纸。 - Equilenin 3 -苄醚
m . Hoehn克利福德·r·多恩,伯纳德·a·纳尔逊
《有机化学》杂志上1965年30.(1),316 - 316
DOI:10.1021 / jo01012a520
本文的一个反应是一个典型的威廉姆森的保护反应酒精在dehydroestrone苄醚,使用苄氯。 - 总合成(+)7-deoxypancratistatin:一个激进的环化方法
斯坦顿·加里•e .凯克McHardy,杰瑞·a·聪聪
美国化学学会杂志》上1995年117年(27),7289 - 7290
DOI:1021 / ja00132a047
在现代有机合成中,用于威廉姆森反应保护醇反应的底物。常见的保护组织包括methoxymethyl(妈妈)和2-methoxyethoxymethyl (MEM)。妈妈保护工作在这个由凯克教授和同事总合成。
实际的例子:
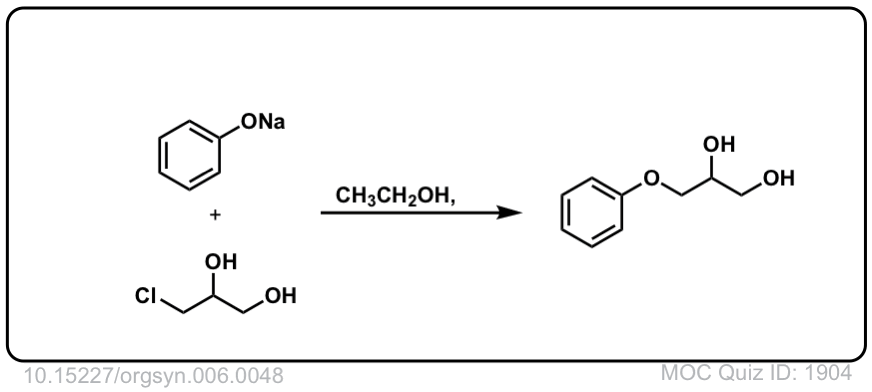
Org。Synth。1926年,48
链接DOI: 10.15227 / orgsyn.006.0048
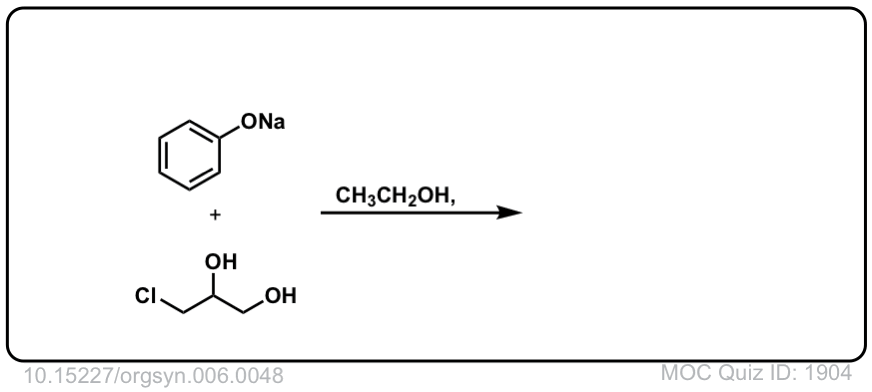 点击翻转
点击翻转
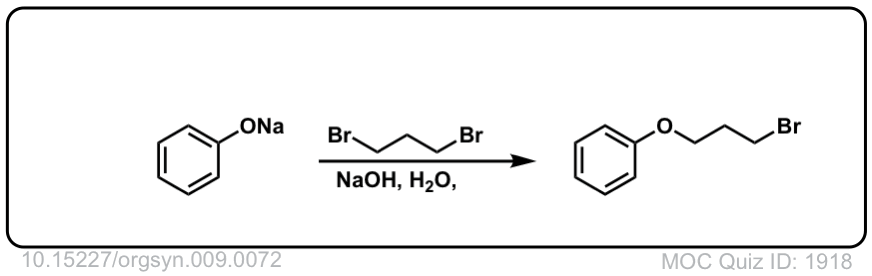
Org。Synth。1929, 72
链接DOI: 10.15227 / orgsyn.009.0072
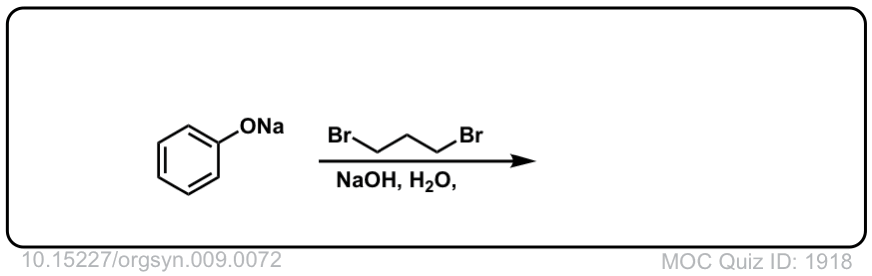 点击翻转
点击翻转
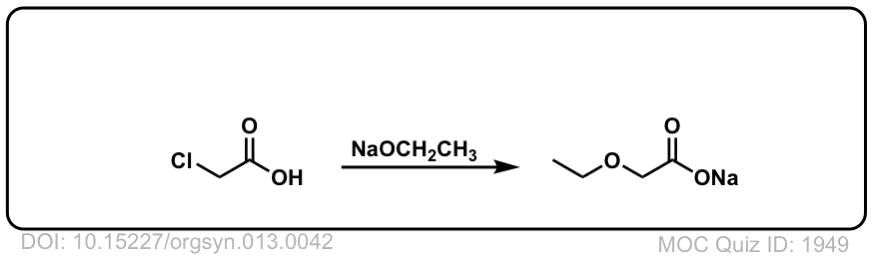
Org。Synth。1933年,13日,42
链接DOI: 10.15227 / orgsyn.013.0042
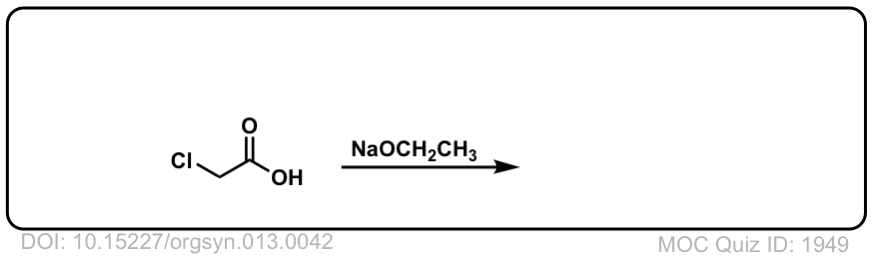 点击翻转
点击翻转
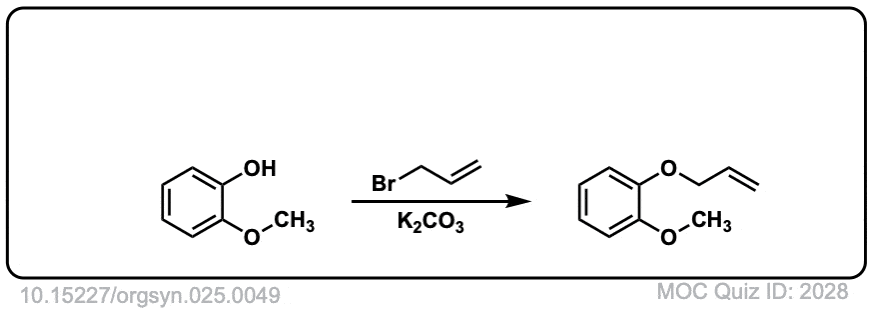
Org。Synth。1945年,25岁的49
链接DOI: 10.15227 / orgsyn.025.0049
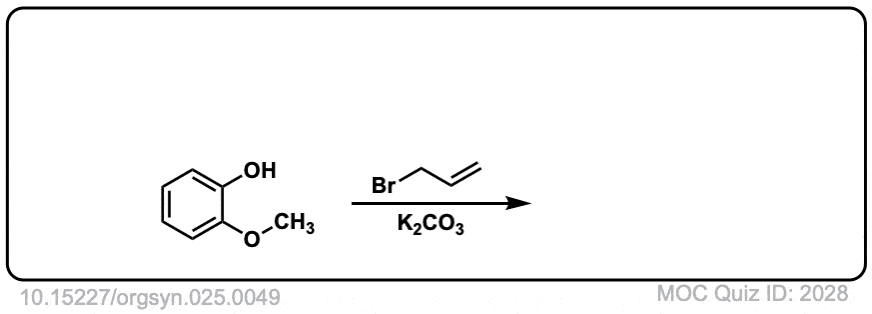 点击翻转
点击翻转
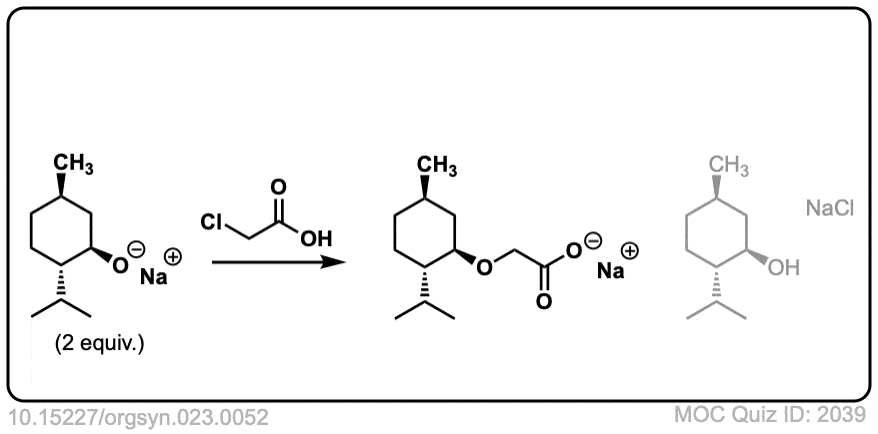
Org。Synth。1943年,23岁,52岁
链接DOI: 10.15227 / orgsyn.023.0052
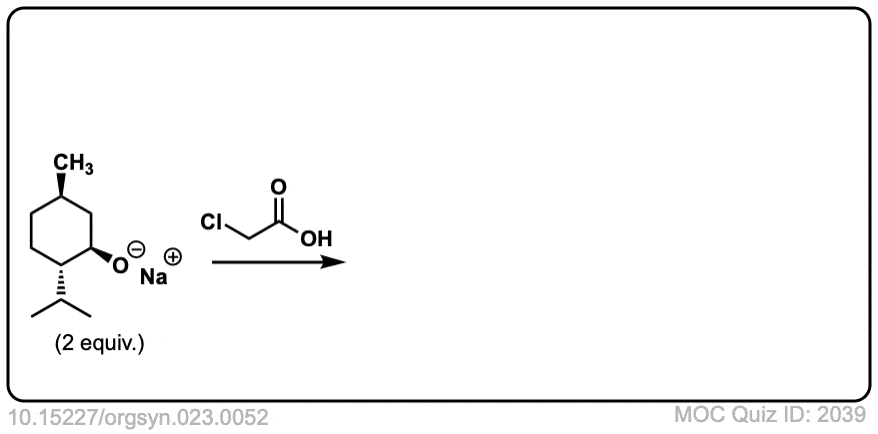 点击翻转
点击翻转
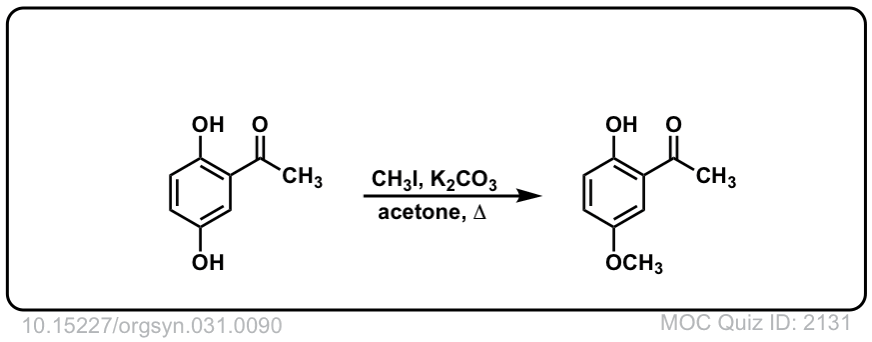
Org。90年Synth。1951年,31日
链接DOI: 10.15227 / orgsyn.031.0090
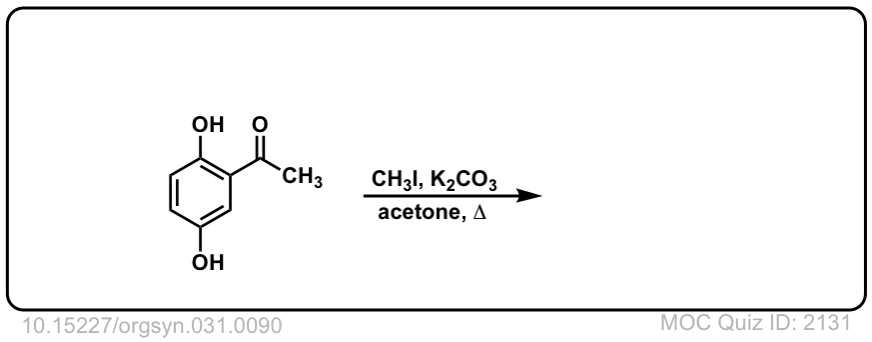 点击翻转
点击翻转
这个反应形成烯烃,以防发生消除?
当然可以,尤其是二次烷基卤化物!我试图强调的形成醚在二级烷基卤化物但我应该注意,我不确定收益。
为什么不e1发生naome和二级溴烷烃链群吗?为什么这个进行替换如果naome也可以成为一个不受阻碍的基础吗?
E1与二溴不是一个选择。损失给碳正离子不会发生没有显著热量。另一方面,二溴,E2是一个真正的问题要注意。取代反应可能会伴随着消除产品(E2)
如果我们使用烯丙基陈词滥调
烯丙基溴化物工作很好!
E2消除时青睐atacking alkoxideion三级但willamsons合成的sn2 rxn青睐在三级醇盐离子的存在怎么可能soooon回复我
在上面的示例中烷基卤化物CH3I和消除是不可能的。
附加在最后一个示例(烷基苯)亲核试剂的方法严重阻碍了所以进行最终产品的反应如何? ?
这不是真的阻碍了。苯是平的。苄基的职位也异常活跃,因为芳香π体系稳定部分正电荷的过渡状态。
rxn你能告诉我如果我使用第二卤化钠醇盐作为我想让一个烯烃的但是我想知道rxn吗
使用强碱,最好是酒精KOH
我怎么找出哪些反应会给更高的收益率?
考虑你是否愿意做SN2主要卤代烷或叔烷基卤化物。
E2为什么不出现在示例2相反吗?
它可能会发生。我刚刚展示的例子如果威廉姆森发生。
我有一个问题。将下列反应的顺序与氯甲烷nuclophiles:
(一)H3C-O ^ - Na +
(B) H5C2-O ^ - Na +
(C) (H3C) 2-CH-O ^ - Na +
(D) (H3C) 3-C-O ^ - Na +
正在改变的关键变量是什么你从H3C-O (-) Na + (CH3) 3-CO(-)钠(+)?你觉得会反应的机制?这些反应敏感类型的因素是什么?
你好,伟大的工作!
我有一个小疑问,虽然。如果叔卤代烷,反应将遵循SN1机制而不是SN2,因此将形成碳正离子。
Q1)将反应不继续给我们一个醚?
Q1 Q2)我的老师的回答是没有。他说,一个碳正离子总是与碱反应给烯烃。是真的吗?
提前谢谢!
你的老师是正确的,E2机制
伟大的工作。你想告诉过三级衬底工作吗
叔醇盐主要或甲基卤化物,是的。叔卤,从来没有。
它可以执行消除反应?
醇盐和二次烷基卤化物,消除反应(E2)将会非常普遍。
如果你从一个醚,并试图确定哪些需要原料,它的离去基卤化物你使用吗?
那绝对是重要的。由于反应是SN2,你想设置的反应,这样你的烷基卤化物(最好)初选。你当然不想让SN2叔烷基溴化工作。
哦,是一个醇盐离子吗?
不,这是一个氢氧根离子。CH3O -醇盐离子的一个例子。
他不需要解释为什么SN2:)
当卤组叶子,如果烷氧基离子不atake同时,你会留下一个主carbo-cation。这些都是非常不稳定的,因为你只有一个碳给主负责。如果你有两个更多的碳与碳卤,你可以有一个SN1反应,因为周围的碳三级carbo-cation将estabilizing正电荷。
我希望我讲清楚了。我葡萄牙语:)
u dnt解释为什么反应是发生在sn2方式。
真的,虽然这是一个相当大的课题。bdapp平台这里,注意,它最适合初级(和在一定程度上辅助)卤代烃。
在氯化苄反应和醇盐虽然主要卤,但形成的碳正离子反应(如果发生在Sn1方式)是高度稳定的,因为它是共振稳定benzyllic碳正离子,但即使在这种情况下,我们说它的Sn2。为什么是这样呢?
在缺乏路易斯酸,电离的氯化苄基的会相对缓慢。半衰期大于几个小时在室温下。你没有指定溶剂,但例如如果你离开PMBCl在板凳上一夜之间,它进入垃圾由于这个过程。
然而,如果一个醇盐(带负电荷的氧气)添加到氯化苄的直接反应,亲核试剂与主卤会多,快得多。反应在几分钟内。