贝克曼重排
描述:贝克曼重排是肟的反应,可以产生酰胺或腈,取决于起始材料。(酮衍生的肟酰胺;由醛衍生的肟提供腈)
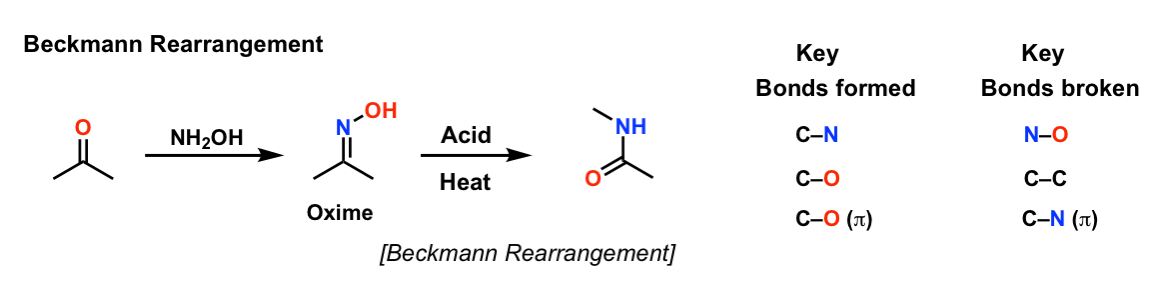
注:注意,第一步(肟的形成)技术上不属于贝克曼重排。贝克曼反应是肟与酰胺的重排反应。这通常是通过将肟氧转化为氧来实现的离去基团,然后是热量,这导致一个烷基(或氢化物)位移,破坏弱的N-O键。第二步是用水捕获碳(形成酰胺),或者,如果发生氢化物转移,氮的脱质子化产生a腈.
例子:
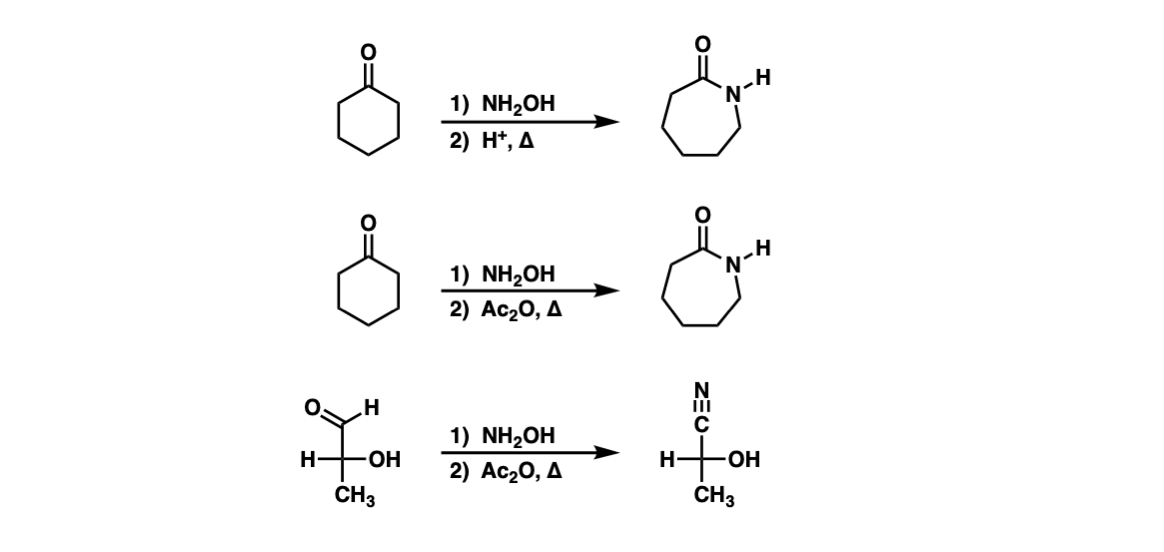
注:贝克曼重排是通过将肟中的氧转化为商品来实现的离去基团,然后加热。在第一个例子中,处理酮与NH2OH形成肟,然后在第二步,用酸加热导致贝克曼重排。在第二个例子中,肟形成后,用Ac2O处理(将肟氧转化为醋酸盐,更好离去基团比OH),然后加热。第三个例子是肟的贝克曼重排醛,结果是a腈.
机制:这个过程的第一步是从醛或酮,其发生顺序类似于亚胺和水螅带的形成。在第一步中,氮加入羰基碳(步骤1,箭头A和B),接着是质子转移(步骤2,箭头C和D)。然后,孤对氮取代氢氧根消去反应(步骤3,箭头E和F),最后氮被碱脱质子(步骤4,箭头G和H),生成肟。
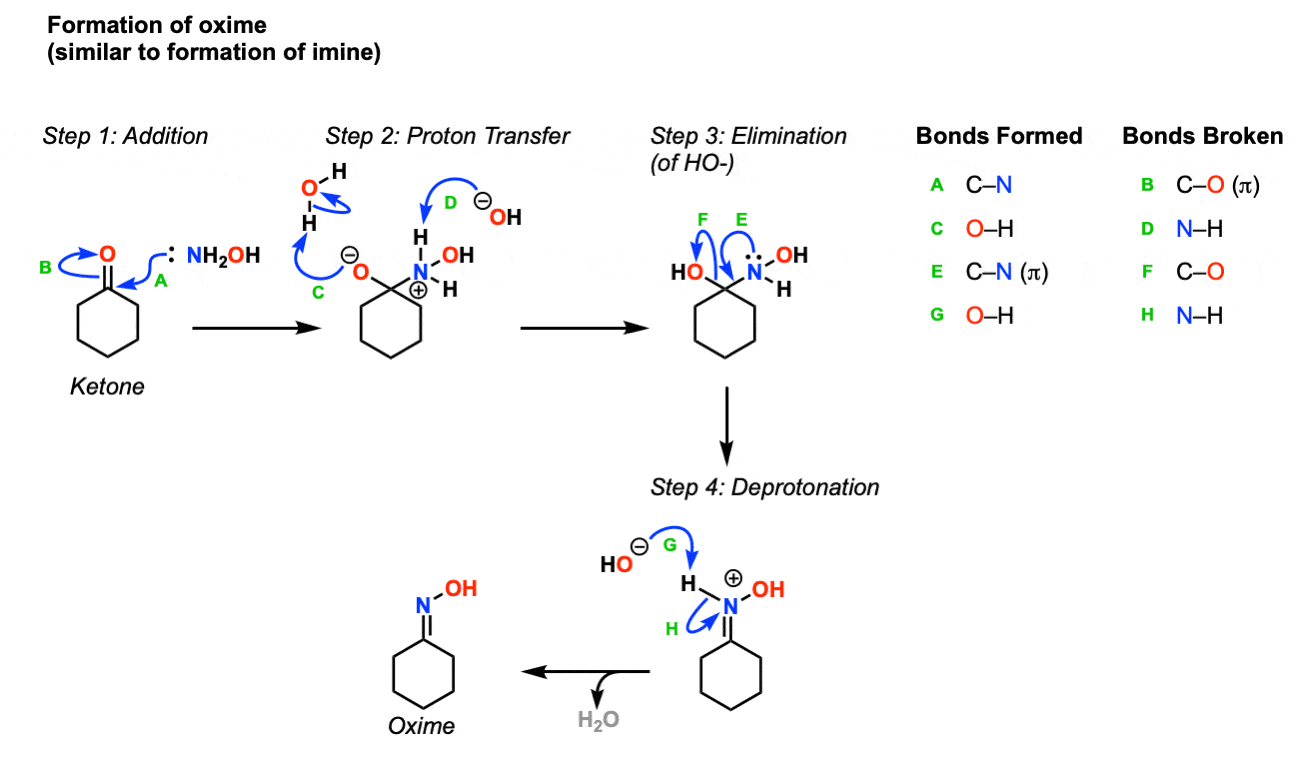
在贝克曼重排步骤中,肟氧被酸质子化(步骤1,箭头A和B)。这导致了OH2+的形成,这是一个更好的离去基团比OH。现在是关键的一步,重排。碳碳键断裂,迁移到氮上,形成一个新的碳氮键,取代水离去基团(步骤2,箭头C和D)。这形成一个自由的碳正离子,然后被水攻击(步骤3,箭头E)。带正电荷的氧被碱脱质子(步骤4,箭头F和G),形成酰胺的互变异构体。步骤5和6表示“互变异构”。首先,氮发生质子化(步骤5,箭头H, I和J),接着是氧的脱质子化(步骤6,箭头K和L),这就产生了酰胺。
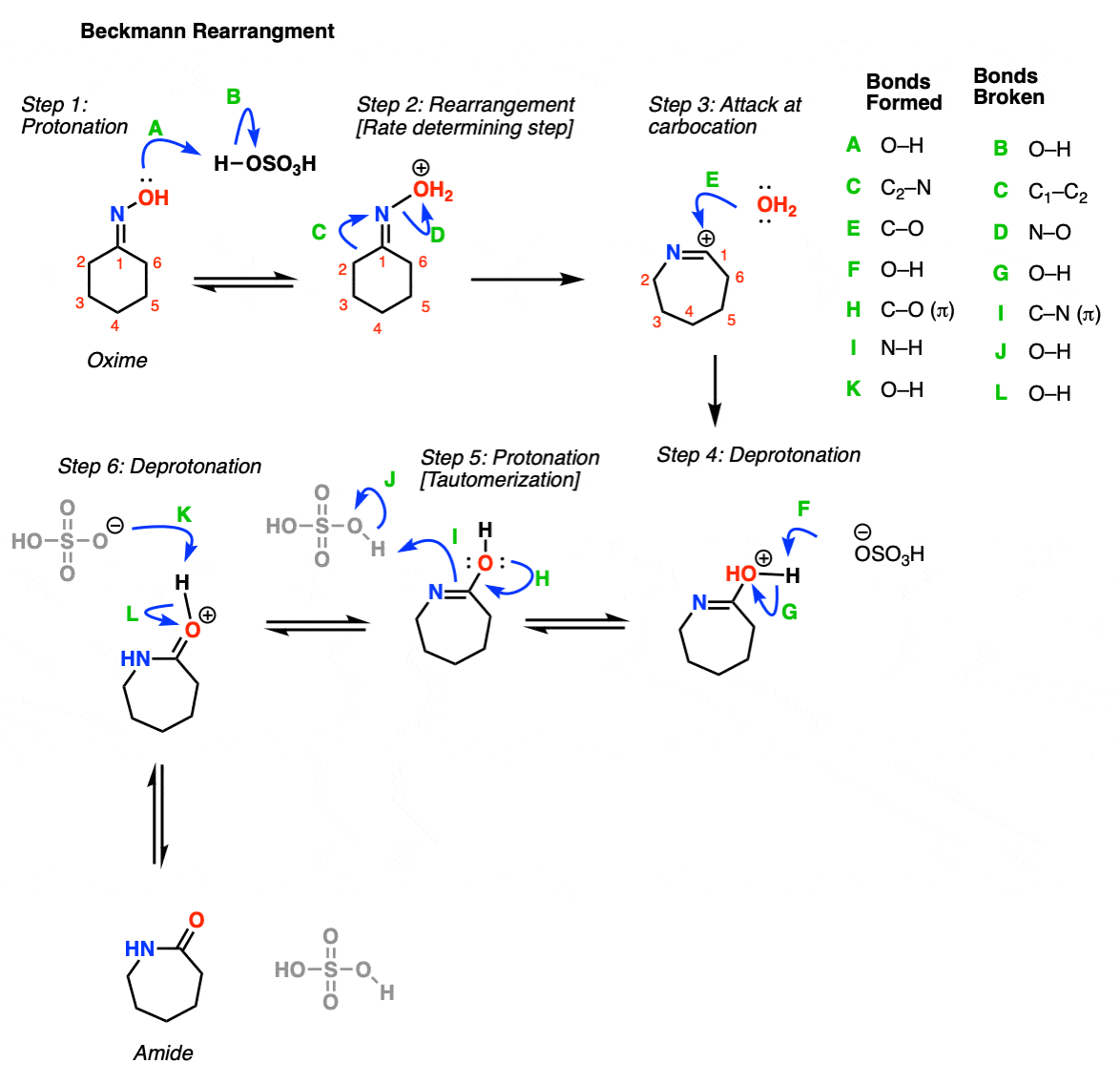
注:关键重排步骤(步骤2)与其他重排反应(如氢化物和化学反应)中的重排步骤相似烷基以及Curtius, Schmidt和Wolff的重排)。这是一个烷基移位,伴随着失落离去基团.
酸的作用是使氧气更好离去基团;O-N键很弱。
请注意,尽管HOSO3-在这里被显示为碱基,但其他物种很可能也可以作为碱基。此外,肟形成中的“质子转移”步骤可以显示为两个不同的步骤,而不是一个步骤。
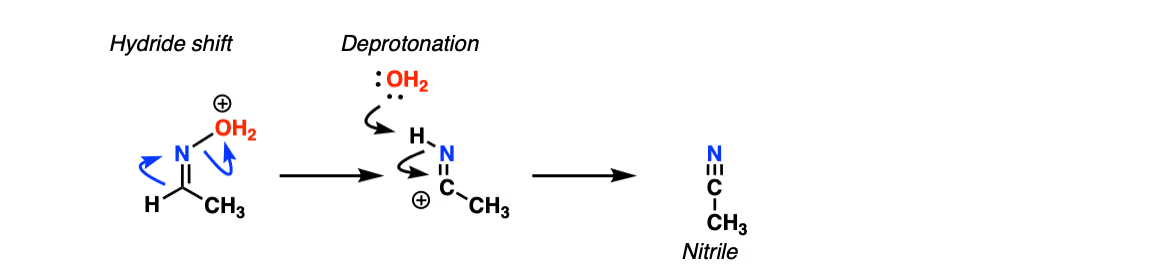
为腈形成的关键步骤是氢化物转移,然后是氮的去质子化。这就给出了腈.
(高级)参考资料和进一步阅读:
- Zur Kenntniss der异硝基硫化物
恩斯特贝克曼
的误码率。1886,19(1), 988 - 993
DOI:10.1002 / cber.188601901222
恩斯特·贝克曼关于肟重排成酰胺的原始论文。 - ε-BENZOYLAMINOCAPROIC酸
C. Eck和C. S. Marvel
Org。Synth。1939,19, 20
DOI:10.15227 / orgsyn.019.0020
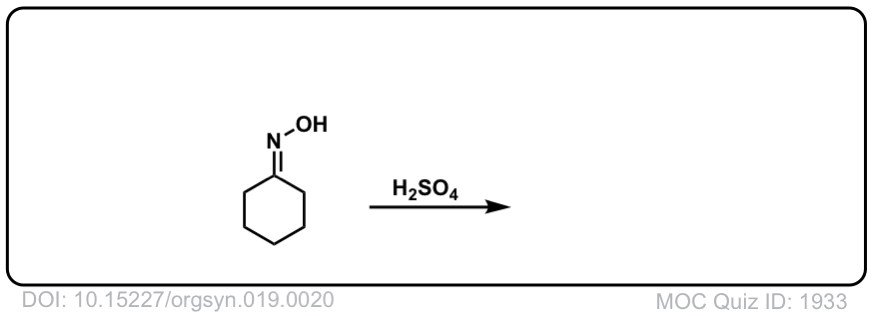
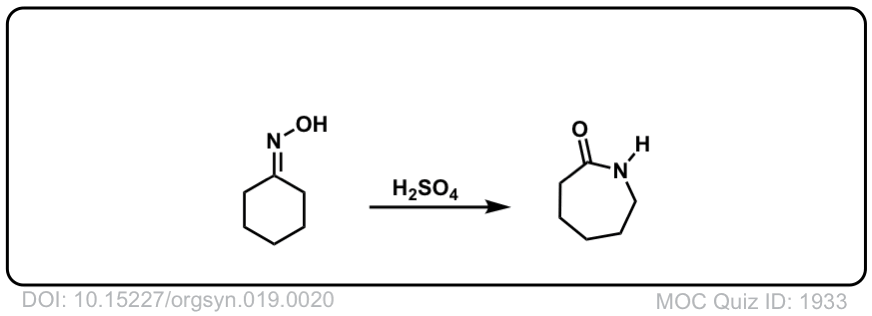
本参考文献中的B部分是环己酮肟的经典和标准贝克曼重排有机合成,一个可重复和独立测试的有机化学实验实验室程序的来源。 - 五氧化二磷-甲烷磺酸。方便替代聚磷酸
菲利普·e·伊顿,格伦·r·卡尔森,詹姆斯·t·李
有机化学杂志197338(23), 4071 - 4073
DOI:1021 / jo00987a028
这篇由P. Eaton教授(因首次合成cubane而闻名)撰写的论文描述了P. Eaton的使用2O5-MSA作为浓硫酸或PPA(聚磷酸)的替代品,后者通常用作贝克曼重排的介质。
- 贝克曼重排的动力学与机理。
b·琼斯。化学评论194435(3), 335 - 350
DOI:10.1021 / cr60112a001
一篇早期综述,描述了为理解贝克曼重排机制所做的工作。 - 微孔分子筛上肟类Beckmann重排分子机制的建立
安娜·B. Fernández,梅赛德斯·博洛纳特,特蕾莎·布拉斯科,阿韦利诺·科玛
Angew。化学。Int。艾德。2005年,44 (16),2370 - 2373
DOI:10.1002 / anie.200462737
贝克曼重排机理的最新工作,使用计算方法和固体核磁共振波谱。
现实生活中的例子:
Org。合成人,1939,19,20
DOI链接:10.15227/orgsyn.019.0020
 点击翻转
点击翻转
关于丁腈的形成,如果用乙酸酐和乙酸钠处理肟(如碳水化合物的Wohl降解反应)会怎样?丁腈是如何形成的?会发生贝克曼重排吗?乙酸酐会使OH成为一个好的离去基吗?
Wohl降解反应:http://en.wikipedia.org/wiki/Wohl_degradation
这本质上也是贝克曼重排。结果是肟上形成了OAc,然后H-从碳原子转移到氮原子上这就破坏了N-O键。在那之后,氮氢的脱质子反应就形成了三键。
在一个贝克曼重排问题中,给出的试剂是NH2OH。HCl, PCl5和热。PCl5能做什么?
和酸的作用一样。让OH变成了一个好的离去基。
SOCl2也起同样的作用吗?
你可以用代替酸(H2SO4,HCl)——PCl5, SOCl2, BF3, POCl3, SO3。这些都有相同的功能。
甚至PCl3, PCl5, SOCl2, Al2O3和P4O10也可以在这里工作!
你能不能让机甲用PCl5代替酸
在这种情况下NaHCO3呢:http://imgur.com/5JoNRNu(如果图像未加载,则在4-chloroaninline上)
谢谢你!
Brad, NaHCO3是用来中和共轭酸的。
我们可以用HN3 / H+吗?
这就是施密特反应。https://en.wikipedia.org/wiki/Schmidt_reaction
P2O5在Beckmann重排中起脱水作用吗?
是的,这可以。它仍然在激活氧,使它成为一个好的离去基。
在发生环膨胀的反应中,它的区域选择性是否和bv氧化反应一样?我的意思是,在我的印象中,扩张环时添加的氧通常会添加到更取代的一侧(尽管这可能也不正确)。假设分子允许,NH也会这样吗?
我的具体例子是一个苄基酮,它位于7元环上。但即使只是对概括性的澄清也会令人惊讶。
谢谢你!这个网站是唯一让我在课堂上保持活力的东西,我把它推荐给每个人
在此机制下,酮生成酰胺,醛生成腈?
在这个反应中R1是乙基R2是甲基或者别的什么(R1和R2不一样)哪个R基团发生了移动,为什么?
是的,醛生成腈。在R1和R2的情况下,有不同的迁移能力,这取决于中间3中心2电子键的稳定性。在相关的Baeyer-Villiger反应中,迁移能力为三级>二级,芳基>一级>甲基。请看这篇文章底部的讨论…//m.deriinvest.com/2018/10/08/nitration-baeyer-villiger/
由于基团迁移步骤与Curtius, Schmidt等的相似:醛一定会生成丁腈吗?
如果要迁移的氢不是相对于OH-处于反位,那不是会生成胺的甲酸衍生物吗?
肟可以相互转换它们的立体化学结构(顺式和反式),所以它仍然会生成醛,除非有一些特殊的限制,阻止了这种立体化学结构的采用。
“好的离去基”在这里是什么意思?
什么是好的离去基?好的离去基是弱碱。HO-不是一个很好的离去基,但是一旦你进入AcO(-) H2O等的区域,反应就会很顺利地进行。
我想你错过了一个非常重要的部分(反应的立体化学)——烷基取代基“反式”向氮迁移。
这是一个很好的观点,但是肟可以通过中间的亚硝基来反转它们的立体化学。
为什么羰基中的C原子与羟胺中的氮原子反应,而不是氧原子?你能给我解释一下吗?
氮通常比氧更亲核,当相邻的杂原子(如氧)存在时,氮甚至更亲核。看到//m.deriinvest.com/2018/05/07/nucleophilicity-of-amines/
用NH2OH和它的酸性盐NH2OH有什么区别?盐酸在肟形成中的作用?
没有,但是对于HCl盐,你需要等量的弱碱来中和HCl盐,这样氮上的孤对就能释放出来。
如果肟是由一个不对称的酮合成的,那么哪个烷基grp会迁移?
迁移性与碳正离子稳定性大致相关。
假设2号碳上有一个甲基。哪个碳会进行重排?C2还是C6?谢谢你!
迁移能力随着碳正离子稳定性的增加而增加,所以可能取代的越多。
NH2OH和PCl5是如何形成产品的
所发生的就是PCl5连着了肟的羟基。让它成为一个好的离去基的不同方法。
如果酮和NH2OH反应然后用LiAlH4还原会怎样?
LiAlH4是一把大锤。你不仅可以减少C=N,还可以减少N- o。最终产物是胺。
为什么迁移基团上的吸电子基团会减慢贝克曼重排的速度?真的需要澄清这一点。
迁移能力一般随着碳正离子稳定性的增加而增加。碳正离子的稳定性随着吸电子基团的加入而降低。我们可以把贝克曼的过渡态想象成一个3中心2电子键,它是缺电子的。
如果质子经过3元环或4元环的过渡态,就像你在肟形成机制的第二步(4元环过渡态)中所做的那样,描述分子内质子转移是非常糟糕的做法。你应该把涉及羟胺的两个质子转移步骤描述为质子穿梭。
好点。
你好,
我有一种苯甲醛的衍生物通过羟胺在甲酸和甲酸钠中形成氧基转化为苯腈。我认为甲酸是溶剂,但是甲酸钠的作用是什么呢?
不确定。可能是为了缓冲溶液的酸度因为当pH值过低时,羟胺就会完全质子化而没有足够的亲核性来进行醛的加成。你从盐酸羟胺开始吗?
苯乙酮对贝克曼重排不出n -甲基苯甲酰胺
这是正确的。苯基具有较高的迁移性。和拜耳·维利格一样。请看这篇文章。//m.deriinvest.com/2018/10/08/nitration-baeyer-villiger/