格氏试剂与腈给酮(水解)
描述:格氏试剂将添加一次腈形成亚胺。可以处理水酸亚胺酮。
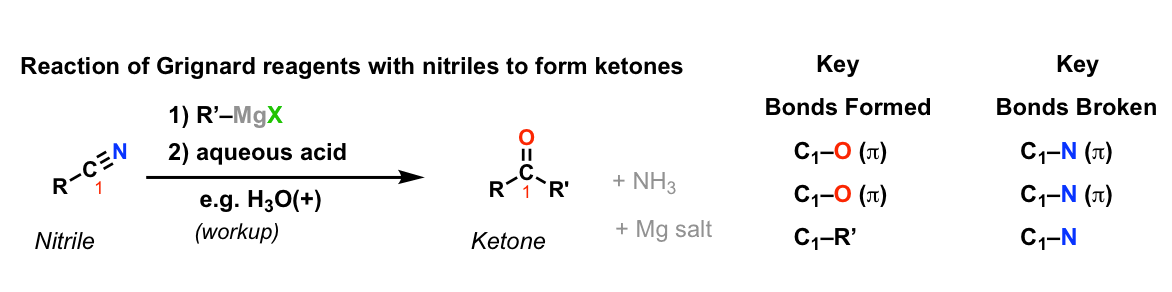
注:
- 第二步的目的是将中间亚胺转化为一个酮。
- 水(H2O)通常是足够虽然水酸(H3O +)更有效。
- X可以Cl, Br或我,取决于如何格氏试剂。
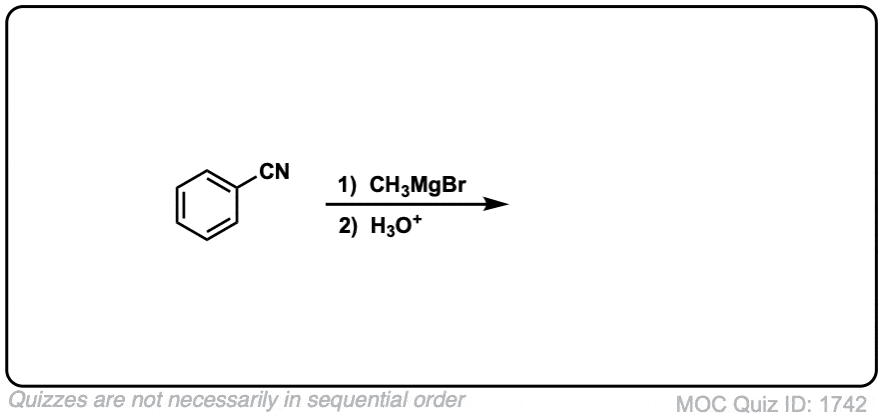
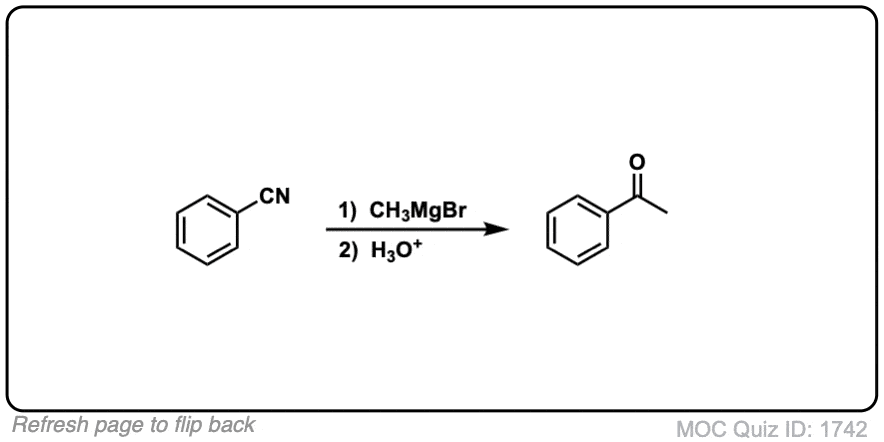
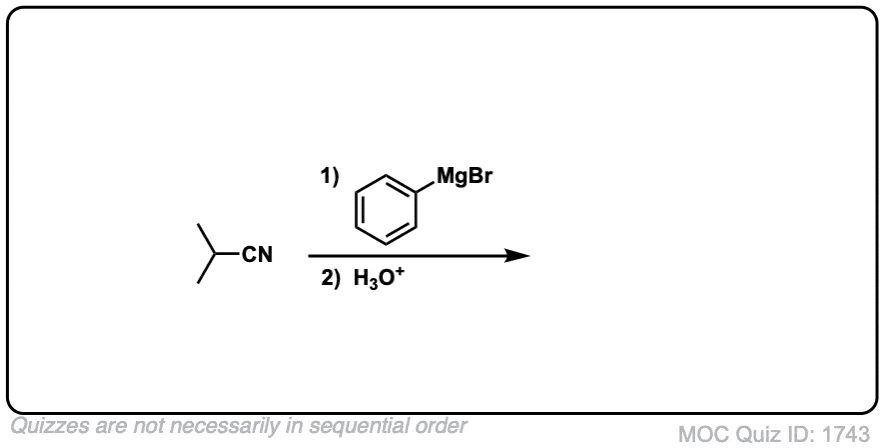
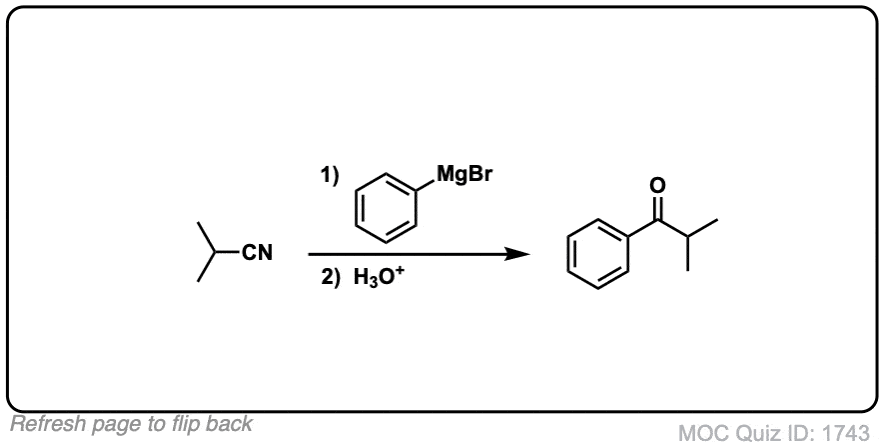
例子:
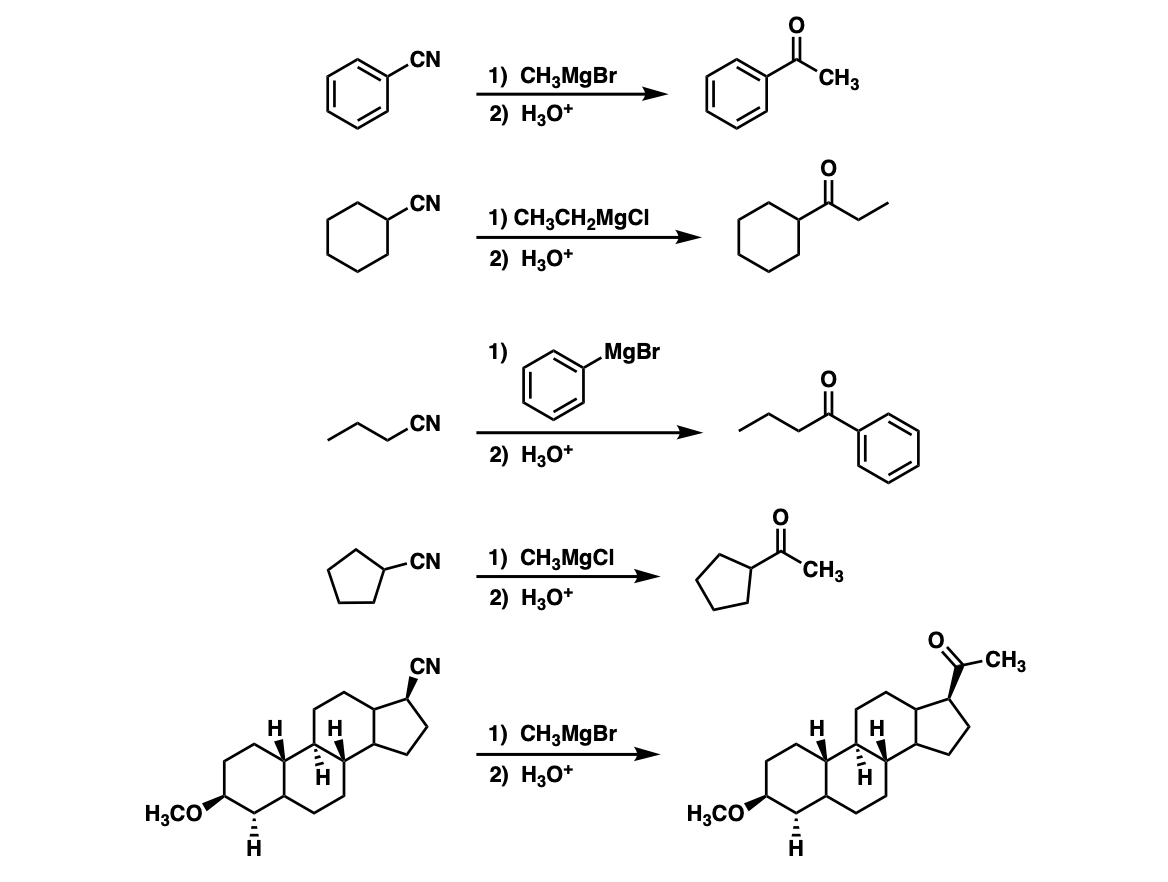
注:第一个反应的产物是一种亚胺,然后水解酮与水(或轻度水酸)。注意最后一个例子(5)——不要分心的巨大分子,只是注意腈!
机制:
格氏试剂添加的碳腈,形成新的碳碳键(步骤1,箭头a和B)。这是稳定的,直到水和酸添加(步骤2,箭头C D)形成亚胺。质子化作用的亚胺氮(步骤3,箭头E和F)导致iminium离子的形成,经历了1,被水的加法(步骤4,
箭头G和H)。这个物种发生质子转移(步骤5中,箭头I和J)允许的损失氨(NH3)在随后的1,2-elimination(步骤6,箭头K和L)。去质子化的羰基氧气与基地(步骤7,箭头M和N),那么结果的酮。
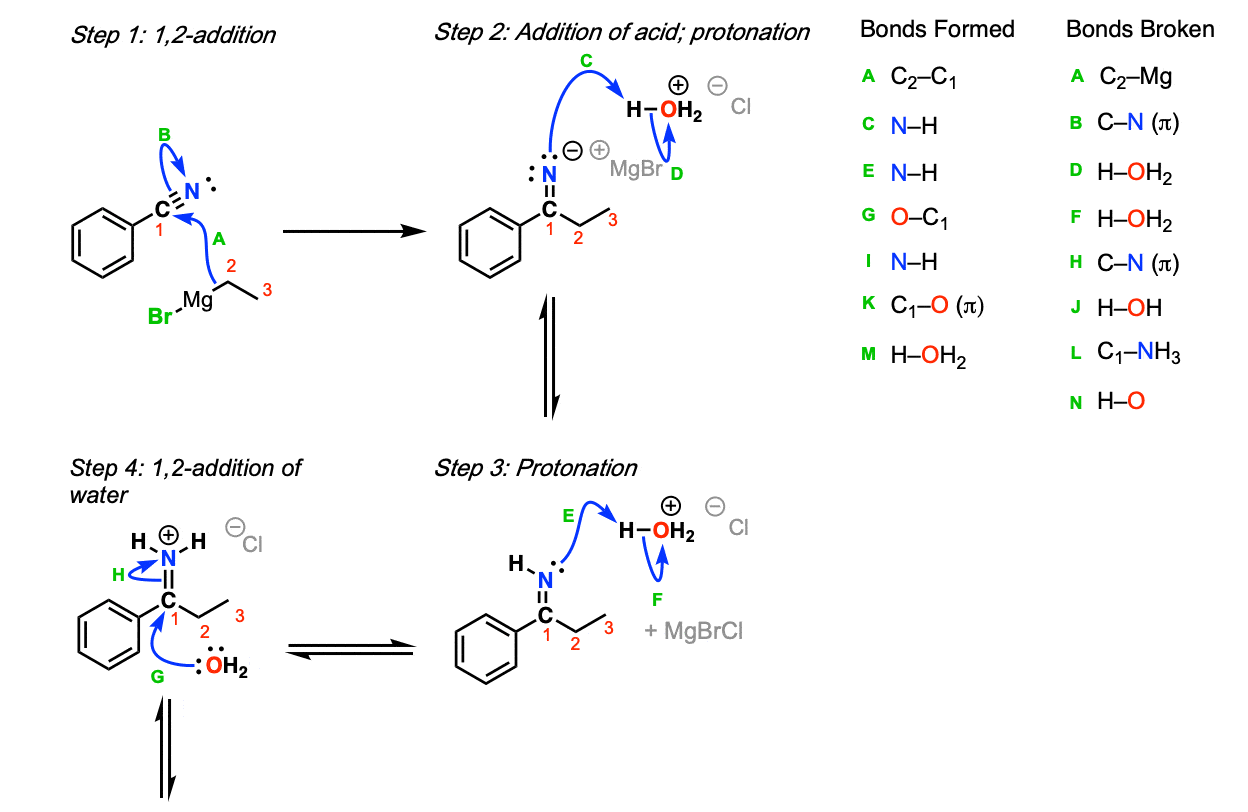
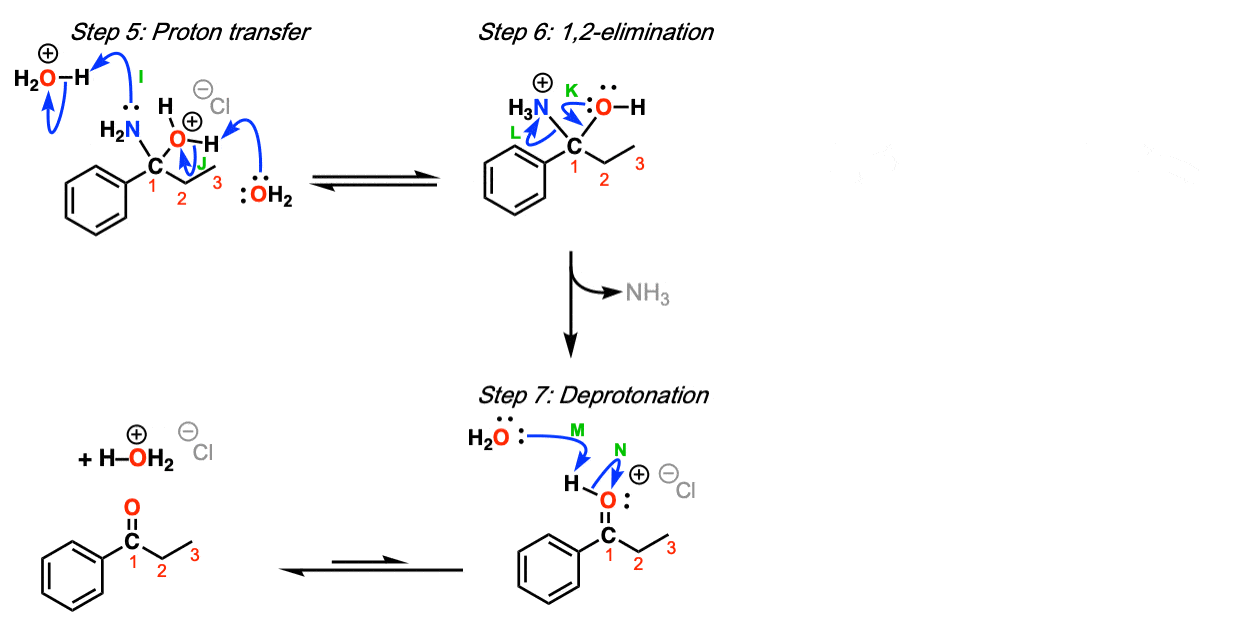
注:
- 步骤2后才发生的酸水。请注意,相当于一个完整的酸来使质子化亚胺是必要的。
- 可以使用其他酸:使用Cl(-)作为抗衡离子——(+)这里是任意的和没有结果的反应除了平衡电荷从水蒸汽(+)。
- 步骤3 - 7亚胺的水解是相同的。
- 其他合理的机制可以对质子转移。
- 其他基地合理可以用来代替水。
- 一个质子化了的亚胺被称为一个“iminium”。
测试你自己!
 点击翻转
点击翻转
 点击翻转
点击翻转
(高级)引用和进一步阅读
- 第一个例子
Kharasch m . s .;Reinmuth, o .格氏反应的非金属物质,新世纪,恩格尔伍德悬崖,新泽西,1954年,页767 - 845 - Effet du de格氏苏尔les苯在反应腈
珀尔塞福涅Canonne乔治•B。Foscolos, Gilles眼肌
四面体的信1980年,155年
DOI:10.1016 / s0040 - 4039 (00) 71400 - 6
使用包含一个相当于的苯醚在格氏反应的溶剂腈在室温下会导致产量的增加相应的酮相比,结果同样的反应醚。 - 有机金属反应机制。十二。methylmagnesium机制溴化苄腈之外
e·c·阿什比Li-Chung。曹国伟,h·m·诺伊曼
美国化学学会杂志》上1973年95 (15),4896 - 4904
DOI:10.1021 / ja00796a022
标题反应的动力学数据显示二阶反应,在格氏试剂和一阶一阶腈。率研究的结果在MgBr补充道2表明,格氏试剂的反应与氰苯发生通过(CH3)2Mg和CH3MgBr物种。 - 格氏试剂与机制腈
c·加德纳情郎
美国化学学会杂志》上的1947年2306年,69 (10)
DOI:10.1021 / ja01202a018
本文是一个早期文献引用这个反应和描述之间的反应动力学研究n-butylmagnesium溴化苄腈,被发现是2nd秩序。 - 铜(I)激活的格氏试剂腈。合成酮亚胺、酮和胺
弗朗茨·j·Weiberth和斯坦·s .大厅
《有机化学》杂志上1987年52 (17),3901 - 390
DOI:10.1021 / jo00226a033
格氏试剂的亲核加成腈,特别是当使用sterically要求组件,由铜(I)盐有效地催化。 - 两倍的有机金属化合物腈:三级Carbinamines向一个访问。
先进的合成与催化,359 (2),179 - 201
Pearson-Long, M . s . M。Boeda F。& Bertus p (2016)。
DOI:10.1002 / adsc.201600727
本文描述了这个反应的一个变体双的有机金属化合物(如格氏试剂或organolithium试剂)腈。
我们得到了一个碳原子或格氏Ch3Ch2MgBr吗
这指的是什么形象?额外的碳排放来自于腈CN。我没有看到一个错误,但是如果有一个错误请让我知道。
测试部分,不应该第一个问题产生苯一侧甲基羰基碳的另一边不是乙?
固定的。谢谢你!
想知道有一个解释涡轮格氏为什么不攻击保罗Knochel腈即使在0学位的工作,也许更复杂的机械化,但我不认为我现在有一个很好的理由。任何想法吗?
我想知道同样的逻辑将适用于胜者的化学、涡轮也将离开硝基江山…
我可以认为你的意思是t-Bu格氏吗?(自动更正化学是一个痛苦)。
不确定。除了腈是最慢的羧酸衍生物和苄腈之外n-BuMgBr出现RT和0。看到的:https://pubs.acs.org/doi/pdf/10.1021/ja01202a018
我想知道t-BuMgBr虽然Schlenk均衡是什么样子。你有点燃Knochel参考的东西?
不确定莎娃但说通常运行< 0°使硝基比腈反应。
你将如何准备从格氏试剂乙腈吗
通常反应另一个方向;与腈格氏反应。
我一直都进行这样的合成。我刚从狂热者不能重复氯胺酮的合成。唯一的区别在于,我买了环戊基溴化镁1 mol / L四氢呋喃的合成。与O-chlorobenzonitrile gingnard试剂反应。
我试过几次但太多在薄层色谱斑点显示。
CuBr添加催化剂,但只会使系统更复杂的产品都没问题。
我想知道的意思加氨与NH4Cl水解反应时。我的反应NH4Cl和盐酸水解。前没有显示任何产品,但第二个shpowed许多薄层色谱斑点。
什么是产品时形成hcn与格氏试剂反应?
HCN是一种酸。你得到当你对待格氏酸?
氧气来自哪里?
氧气来自检查步骤中加入水,水解的酮亚胺。
添加腈格氏时,它应该是溶解在苯和添加滴一个适当的速度控制的事情吗?
一般的溶剂往往用于格氏反应(如四氢呋喃、二乙醚),但根据先进的有机化学第五埃德。3月,p。1216年,用苯作为co-solvent增加产量。在一个预备我发现格氏然后添加了腈迅速在0°C,然后搅拌3 h。有趣的是与腈反应相当慢(近乎即时的酮和醛相比)。双是罕见的。看到这个预科。http://www.orgsyn.org/Result.aspx?ga=na(Org Syn科尔。3,26页)
如果我使用HCN那么RCHO形式吗?
不,H与格氏反应,它将被摧毁。
与末端炔格氏试剂反应形式与氰化氢烷烃但反应烷烃…它不形式。为什么? ? ?
我认为N通常不离开?
如果是质子化了的,那么它就会出现。
这是一个Sn1或Sn2反应吗?
既不。亲核加成(1、2添加)
可能是烷基cynide与两摩尔的格氏试剂反应给烷基胺吗?
你不能。因为这将形成2 -氮就是高度不稳定。这里有另一件更不用说,表单- 1氮首先然后添加水或酸。
将相同的HCN reactin发生或将得到CH4和CH3MgBr烷烃反应?
HCN的将相同的反应发生或H被删除,我们将获得CH4和NCMgBr ?
为什么你不能和另一枚格氏攻击第二次吗?谢谢!
问题是,你基本上有氮两个负电荷,非常不稳定。所以它往往只是做mono-addition。
没有我认为杰瑞德问为什么不酮形成进一步与格氏试剂反应给3度酒精…。如果真的是这个反应消极的方面? ?(如果我们想要得到酮)
酮并不成立,直到添加水,会破坏任何格氏礼物。
我记得亚胺盐腈与格氏试剂反应后生成。有可能两枚格氏和一枚腈形成亚胺盐像R2C-N (MgX) 2 ? ?氮上的负电荷可以稳定镁阳离子? ?
双是罕见的。
如果我不加酸将在亚胺反应停止
特别是如果R是芳香。