酸性的乳沟醚(SN2)
描述:当醚对强酸的存在亲核试剂比如,他们可以给醇类和分开烷基卤化物。如果醚是一个主要的碳通过S可能发生吗N2通路。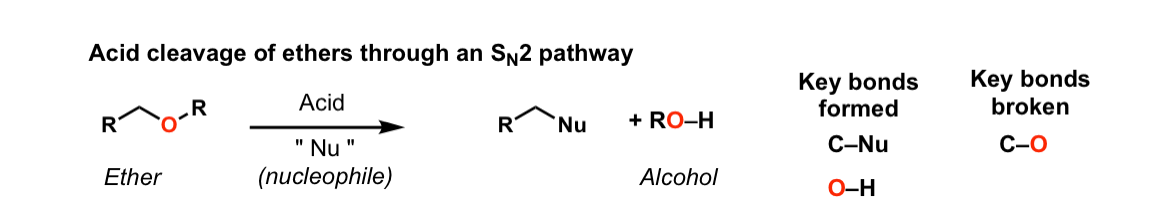
注:常见的酸为此嗨和其他氢卤化物,以及H2所以4在H2O。
在的情况醚裂解是次要的,异构中心,会有反转的配置。
例子:
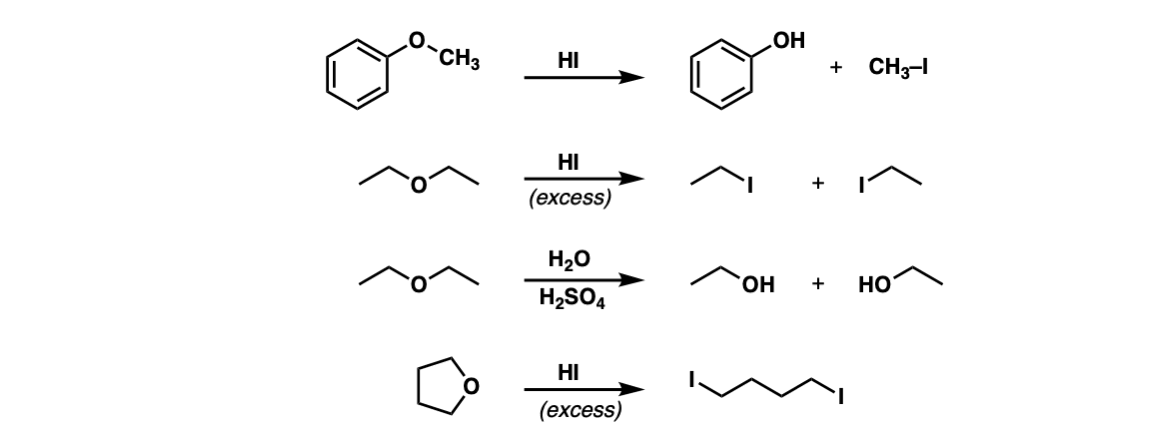
注:第三个例子也可以写“H3O +”。注意,嗨将主要醇转化为过剩烷基卤化物通过SN2,但不是苯酚(C6H5sp以来哦)2杂化碳原子不接受N1或年代N2反应。
机制:强酸(HI)使质子化醚氧,把它变成一个更好的离去基团(步骤1,箭头A和B)。接下来,碘离子攻击碳年代N箭头2反应(步骤2,C和D)给的酒精和碘甲烷。
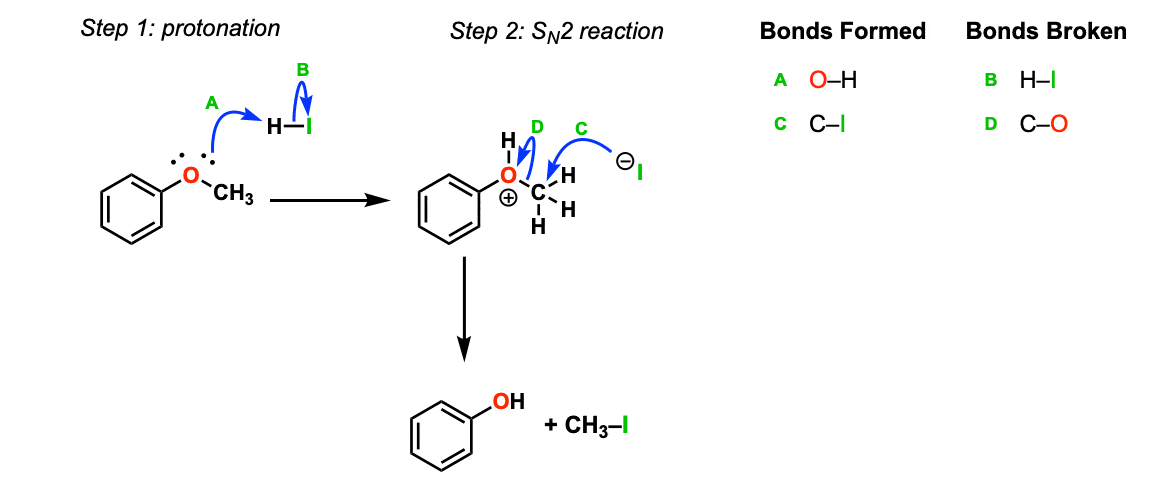
注:的情况下醚裂解是次要的,异构中心,会有反转的配置。
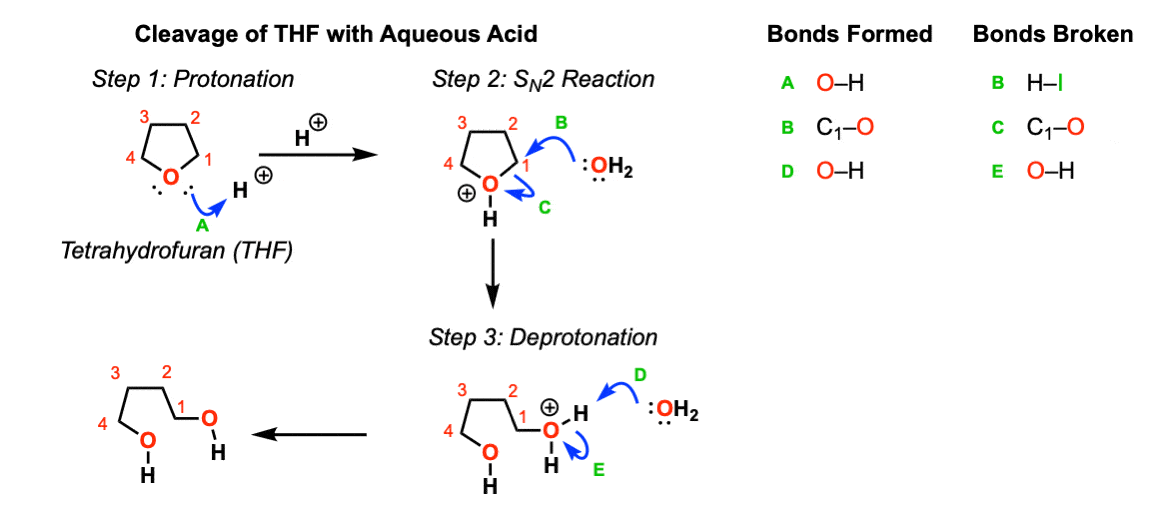
测试你自己!
 点击翻转
点击翻转
 点击翻转
点击翻转
 点击翻转
点击翻转
(高级)引用和进一步阅读
醚广泛惰性很多条件,从而找到常用的溶剂(如。乙醚,四氢呋喃(四氢呋喃),二氧六环,glyme等等)。醚乳沟通常需要强酸和热量,这迫使条件。或者,可以使用硅烷试剂,在室温下反应。
- 一种新方法制备的有机碘化
赫尔曼·斯通和哈罗德SHECHTER
《有机化学》杂志上1950年,15(3),491 - 495
DOI:10.1021 / jo01149a008
而不是使用你好,这是昂贵的(难以忽视的气体),一个可以用磷酸+ KI的结合醚乳沟,你好原位。 - 1,4-DIIODOBUTANE
赫尔曼·斯通和哈罗德Shechter
Org。Synth。1950年,30.,33岁
DOI:10.15227 / orgsyn.030.0033
这个过程从有机合成可靠来源的独立测试实验室有机合成过程,演示了的乳沟四氢呋喃与回流强酸。下面是各种各样的论文使用silane-based试剂醚乳沟。诺贝尔奖得主已故教授乔治Olah在这个领域做了大量的工作在他的职业生涯。 - 劈理的酯类和醚Iodotrimethylsilane
谢霆锋洛克Ho博士教授乔治·a·Olah
Angew。化学。Int。。1976年,15(12),774 - 775
DOI:10.1002 / anie.197607741 - 轻微的乳沟methoxymethyl (MOM)与溴化三甲基硅烷基醚
丹尼尔Delorme斯蒂芬•Hanessian伊夫
列托人。1984年,25(24),2515 - 2518
DOI:10.1016 / s0040 - 4039 (01) 81219 - 3
妈妈醚通常用作保护团体在有机合成-哦,所以妈妈醚的选择性去保护策略下温和的乳沟是无价的。
现实生活中的例子:
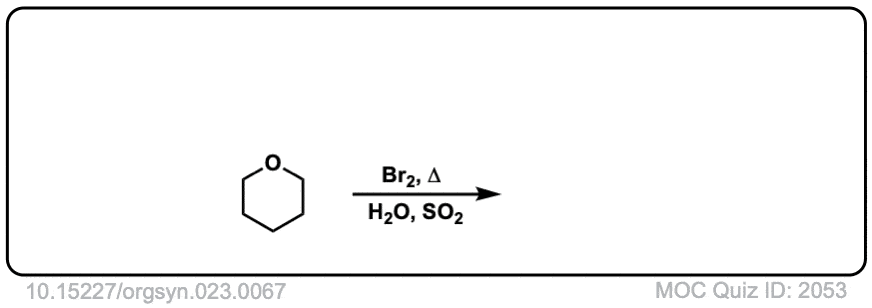
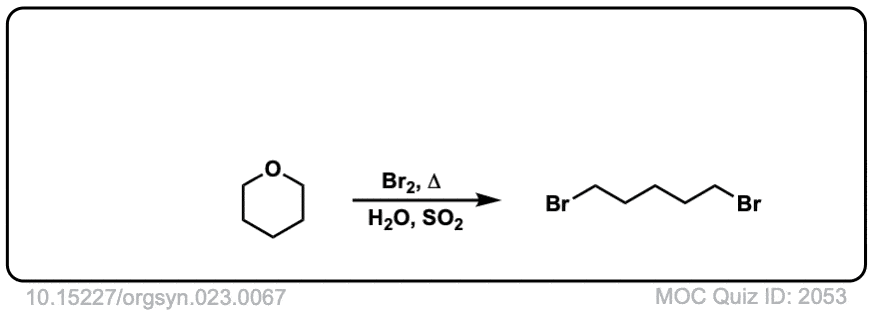
Org。Synth。1943年,23岁,67年
链接DOI: 10.15227 / orgsyn.023.0067
 点击翻转
点击翻转
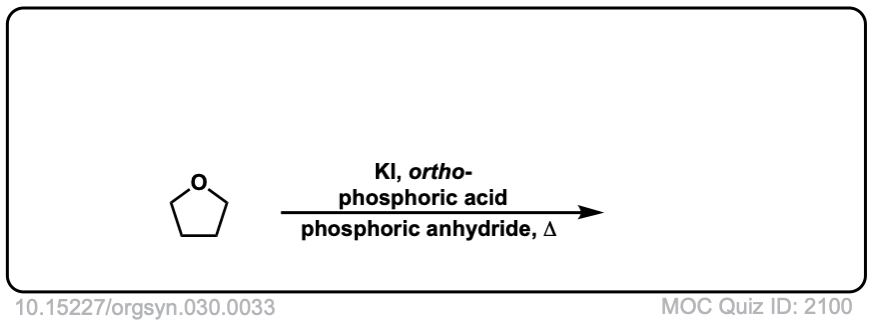
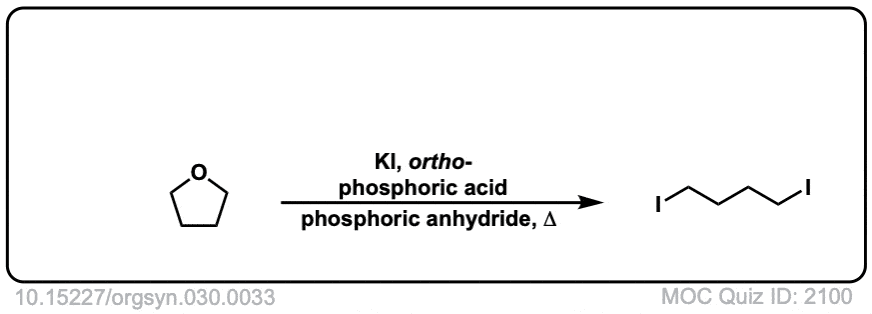
Org。Synth。1950年,30岁,33
链接DOI: 10.15227 / orgsyn.030.0033
 点击翻转
点击翻转
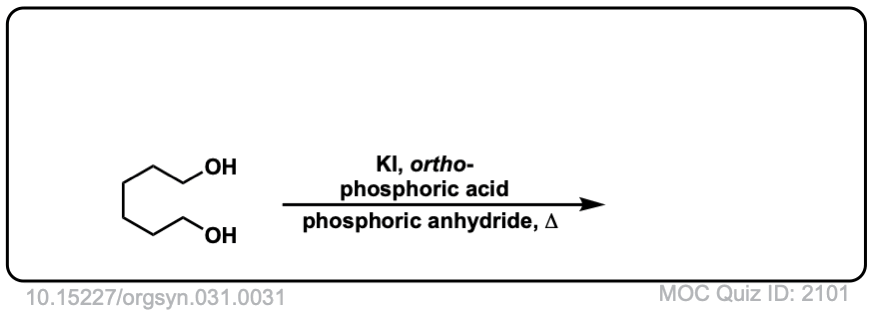
Org。Synth。1951年,31岁,31日
链接DOI: 10.15227 / orgsyn.031.0031
 点击翻转
点击翻转
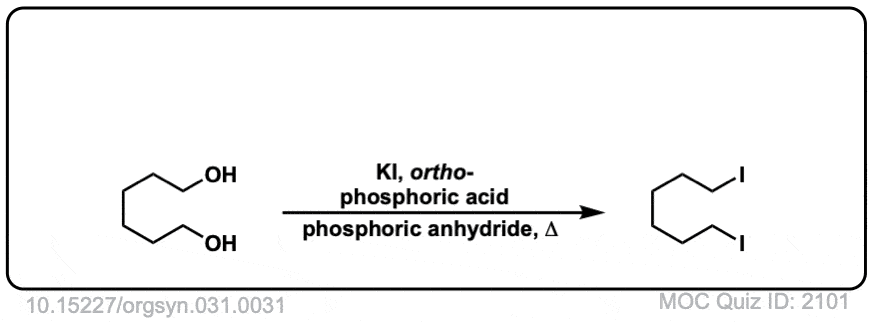
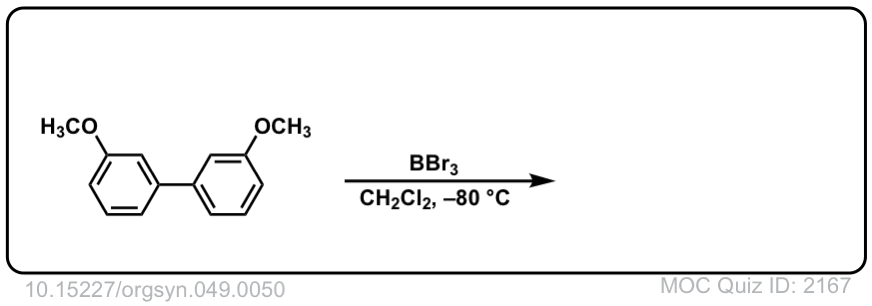
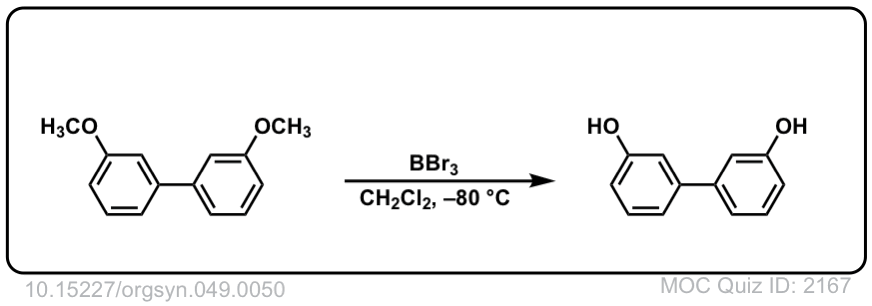
Org。Synth。1969年,49岁,50岁
链接DOI: 10.15227 / orgsyn.049.0050
 点击翻转
点击翻转
CF3CO2H的用途是什么?它可以用来分裂醚?我已经要求表明会发生什么就在这个试剂,在热的存在,一个化合物,其中包含醚组与苯环相连,酮基,烯烃集团和苯基环。
多谢。
嗨。我不知道这个网站仍然是活跃的。
会发生什么当异丙基甲醚反应和你好吗?
如果你有多余的嗨,你会得到一个CH3-I和异丙基碘。
你好,只是我错过了一个细节:如果我们希望ro ckeave Ph-O-R(苯甲醚)使用一种以水为溶剂,这有什么teperature要做吗?和我们要持续多久完整性的反应吗?谢谢你!
苯甲醚,R = CH3,通常的方法是使用嗨(碘离子将作为亲核试剂将甲基组)不是硫酸,因为就是HSO4(-)离子是一个非常贫穷的亲核试剂。你可能需要等待一段时间,甲基裂开。另一种方法是使用一个很强的路易斯酸,如BBr3,如这个有机合成的例子所示。
http://www.orgsyn.org/demo.aspx?prep=CV5P0412
亲核试剂会小烷基和打破切断债券在第一R-c-o-R反应
什么是一个很好的问题。在这种情况下,因为我们正在讨论SN2,答案是肯定的,自从SN2收益最快在小烷基组。
当烯丙基碘化反应超过你好吗?
可能会有增加嗨在烯丙基碘的π键。
先生,
请解释的情况下CH3-O-tBut存在嗨{不是无水}?
谢谢。
第一步是质子化作用的氧。之后,有两个相互矛盾的可能性会发生什么:攻击的I -甲基给CH3I tBuOH,或电离,给叔丁基阳离子和CH3OH。我不确定目前的路径最初将占主导地位,但你好,多余的都将转化为烷基碘化。
谢谢你先生对于这样一个巨大的资源……。真的很有帮助。
我有一个问题关于如何决定的亲核试剂进攻的不对称醚?…. .一些表示,它的攻击主要碳(更少的阻碍)生产1°烷基卤化物。在另一个实例表示,它产生3°烷基卤化物……你能帮我在这里…非常感谢。
如果任何一方的碳- o -债券有三个学位。收益机制通过Sn1类型机制。这导致对碳正离子的攻击更稳定。所以三度烷基卤化物的成果。
在其他情况下。Sn2机制。Hence a primary alkyl halide is formed.
1-ethoxy-2 -苯(1-methoxyethyl) +嗨- > ? ?
这是一个还原反应吗?
- - - - - -
不,这是一个替换。
Rxn btwn C6H5CH (CH3)甲基嗨
质子化作用后,嗨,可能第一步是电离给二级苄基的碳正离子,解放甲醇。攻击嗨的碳正离子然后给一个烷基碘。但你好,过量的甲醇将转换为CH3I。
小环醚比脂肪醚对质子反应吗
根据埃文斯pKa表质子化了的二甲醚的酸度系数是-3.8和质子化了的四氢呋喃的酸度系数是-2.0。因为酸性越强,较弱的共轭碱,它是公平地说,四氢呋喃是一种比二甲醚稍强的基础。
二异丙醚+ bbr3这是如何工作的呢? ?
坐标硼氧首先,离子对。在这一点上,要么SN2攻击通过溴异丙基集团之一的仲碳,或电离给仲碳的溴紧随其后。
嗨,詹姆斯
是HOOC-C6H5-O-CH2-C6H5芳基苄醚,结果从保护酚苄氯化物,这种化合物稳定如果l使用chloropropanol estirification反应吗
Chloropropanol吗?这是不稳定的
我们将如何碱性水解醚怎么样
通常是非常困难的,因为你的离去基团alkodie,这往往是很基本的。
什么时候这个反应遵循SN1和什么时候遵循SN2。因为我的课本说这取决于氧鎓离子形成稳定的碳正离子。如果它那么SN1否则SN2稳定。请帮助
这绝对是真的。它取决于碳正离子的稳定性。这个特定的页面覆盖了SN2例子。一个明确的情况的情况下苯甲醚,SN1乳沟是不可能由于不稳定的甲基苯基阳离子和阳离子。
在第三例中有两个-哦。
这是正确的结果或需要修正吗?我有一个任务(转换)= > CH3-O-CH2CH3 = = > CH3-CH2-OH
在嗨这将被转换成CH3CH2-I过剩
如果物质就像一个四氢呋喃但双键。先将盐酸与双键发生反应吗?
是的。假定氧双键是邻,你会有一个烯醇酯。画一些共振形式的这个物种,你会看到有一个负电荷的碳。的位置将质子化了的。
詹姆斯爵士当我们r的四氢呋喃作为溶剂使用reacion没有需要添加的添加剂特别organometalic反应但在以太的存在,他们需要添加添加剂。为什么?
吗?你必须提供一个具体的例子。
在循环二醚的情况下会发生什么?将两个醚裂解也许还不止一个?
无法确定你的意思,“二醚”。你是否指的是一个实际的di-ether缩醛吗?
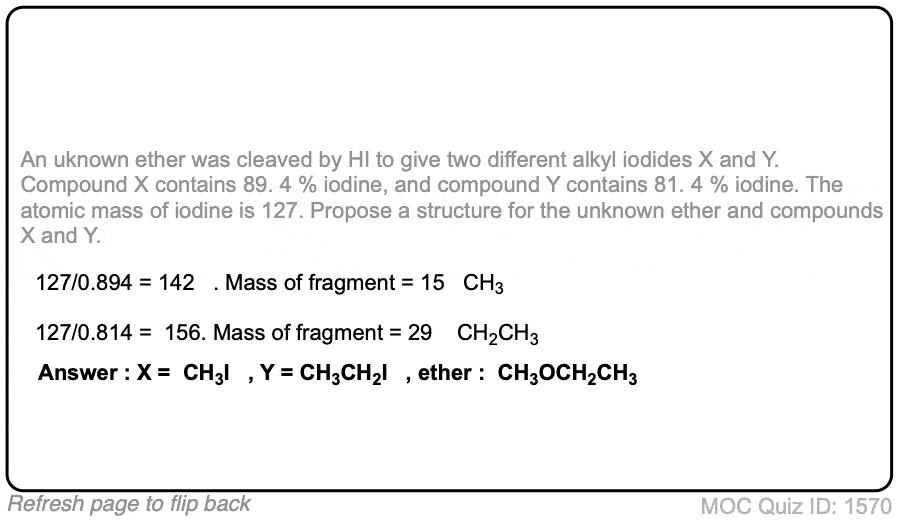
CH3-O-CH2-CH3 +嗨给CH3I酒精和为什么不CH3OH CH3CH2I ? ?
攻击甲基将大大快于主要的碳。然而,注意,如果过量添加你好,所有醇将转换为烷基碘化。
永远记住这个经验法则
如果你有ROR类型组和R和R H + 1度那么首先将附加在O和第二步我将做Sn2攻击少阻碍了C(如果R是甲基和R’是C2H5然后R是阻碍少)。
如果任何两个R组是sec或叔组第一个C +将形成,然后我将附上(C +将形成更稳定的地方)
注意的SN2反应位阻起着很大的作用。,科举制CH3CH2I,亲核试剂进攻更多的位阻碳只有CH3相比,所以最好是少的亲核试剂达到阻碍CH3的攻击给CH3I和酒精而不是CH3OH和CH3CH2I。
嗨,做环醚(不是环氧化合物)也遵循这些类型的反应?
是的,他们做的。例如环醚四氢呋喃(四氢呋喃)与强酸可以打开的亲核试剂。路易斯酸四氯化钛也特别好…。
这与盐酸反应吗?例如:盐酸乙醇+ =氯乙烷?
是的,这是可能的。
嗨,二、三级分裂会SN1吗?
叔分歧肯定会SN1。
你好詹姆斯,
你也可以做这个裂开醚定量分析确定聚醚单体的组件?
理论上是的,但我认为这将是非常困难的实际水平。
当你把一个试剂与四氢呋喃发生了什么?它是如何反应?
三级醚反应,说,发生在高温在酸性介质,可以通过消除烯烃形成(提供阴离子是弱亲核试剂)?
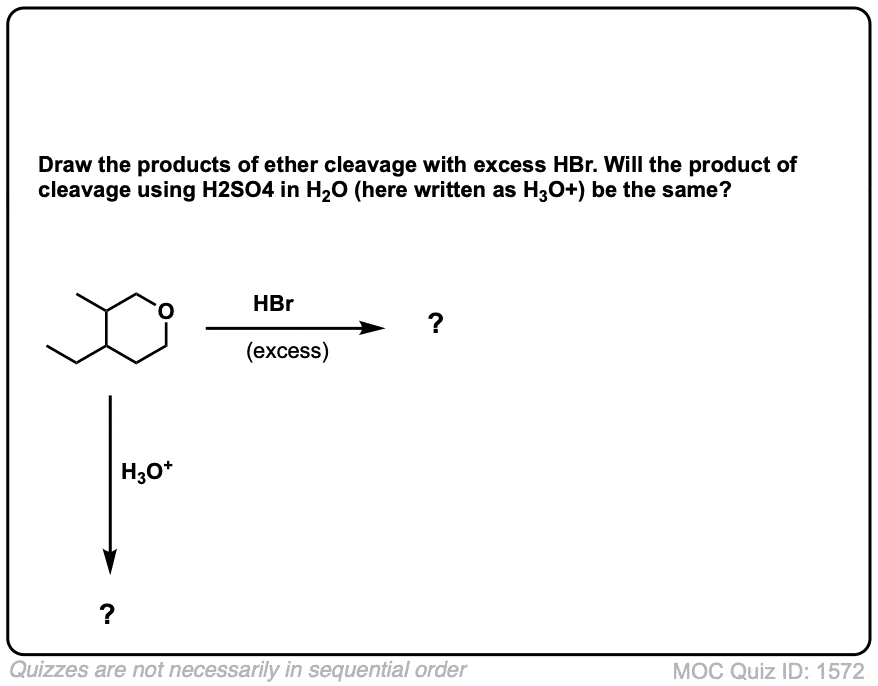
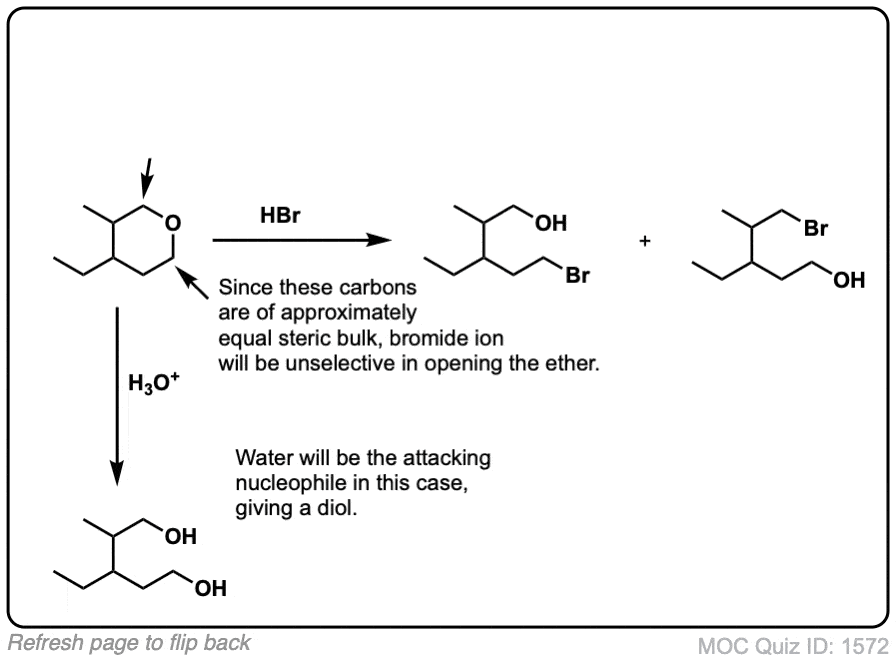
请在四氢呋喃和h3o +之间的反应?
好问题。补充说,作为一个“附录”,见上图。
你好,詹姆斯,
你能给一些建议aequeous劈理的四氢呋喃的反应条件?因为水是一个很坏的亲核试剂的反应将年龄而给不满意的收益率。除了这样一个东西对温度和硫酸/水之间的比率。也许还存在一个可用的催化剂?
你为什么想做水劈理的四氢呋喃?
如果有一个叔烷基其中,会一直以来SN1碳正离子机理可以稳定现在我+效果呢?
很难推广。这个特定的文章是关于SN2乳沟。
C6H5OCH3劈理的第一个例子,C6H5I CH3OH不怎么形成的?
啊!这是…的SN2反应。和的SN2反应需要一个背后攻击。背后袭击会发生在芳环这是不可能的(非常拥挤)。同时,SN2反应不要工作在sp2杂化碳原子(如烯基卤化物)
这种方法适用于复杂的分子喜欢木质素含有大量的醚联系吗?
关于反应活性,更少取代碳中心反应,因为在背后攻击有更多空间皇权?
是的,完全正确!(不管怎样的SN2反应)
嘿,我有一个问题关于这个反应的发生。如果我可以这么说有卤化氢条件支持激进的形成(过氧化氢、UV)我能控制这个反应,或导致激进的替换发生的可能性高于醚乳沟吗?
取决于醚,但是大多数醚对哈佛商业评论是相对稳定的。醚不只是脱落,需要用锤子打击他们。
这是如此有用的!谢谢你这么多!你有什么在环氧开环吗?
假设我有一个聚合物结构,与多个醚联系,举例来说,一个聚乙烯乙二醇醚。劈理的概率是什么影响终端连接,而不是其他醚债券? ? ?谢谢。
嗨
这我的问题请answ ? ?
(假设我有一个聚合物结构,多个醚联系,举例来说,一个聚乙烯乙二醇醚。劈理的概率是什么影响终端连接,而不是其他醚债券? ? ?谢谢。)
非常低。如果你有条件离开终端连接,它将断开的内部联系。你需要修改挂钩,因此只有终端残渣可以删除。
嗨,在Ph-OH + CH3I产生的机制。为什么没有产生Ph-I + CH3-OH ?谢谢,P。
因为这将涉及的SN2我——一个sp2杂化碳,这是非常缓慢的,更不用说,“背后攻击”会发生从苯环中间!
柜内的叔。醚and resonance stabilised ether we can use SN1 Mechanism
不对称醚乳沟呢? ? ? ? ? ? ?
你好,是一个更强的亲核试剂比盐酸吗?如果要求列出所有的氢卤化物的乳沟速度与醚侧链,你应该安排他们什么顺序?我一直认为高频是最强的,当你沿着它变得较弱。但事实不是如此?你能向我解释为什么。
谢谢,
郝
嗨亲核试剂比盐酸,因为碘原子更可极化,因此更能够发生的SN2反应。当你沿着卤化物集团电子壳越来越远离原子核,因此更多的可极化的。因此他们得到更多的亲核gorup
你一定在想,F为电负性最稳定的负电荷。但记住这不是唯一依据u决定酸度。氢氟键债券是氢键(强烈的)所以裂开,那将是最困难的。而对于其他的水化能量中也扮演了重要的角色。所以正确的系列:
你好>盐酸哈佛商业评论> >高频
根据他们的酸性强度。
所以我——作为一个很好的亲核试剂的亲核试剂,因为它是一个稳定。
但是位阻呢?我希望比碘化反应的氯离子由于其规模要小得多。也变得更加重要考虑的Sn2反应的事实。
位阻大小与卤化物不是一个真正的问题,因为通常是债券的长度成反比与碳(即形成。小Cl,短的键长,大的我,不再键长),这两个因素在很大程度上抵消了。更重要的是溶剂的类型。在极性质子溶剂(溶剂氢键)比氯化碘离子的亲核试剂较强。看到这个posthttps: / /m.deriinvest.com/2012/06/18/what-makes-a-good-nucleophile/
首先我们必须了解债券分布在任何类型的# neucleophilic反应
氢氟键(至少倾向分布的离子)由于最小的表面积
设定h(快速或好/快离子分布的倾向),由于最大的表面积
在反应性秩序的基础
F > CL > <氯< H-Br < BR >我或氢氟键设定h
如果你看一下机制,显示了第一步Hydrogen-Iodine债券打破。发生这种情况是因为碘原子是一个大型和价电子是远离原子核,因此很容易裂开债券的小s轨道h .如果你看看卤化物的共轭碱碘是最大的,因此比其他可极化的它可以稳定一个负电荷更好。你可以进一步扩大这个逻辑卤化物和观察到的趋势。
是的,谢谢你的阿里置评。