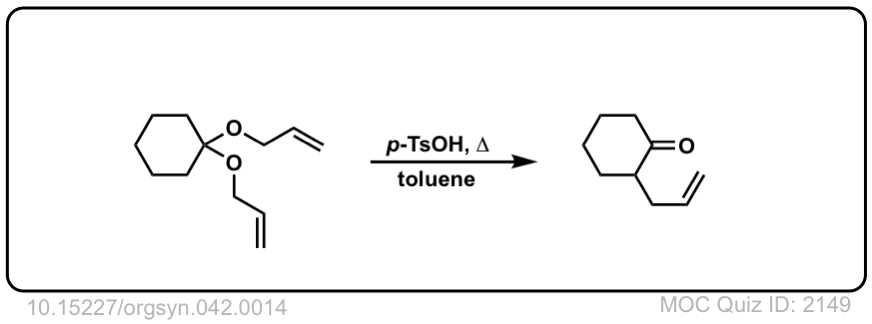
克莱森重排
描述:Claisen重排是烯丙基的[3,3]- sigmattic重排乙烯基醚。结果是不饱和的羰基.
注:该反应的产物比反应物更稳定约20千卡/摩尔,主要是由于C-O (pi)键(80千卡/摩尔)比C-C (pi)键(60千卡/摩尔)的强度更大。
例子:
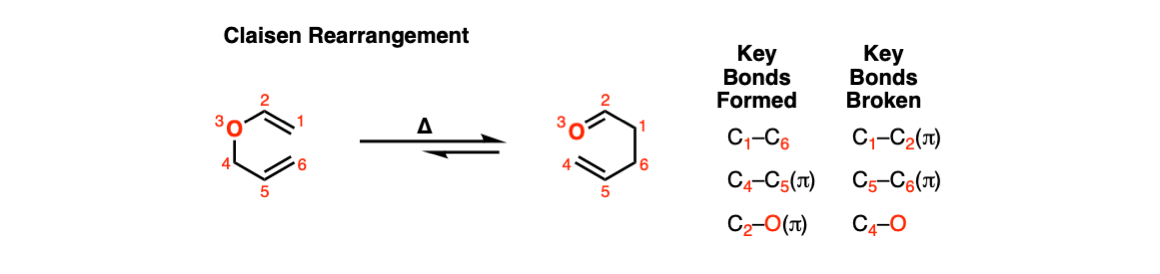
笔记:在前两个例子中,加热导致γ, δ -不饱和的形成羰基.
第三个例子涉及烯丙基醚苯酚的。在这种情况下,芳香环上的π键起着"乙烯基醚”组件。第一个产物是不饱和的羰基,没有芳香。然后是酮-烯醇互变异构恢复芳香。
第四个例子有点棘手。酸(TsOH)是一种质子酸缩醛氧,这使它成为一个好东西离去基团.另一对的孤对缩醛氧与碳形成了一个新的PI键,从而消除了一个当量的烯丙基醚.这个新物种是氧离子(带正电的氧),然后失去一个质子形成一个烯醇醚(很像珐琅的形成)。由此产生的乙烯基烯丙基醚然后进行Claisen重排,得到所示的产物。
第五个例子也很棘手!第一步是克莱森重排,以安装烯丙基在昊图公司的位置。然而,这不能失去氢来恢复芳香,因为那里有一个CH3 !相反,Cope重排发生在帕拉-位置给出最终产品。
机制:
克雷森重排的第一步(也是唯一的一步)是协同的周环反应乙烯基烯丙基醚,经过循环过渡状态(步骤1,箭头a, B和C)。
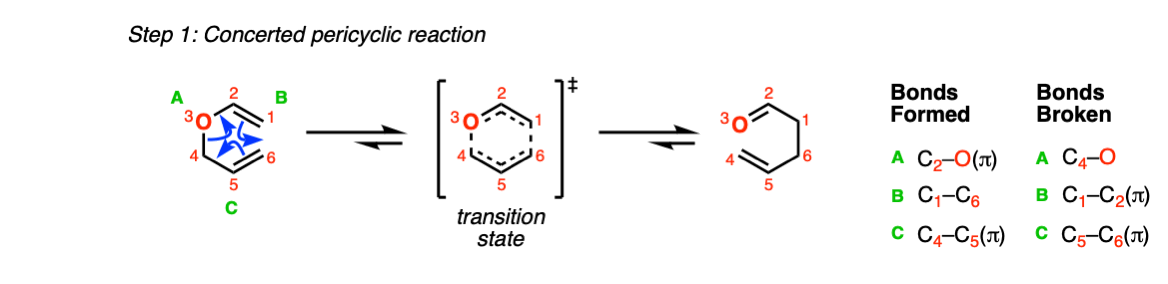
注:
我们可以通过比较断开和形成的化学键的强度来计算反应的驱动力。
键断:C-C pi(65千卡/摩尔)和C-O sigma(85千卡/摩尔)
键形成:C-O pi(85千卡/摩尔)和C-O sigma(85千卡/摩尔)。
净:20千卡/摩尔,使反应基本上不可逆。
现实生活中的例子:
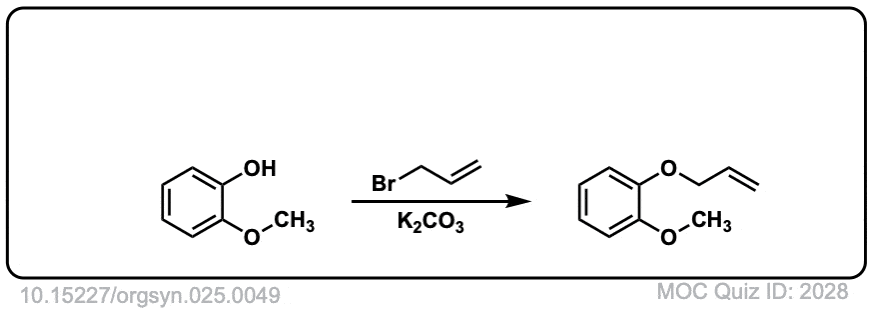
Org。合成人,1945,25,49
DOI链接:10.15227/orgsyn.025.0049
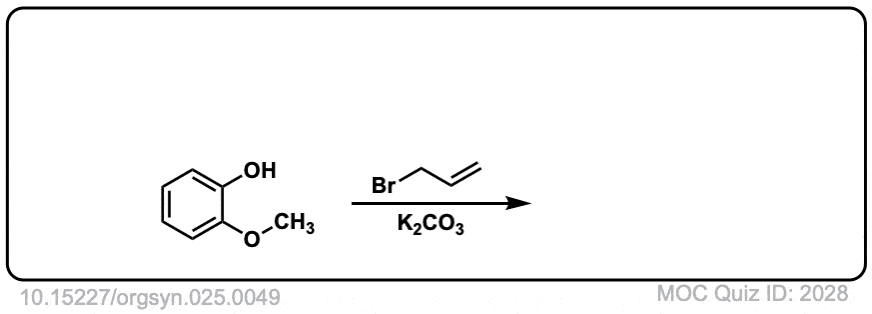 点击翻转
点击翻转
Org。Synth, 1962, 42, 14
DOI链接:10.15227/orgsyn.042.0014
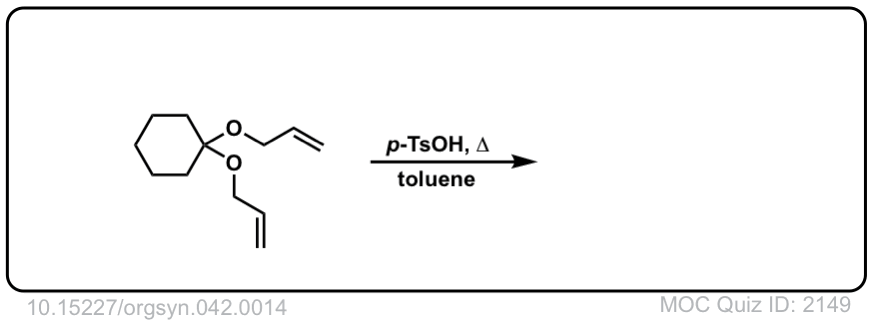 点击翻转
点击翻转