胺保护和去保护
描述:胺可以被保护为氨基甲酸酯使用Boc2O, CBzCl和FMOC-Cl等试剂进行分组。这些氨基甲酸酯可以分别用酸(如Boc用三氟乙酸)、催化加氢(Pd-C, CBz组用H2)或基本条件(FMOC用哌啶)去除。
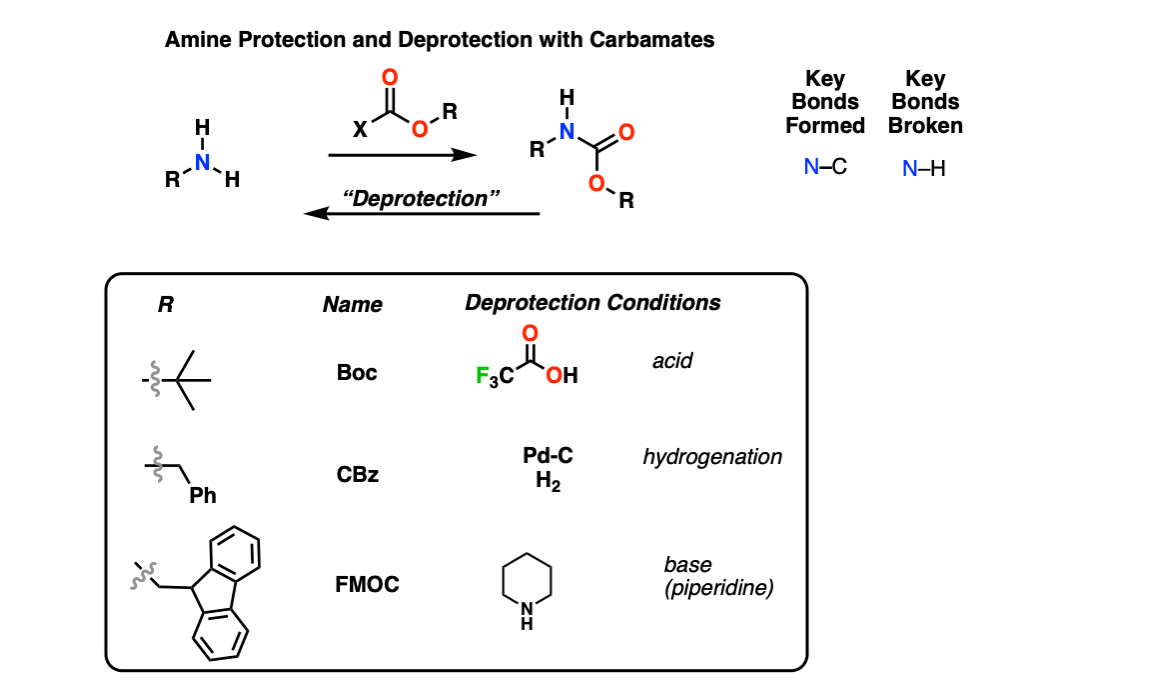
注:胺保护对于肽合成尤为重要。
例子:
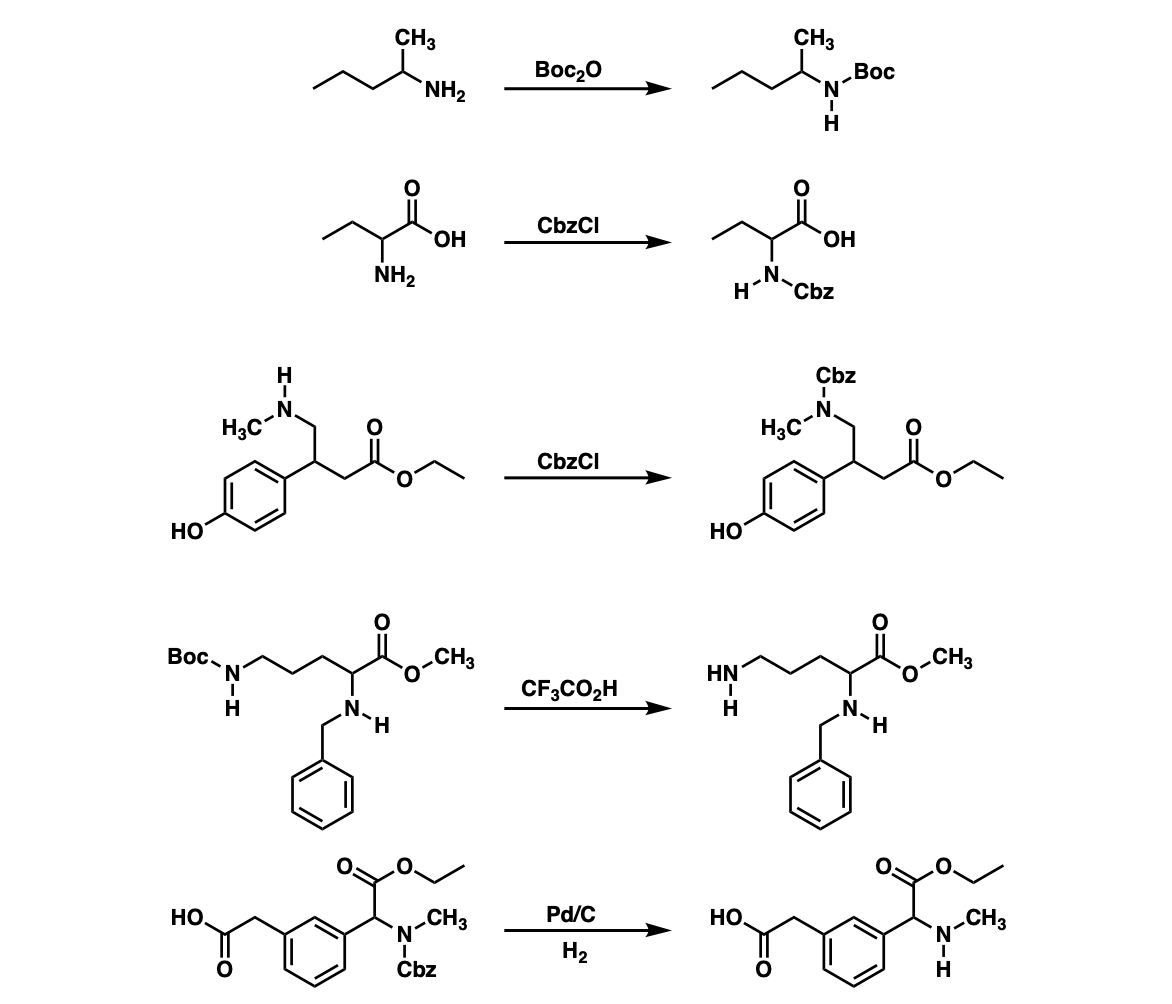
注:例1显示Boc保护。例2和例3显示了CBz保护。的Boc去保护胺在酸性条件下,使CBz受到保护胺不受影响。
例5显示了从胺使用催化氢化。
机制:保护胺使用中国银行2O(二碳酸二丁酯)。
在第一步,胺攻击羰基碳酸盐的碳(步骤1,箭头A和B),形成新的四面体中间体。氧的消除(步骤2,箭头C和D)导致碳酸盐岩的损失,碳酸盐岩本身可以作为碱,或自发脱羧(失去CO2)生成t-丁氧,然后中和质子化氨基甲酸酯.
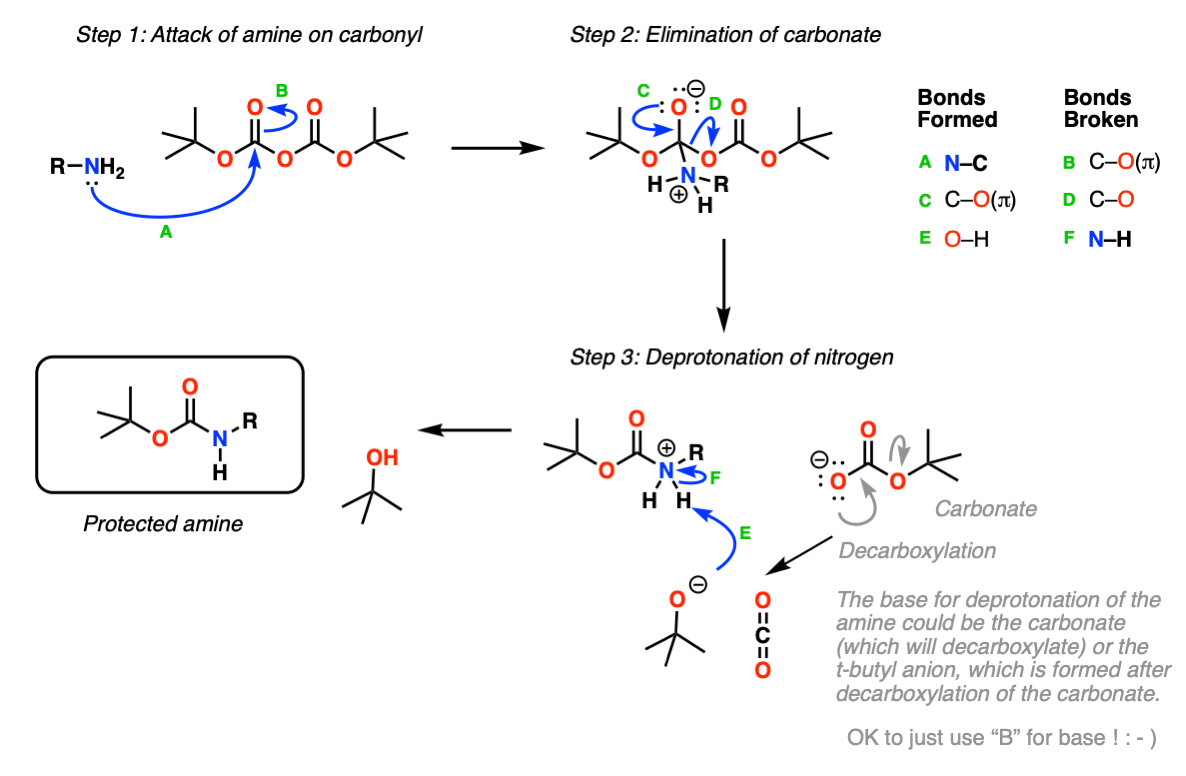
这可能把事情简单化了一点;在第一步之后,质子从氮转移到氧也是可能的,最终也会得到同样的结果,这里我们只是为了简单起见。
去:质子化氨基甲酸酯氧与强酸,如三氟乙酸(TFA)(步骤1,箭头a和B),然后导致t-丁基碳正离子的损失(步骤2,箭头C和D)。产生的“氨基甲酸”(一种附着在二氧化碳上的氮)经过质子转移(步骤3,箭头E和F),然后脱羧(步骤4,箭头G和H),得到中性的,去保护的胺.
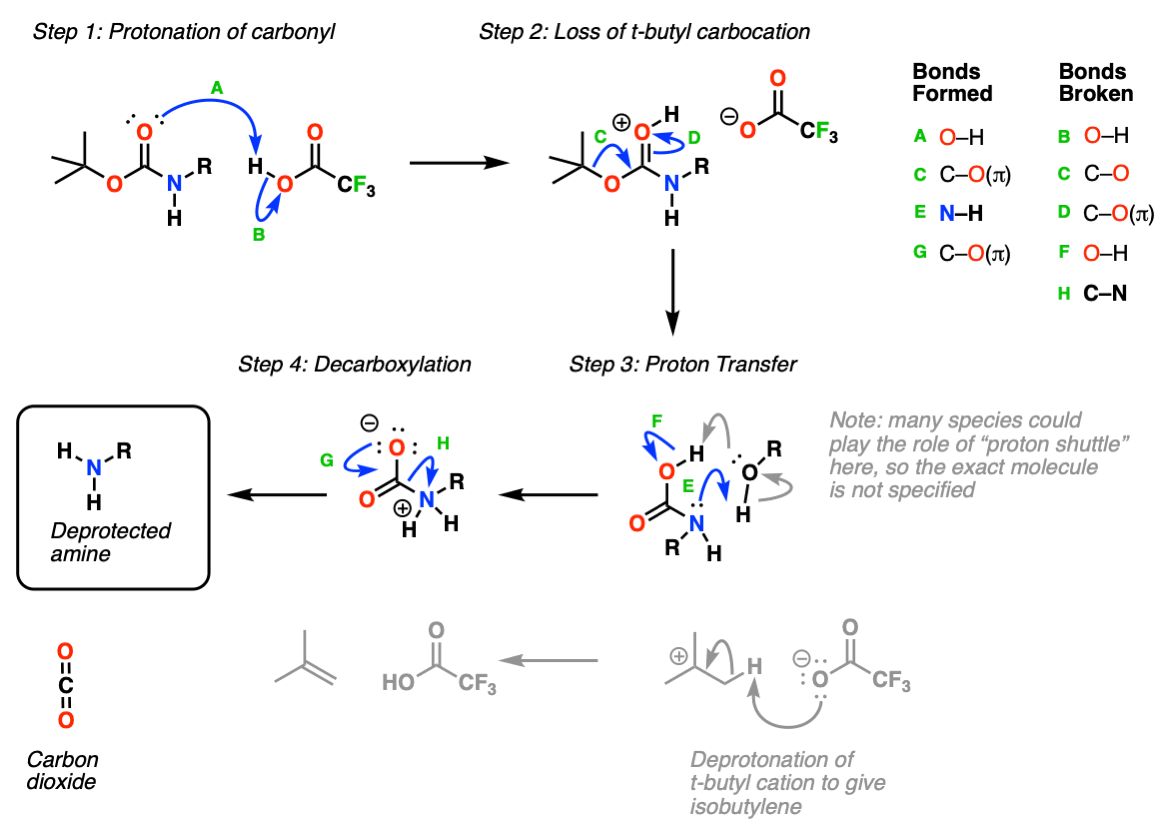
注:实际上,这是所有有机化学中最简单的反应之一。只需将“纯”TFA添加到受保护的稀释(~ 0.2 M)溶液中胺,流行!火车开了氨基甲酸酯.观察CO2泡掉是很令人满意的。
或者,加热被保护的东西胺(真空下约180°C)也会导致保护基团的损失。
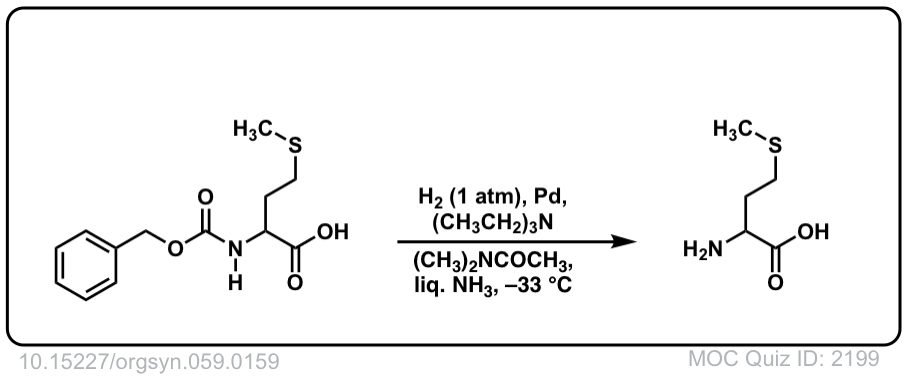
现实生活中的例子:
Org。Synth, 1979, 59, 159
DOI链接:10.15227/orgsyn.059.0159
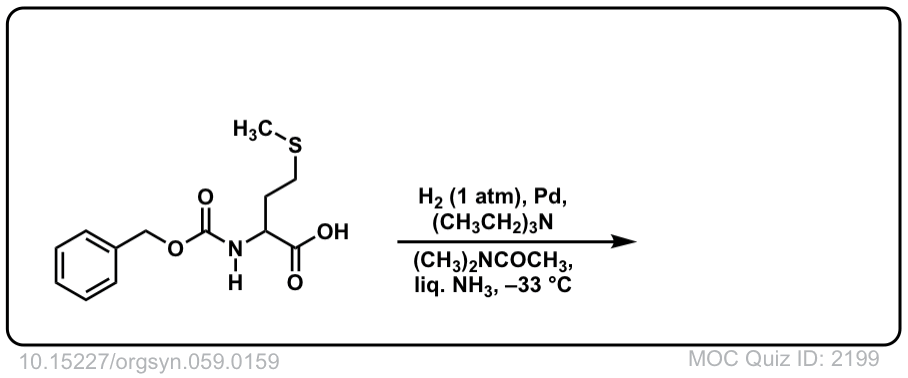 点击翻转
点击翻转